乳腺癌是全球女性最常见的恶性肿瘤。在肿瘤转移过程中,患者会遭遇内脏危象,尤其当出现恶性心包积液,如处理不及时,可迅速进展为急性心包填塞,导致心力和呼吸衰竭,严重威胁患者生命安全。传统治疗手段,如心包穿刺和心包腔内药物灌注只能暂时缓解症状,但若未从根源上控制肿瘤,疾病将迅速进展恶化,对患者生命构成严重威胁。针对晚期乳腺癌合并恶性心包积液,其治疗策略需把控局部与全身治疗时机、方案,达到迅速控制症状、延缓肿瘤进展、延长生存期和提高患者生存质量的目标。
中山大学孙逸仙纪念医院乳腺外科龚畅教授 和 乳腺肿瘤内科曾银朵教授 分享了一例HR高度异质性、HER2低表达的晚期乳腺癌病例,该患者因恶性心包积液引发急性心包填塞,生命悬于一线。经过数次、高效的多学科会诊,患者接受了及时的心包积液引流及有效的抗肿瘤治疗,最终化险为夷。在病例点评环节,专家将深入探讨真实世界中抗HER2-ADC对于此类伴心包填塞重症患者的临床应用价值。
初次就诊
2024年春节前夕,33岁的王女士(佚名)被家人急匆匆地推进了乳腺外科龚畅教授的诊室。患者气喘吁吁、表情痛苦,自诉胸闷和憋喘,患者和家人自诉临近年关,病情比较重,辗转多家医院都表示“无能为力”,希望教授能帮助一下她们,至少能够和家人一起度过“最后”这个春节。
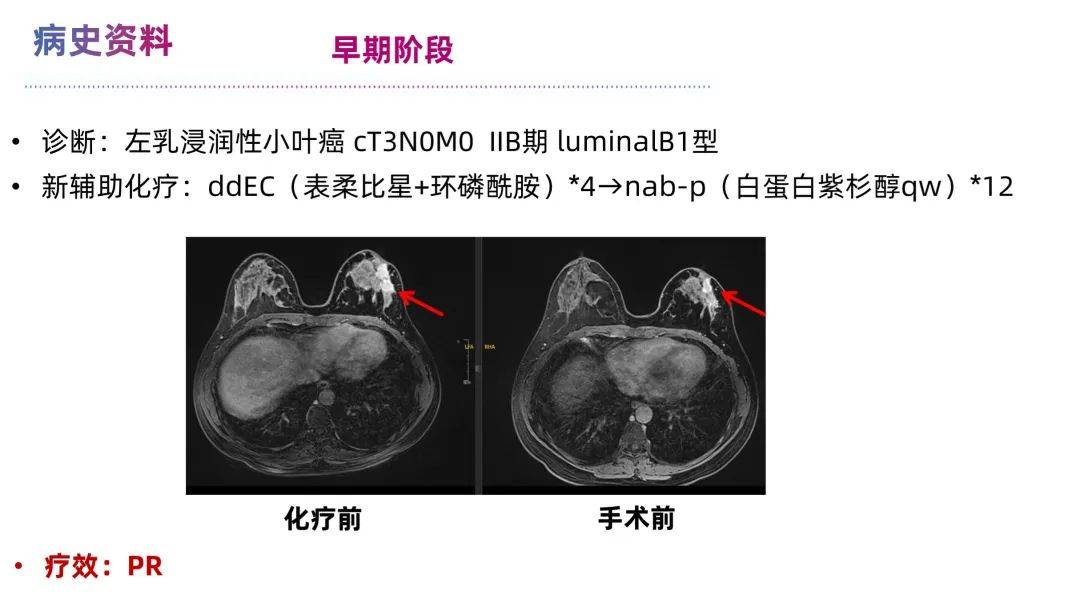
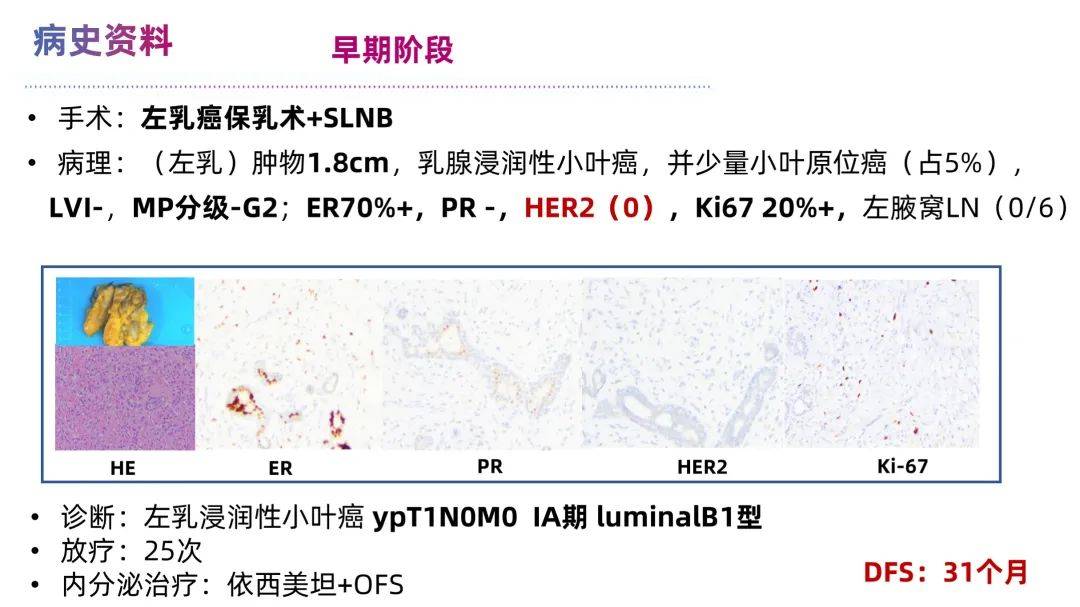
经过详细问诊,龚教授获悉该患者 初诊左乳浸润性小叶癌,cT3N0M0 IIB期,LuminalB1型 , 经过新辅助化疗8周期后,未达病理完全缓解(ypT1N0M0,I A期 luminalB1)。内分泌治疗仅2年余出现多发淋巴结和骨转移,转移后经过 淋巴结 活检病理结果转变为 三阴型 ,接受化疗和免疫治疗后,再次进展, 骨活检 转变为 L uminalB1 ,但经过CDK4/6抑制剂和内分泌治疗1周后,出现呼吸急促、胸闷、心悸,ECOG 3-4分;面对这一紧急状况以及患者家属的迫切需求,龚畅教授和曾银朵教授在最短时间内对患者的病情进行全面回顾与评估。
危急病情评估及局部处理
就诊当日,超声检查显示双侧大量胸腔积液并行双侧胸腔积液引流。
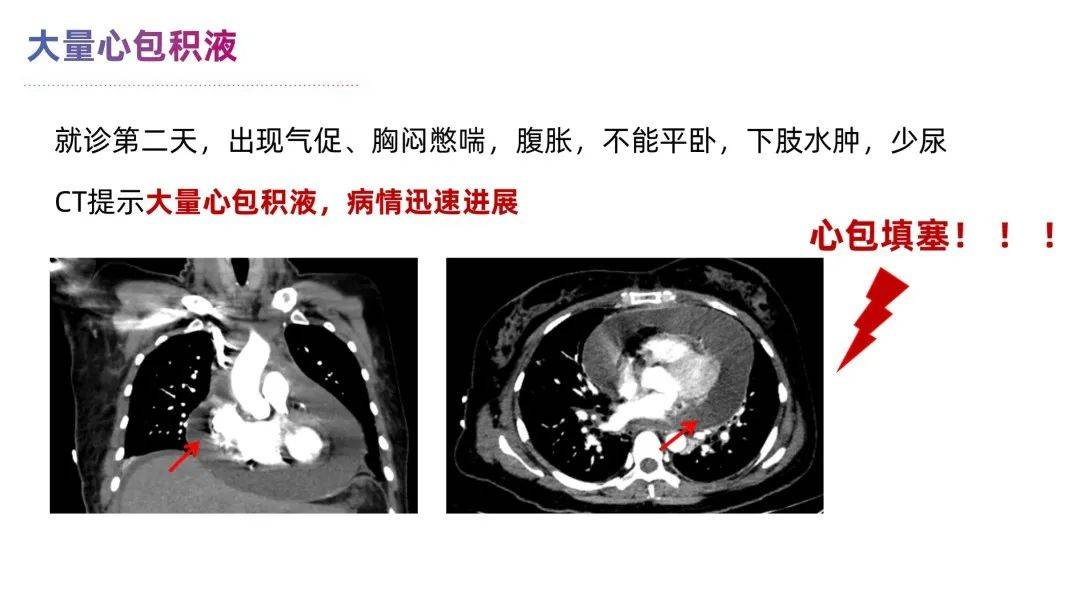
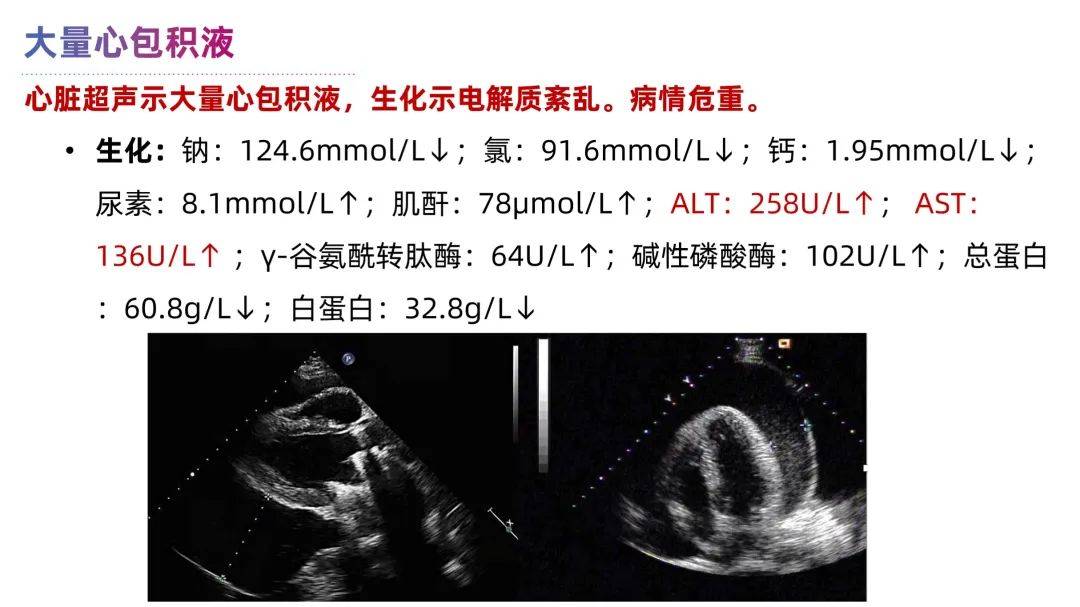
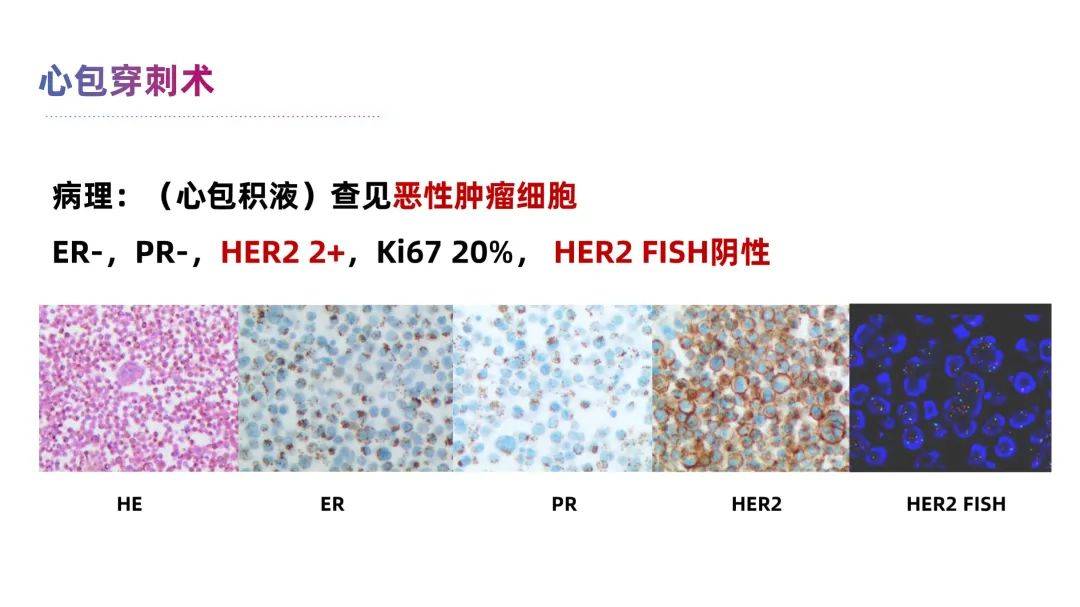
就诊第二天,患者病情进一步加重,表现为气促、胸闷憋喘,腹胀,无法平卧,少尿,下肢水肿。CT及心脏超声提示:出现心包大量积液。乳腺外科,乳腺肿瘤内科,肿瘤心血管科 MDT会诊,决定立即对患者执行心包穿刺引流术,引流心包积液,我院细胞学病理报告心包积液和胸水均见恶性肿瘤细胞,提示乳腺癌转移,且分子亚型转为 三阴型 (肿瘤细胞免疫化学 ER-,PR-,HER2 2+,HER2 FISH阴性)。
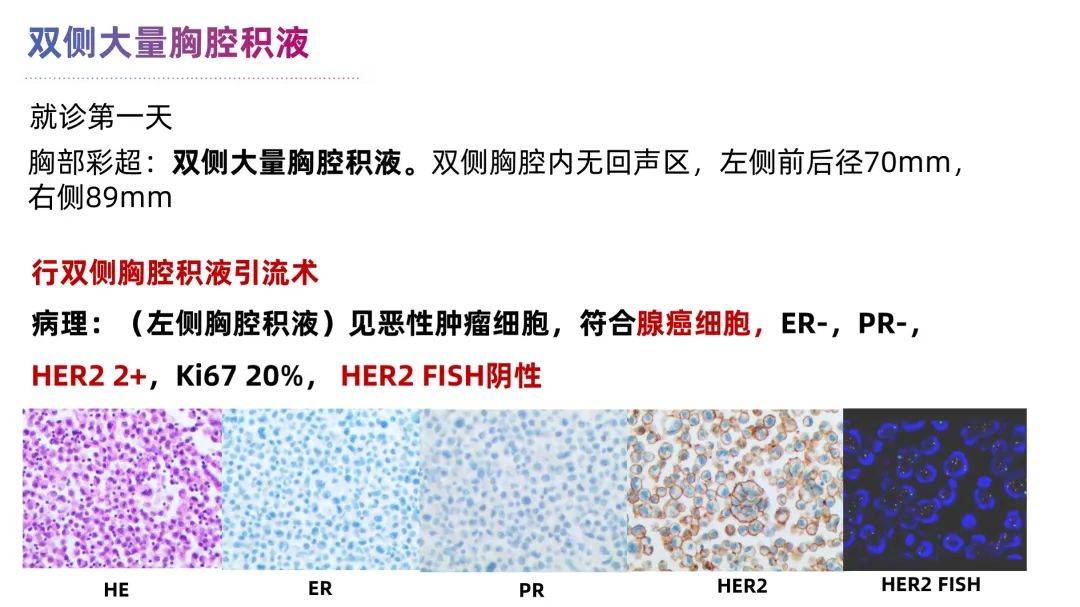
左右滑动查看更多
患者既往诊疗情况回顾
01
病史资料
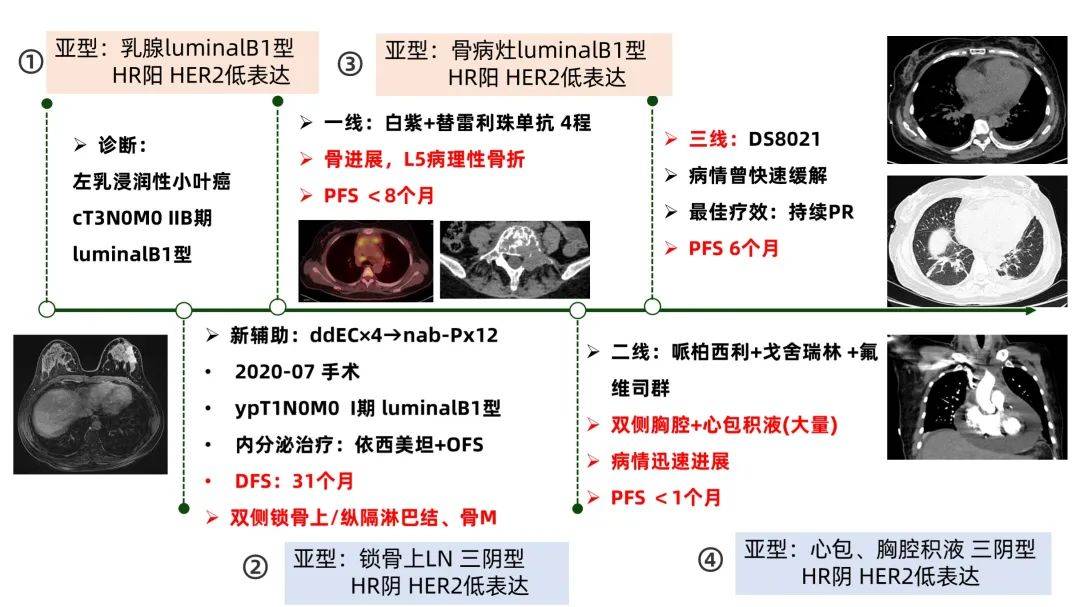
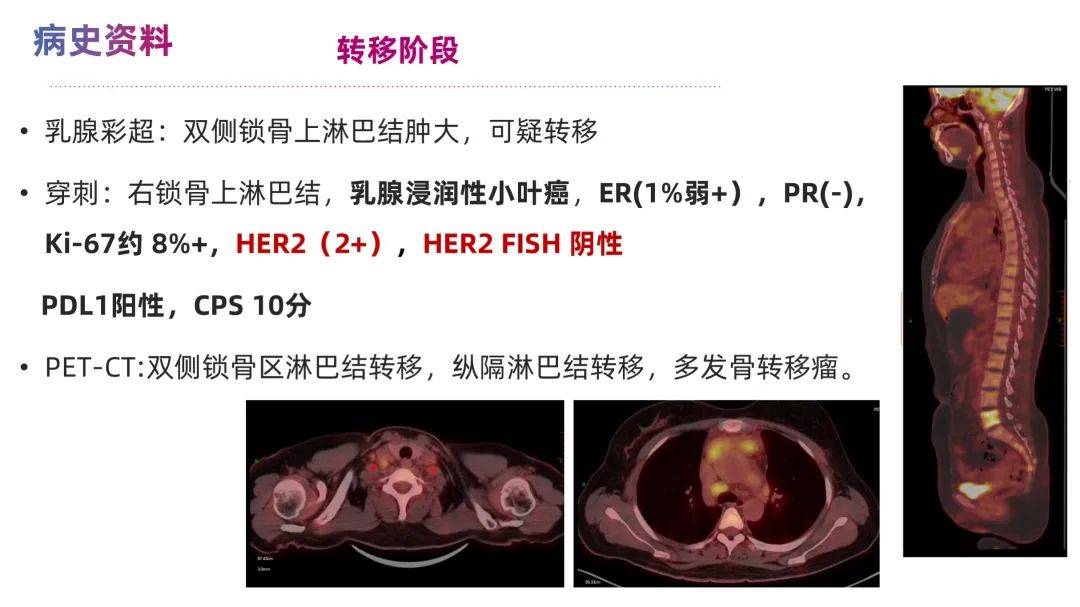
患者初诊为左乳浸润性小叶癌cT3N0M0 IIB期, LuminalB1型(HR阳性,HER2低表达)。

02
早期新辅助化疗+手术+术后辅助内分泌治疗
术后31个月,患者出现双侧锁骨上/纵隔淋巴结、骨转移,锁骨淋巴结活检显示分子类型由初始LuminalB1型转变为 三阴型(HR阴性、HER2低表达)。
左右滑动查看更多
03
晚期一线治疗
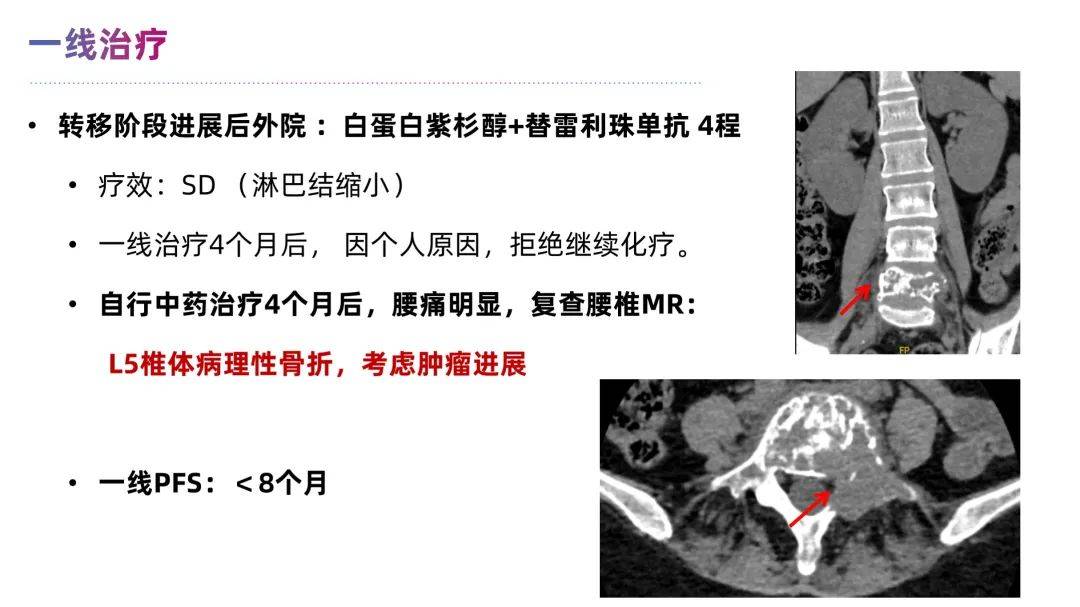
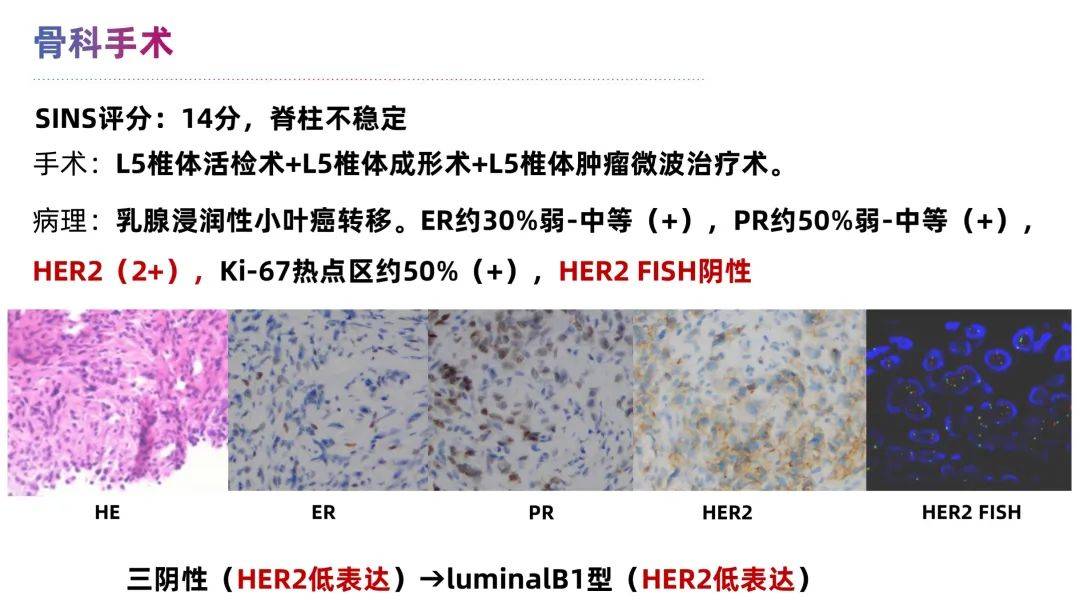
患者锁骨上淋巴结活检提示亚型转变为 三阴型乳腺癌,一线治疗接受白蛋白紫杉醇+替雷利珠单抗,4程后肿瘤缩小,但自行停药改为中药,后因骨转移进展导致腰椎病理性骨折,脊柱外科协助行椎体固定术。骨转移灶活检显示转变为 LuminalB1型(HR阳性、HER2低表达)。
左右滑动查看更多
04
晚期二线治疗
患者骨活检病理提示 激素受体转为阳性,CT提示 双侧胸腔中量积液和心包少量积液,多发淋巴结和骨转移。二线接受哌柏西利+戈舍瑞林+氟维司群治疗,1周后疾病快速进展,呼吸困难加重。复查彩超提示双侧胸腔大量积液,行胸腔积液引流术后呼吸困难症状缓解不明显,进一步行CT,提示 心包大量积液,并引发急性心包填塞。心血管内科参与多学科会诊,患者精神疲倦、端坐呼吸、呼吸浅速、面色苍白,诉腹胀,下肢水肿。查体:心率125次/分,R25次/分,BP102/81mmHg,SPO2 99%(中流量吸氧期间);颈静脉怒张,心率快,律齐,心音遥远,叩诊浊音界变宽,双下肺呼吸音减弱。另外因体循环淤血导致双肺水肿及肝功能损害(ALT:258U/L↑;AST:136U/L↑)。分析患者已存在明显心脏压塞相关症状及体征,需行心包积液穿刺引流缓解症状,遂转至心血管内科监护病房(CCU),实施心包积液穿刺引流术后患者症状显著改善,转氨酶水平逐渐降低,6天后ALT和AST恢复正常。 胸腔及心包积液细胞病理检查提示乳腺癌转移,亚型又转变为三阴型 (ER-,PR-, HER2 2+,FISH阴性)。

04
晚期三线方案考虑及疗效
患者病情危重,在完成局部治疗(心包穿刺术)后,需要尽快控制疾病。龚畅教授和曾银朵教授再次召集了MDT会诊对患者治疗过程、影像、病理分析及基因检测数据进行了详尽的分析与解读。
*MDT团队(乳腺外科;乳腺肿瘤内科;乳腺诊断专科;放射影像专科;乳腺放疗科;病理科;分子诊断专科,乳腺肿瘤遗传咨询)
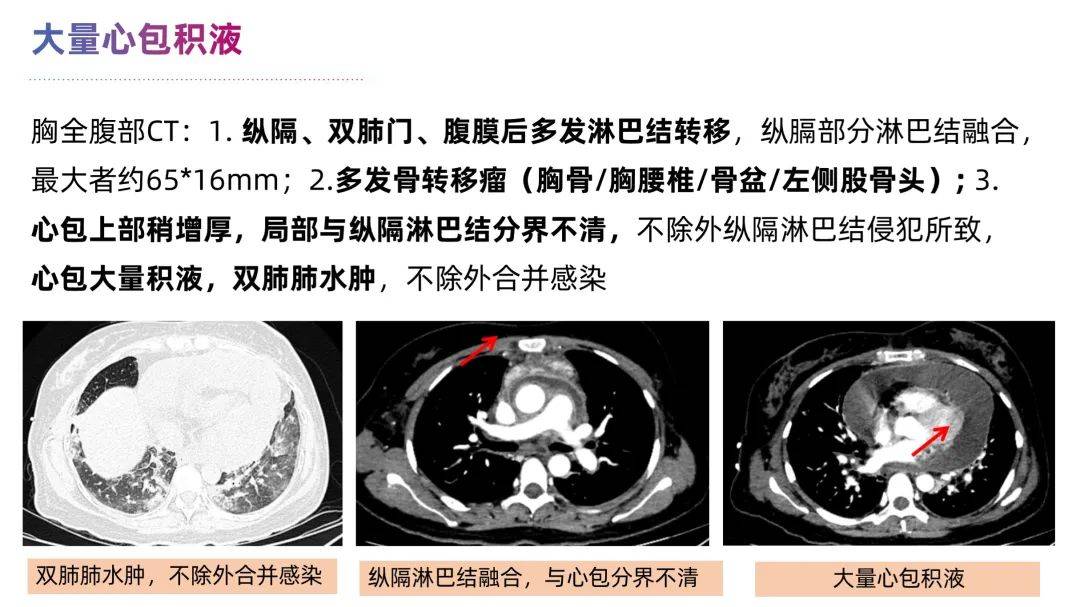
乳腺诊断专科和放射影像专科 :审阅CT影像显示,肿瘤负荷显著且分布广泛,累及纵隔、肺门及腹腔内多个淋巴结;胸膜和心包的受累导致了双侧大量胸腔积液和心包积液的生成,继而引起双肺肺水肿、肝脏灌注异常、glisson鞘水肿和胸腹部皮下水肿。此外,存在多处骨转移现象(胸骨、全脊柱、左侧股骨、骨盆),但目前承重骨稳定性尚可,未发现新的压缩性骨折。
病理科 :与浸润性导管癌(IDC)相比,浸润性小叶癌(ILC)患者的预后显著较差 [1] 。该病患者面临更高的复发和转移风险,且肿瘤更倾向于扩散至骨骼、胃肠道、子宫、脑膜、卵巢等部位,同时更易出现 弥漫性浆膜转移 。
分子诊断科和乳腺肿瘤遗传咨询 :鉴于患者BRCA基因检测结果未发现致病变异,目前尚无靶向药物治疗的明确指征,因此建议进行下一代测序(NGS)基因检测,以进一步探索可能的治疗靶点。
乳腺放疗科 :当前患者肿瘤转移广泛,针对骨转移灶已实施了固定手术,目前不具备放疗的适应症。
乳腺外科 和 乳腺内科 教授综合分析,患者为年轻女性,确诊为浸润性小叶癌,激素受体阳性型;尽管初次治疗时肿瘤分期较早,但不到三年内出现了复发和转移;一线治疗失败后,随后肿瘤迅速进展;在启动二线治疗仅数天后,胸腔积液和心包积液急剧增加,这一情况显著反映了肿瘤对治疗具有较强的耐药性。
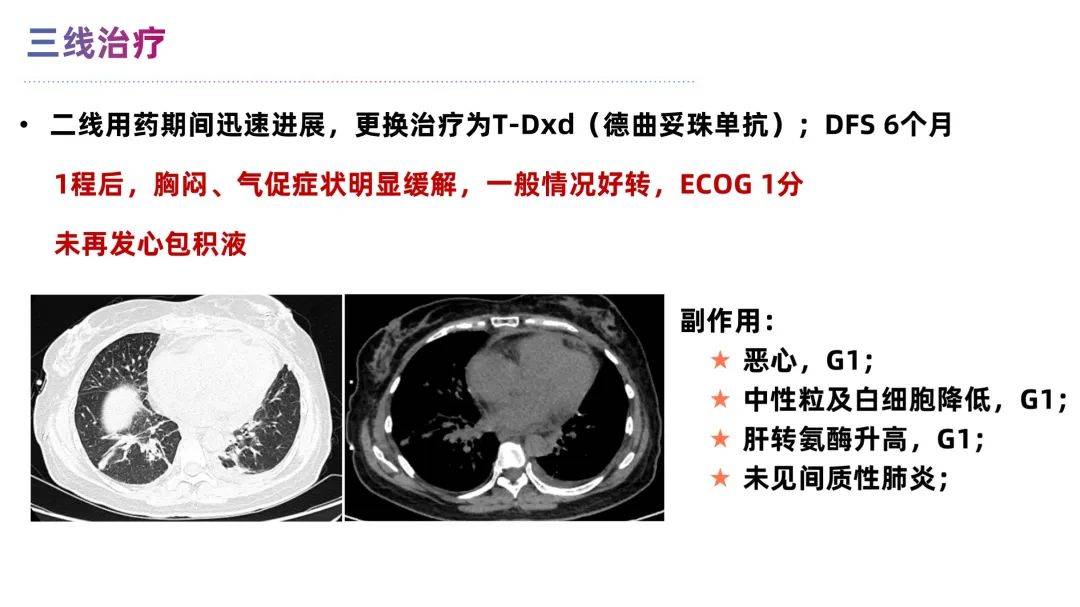
结合既往治疗反应及整体疾病进展情况,考虑到患者分子亚型存在空间和时间的异质性,激素受体表达发生多次转变,但HER2低表达几乎一致。结合DESTINY-Breast04研究结果 [2] ,对于在转移性疾病阶段接受过1-2线化疗的HER2低表达乳腺癌患者,使用德曲妥珠单抗(T-Dxd)中位PFS9.9个月,化疗组仅为5.1个月。建议优选靶向HER2-ADC治疗,但考虑到ECOG评分高,予减量使用抗HER2-ADC拟控制疾病发展。
2024年2月该患者首次接受T-Dxd 4.8mg/kg治疗。首次用药后3天后,患者症状迅速缓解,心包积液和胸腔积液明显减少,顺利出院回家过个团圆年。
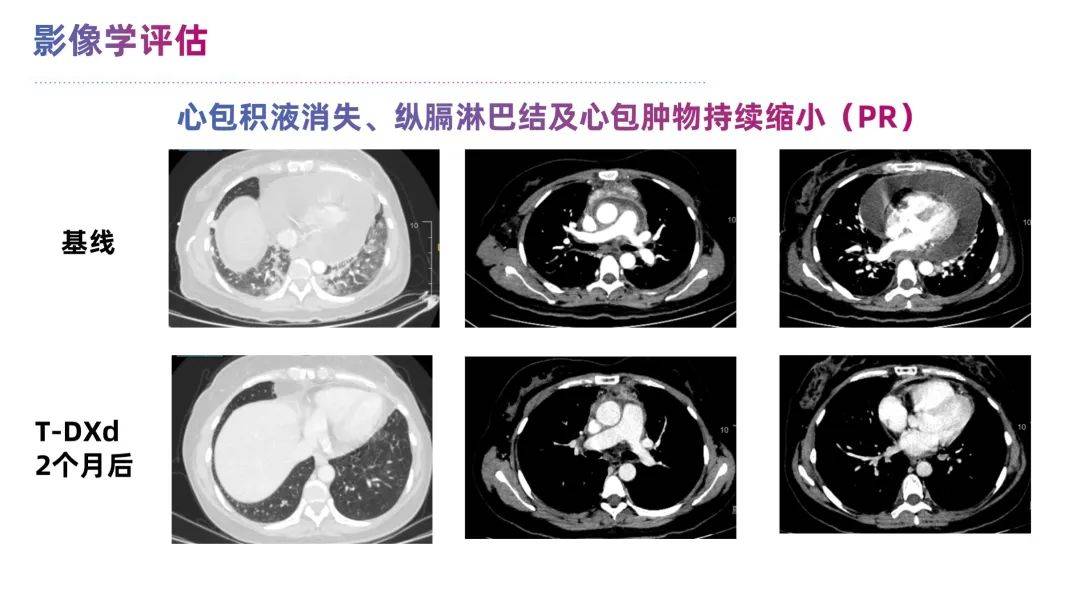
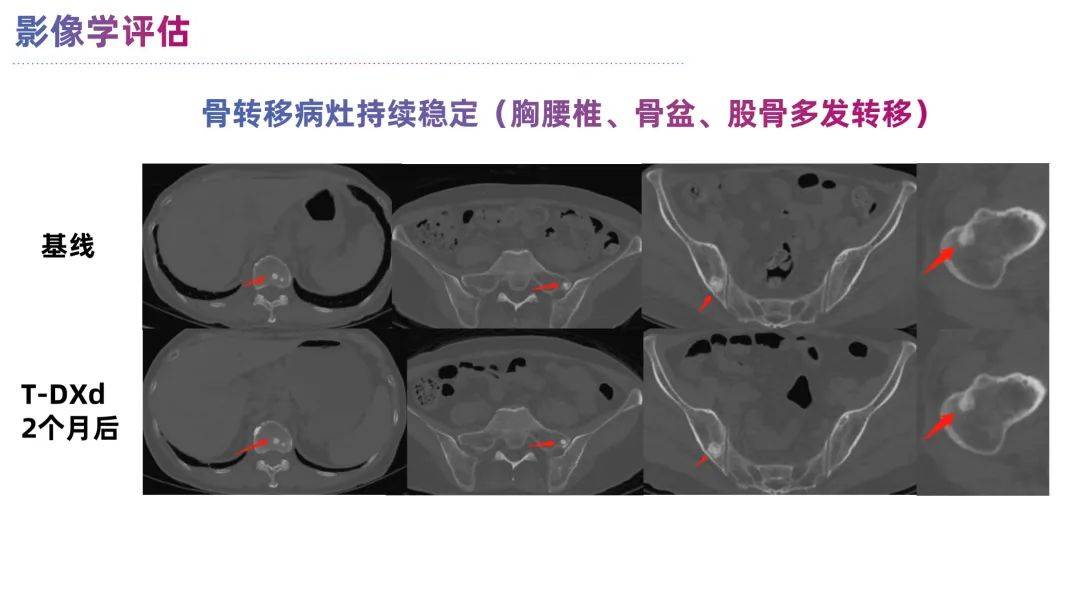
患者一般状态明显好转后,第二疗程剂量调整为5.4mg/kg直至2024年7月30日。CT复查疗效示持续的部分缓解(PR),并且骨转移病灶保持稳定,心包积液和胸腔积液控制佳。该治疗方案的无进展生存期(PFS)达6个月。
左右滑动查看更多
病例总结
专家点评
龚畅教授
中山大学孙逸仙纪念医院
在本案例中,患者是一位年轻女性,初诊为Luminal B1型(激素受体阳性,HER2低表达)的早期乳腺癌。在四年诊疗过程中,通过多次转移灶的活检发现, 激素受体状态呈现出显著的高度异质性 ,而HER2的检测结果始终保持在低表达水平 。根据其分子亚型和既往治疗情况,在晚期一线、二线治疗阶段,分别按照TNBC和HR+乳腺癌的指南推荐接受标准治疗,但是患者病情进展较为迅速,晚期一线PFS小于8个月,晚期二线PFS<1个月,尤其在晚期二线阶段 出现“致命”性的进展模式 ,患者双侧胸腔和心包均出现大量积液,并且 心包积液快速恶化,引发心包填塞,患者伴发气促、胸闷、憋喘等症状 ,情况危急,也极大地增加了救治难度。
曾银朵教授
中山大学孙逸仙纪念医院
既往报道中,恶性心包积液的肿瘤患者多采用化疗进行治疗,不良反应发生率较高,总体生存获益仍待进一步改善。根据《中国抗癌协会乳腺癌诊治指南与规范(2024年版)》 [3] ,对于HR+/HER2-晚期乳腺癌,即使存在内脏转移,伴或不伴有内脏危象,内分泌治疗联合CDK4/6抑制剂或内分泌治疗为基础的治疗仍然是优选的治疗方案。对于既往内分泌治疗失败或者判定不再适合内分泌治疗的患者,以及伴有内脏危象的患者,应该推荐化疗或者新型ADC药物。乳腺癌合并恶性心包积液可以被视为内脏危象,特别是在急性心包填塞导致显著心脏功能受损或患者出现症状的情况下。2023年ESMO乳腺癌指南 [4] 和2024年NCCN指南 [5] 指出,HR+/HER2-晚期乳腺癌合并内脏危象患者可以使用化疗,而对于既往CDK4/6抑制剂联合内分泌治疗快速进展或出现内脏危象的患者,可以使用新型ADC药物,如HER2低表达患者选择T-DXd。
龚畅教授
中山大学孙逸仙纪念医院
值得一提的是,恶性心包积液局部治疗尤为重要,包括心包穿刺术、心包腔内药物灌注(如细胞抑制剂或硬化剂)和心包开窗术 [6] 。既往研究表明,心包开窗术侵袭性相对较大,且对技术和患者耐受性要求高,通常作为不作为首选治疗 [7] 。心包穿刺和心包腔灌注药物是首选治疗 [8] 。尽管这种局部联合手段的有效率高达70%-90% [9] ,但是有效控制时间短、灌注药物容易引起心脏损害。对于乳腺癌合并恶性心包积液患者,采用局部与全身治疗相结合的模式显得尤为重要。这种综合治疗模式已被多个临床案例所证实,能够有效改善患者的生存预后 [10-13] 。因此,针对该例患者,有必要在局部治疗后,考虑尽快开始全身治疗以控制肿瘤的进展和转移,从而有效改善患者预后。
曾银朵教授
中山大学孙逸仙纪念医院
该案例患者既往经历两次内分泌治疗及一线化疗失败,在诊疗过程中病灶呈现 HR高度异质性且对标准治疗不佳,但HER2检测始终稳定为低表达状态 。综合指南推荐、研究证据等,T-DXd可考虑作为HER2低表达晚期乳腺癌伴有恶性心包积液局部治疗后的全身治疗联用方案,因考虑到患者的耐受情况, 遂从小剂量逐渐调整到足量 ,其疗效超出预期。仅经过1个疗程,患者因心包积液引起的胸闷和气促症状显著改善,整体状况得到提升,ECOG评分降至1分,且未再出现心包积液。治疗2个月后,患者的心包积液完全消失,纵膈淋巴结及心包肿物持续缩小,疗效评估达到PR。同时,骨转移病灶也保持稳定。鉴于既往尚未有合并恶性心包积液乳腺癌患者使用T-DXd作为全身解救治疗的病例报道,团队从真实世界角度,首次报告了T-DXd治疗HER2低表达乳腺癌合并恶性心包积液的内脏危象患者显著生存获益案例,具有重要的临床参考价值。
龚畅教授
中山大学孙逸仙纪念医院
T-DXd作为全身治疗方案,为发生心包填塞的HER2低表达的晚期乳腺癌患者带来了长达半年的生存质量提升和生存获益,实现了患者与家人共度春节的美好愿望,也更让患者满怀期待地迎接新一年的美好生活。逸仙乳腺肿瘤医院MDT团队,为每一位乳腺癌患者提供全程、全生命周期的最佳诊疗策略,为患者健康保健护航。
龚畅 教授
中山大学孙逸仙纪念医院 逸仙乳腺肿瘤医院
乳腺外科三级教授/二级主任医师 外科学博士 博士生导师
乳腺诊断专科主任 乳腺肿瘤中心第二职工党支部书记
中国抗癌协会乳腺癌整合防筛专委会常委 中国抗癌协会乳腺癌专委会委员 中国女医师协会乳腺专委会 常委 中国女医师协会临床肿瘤专委会 委员 广东省医师协会乳腺专科医师分会副主委 广东省精准医学应用分会癌症早筛早诊分会副主委 广东省抗癌协会癌症筛查与早诊早治专委会副主委 广东省临床医学学会泛家族遗传性肿瘤防控专委会副主委 广东省医学会乳腺病学分会常委 主持科技部国家重点研发计划(课题组长)1项、国家科技重大专项(课题组长)1项,国家自然科学基金7项,省部级基金7项。CSCO基金2项。入选科技部、教育部、广东省杰青等人才项目5项。主编人卫出版社专著《组织标记在乳腺疾病精准诊疗中的应用》。研究成果获广东省科技进步二等奖(第一完成人),并被中国年轻乳腺癌诊疗专家共识以及包括研究生教材《疾病学基础》《肿瘤学》在内的17本参与编写的专著引用。获专利10项,开发软件2项。以第一/通讯在Cancer Cell,Cell Reports Medicine,Medcomm,Molecular Cancer,Cancer Research,Advanced Science,Nature Communications 发表论文42篇,总引用2771次,高被引论文3篇。
曾银朵 教授
中山大学孙逸仙纪念医院 乳腺内科副主任医师
博士,硕士生导师
广东省胸部肿瘤防治研究会乳腺肿瘤内科专业委员会主任委员
广东省医疗行业协会乳腺专科管理分会常委
广东省医疗行业协会乳腺肿瘤内科管理分会常委
广东省胸部肿瘤防治研究会青年委员会常委
广东省胸部肿瘤防治研究会胸部肿瘤脑转移专业委员会委员
广东省临床医学学会泛家族遗传性肿瘤防控专业委员会常委
中国抗癌协会肿瘤分子医学专业委员会委员
主持国家自然科学基金青年基金1项
主持中山大学5010培育项目1项
主持逸仙临床研究培育项目1项
参加编写《临床肿瘤内科学》和《乳腺癌保乳治疗》
英国卡迪夫大学访问学者


















 苏公网安备32059002004080号
苏公网安备32059002004080号


