结直肠癌的发病率及病死率仍处于上升趋势,其中40%~50%的患者在初诊时已有远处转移,因此转移性结直肠癌(metastatic CRC,mCRC)的治疗尤为重要。对于一线、二线治疗后失败的mCRC患者,三线治疗除了选择参加临床研究,能够选择的治疗药物有瑞戈非尼、呋喹替尼、TAS-102、“西妥昔单抗再挑战”[1-5]等。指南推荐的三线治疗靶向药物和化疗药物疗效总体并不令人满意,客观缓解率仅为2%~5%,中位无进展生存期的延长不超过2个月,且不良反应发生率还是很高的。以上治疗都是在没有经过分子生物学指标检测筛选后得到的疗效,因此在极大程度上并不能反映目前肿瘤精准治疗的需求。此次分享一例后线转移性结直肠癌患者接受靶免化治疗的探索并获得良好疗效的病例。
患者基本信息和前线治疗情况
患者男性,55岁
【一线治疗】
2019-8-1肠梗阻起病。2019-8 PET-CT及肝穿刺确诊降结肠癌伴多发肝转移,RAS、BRAF野生型。2019-8至2019-10行西妥昔单抗联合FOLFOXIRI转化治疗4周期,疗效达PR。2019-11-8行肝转移灶切除及结肠癌根治术,术后病理:(结肠)腺癌,浸润浆膜下,神经束,脉管(+),残余瘤90%,淋巴结(0/14),癌结节1枚,(肝脏)腺癌(8灶)符合肠腺癌肝转移,RAS、BRAF野生型,pMMR。术后2019-12至2020-3行西妥昔单抗+FOLFOX治疗8周期,完成围手术期治疗停药。PFS 1=19个月
【二线治疗】
2020-7-2 CT提示:肝右叶复发灶可能。2020-7-27于我院行TACE术,术后未见肿瘤活性,2020-8-19起口服卡培他滨治疗至2020-12-22。PFS 2=5个月
【三线治疗】
2020-12-22 CT提示肝内转移灶进展。2020-12-22口服呋喹替尼至2021-5-10,期间联合肝病灶射频和TACE治疗。PFS 3=5个月
【四线治疗】
2021-7-29 MRI提示:肝内病灶增大,PD。2021-8至2021-11行贝伐珠单抗+FOLFIRI治疗。2021-12-10 CT提示肝内病灶部分增大。PFS 4=4.5个月
【五线治疗】
2022-3-8至2022-5-8参加HH30134项目,因肝功能异常停药。2022-5疾病进展出组。
2022-6行肝脏TACE+活检,病理:PD-L1(28-8)(肿瘤-,间质-);PD-L1(E1L3N)(肿瘤-,间质-);基因:KRAS、NRAS、BRAF未见突变。NGS(血液)二级:APC、TP53突变;TMB-H;MSS。NGS(组织):TMB-L;MSS,RAS、BARF野生型。PFS 5=2个月
治疗过程
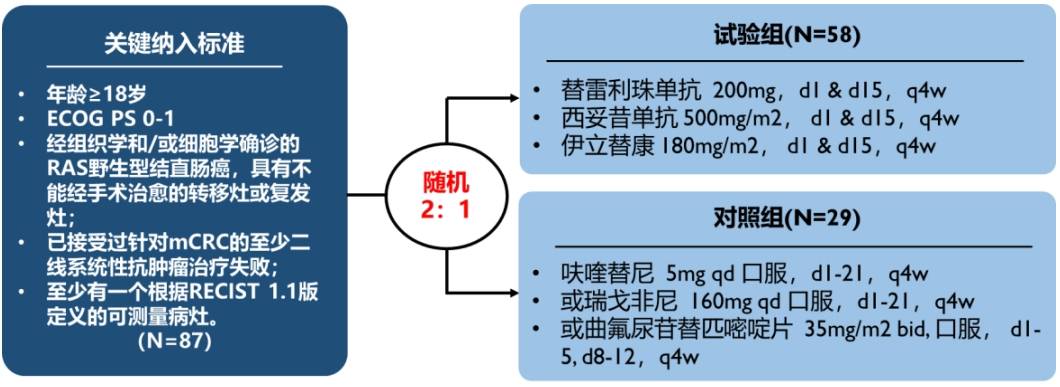
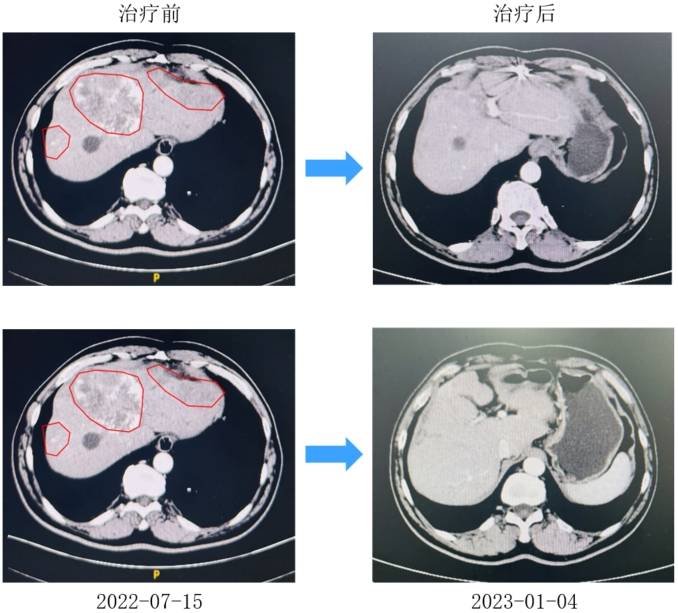
患者于2022-7参加“替雷利珠单抗联合西妥昔单抗和伊立替康对比研究者选择的三线方案治疗RAS野生型复发难治性转移性结直肠癌的多中心、随机、对照临床研究(BGB-A317-2009-IIT)”(即TEC2研究),随机至TEC组:接受替雷利珠单抗+西妥昔单抗+伊立替康治疗。最佳疗效达PR(缩小90%以上)。2023-6疾病进展,无进展生存期为11个月。治疗期间安全性可控(1级呕吐,1-2级皮疹)。
本期特邀专家——余一祎 教授
复旦大学附属中山医院肿瘤内科副主任医师
复旦大学附属中山医院临床医学研究院办公室主任
CSCO青年委员会委员
CSCO临床研究专委会委员
中国老年学和老年医学学会肿瘤康复分会精准医疗专家委员会副主任委员
中国抗癌协会肿瘤大数据与真实世界研究青委会委员
上海市抗癌协会肿瘤药物临床研究专委会委员
上海市药学会药物治疗专委会委员
本期特邀专家——徐晓晶 教授
复旦大学 肿瘤学 博士
复旦大学附属中山医院肿瘤内科 主治医师
主要从事胃肠道恶性肿瘤的基础和临床研究
发表学术论文20余篇,其中SCI收录10篇
主持国家自然科学基金1项
专家点评
大部分晚期结直肠癌(占 90%~95%)为微卫星稳定(MSS)或错配修复基因正常的患者(pMMR),这部分患者对于免疫检查点抑制剂单药治疗作用有限,通常被认为是免疫沙漠或免疫排斥型[6],因此需要联合其他药物(包括靶向药物、化疗药物等),通过对免疫微环境的调节,增强抗肿瘤活性。临床前实验数据显示,西妥昔单抗阻断EGFR通路可以调节免疫浸润,进而激活免疫系统的抗肿瘤活性[7,8]。肿瘤微环境中髓样细胞的EGFR表达通过产生免疫调节因子(如白介素 6)促进肿瘤的发生和发展[9]。西妥昔单抗可通过刺激肿瘤抗原呈递给 T 细胞来促进树突状细胞对人结肠癌细胞的调节作用和吞噬作用,因此能够潜在地激活免疫应答[10]。同时可以诱导自然杀伤细胞介导的抗体依赖性细胞毒性作用[11,12]。
基于此我们中心开展了一项“替雷利珠单抗联合西妥昔单抗和伊立替康治疗RAS野生型复发难治性MSS型mCRC的探索性研究”, 2021-2至2021-9共纳入35例受试者,2例患者因个人原因撤回知情同意。对研究中的33例受试者进行了疗效评估:确认后的ORR为33.3%,DCR为78.8%。中位PFS 7.3个月,6个月PFS率为60%;中位OS 17.4个月,1年OS率为85%。33例接受治疗的受试者中,32例(97.0%)发生治疗相关不良反应,3例(9.1%)发生3级或以上不良反应,包括1例皮疹和2例中性粒细胞减少,疗效高且总体不良反应可控[13]。
在此基础上为了进一步验证此方案的有效性,我们中心牵头开展了“替雷利珠单抗联合西妥昔单抗和伊立替康对比研究者选择的三线方案治疗RAS野生型复发难治性转移性结直肠癌的多中心、随机、对照临床研究”。这一例多线治疗后的晚期结肠癌患者,在入组此研究前再次活检提示RAS、BRAF仍为野生型,在接受TEC方案的治疗后,肿瘤达到深度缓解,总体安全性良好,未出现非预期不良事件。并且在6线治疗时取得了11个月的无疾病进展生存。本案例充分体现了免疫检查点抑制剂与靶向药物联合治疗的效果。
[1] Grothey A, Van Cutsem E, Sobrero A, et al. Regorafenib monotherapy for previously treated metastatic colorectal cancer (CORRECT): An international, multicentre, randomised, placebo-controlled, phase 3 trial[J]. LANCET. 2013,381(9863):303-312.
[2] Li J, Qin S, Xu R, et al. Regorafenib plus best supportive care versus placebo plus best supportive care in Asian patients with previously treated metastatic colorectal cancer (CONCUR): A randomised, double-blind, placebo-controlled, phase 3 trial[J]. LANCET ONCOL. 2015,16(6):619-629.
[3] Li J, Qin S, Xu RH, et al. Effect of fruquintinib vs placebo on overall survival in patients with previously treated metastatic colorectal cancer: The FRESCO randomized clinical trial[J]. JAMA. 2018,319(24): 2486-2496.
[4] Xu J, Kim TW, Shen L, et al. Results of a randomized, Double-Blind, Placebo-Controlled, phase III trial of Trifluridine/Tipiracil (TAS-102) monotherapy in asian patients with previously treated metastatic colorectal cancer: The TERRA study[J]. J CLIN ONCOL. 2018,36(4):350-358.
[5] Cremolini C, Rossini D, Dell'Aquila E, et al. Rechallenge for patients with RAS and BRAF Wild-Type metastatic colorectal cancer with acquired resistance to first-line cetuximab and irinotecan: A phase 2 Single-Arm clinical trial[J]. JAMA ONCOL. 2019,5(3):343-350.
[6] Dawood S. The evolving role of immune oncology in colorectal cancer[J]. Chin Clin Oncol. 2018,7(2): 17.
[7] Ferris RL, Lenz HJ, Trotta AM, et al. Rationale for combination of therapeutic antibodies targeting tumor cells and immune checkpoint receptors: Harnessing innate and adaptive immunity through IgG1 isotype immune effector stimulation[J]. CANCER TREAT REV. 2018,63:48-60.
[8] Srivatsa S, Paul MC, Cardone C, et al. EGFR in Tumor-Associated myeloid cells promote development of colorectal cancer in mice and associates with outcomes of patients[J]. GASTROENTEROLOGY. 2017,153(1):178-190.
[9] Bokemeyer C, Van Cutsem E, Rougier P, et al. Addition of cetuximab to chemotherapy as first-line treatment for KRAS wild-type metastatic colorectal cancer: Pooled analysis of the CRYSTAL and OPUS randomised clinical trials[J]. EUR J CANCER. 2012,48(10):1466-1475.
[10] Botta C, Bestoso E, Apollinari S, et al. Immune-modulating effects of the newest cetuximab-based chemoimmunotherapy regimen in advanced colorectal cancer patients[J]. J IMMUNOTHER. 2012,35(5):440-447.
[11] Klausz K, Berger S, Lammerts VBJ, et al. Complement-mediated tumor-specific cell lysis by antibody combinations targeting epidermal growth factor receptor (EGFR) and its variant III (EGFRvIII)[J]. CANCER SCI. 2011,102(10):1761-1768.
[12] Dechant M, Weisner W, Berger S, et al. Complement-dependent tumor cell lysis triggered by combinations of epidermal growth factor receptor antibodies[J]. CANCER RES. 2008,68(13) :4998- 5003.
[13] Xiaojing Xu, Luoyan Ai,KeshuHu,et al. Tislelizumab plus cetuximab and irinotecan in refractory microsatellite stable and RAS wild-type metastatic colorectal cancer: a single-arm phase 2 study[J]. Nat Commun 15, 7255.
排版编辑:肿瘤资讯-高惠
下期预告
初始不可手术食管鳞癌患者经化疗联合免疫治疗获得手术机会并达到pCR











 苏公网安备32059002004080号
苏公网安备32059002004080号


