肝胆恶性肿瘤起病隐匿,侵袭性强,发现时多为晚期,预后极差,是我国发病率高、致死率高的恶性肿瘤。在肿瘤精准治疗观念下,免疫联合化疗/靶向治疗将成为肝胆恶性肿瘤的未来主要发展趋势。肝癌方面,EMERALD-1 研究谱写了TACE联合靶向+免疫的传奇;胆道癌方面,TOPAZ-1研究作为全球首个也是唯一一个获得三阳结果(OS、PFS、ORR)的III期研究,开启了免疫一线治疗的新篇章。
度伐利尤单抗联合化疗快速起效,TTR仅1.6个月,相较单纯化疗,ORR提升43%,且显著延长了患者的无进展生存(PFS)与总生存(OS),降低26%的死亡风险(HR 0.74),3年OS率翻倍,高达14.6%[1-2],实现全面生存获益。
《例例非凡》——肝胆肿瘤临床病例解析,将从不同视角提升临床思维,促进专业学术及临床经验分享。
本期由华中科技大学同济医学院附属同济医院肝脏外科中心黄志勇教授诊疗团队分享了1例晚期肝细胞癌综合治疗病例:患者男性,45岁,确诊为肝细胞癌(CNLC-Ia期,BCLC-A期)及乙型病毒性肝炎。患者接受手术切除后,进行了抗乙肝病毒、靶向联合PD-1单抗辅助治疗及预防性TACE治疗。然而,在后续随访中出现了肿瘤复发,AFP、PIVKA升高,影像学提示肝内多发实质性病灶。经MDT讨论,决定调整治疗方案为STRIDE方案(度伐利尤单抗+替西木单抗)联合局部TACE 及抗病毒治疗。调整治疗方案后,AFP下降并持续维持在较低水平,影像学复查结果提示肿瘤得到有效控制。
病例介绍
华中科技大学附属同济医院肝脏外科
外科学博士,副主任医师
国际肝胆胰协会/亚太肝胆胰协会会员
中国抗癌协会肝癌专业委员会委员
中国民族医药学会外科分会理事
中华志愿者协会中西医结合专委会委员
湖北省抗癌协会肝癌专业委员会委员
湖北省医学会普通外科分会转化医学与实验外科学组委员兼秘书
以第一作者或者通讯作者发表SCI论文34篇。
主持国家自然科学基金1项,参与国家自然科学基金及重大专项共6项,担任Frontiers in Immunology杂志编委,专刊客座主编。参编专著1部。
基本情况
患者,男性,45岁。
主诉:因“肝癌TAE术后1月余”于2022-11-07入院。
现病史:患者2022年10月6日因肝癌破裂出血于外院行急诊TAE,术后恢复顺利出院。2022-10-26外院腹部CT:肝内多发散在高密度碘油沉积影,肝尾状叶高密度致密碘油沉积影,考虑介入术后改变。2022-10-27腹部MRI:肝内多发异常信号影,考虑肝癌介入术后改变。今为求进一步治疗来我院就诊。
既往史:乙肝病史30余年。2007年因直肠脱垂行“直肠悬吊固定术”。否认其他疾病。
辅助检查
2022-11-07入院检查:Child-Pugh A级,AFP 2794.00ng/ml,乙肝DNA<1.0×102IU/mL,肝功能、凝血功能均正常范围,ICGR15 5.4%,无脾功能亢进,胃镜未见异常。
2022-11-14MRI增强:肝尾叶占位(3.3*3.0cm),考虑肿瘤性病变合并治疗后改变;肝左叶异常信号,鉴别于治疗后改变或其他小占位性病变所致(图1)。肺部CT未见明显异常。
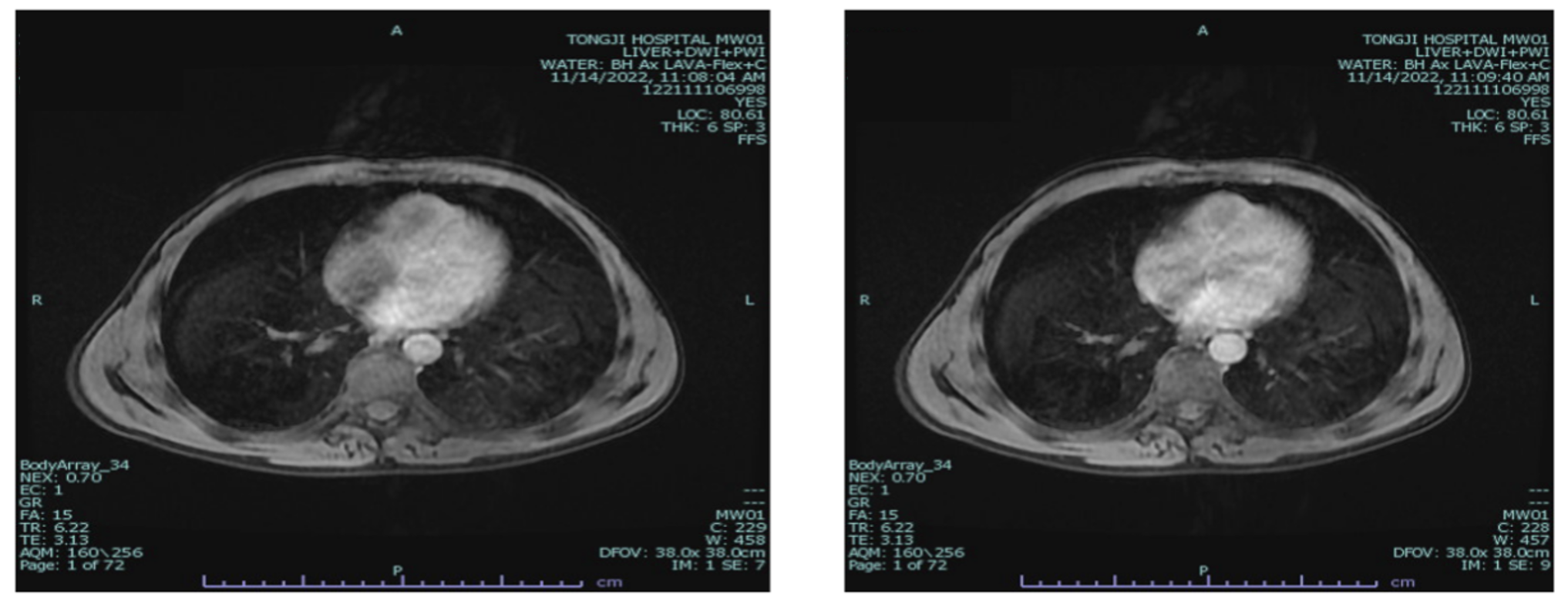 图1 2022-11 MRI增强
图1 2022-11 MRI增强
诊断
肝细胞癌(CNLC-Ia期,BCLC-A期)
乙型病毒性肝炎
治疗经过
2022-11-17行肝尾状叶部分切除+2段部分切除+4段部分切除+腹腔灌注化疗术。
术后行抗乙肝病毒治疗+仑伐替尼(2022-12-22)+PD-1单抗(替雷利珠单抗)治疗(2022-11-24),每3个月复查肝胆超声、甲胎蛋白(AFP)、肝功能。
2023-01-10第一次复诊后行预防性经皮动脉化疗栓塞术(TACE),术后CT平扫见肝内多发结节状、条片状、线状高密度影(图2)。继续行仑伐替尼+替雷利珠单抗治疗。
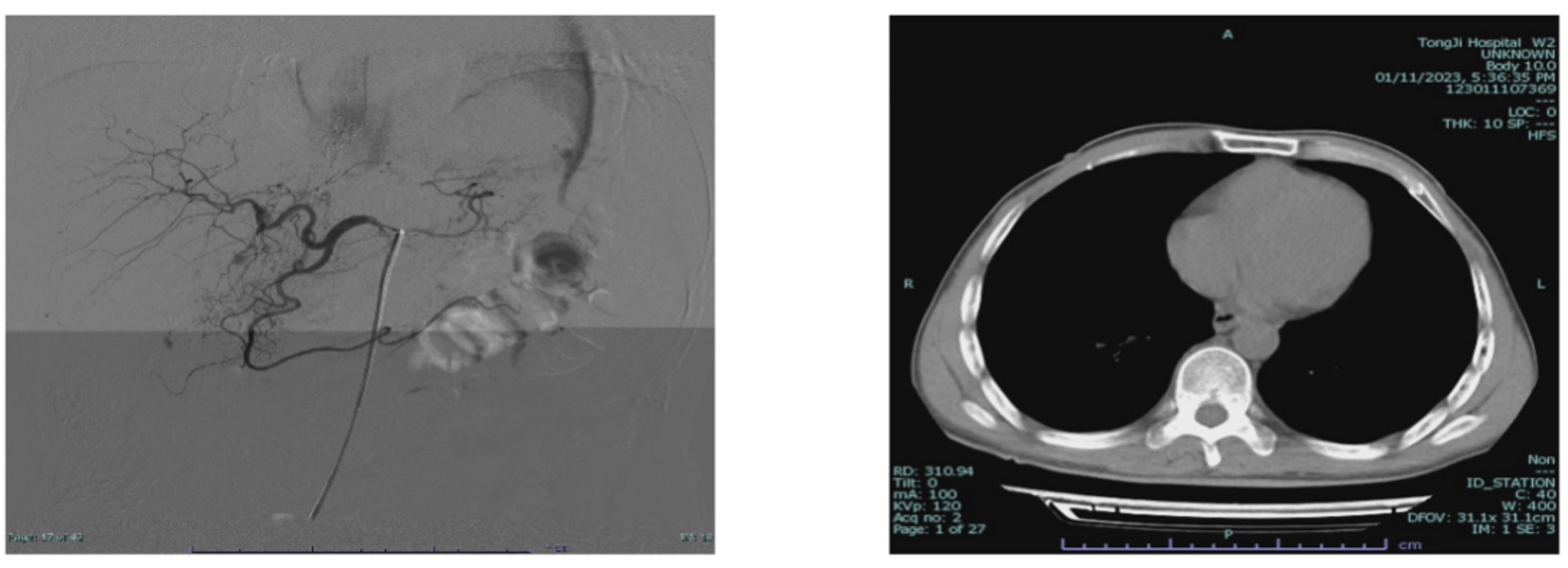 图2 2023-01预防性TACE(左)和术后CT平扫(右)
图2 2023-01预防性TACE(左)和术后CT平扫(右)
2023-06-25第二次复诊后再次行TACE,动脉造影见肝内多发小片状异常染色,考虑肿瘤性病变,术后行CT平扫见肝脏异常高密度灶,较前2023-01-11减少(图3)。
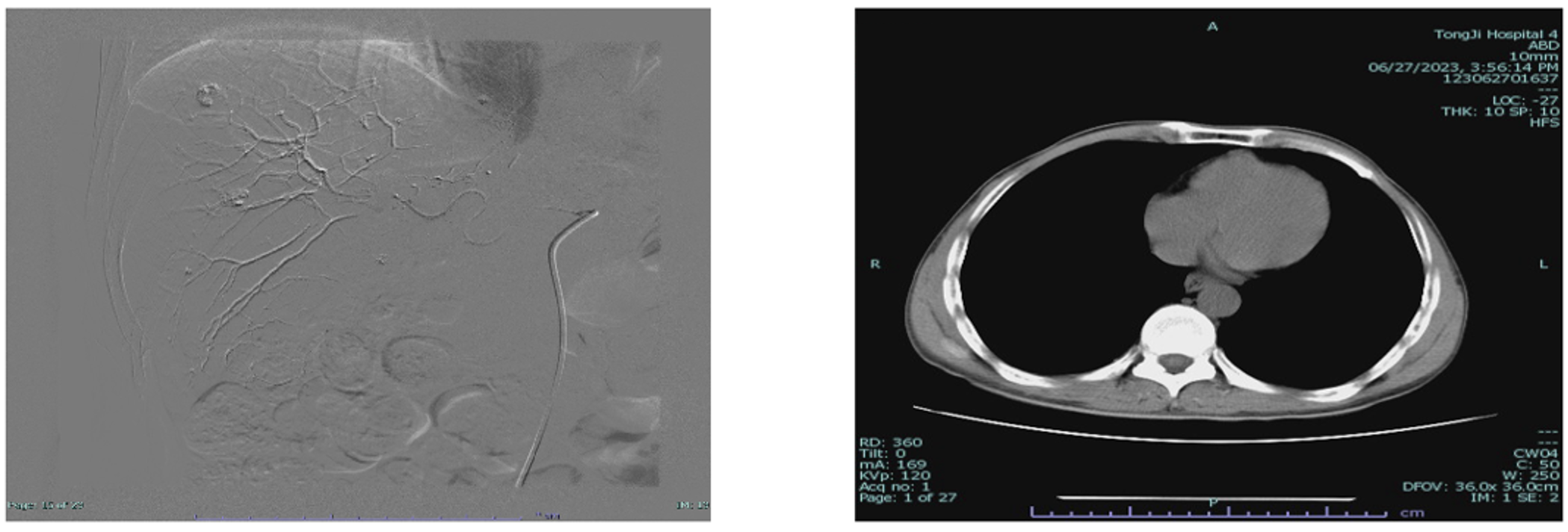 图3 2023-06 TACE(左)和术后CT平扫(右)
图3 2023-06 TACE(左)和术后CT平扫(右)
2023-07-04肝功能恢复后经MDT讨论行STRIDE方案(度伐利尤单抗+替西木单抗)联合局部和抗病毒治疗。
2023-10-09第三次复诊后再次行TACE,术后CT平扫见肝脏异常高密度灶,较前2023-06-27明显增多,多为治疗后改变(图4)。
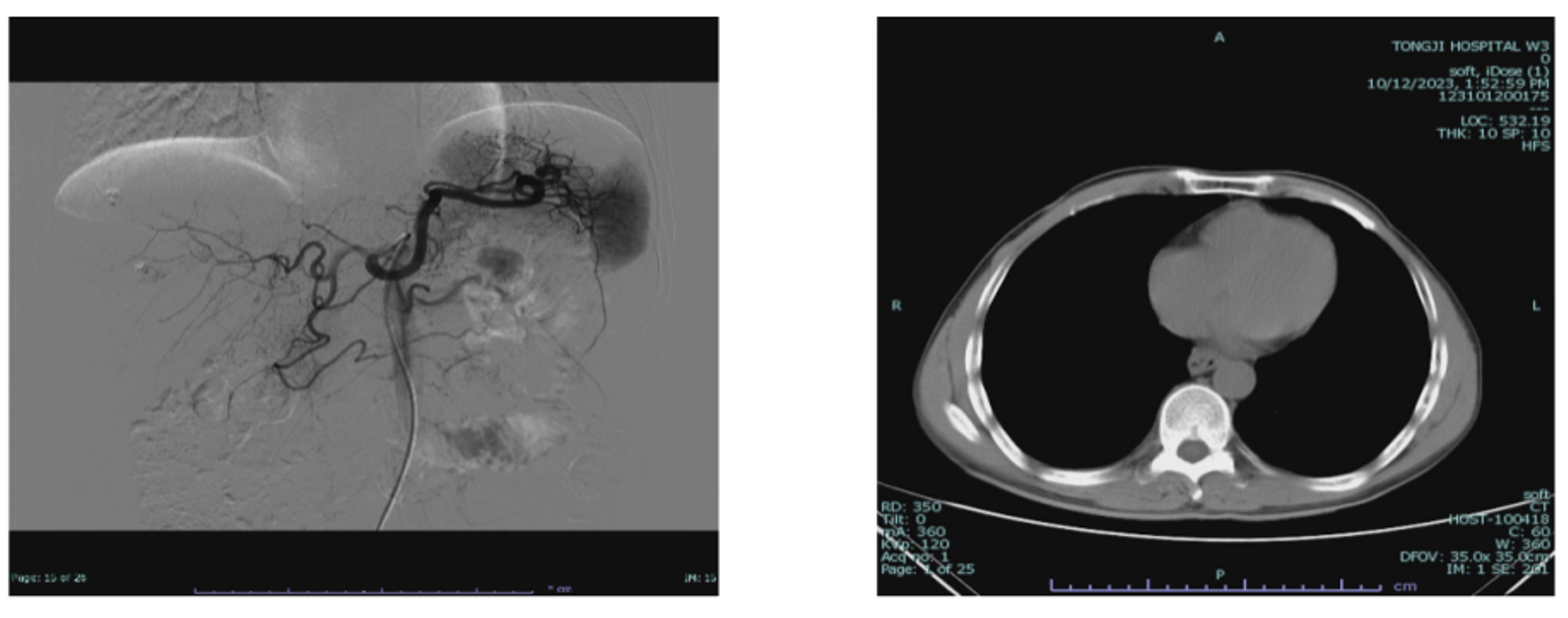 图4 2023-10 TACE(左)和术后CT平扫(右)
图4 2023-10 TACE(左)和术后CT平扫(右)
复查结果及疗效评估
2022-11-17术后病理检查:1.(肝尾状叶)肝细胞癌(低分化,团块状生长)伴坏死;(脉管侵犯,或发生于远癌旁肝组织;未见周围神经侵犯;肿块周围淋巴结1枚,镜下未见癌。
免疫组化:Hepatocyte(+),Glypican-3(+),Arginase-1(+),AFP(散在+),GS(散在+),CD34(血窦+),EGFR (+),B-catenin(+),CD8(散在+),CK19(-),EMA(-),CK7(-),Her-2(0,阳性对照+),Ki-67(约35%)。2.(肝II段、肝III段、肝IV段)送检结节均全取制片,镜下为纤维包裹凝固性坏死,未见明确肿瘤细胞,结节周围肝组织呈结节性肝硬化改变。
2023-01-08第一次复诊。AFP 7.90ng/ml,PIVKA 15.82mAu/mL。
2023-06-19第二次复诊。发现AFP明显升高(183.30ng/ml↑),PIVKA 35.97mAu/mL。彩超检查提示:肝内多发实质性病灶(性质待定)。
2023-07-22经STRIDE方案(度伐利尤单抗+替西木单抗)联合局部治疗后复查,AFP 17.51 ng/ml。
2023-09-26于外院复查行MRI:肝左内叶、右前叶上段及下段多发结节伴异常强化;最大者位于右前叶下段约1.6*2.3cm(图5)。
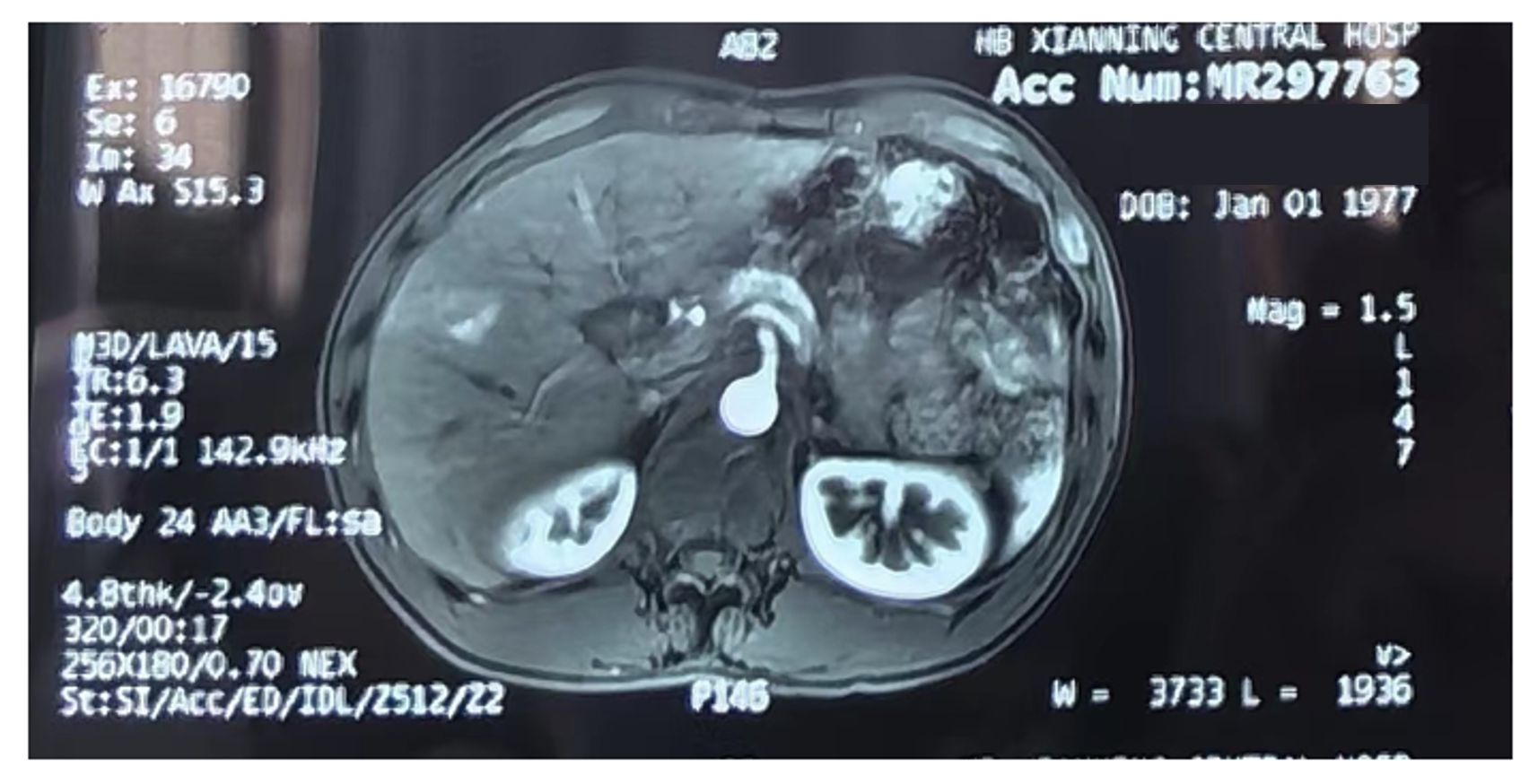 图5 2023-09外院MRI
图5 2023-09外院MRI
2023-10-09第三次复诊。AFP 60.05ng/ml,PIVKA:18.12mAu/mL。
2023-12-19复查发现,AFP 3.33ng/ml,PIVKA 14.05mAu/mL。
2023-12-20行MRI:肝左内叶、右前叶上段及下段多发结节伴异常强化,较前片(2023-09-26)肝右叶前下段稍增大,最大病灶1.6*2.3cm,其余病灶缩小(图6)。
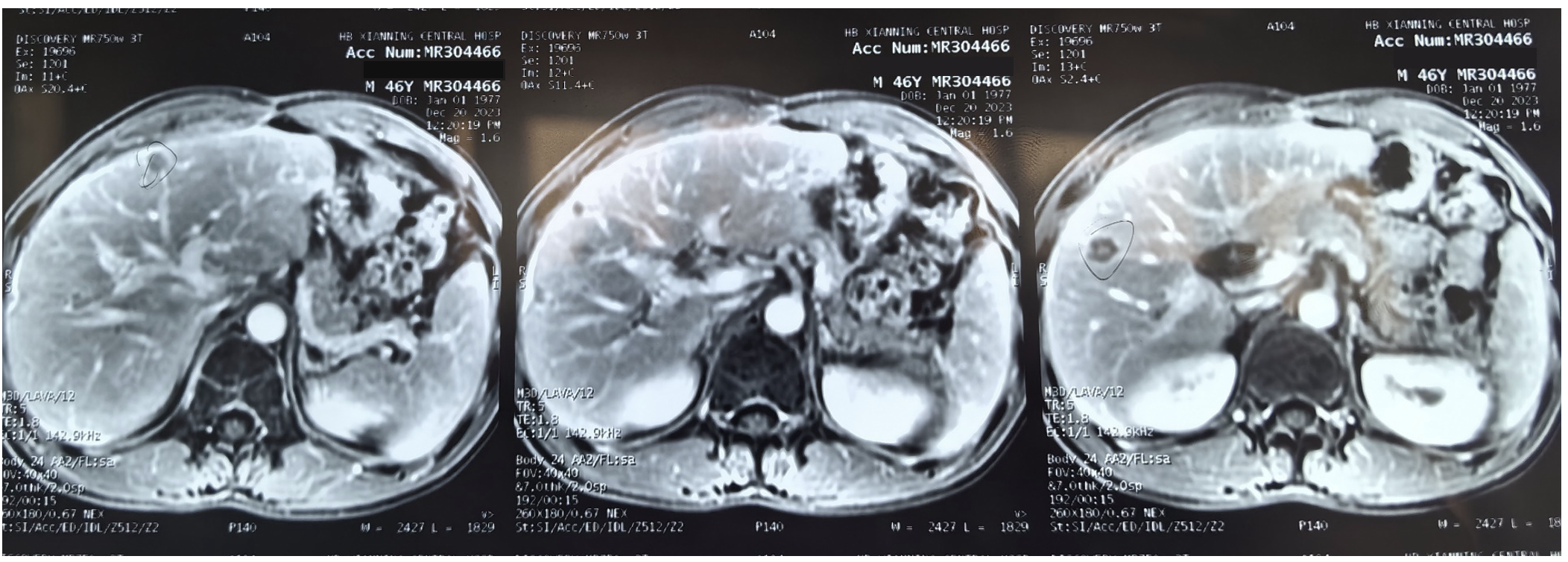 图6 2023-12 MRI
图6 2023-12 MRI
2024-04-08第四次复诊。行MRI:1.肝肿瘤综合治疗后改变;2.肝多发异常异常结节,较大者直径约14mm,考虑转移治疗后改变(图7)。
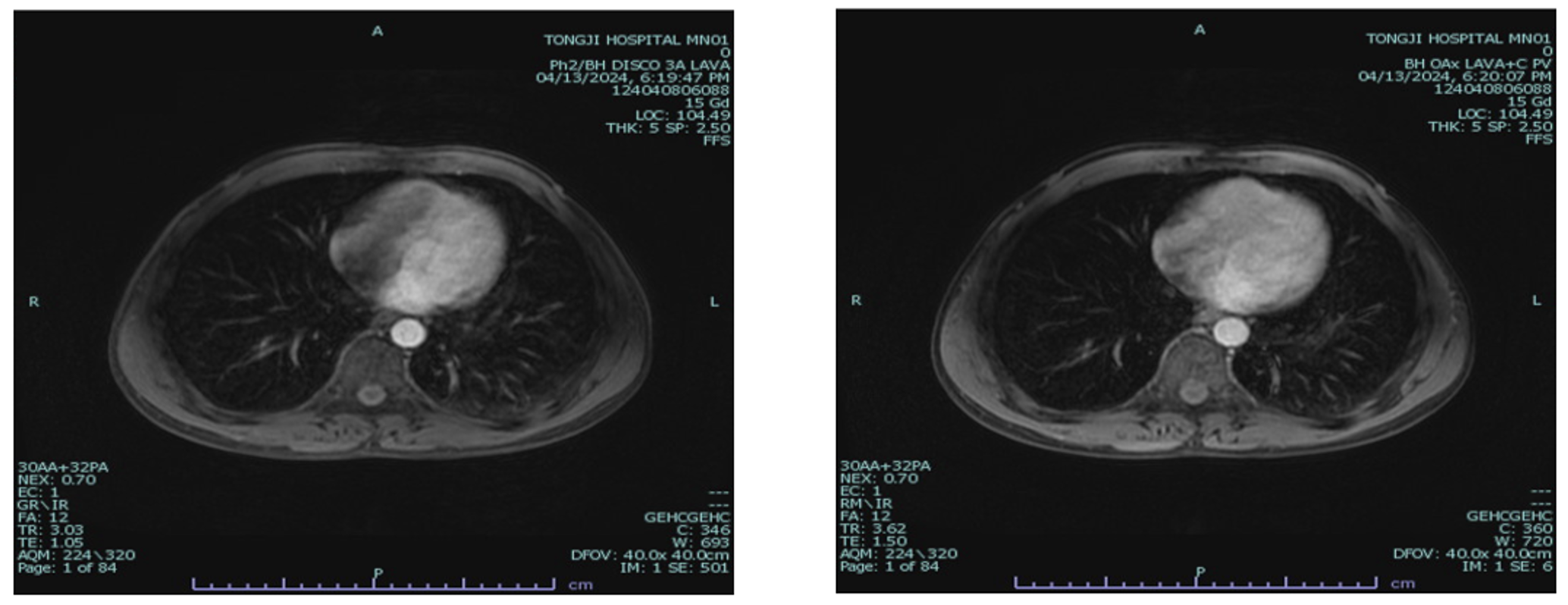 图7 2024-04 MRI
图7 2024-04 MRI
治疗过程中AFP变化趋势见图8。
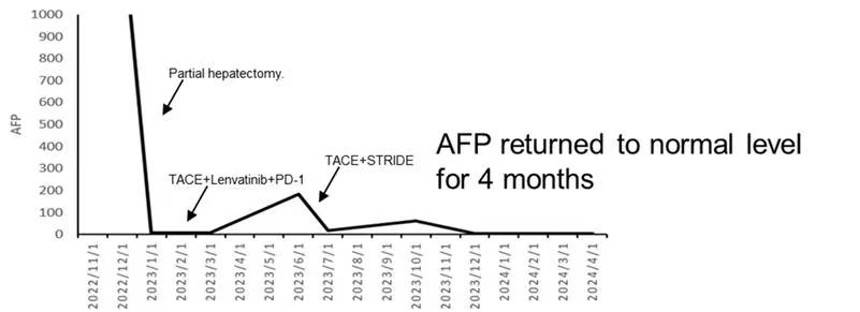
图8 AFP变化趋势
病例点评
华中科技大学附属同济医院肝脏外科中心
二级教授、主任医师、博士生导师;普外科副主任
亚太肝胆胰协会(A-PHPBA)候任主席
国际肝胆胰协会(IHPBA)理事
国际肝胆胰协会中国分会副主任委员兼秘书长
国际肝胆胰协会中国分会胆道肿瘤专委会主任委员
中国医师协会胆道外科专家工作组名誉组长
中国抗癌协会肝癌专业委员会常务委员
国家癌症中心肿瘤质控中心肝癌质控委员会委员
湖北省抗癌协会肝癌专委会副主任委员兼秘书长
Oncology and Translational Medicine 副主编
临床外科杂志副总编辑
入选2023年“国之名医•卓越建树”榜
获新世纪人才支持计划奖
肝癌作为我国常见的消化系统恶性肿瘤之一,疾病负担沉重。根据国家癌症中心发布的2022年中国恶性肿瘤疾病负担情况,肝癌新发病例在所有恶性肿瘤中排名第4,死亡病例排名第2[3],凸显了肝癌治疗的严峻性和复杂性。外科治疗是肝癌患者获得长期生存甚至治愈的重要手段,但术后5年复发转移率高达50%~70%,无疑增加了治疗的挑战性。
本病例患者为45岁男性,既往有30余年乙肝病史,经过详细的辅助检查,被诊断为肝细胞癌(CNLC-Ia期,BCLC-A期)及乙型病毒性肝炎。入院后MRI增强提示肝尾状叶占位,考虑肿瘤性病变合并治疗后改变。患者Child-Pugh肝功能分级为A级,AFP显著升高(2794.00ng/ml),根据《BCLC肝癌分期诊疗指南(2022版)》和《原发性肝癌诊疗指南(2024版)》[4-5]的推荐意见,患者接受了肝尾状叶切除术。术后病理结果证实了肝尾状叶肝细胞癌(低分化),并伴脉管侵犯,属于高危复发因素。根据《肝癌术后辅助治疗中国专家共识(2023版)》[6],推荐术后行靶向药物、免疫检查点抑制剂单药或联合应用以降低复发风险。患者术后接受了抗乙肝病毒治疗、仑伐替尼联合PD-1单抗替雷利珠单抗治疗,并辅以预防性TACE。在后续的随访中,根据病情变化调整了治疗方案。术后第一次复诊时,AFP、PIVKA均明显下降,提示治疗有效。但第二次复诊时,AFP出现明显升高,PIVKA也有所上升,影像学检查提示肝内多发实质性病灶(性质待定),考虑肿瘤复发。
国际多中心、开放标签、随机对照III期临床研究HIMALAYA证实了STRIDE方案(雷管方案,度伐利尤单抗+曲美木单抗)相较索拉非尼一线治疗不可切除肝细胞癌(HCC)的显著生存优势。2023WCGIC大会上公布了4年OS数据,中位随访时间延长至49.12个月,STRIDE组4年OS率达到25.2%,约四分之一人群可以活过4年,相较于索拉非尼组提升66.7%[7],充分体现STRIDE方案的长拖尾效应。2023ASCO年会上中国学者开展的一项前瞻性、单臂、单中心II期研究发现,TACE+SBRT后序贯STRIDE方案治疗局部晚期不可切除HCC患者,客观缓解率(ORR)高达81.3%,完全缓解(CR)率为43.8%[8]。这些临床研究数据为TACE联合STRIDE方案的临床应用提供了重要的循证医学证据。经MDT讨论,患者肝功能恢复后决定调整治疗方案为STRIDE方案(度伐利尤单抗+替西木单抗)联合局部TACE 及抗病毒治疗。经治疗,患者的AFP下降并持续维持在较低水平,治疗5个周期获得PR,且无疾病进展已超过10+个月,提示该联合方案对此患者有效。值得关注的是,国际多中心、开放标签、随机对照III期EMERALD-3研究评估了STRIDE方案±仑伐替尼+TACE对比单纯TACE治疗局灶性HCC的疗效和安全性。该研究的主要终点为A组(STRIDE+仑伐替尼+TACE)与C组(仅TACE)的PFS,其他终点包括B组(STRIDE+TACE)与C组的PFS、OS、与健康相关的生活质量和安全性[9]。目前研究正在进行中,期待未来这项研究的结果为STRIDE方案联合TACE治疗HCC提供更高级别依据。
总体来看,该病例的诊疗过程带来以下启示:早期肝癌术后复发风险高,需要警惕并积极进行术后辅助治疗;STRIDE方案联合局部为接受局部联合靶免治疗进展的肝癌患者提供了有效治疗选择,能带来明显临床获益;在治疗过程中,需要根据肝癌患者的个体情况制定合适的治疗方案,并进行动态监测和密切随访,及时调整治疗策略,以期获得最佳治疗效果。
[1] Do-Youn Oh, et al. A phase 3 randomized, double-blind, placebo-controlled study of durvalumab in combination with gemcitabine plus cisplatin (GemCis) in patients (pts) with advanced biliary tract cancer (BTC): TOPAZ-1. 2022 ASCO GI, Abstract #378.
[2] https://www.astrazeneca.com/media-centre/press-releases/2024/imfinzi-plus-chemotherapy-doubled-overall-survival-rate-at-three-years-for-patients-with-advanced-biliary-tract-cancer-in-topaz-1-phase-iii-trial.html.
[3] 郑荣寿, 陈茹, 韩冰峰, 等. 2022年中国恶性肿瘤流行情况分析[J]. 中华肿瘤杂志, 2024, 46(3):221-231.
[4]《BCLC肝癌分期诊疗指南(2022版)》.
[5]《原发性肝癌诊疗指南(2024版)》.
[6]《肝癌术后辅助治疗中国专家共识(2023版)》.
[7] Abou-Alfa, et al. 2023WCGIC, Abstract SO-15.
[8] 2023 ASCO, Abstract 4124.
[9] G.K. Abou-Alfa, et al. 2022 ESMO, Abstract 727TiP.
排版编辑:肿瘤资讯-Chloe











 苏公网安备32059002004080号
苏公网安备32059002004080号


