复发/难治性(R/R)中枢神经系统淋巴瘤(CNSL)患者预后极差,中位总生存期(OS)仅为4个月。近年来,嵌合抗原受体(CAR)T细胞疗法彻底改变了R/R 大B细胞淋巴瘤(LBCL)的治疗格局。然而,该疗法在CNSL中的临床应用仍有限,尤其是在亚洲患者中。瑞基奥仑赛注射液(Relmacabtagene autoeucel,relma-cel)已在关键性Reliance研究中已展现出较高的持久缓解率及可控的安全性。基于这些积极的研究结果,瑞基奥仑赛已在中国获批上市,用于治疗R/R LBCL患者。然而,目前尚无瑞基奥仑赛的真实世界数据,尤其是对中枢神经系统(CNS)受累的患者。
基于此,上海交通大学医学院附属瑞金医院糜坚青教授及其团队开展了一项多中心回顾性研究,分析了国内12家中心接受瑞基奥仑赛治疗的R/R CNSL患者的真实世界数据。据悉,这是迄今第一项,也是最大样本量的瑞基奥仑赛治疗R/R CNSL的真实世界研究。近期,该研究结果已发表于Journal for ImmunoTherapy of Cancer杂志。【肿瘤资讯】现将重点研究内容整理如下,以飨读者。

研究方法
本研究对国内12家中心的接受瑞基奥仑赛治疗的R/R CNSL患者进行了回顾性分析。纳入的是年龄≥18岁,按照WHO2016标准,组织学确诊为CD19阳性的R/R CNSL患者,且既往接受过系统治疗,包括含CD20单抗的免疫化疗以及基于大剂量甲氨蝶呤(MTX)的治疗方案。
主要研究终点为:3个月的完全缓解(CR)率,次要研究终点为:最佳完全缓解(BCR)、无进展生存期(PFS)、缓解持续时间(DOR)、OS和不良事件(AE)发生率。
研究结果
入组患者基线人口统计学特征和临床特征
本研究共纳入了22例中枢神经系统弥漫大B细胞淋巴瘤患者(CNS-DLBCL;12例为原发;10例为继发),他们分别于2021年10月至2023年2月期间接受瑞基奥仑赛治疗。患者中位年龄56岁,45.5%的患者>60岁,一半患者的卡氏体能评分(KPS)≤60分。在生发中心(GCB)亚型中,3例(3/13, 23.1%)患者为双打击淋巴瘤(DHL)或三打击淋巴瘤(THL),在非生发中心(non-GCB)亚型中,仅有1例(1/9, 11.1%)患者为DHL。患者的中位既往治疗线数为2(1~5)线。
在接受瑞基奥仑赛输注的22例患者中,有8例(36.4%)患者将其作为巩固治疗,这些患者在接受白细胞介素治疗前就已获得CR或部分缓解(PR),但仍被临床视为高危患者(其中包括原发难治性疾病、既往接受过大量治疗、THL或不适合ASCT)。除2例患者外,其余患者均接受桥接治疗,大部分患者病情得以控制,即在接受输注前,22例患者中10例患者已达CR或PR,9例患者疾病稳定(SD),3例患者疾病进展(PD)。在可评估病灶的17例患者中,大多数都有实质受累,包括2例仅脊髓局部受累,1例经核磁共振成像和脑脊液证实有孤立性软脑膜病变。
治疗结局
从细胞单采到输注的中位间隔时间为32天(28~37天)。13例(59.1%)患者接受单次CAR-T细胞输注,其余9例患者接受ASCT联合CAR-T细胞输注(ASCT在-3天进行)。18例(81.8%)患者在输注后中位31天(3~42天)接受联合其他药物治疗,中位持续时间为180天,联合治疗包括使用单靶点或双靶点药物,包括BTKi(n=15)、PD-1抑制剂(n=5)或来那度胺(n=4)。
最佳总缓解率(ORR)为90.9%,BCR率为68.2%。其中3例患者1个⽉时达到早期PR,3个⽉时达CR;4例患者最初达SD,3个月时达PR;值得注意的是,1例患者在6个⽉时进⼀步达CR。所有患者均获得CNS缓解,其中16例(72.7%)患者获得CNS最佳CR,中位至缓解时间为1个月。
中位随访316天,在16例达CNS缓解的患者中,13例(81.3%)患者仍存活并持续缓解,其中8例(50.0%)患者CNS缓解持续超过1年。总体而言,6例(27.3%)患者PD,包括4例在6个月内PD(1例仅全⾝性PD,3 例CNS PD,2例同时出现全⾝性和CNS PD),3例因快速进展而在2周内死亡。1年PFS率、DOR率和OS率分别为64.4%、71.5%和79.2%,中位PFS、DOR和OS均未达到。
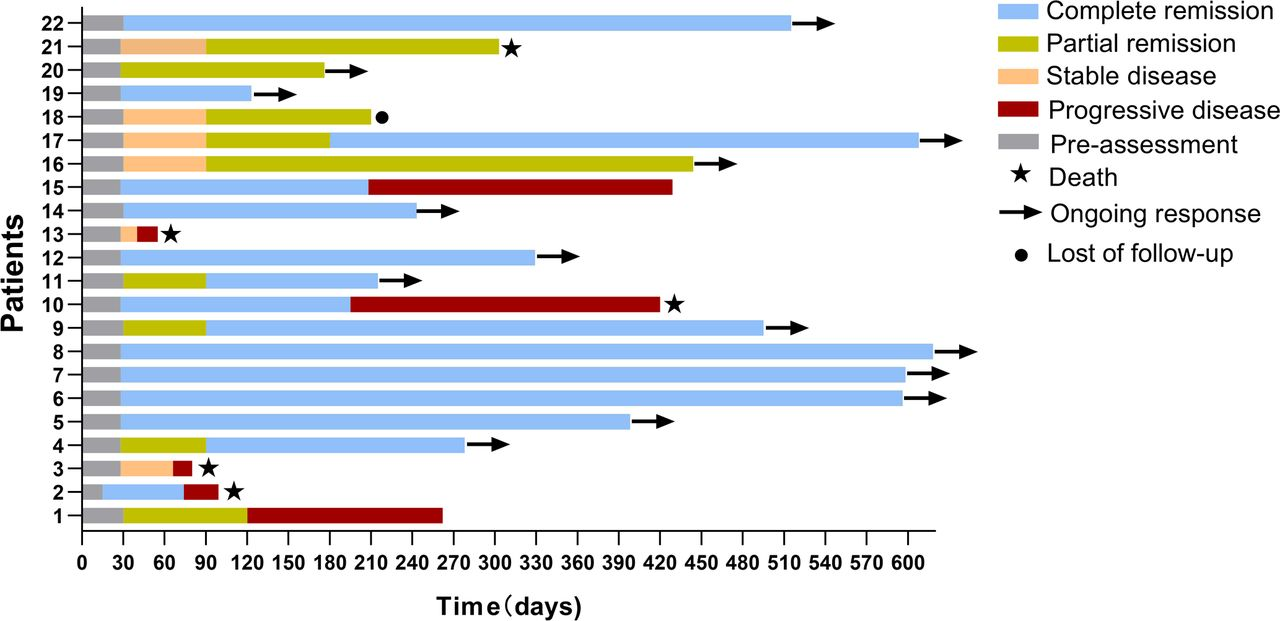
图1.22例患者的治疗反应特征随时间变化情况
预后分析
瑞基奥仑赛输注在不同亚组人群中均有临床疗效,包括年龄、性别、细胞来源亚型、疾病性质(PCNSL vs. SCNSL)、高危基因型和既往治疗线数等。同时,全身受累是PFS的预测因素(P=0.02);输注时的疾病缓解状态(CR vs. PR vs. SD/PD)似乎也与预后相关。所有输注前无活动性疾病的患者都能在3个月内均维持CR,生存率较高,1年PFS率为100%,而输注前仅达SD/PD的患者失败风险更高,1年PFS率仅为46.9%。ASCT+CAR-T组较单次CAR-T输注组的临床结局似乎略差,包括BCR率(55.6% vs. 76.9%,P=0.28)和1年PFS率 (62.2% vs. 67.3%,P=0.51),但不同的输注方式并无显著差异。在主要终点上,输注后3个月未达CR似乎预示较差预后,估计的1年PFS率分别为83.3%和37.0%(P=0.03)。
值得注意的是,患者对既往末次治疗的缓解状态对短期和长期临床结局都有显著影响。单采前持续CR/PR患者(n=8)较R/R患者的缓解率更佳(3个月CR率:P=0.01;BCR率:P=0.02),8例患者在末次随访前均保持CR,其中5例保持无进展超过12个月。相反,对既往末次治疗耐药或复发则会对PFS和DOR产生显著不利影响(1年PFS率:CR/PR 100.0% vs. R/R 41.7%,P=0.02;1年DOR率:100.0% vs. 50%,P=0.03),且对OS的不利因素呈临界显著(1年OS率: 100.0% vs. 65.5%,P=0.05)(图2)。
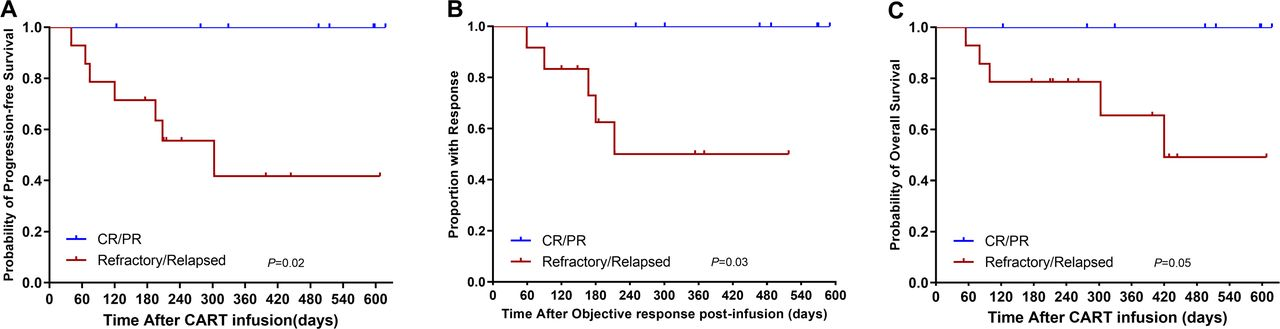
图2.基于患者对既往末次治疗反应分层的PFS、DOR和OS
安全性与耐受性
研究共报告了5例死亡(22.7%),其中3例(13.6%)死于PD,2例(9.1%)死于非疾病原因(新冠),并无CAR-T相关死亡。16/22(72.7%)的患者发生任何级别的细胞因子释放综合征(CRS),大多数为1级或2级(15/16,93.7%)。8例(36.4%)患者发生不同级别的免疫效应细胞相关神经毒性综合征(ICANS),其中仅1例(4.5%)为3级。所有神经毒性(NT)病例均与CRS同时报告。没有患者出现4-5级CRS或NT。为缓解毒性症状,10/22(45.4%)患者接受托珠单抗治疗,其中13.6%接受两次治疗,另有9/22(40.9%)患者接受类固醇治疗。
其他重要AE中,2例患者在输注≥28天出现≥3级的血细胞减少。1例患者发生持续3级中性粒细胞减少,持续3个月,但骨髓未见疾病进展。8例患者发生感染性AE(上呼吸道感染5例,3例患者感染新冠重症肺炎,其中直接导致2例死亡)。1例患者在输注1年后出现短暂的幻觉,但PET/MRI显示持续PR。
CAR-T细胞扩增和CSF转运
药代动力学(PK)检测显示,在21例可评估的患者中,在输注后的前28天内瑞基奥仑赛在外周血中显著扩增;9/21例可通过流式细胞术(FCM)检测到,17/21例通过定量PCR (qPCR)检测到。图3所示,qPCR检测到的CD19 CAR-T细胞峰值中位数为79646.5拷贝/μDNA,而FCM检测到的CD3+CAR+T细胞峰值中位数为139.8拷贝/µL,达到峰值水平的中位时间为1.43周。在8例可评估患者的脑脊液中均检测出瑞基奥仑赛。现有扩增数据表明,无论是否存在全身性淋巴瘤或不可测量病灶,CAR-T细胞都可以进入脑脊液。
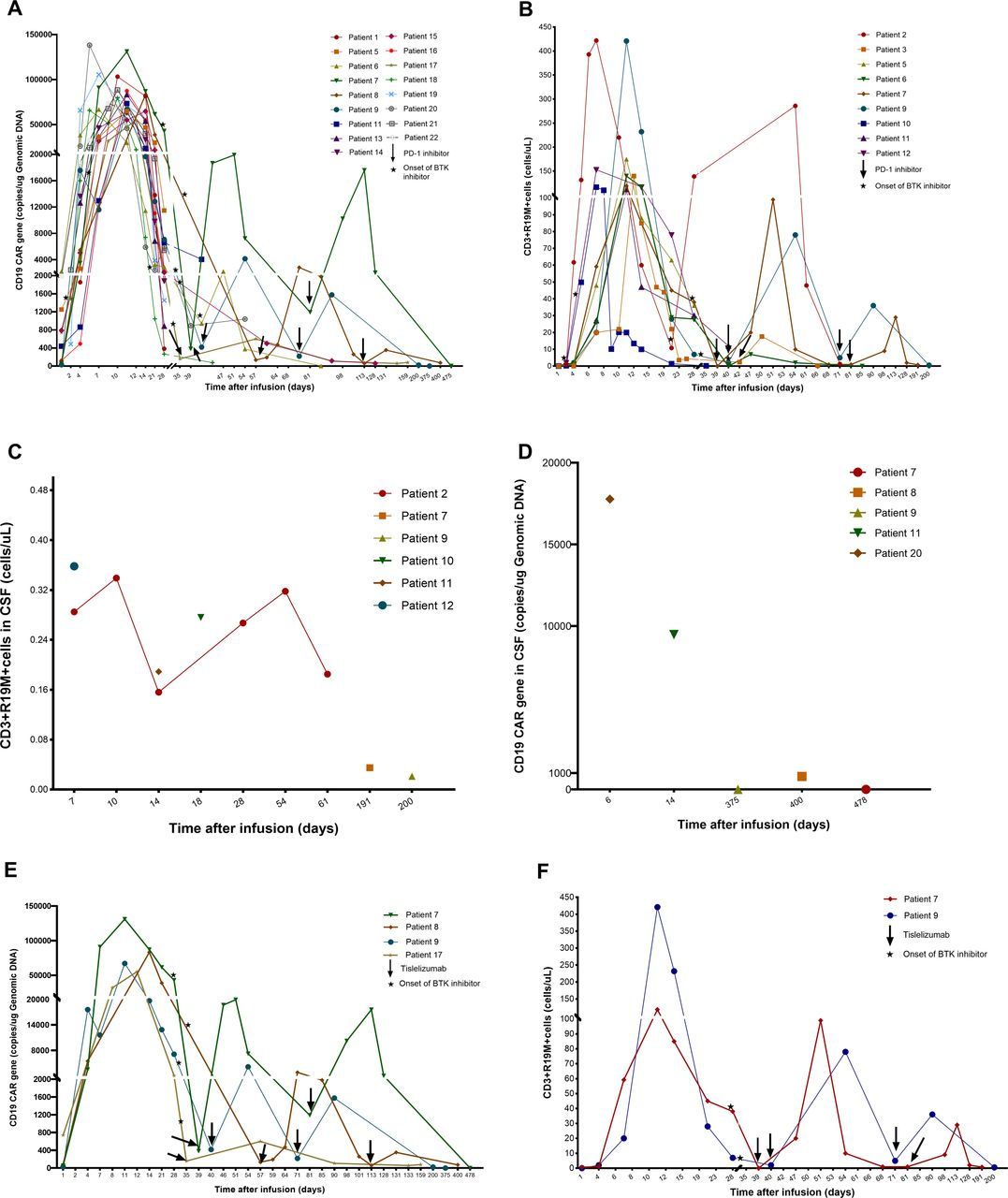
图3.输注瑞基奥仑赛后PK分析
瑞基奥仑赛与PD-1抑制剂和BTKi联合治疗的PK
CAR-T细胞在血液中的持久性随着时间的推移而降低。在单用BTKi或单用PD-1抑制剂的可评估患者中,可以观察到循环CAR-T细胞的再扩增。4例患者同时接受双免疫治疗(PD-1抑制剂和BTKi)治疗超过1年。如图3E,F所示,在BTKi治疗时引入替雷利珠单抗,且在注射替雷利珠单抗后中位时间2周(12~32天),通过qPCR或FCM检测到CAR-T细胞显著再扩增。总体而言,这4例患者在15.5个月内持续缓解,其中1例患者的疗效持续改善(SD-PR-CR)。3个月后,这些患者中也可检测到循环CAR-T细胞。尽管6个月后,2例患者外周血(0.8和0.55个细胞/µL)和CSF(0.035和0.021个细胞/µL)中通过FCM检测到的CAR-T细胞水平相对较低,甚至从第478天和第375天起不再能检测到,但患者仍在持续缓解。值得注意的是,有1例患者的CAR-T细胞持续时间最长,直到第400天,其CSF中的CAR转基因水平远高于血液样本(797 vs. 73拷贝/μg DNA)。
CAR-T细胞扩增与缓解和安全性的相关性
研究进一步分析了血清CAR转基因(拷贝数/每微克DNA)与疗效和CRS/ICANS的相关性。在达到BCR的可评估患者中,观察到了瑞基奥仑赛持续时间更长的趋势。与未达到CR患者相比,这种相关性与较高的中位AUC0-28 (911,052拷贝/μg DNA天)相关(AUC0-28定义为瑞基奥仑赛治疗后前28天内血液中CAR基因拷贝数蓄积)。在安全性方面,在发生任何级别神经系统事件的患者中,CAR-T细胞的峰值扩增明显更高;每微克DNA的中位拷贝数为100,167,而没有任何NT的患者的中位拷贝数为74,019(P=0.01)。然而,ICANS的严重程度无显著差异(ICANS分级≥2级vs. 1级,中位Cmax:108,249 vs. 92,085,P=0.43)。此外,CAR+ T细胞的AUC0-28与CRS/ICANS的发生或严重程度之间没有统计学上的显著关联。CAR+ T细胞的峰值水平或AUC0-28与CRS/ICANS持续时间之间也没有正相关性。
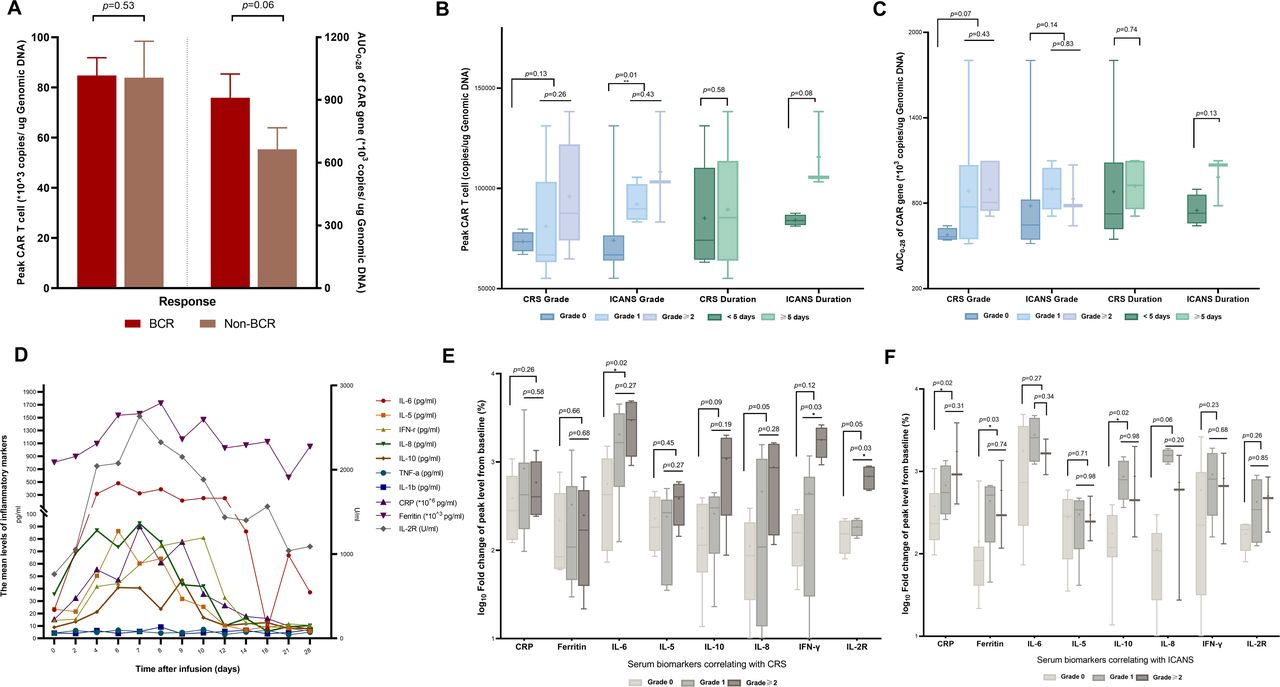
图4.PK与血清生物标志物与治疗反应或安全性的相关性
生物标志物分析
图4D也显示了白细胞介素(IL)-2R、IL-6、IL-5、IL-8、IL-10、γ干扰素(IFN-γ)、CRP和铁蛋白水平的动态波动,但IL-1b和肿瘤坏死因子α (TNF-α)等细胞因子的水平似乎较低且平缓。就ICANS而言,CRP、铁蛋白和IL-10的峰值水平(Δpeak)升高较基线的中位倍数变化似乎与ICANS的发生相关,但与严重程度无关。此外,CRS的发生与血清IL-6的中位Δpeak呈正相关。与1级CRS患者相比,高级别CRS(≥2级)患者的血清IFN-γ和可溶性IL-2R的中位Δpeak显著升高(图4E、F)。
总结
本研究证实了瑞基奥仑赛治疗CNSL 具有临床意义的疗效和可接受的安全性,同时再次证实BTKi 或PD-1抑制剂等对CAR-T细胞再扩增的获益且进一步改善治疗反应。CAR-T细胞治疗联合双免疫疗法可能存在潜在的协同作用。此外,本研究建议早期使用CAR-T细胞治疗作为挽救治疗敏感患者的巩固治疗,这也为未来的策略提供了动力和启发。作为一项回顾性研究,研究者也认为还需要更大样本量的研究以验证相关发现,更期待开展随机前瞻性研究来进一步比较CAR-T细胞治疗与ASCT对挽救治疗有效的R/R CNSL患者的疗效,从而进一步明确CAR-T细胞疗法作为巩固治疗的作用。
Yu W, Huang L, Mei H, et al. Real-world experience of commercial relmacabtagene autoleucel (relma-cel) for relapsed/refractory central nervous system lymphoma: a multicenter retrospective analysis of patients in China.Journal for ImmunoTherapy of Cancer 2024;12:e008553.doi:10.1136/jitc-2023-008553
排版编辑:Mathilda











 苏公网安备32059002004080号
苏公网安备32059002004080号


