肝胆恶性肿瘤起病隐匿,侵袭性强,发现时多为晚期,预后极差,是我国发病率高、致死率高的恶性肿瘤。在肿瘤精准治疗观念下,免疫联合化疗/靶向治疗将成为肝胆恶性肿瘤的未来主要发展趋势。肝癌方面,EMERALD-1 研究谱写了TACE联合靶向+免疫的传奇;胆道癌方面,TOPAZ-1研究作为全球首个也是唯一一个获得三阳结果(OS、PFS、ORR)的III期研究,开启了免疫一线治疗的新篇章。化疗联合度伐利尤单抗快速起效,TTR仅1.6个月;有效率从18.7%提高到26.7%(ORR),实现全面获益,显著延长了患者的无进展生存(PFS)与总生存(OS)[1]。
《例例非凡》——肝胆肿瘤临床病例解析,将从不同视角提升临床思维,促进专业学术及临床经验分享。
本期由北京清华长庚医院肝胆胰中心杨世忠教授团队分享2例肝内胆管细胞癌(ICC)病例。病例1为初始不可切除ICC伴肝内多发转移,入院CA199 79710.59U/mL,患者拒绝化疗,经度伐利尤单抗单药治疗8周期后,达到大PR接近CR,CA199降至63.81U/mL,并成功转化,接受右半肝切除术+胆囊切除术+腹腔淋巴结清扫术,术后病理结果显示达到pCR,随访1年未见复发。病例2为肝内胆管低分化腺癌伴肝内多发转移与肝胃间隙、肝门部、腹膜后淋巴结转移,经过奥沙利铂经肝动脉灌注化疗(HAIC)+吉西他滨和度伐利尤单抗治疗2周期后便达到PR,治疗4周期后疗效维持PR。
病例介绍
医学博士,主任医师
中华医学会肝病学分会肝癌学组秘书
北京医学会肝病学分会青年委员
主要研究方向为肝胆胰肿瘤、病毒性肝炎、脂肪肝
参与国家十一五、十二五、十三五重大科技专项传染病防治课题研究
曾获美国国立卫生研究院Fogarty Global Health Fellowships资助
参与多项临床药物试验
首次就诊
患者男性,60岁。2022年1月因间断上腹痛至当地医院就诊。
既往史
诊断为原发性胆汁性胆管炎4年,接受熊去氧胆酸治疗。
睡眠呼吸暂停20余年。
腰椎间盘突出2年。
否认高血压、冠心病、糖尿病等慢性病史。
否认乙肝、丙肝病史。
化验检查
肿瘤标志物:AFP 3.4IU/mL,CA199>1000U/mL,CEA 4.3ng/mL,CA125 42.3U/mL,CA724 21.3U/mL。
腹部超声:肝内异常回声,建议进一步检查。
腹部平扫CT:肝内多发占位,考虑癌伴肝内多发转移可能,建议增强;前列腺增生。
遂到我院进一步就诊。
我院就诊
化验检查
2022-2-25
血常规、肝功能、凝血功能正常。
肿瘤标志物:CA199 79710.59U/mL。
腹部增强CT:肝内多发病灶,考虑恶性,肝内胆管细胞癌伴肝内多发转移可能,伴周围淋巴结转移可能。结肠管壁略增厚,建议随诊。胸部CT:两肺多发磨玻璃微结节,建议复查。
影像学检查
2022-2-25
全腹部增强CT:右半肝可见多发结节、肿块影,呈融合状,邻近肝包膜略显皱缩,增强扫描病灶呈不均匀渐进性强化,大者大小约90x112mm,病灶周围见轻度的扩张胆管。肝门部、肝胃间隙可见肿大淋巴结,大者大小约15x19mm,增强扫描呈边缘强化(图1)。
图1 2022-2-25全腹部增强CT结果
肝穿刺活检
2022-3-1
(肝肿物组织条)纤维组织中见肿瘤呈腺样生长,肿瘤细胞中度异型。
免疫组化:CK7(-)、CK19(+)、CK20(个别+)、CDX-2(部分+)、CEA(+)、Muc-1(+)、Muc-2(-)、Muc-5AC(+)、Muc-6(部分+)、Ki67(50%+)。
综上,腺癌,中分化,符合胆管细胞癌。
诊断
1. 肝内胆管细胞癌
肝内转移
肝门部、肝胃间隙淋巴结转移
2. 原发性胆汁性胆管炎
3. 睡眠呼吸暂停
4. 腰椎间盘突出
治疗方案
外科认为不适合直接切除,建议药物治疗。
患者家属不想让患者知道病情,坚决拒绝化疗。
度伐利尤单抗单药治疗1500mg ivgtt q21d,共8次。
复查结果
8周期评效:大部分缓解(PR)或完全缓解(CR)(图2)。
2022-11-7 CA199:由79710.59U/mL降至63.81U/mL;
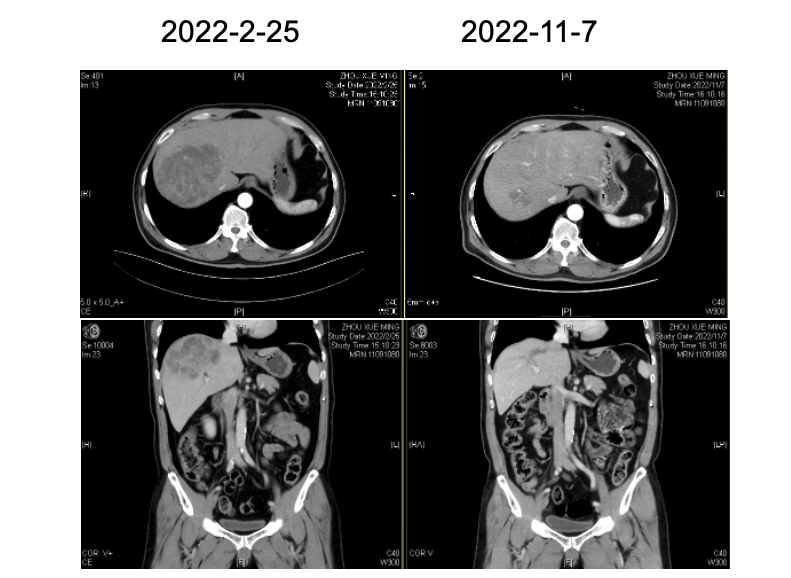
图2 度伐利尤单抗治疗前后影像学检查结果
2022-11-11 PET-CT:
肝脏肿瘤治疗后,肝S7/8不规则稍低密度影,FDG代谢低于周围肝实质,考虑肝脏肿瘤治疗后未见明显肿瘤活性存在;肝门部及腹膜后淋巴结影,未见明显FDG代谢增高;两肺多发磨玻璃密度小结节影,未见FDG代谢增高。
手术
2022-11-30 行右半肝切除术+胆囊切除术+腹腔淋巴结清扫术(图3)。
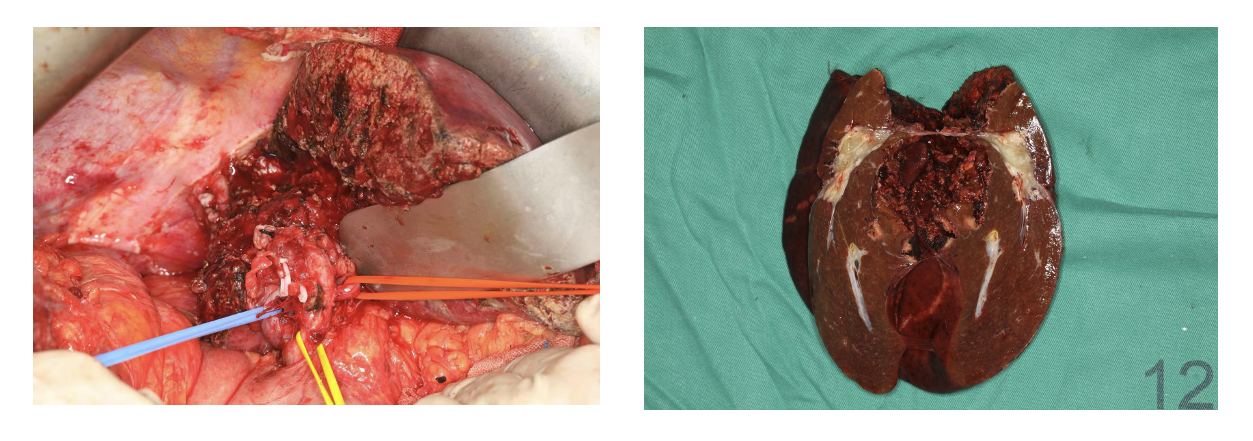
图3 2022-11-30手术切除
术后病理结果提示达到pCR
(右半肝)肝组织,局灶肝实质结构消失,纤维组织增生伴胶原纤维沉积,其间小血管增生,慢性炎细胞浸润,组织细胞反应,多处小灶钙化伴多核巨细胞反应,病变大小2*2*2cm,考虑瘤床改变,未见健活肿瘤细胞残留。
(胆囊)慢性胆囊炎,上皮自溶。
(8A组)淋巴结1枚,呈反应性增生,小灶钙化。
(8P组)淋巴结2枚,呈反应性增生。
(12组)纤维脂肪组织。
(13组)纤维脂肪组织。
术后定期复查未见复发。以下为2023-11-10复查影像学结果(图4)。
图4 2023-11-10影像学复查结果
首次就诊
患者男性,60岁。2023年5月因腹部不适至当地医院就诊。
既往史
20余年前患乙型病毒性肝炎,予中药治疗,2022-5复查HBsAg(-),HBV DNA(-)。
否认高血压、糖尿病、冠心病、脑血管病病史。
吸烟40年,20支/日;饮酒40年,1周1次,每次3-4两白酒。
否认肝癌家族史。
化验检查
肿瘤标志物:CA199 46U/mL,AFP、PIVKA、CEA、CA724正常。
腹部增强CT:肝内多发占位,较大者位于右叶,约8.6*6.3cm,考虑弥漫性肝癌并肝门区多发淋巴结转移。
遂到我院进一步就诊。
我院就诊
化验检查
2023-6
血常规、肝肾功能、凝血功能正常。
肿瘤标志物:CA199 18.78U/mL,CA125 111.2U/mL,CEA、AFP、PIVKA、NSE正常。
胸部CT:两肺肺气肿、肺大疱。
影像学检查
2023-6-9
腹部增强CT:肝内多发占位,考虑恶性,肝内胆管细胞癌伴肝内多发转移,肝胃间隙、肝门部、腹膜后淋巴结多发转移可能大,肝硬化(图5)。
图5 2023-6-9腹部增强CT
肝穿刺活检
2023-6-14
肝穿刺活检病理:(肝肿物组织条)肝穿刺组织中见肿瘤细胞呈巢团状、腺管状浸润性生长,细胞中度异型,小灶坏死,间质纤维组织增生,散在急慢性炎细胞浸润。免疫组化:CK7(局灶+)、CK19(+)、CK20(-)、Muc-1(部分+)、Muc-2(-)、Muc-5AC(-)、Muc-6(局灶+)、HepPar-1(-)、GPC3(-)、Syn(-)、CgA(-)、NSE(-)、MLH1(+)、MSH2(+)、MSH6(+)、PMS2(+)、EGFR(+)、HER-2(0)、Ki67(90%+)。
综上,分化差的癌,考虑为中-低分化胆管细胞癌。
诊断
肝内胆管低分化腺癌 cT2N1M1,IV期
肝内多发转移
肝胃间隙、肝门部、腹膜后淋巴结转移
治疗方案
奥沙利铂经肝动脉灌注化疗(HAIC)+吉西他滨和度伐利尤单抗
具体为:经肝动脉灌注奥沙利铂85mg/m2 150mg d1+吉西他滨800mg/m2 1.6g d1、d8+度伐利尤单抗1500mg d1,q21d
复查结果
2周期评效:PR(图6)。
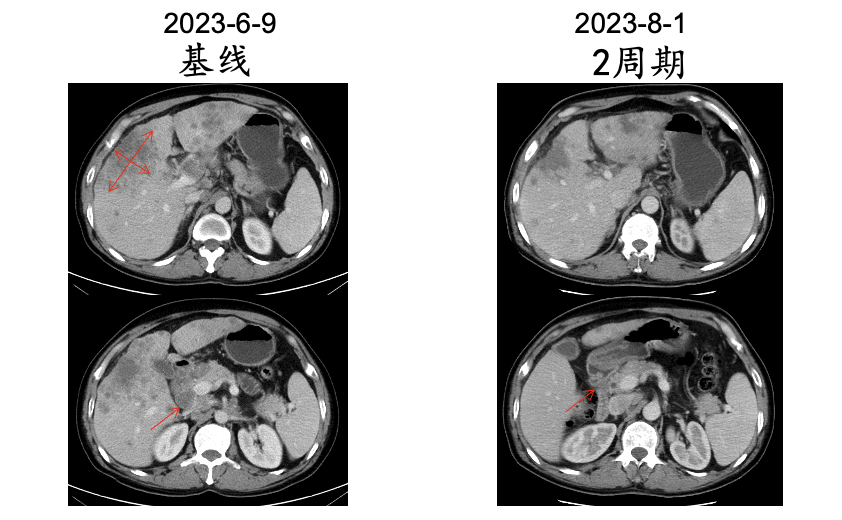
图6 基线和2周期影像学检查结果
4周期评效:维持PR(图7)。
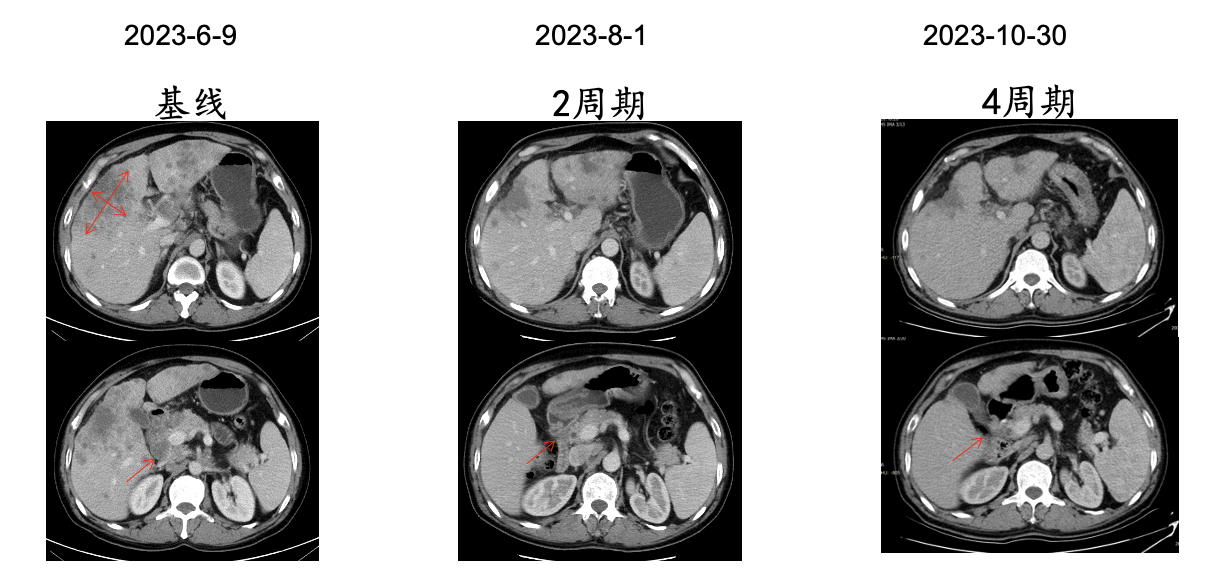 图7 基线、2周期、4周期影像学检查结果
图7 基线、2周期、4周期影像学检查结果
病例点评
外科博士/博士后
肝胆胰外科主任级Attending医师
精准诊疗肝癌中心主任
肝胆胰临床研究中心主任
日本国立国际医学研究中心/东京大学肝胆胰外科访问学者
学术任职:
中国研究型医院学会肝胆胰专业委员会常务委员
中国老年保健学会数智健康分会常务委员
北京健康促进会肝胆胰肿瘤专家委员会常务委员
北京癌症防治学会原发性肝癌外科治疗委员会副主任委员
《中华消化外科杂志》、《中华肝胆外科杂志》、《中华普通外科杂志》、《临床普外科电子杂志》、《中国现代普通外科进展杂志》 《中国医学前沿杂志》编委/通讯编委
肝内胆管细胞癌(ICC)是胆系恶性肿瘤(BTC)的一种,约占所有原发性肝癌的10%,是第二常见的原发性肝恶性肿瘤,东亚地区是其发病率最高的地区之一。ICC发病隐匿,侵袭性强,易转移,并且术后复发率高,1年和5年的总生存(OS)率分别为30%和18%[2-4]。绝大多数ICC患者就诊时已处于疾病中晚期,失去了手术机会,中位生存期仅为3~6个月[2-4],既往其一线标准治疗方案为化疗,常用方案如吉西他滨联合顺铂(GC方案)、吉西他滨联合替吉奥(GS方案),但疗效有限,中位OS仍难以达到1年[2,5]。
近年来,随着精准医疗的发展,免疫治疗在ICC中显示了优异的疗效及安全性,为晚期ICC的治疗带来了新希望。TOPAZ-1研究是一项随机、双盲、安慰剂对照、全球多中心Ⅲ期临床试验,共纳入685例不可切除的局部晚期或转移性BTC患者。研究结果显示[6],度伐利尤单抗联合化疗组一线治疗晚期BTC起效迅速,中位至缓解时间(TTR)仅1.6个月。对比单独化疗组,度伐利尤单抗联合化疗组使ORR从18.7%提高至26.7%。在主要终点OS方面,度伐利尤单抗联合化疗组的中位OS达到12.9个月,高于单独化疗组的11.3个月(HR 0.76),且随着随访时间的延长,进一步展现了免疫治疗的“拖尾效应”带来的长生存优势,3年OS率是单独化疗组的2倍多,实现翻倍(14.6% vs 6.9%)[7]。
针对本次病例分享中所关注的ICC患者,TOPAZ-1研究的亚组分析结果也显示,度伐利尤单抗联合化疗组的获益与整体人群一致,相较对照组可降低ICC患者24%的死亡风险(HR 0.76)。该研究的成功一举奠定了免疫治疗在包括ICC在内的BTC患者中的一线地位,为ICC患者带来了新的有效治疗选择。目前,《CSCO胆道恶性肿瘤诊疗指南》中,ICC患者一线治疗I级推荐度伐利尤单抗+化疗(1A类证据)。
病例1为一例初始不可切除ICC患者,影像学检查结果提示右肝可见多发占位伴肝门部、肝胃间隙肿大淋巴结。由于患者拒绝化疗,因此经多学科团队(MDT)讨论采用了度伐利尤单抗单药治疗,经过8周期治疗,患者的肿瘤标志物CA199降至63.81U/mL。疗效评估显示为大PR或CR,成功转化获得手术切除机会,术后病理显示为pCR,术后1年复查未见复发。该患者的诊疗经过体现了度伐利尤单抗在初始不可切除ICC患者转化治疗中的应用潜力,未来基于此方向或可深入开展前瞻性研究,拓展度伐利尤单抗的更多应用空间。
病例2是一例晚期ICC患者,肿瘤分期晚,肝内肿瘤负荷较重。病理提示中-低分化胆管细胞癌,Ki67(90%+),肿瘤分化差。该患者经过奥沙利铂经肝动脉灌注化疗(HAIC)+吉西他滨和度伐利尤单抗联合治疗2周期后,疗效评估为PR。经过4周期治疗,患者维持PR状态。度伐利尤单抗联合化疗方案帮助该晚期ICC患者有效控制疾病进展。
以上2个病例在真实临床环境中验证了度伐利尤单抗单药或联合化疗治疗ICC的出色疗效。度伐利尤单抗联合化疗已于2023年11月7日正式获得NMPA批准,用于局部晚期或转移性BTC成人患者的一线治疗。期待未来度伐利尤单抗进一步开展更多临床研究,探索更广阔的应用前景,最终造福更多患者。
[1] Do-Youn Oh, et al. A phase 3 randomized, double-blind, placebo-controlled study of durvalumab in combination with gemcitabine plus cisplatin (GemCis) in patients (pts) with advanced biliary tract cancer (BTC): TOPAZ-1. 2022 ASCO GI, Abstract #378.
[2] 2023CSCO胆道恶性肿瘤诊疗指南.
[3] Khan SA, et al. Cholangiocarcinoma: Epidemiology and risk factors. Liver Int.2019;39 Suppl 1:19-31.
[4] Bertuccio P, et al. Global trends in mortality from intrahepatic and extrahepatic cholangiocarcinoma. J Hepatol.2019;71(1):104-114.
[5] Echel F, et al. Chemotherapy and targeted therapy in advanced biliary tract carcinoma: a pooled analysis of clinical trials[J].Chemotherapy.2014;60(1):13-23.
[6] Do-Youn Oh,et al. 2022 ESMO P56.
[7] https://www.astrazeneca.com/media-centre/press-releases/2024/imfinzi-plus-chemotherapy-doubled-overall-survival-rate-at-three-years-for-patients-with-advanced-biliary-tract-cancer-in-topaz-1-phase-iii-trial.html
排版编辑:肿瘤资讯-Chloe











 苏公网安备32059002004080号
苏公网安备32059002004080号


