美国癌症研究协会(AACR)年会是全球肿瘤领域最具影响力的学术盛会之一。会议关注高质量肿瘤研究及创新研究,聚焦肿瘤领域热点。第115届AACR年会于美国东部时间2024年4月5~10日在美国圣迭戈举行。美国约翰霍普金斯大学医学院Dr. Marina Baretti团队联合多个中心开展的胰腺导管腺癌(PDA)研究重磅入选临床试验全体会议(Clinical Trials Plenary Session),Dr. Marina Baretti在AACR现场口头报告了该研究结果。该研究发现,组蛋白去乙酰化酶(HDAC)抑制剂entinostat联合纳武利尤单抗在部分患者中可产生持续应答,这为PDA患者的治疗带来了新希望。【肿瘤资讯】紧跟AACR最新进展,特邀中国解放军总医院苟苗苗教授和Dr. Marina Baretti云端对话。通过国际连线,两位专家围绕该研究的设计、结果和胰腺癌治疗的未来发展方向进行了深入探讨和交流。
约翰霍普金斯大学医学院助理教授
约翰霍普金斯大学Sidney Kimmel综合癌症中心(SKCCC)肝胆肿瘤多学科诊所内科主任
美国临床肿瘤学会(ASCO)成员
美国癌症研究协会(AACR)成员
欧洲肿瘤内科学会(ESMO)成员
学术研究集中在开发胃肠道肿瘤新药上,特别关注免疫疗法和表观遗传疗法的联合方法。
目前是约翰霍普金斯大学肝癌和胆管癌多项临床试验的首席研究员,与实验室研究人员密切合作,将实验室发现应用于患者
日本国立癌研医院 高级访问学者
北京癌症防治学会胃癌防治青年委员会常务委员
中国研究型医院学会精准医学与肿瘤MDT专委青年委员、肿瘤外科委员会委员
中国医师协会结直肠肿瘤MDT专委会青年委员
中国抗癌协会头颈肿瘤整合康复专委会委员
中国老年保健协会老年医学分会常务委员
长期以来从事消化道肿瘤的综合治疗,以第一作者发表15余SCI
多次参与ASCO和ASCO-GI及国内会议交流
CSCO化疗安全管理大赛第一名,个人风采奖
主持一项青年成长课题,参与2项国自然课题和2项重大课题的研究,
撰写中国胆管肿瘤多学科综合治疗专家共识以及2023人卫出版社《结肠癌肿瘤学》
AACR国际连线-精彩视频

关于研究设计、作用机制
苟苗苗教授:我们非常关注您此次入选AACR的研究课题——HDAC抑制剂entinostat联合纳武利尤单抗治疗胰腺导管腺癌(PDA)的2期临床研究[1]。胰腺癌恶性程度高,常危及患者生命,且治疗效果差。虽然目前免疫治疗已成为多种肿瘤的标准治疗方法,但在2017年您们启动本研究时,胰腺癌的标准治疗还只是化疗,免疫检查点抑制剂(ICI)还不常见。您们是如何提出这一研究设想的?在药物选择上,您们为何决定使用entinostat与纳武利尤单抗联合,而非化疗或其他药物?
Dr. Marina Baretti:我们的研究设计和假设是基于前期实验室的工作。我们观察到某些HDAC抑制剂(HDACi)能够有效调节胰腺癌微环境,并降低免疫抑制作用,从而促进T细胞的聚集/浸润。在小鼠模型中,进一步证实了entinostat与ICI联合使用能够显著提高小鼠的生存率。其作用机制是,entinostat通过影响肿瘤细胞内的髓系细胞转录编码,降低免疫抑制,从而有利于T细胞在肿瘤内的聚集/浸润。基于这些发现,我们确立了本研究假设。
我们这项研究招募的都是经治PDA患者,已经是二线、甚至三线治疗后无效的患者,他们之前经受过多线/多重化疗,我们希望排除之前化疗对研究结果的影响,所以没有联合化疗等。
苟苗苗教授:在您的研究设计中,治疗分为三个阶段,首先是entinostat 5mg单药2周的导入期,随后是联合纳武利尤单抗240mg治疗Q2W,4个月后纳武利尤单抗增加至480mg Q4W。您是如何考虑设计这样的三阶段治疗方案的?
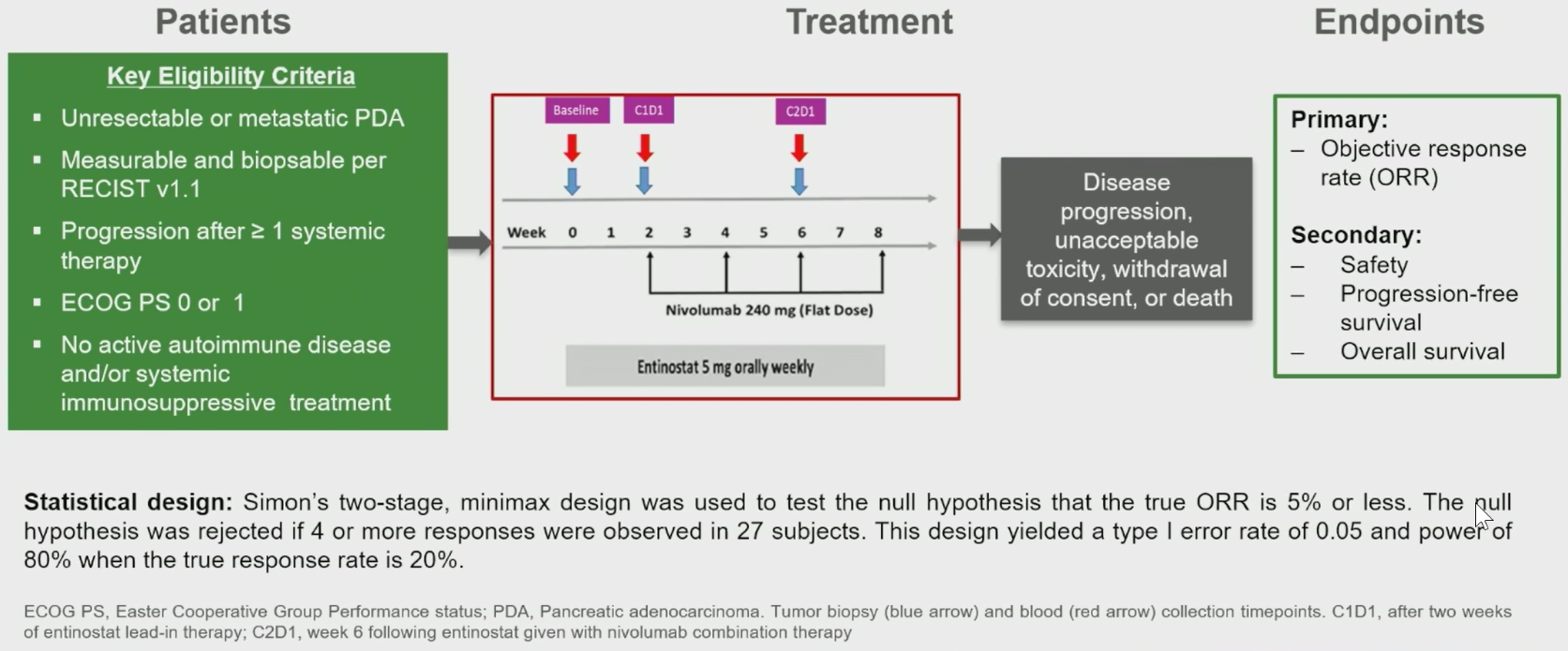
图1 研究设计
Dr. Marina Baretti:我们希望首先观察entinostat单药治疗的效果,了解其对胰腺癌患者的作用。因此,我们先设计了2周的entinostat单药治疗,并在治疗前后收集了血液和活检样本进行比较。鉴于entinostat单药治疗的临床活性尚不明确,我们选择了最短的治疗期限(2周),以免影响后续联合治疗的进行。在联合治疗阶段,我们旨在评估该方案的疗效和安全性。随着治疗的进行,我们积累了越来越多的疗效和安全性数据,因此允许患者进入下一阶段的治疗。
苟苗苗教授:您们的这项研究从2017年启动,直到2020年结束。我很好奇,为什么经过这么长时间,大约4年后,才公布研究结果?
Dr. Marina Baretti :最主要的延迟原因是新冠疫情的爆发。在试验的后期,招募最后几位患者时遇到了一些困难/延迟。此外,我们还需要检测大量的生物标志物,并且希望将肿瘤活检样本集中进行检测,以避免不同批次检测结果的差异,这同样适用于血液样本。所有样本的收集、分析以及综合评估疗效的过程都需要一定时间。
苟苗苗教授:关于肿瘤微环境,我们知道胰腺癌通常被认为是一种“冷”肿瘤,缺乏浸润淋巴细胞,导致预后不佳。您刚提到了entinostat的作用机制,我想知道,您认为它是在T细胞环境中发挥作用,还是与PD-1抑制剂有协同效应?
Dr. Marina Baretti:我们在治疗后的患者的髓系细胞中观察到了一些有趣的变化,这些细胞在抗原呈递、抗肿瘤免疫反应以及促进T细胞聚集方面发挥着关键作用。我们认为这是一个重要的免疫学发现,可能揭示了另一种作用机制,使得entinostat能够重新编程胰腺癌的微环境。我们在基线时进行了活检,并在2周后复查,但并未观察到肿瘤内T细胞数量的显著变化。这可能是因为复查时间过早,或者是T细胞的增殖首先发生在外周血或局部区域,随后才能进入肿瘤部位。然而,在观察到外周髓细胞群的变化的同时,我们也发现了外周记忆T细胞的增殖。结合研究中有患者对治疗持续响应的事实,我们相信HDACi与ICI的组合可能存在某种协同增效机制,这值得我们进一步探索和研究。
苟苗苗教授:最近中国的研究者(徐瑞华教授、王峰教授领衔)在Nature Medicine上发表了一篇关于HDACi达本胺与抗VEGF药物(贝伐珠单抗)和PD-1抑制剂(信迪利单抗)联合治疗经治微卫星稳定/错配修复功能完整(MSS/pMMR)型转移性结直肠癌(mCRC)患者的随机II期研究(CAPability-01)。该研究的客观缓解率(ORR)达到了44%[2],显示出非常有希望的疗效。该组合通过增强微环境中的T细胞,特别是CD 8+ T细胞的功能,从而使CTL可以很好地发挥作用并且具有反应性。您如何看待HDACi西达本胺与entinostat之间的差异?
Dr. Marina Baretti:我对您提到的这项研究不太了解。不过不同的HDACi由于功能的差异,可能会有不同的作用效果。而且,越来越多的证据表明,不同的肿瘤背景和肿瘤微环境也会影响HDACi的疗效。
关于研究结果、生物标志物探索和优势人群筛选
苟苗苗教授:在此次AACR公布的研究结果中,3例患者达到部分缓解(PR)(RECIST v1.1标准),ORR 为11%,中位缓解持续时间(mDoR)为10.2个月,这一结果令人瞩目。 请问研究中的无进展生存期(PFS)是多少?未来是否有计划公布总生存期(OS)数据?
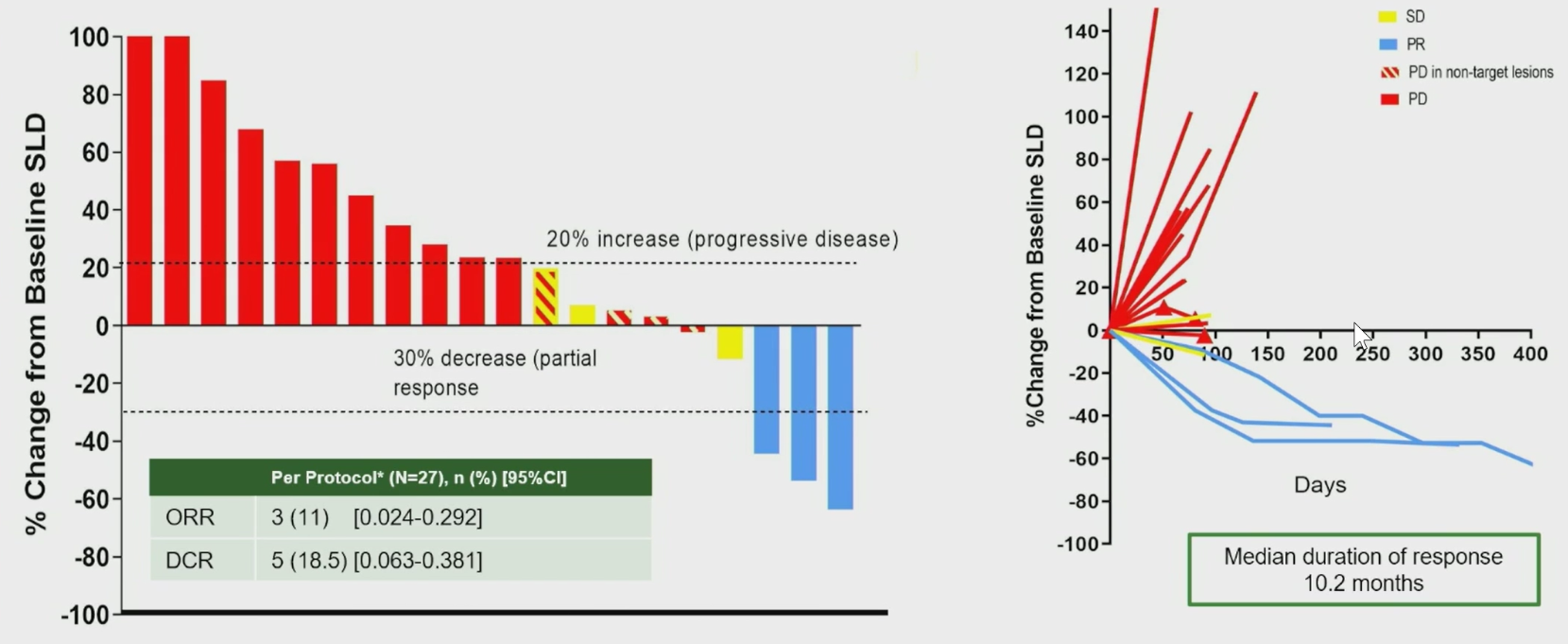
图2 ORR、DCR、mDoR
Dr. Marina Baretti:研究入组的患者都是经二线、三线甚至更多线治疗过的晚期胰腺癌,大部分患者的中位进展时间都非常短,总体基本为2个月。至于中位OS数据,目前尚未公布,但预期同样较短,估计约为3个月,不过这些数据与该类患者的历史数据相符/一致。
苟苗苗教授:在未来的研究中,是否有可能通过筛选特定的优势人群,以期从这种联合治疗中获得更大获益,提高PFS及OS?目前有哪些有潜力的生物标志物?
Dr. Marina Baretti:非常同意您的观点。在精准医学时代,我们要选择对我们研究治疗敏感、潜在有反应的患者,但目前还没有找到非常具体/明确的生物标志物。 我们观察到个别患者的PD-L1、PD-L2表达有所升高,尤其是有反应与无反应患者相比。但鉴于样本量有限、有反应的患者数量也有限,目前很难仅凭这一点就预测其对联合治疗的反应。将来进一步的工作是尝试了解哪类患者可能从这种治疗组合中获益更多。
关于胰腺癌治疗的未来探索
苟苗苗教授:在您这项研究中,纳入的患者均已接受了多线治疗,主要是大量化疗的晚期胰腺癌患者。您是否有计划开展新的研究,以评估该联合治疗方案在胰腺癌的一线治疗、辅助治疗或术前新辅助治疗中的疗效?
Dr. Marina Baretti:实际上,我们正在进行进一步的临床前研究,并探索将Entinostat与其他新型ICI及其他药物联合使用的可能性。希望依然是基于 HDACi的科学合理的组合方法,作为主要的免疫调节策略。
苟苗苗教授:尽管在中国出现了许多新药物,但对胰腺癌患者的疗效仍然非常有限,生存率依然较低。您认为应如何改善这类患者的生存状况?
Dr. Marina Baretti:一方面,我们在胰腺癌的生物学和分子学研究方面取得了前所未有的进展,药物研发也在不断取得令人鼓舞的成果,我们正在尝试更精准的靶向治疗方法。基于这些进展,我们需要更深入地理解免疫疗法及其耐药机制,以提高患者对免疫治疗的敏感性。另一方面,我们需要在早期诊断甚至预防肿瘤发生方面做出更多努力。我们正在研发预防性癌症疫苗,并计划为高风险胰腺癌人群接种。此外,我们还可以努力提高早期诊断的水平,例如关注早期胰腺癌患者中出现的KRAS突变等。
苟苗苗教授:您刚才提到的KRAS突变,其抑制剂在胃肠道肿瘤和肺癌的临床研究中表现出良好的效果。此外,靶向Claudin18.2的IgG1单克隆抗体Zolbetuximab已在某些国家获批联合化疗用于局部晚期不可切除或转移性胃或胃食管交界处(G/GEJ)腺癌患者,目前也有针对胰腺癌的临床试验在进行中。您认为这可能是未来胰腺癌治疗的另一个重要方向吗?在美国,是否还有针对这类突变以及其他突变的靶向药物?
Dr. Marina Baretti:确实如此。目前,无论肿瘤的生物学特征如何,所有患者都接受相同的化疗。如果能根据肿瘤的具体特征对患者进行亚型分类并给予相应的治疗,可能会获得更好的疗效,实现个体化治疗的目标。针对KRAS、Claudin18.2的靶向药物的出现为我们带来新希望,我们正在寻找最佳联合治疗方案。约90%的胰腺癌患者携带KRAS突变,在美国除了针对KRAS G12C和G12D突变的抑制剂外,还有针对胰腺导管上皮内瘤变(PanIN)的抑制剂等靶向药物,目前正在持续研发中。
[1]Baretti M, et al. Immunomodulation of the tumor microenvironment of pancreatic ductal adenocarcinoma with histone deacetylase inhibition: Results of a phase 2 clinical trial of entinostat in combination with nivolumab. 2024 AACR,abstract CT016.
[2]Wang, F., Jin, Y., Wang, M. et al. Combined anti-PD-1, HDAC inhibitor and anti-VEGF for MSS/pMMR colorectal cancer: a randomized phase 2 trial. Nat Med (2024).
排版编辑:肿瘤资讯-Marie











 苏公网安备32059002004080号
苏公网安备32059002004080号


