通过对2024.03.01-2024.03.31期间发表的乳腺癌领域最新文献进行检索和梳理,本期“乳腺癌新文连播”主要介绍了NETALLE研究的最新结果以及早期HR+乳腺癌辅助内分泌治疗未来探索方向;同时介绍了卵巢功能抑制(OFS)在绝经前乳腺癌患者中的作用。接下来,让我们一起来了解这些最新文献吧!
NETALEE研究:瑞波西利联合内分泌辅助治疗早期乳腺癌
Ribociclib plus Endocrine Therapy in Early Breast Cancer
PMID: 38507751 【New England Journal of Medicine, IF=158.5, JCR: Q1】
背景
研究表明,瑞波西利对激素受体阳性(HR+)、人表皮生长因子受体2阴性(HER2-)的晚期乳腺癌患者有明显的总体生存获益。这种对晚期乳腺癌的益处是否会延伸到早期乳腺癌尚不清楚。
方法
NATALEE研究是一项国际、开放标签、随机对照、III期临床研究,旨在评估瑞波西利联合非甾体芳香化酶抑制剂(NSAI)在II-III期HR+/HER2-早期乳腺癌(包括无淋巴结转移)患者辅助治疗的有效性和安全性。入组的绝经前/绝经后II-III期HR+/HER2-乳腺癌患者按1:1随机分组,接受瑞波西利(400 mg/天;持续3周,然后停药1周,持续3年)+NSAI(来曲唑2.5 mg/天或阿那曲唑1 mg/天,持续≥5年)或单独接受NSAI治疗。入组的绝经前女性和男性患者还需接受GnRHa治疗。在此,报告了主要终点无浸润性疾病生存期(iDFS)的预设中期分析结果;同时还报告了其他疗效和安全性结果。iDFS采用Kaplan-Meier进行评估。采用log-rank test进行统计比较,方案规定的终止界限为单侧P值阈值为0.0128时疗效更佳。
结果
截至本次预设中期分析的数据截止日(2023年1月11日),5101名患者中,共有426名患者出现了侵袭性疾病、复发或死亡,其中瑞波西利联合NSAI组发生率为7.4%(189/2549),单独NSAI治疗组发生率为9.3%(237/2552)。与单用NSAI相比,瑞波西利联合组可明显提高iDFS。瑞波西利联合NSAI组的3年iDFS率为90.4%,而单独使用NSAI的3年iDFS率为87.1%(侵袭性疾病、复发或死亡的危险比为0.75;95%CI:0.62-0.91;P=0.003)。次要终点无远处疾病生存期(DDFS)和无复发生存期(RFS)也倾向于使用利瑞波西利联合NASI。3年DDFS率分别为90.8% vs. 88.6%(HR=0.74;95%CI:0.60-0.91),3年RFS率分别为91.7% vs. 88.6%(HR=0.72;95%CI:0.58-0.88)。起始剂量为400毫克的瑞波西利联合一种NASI的3年治疗方案与任何新的安全性信号无关。
结论
本研究结果表明,瑞波西利联合NSAI可显著提高HR+/HER2-的II期或III期早期乳腺癌患者的iDFS,瑞波西利强化内分泌治疗可以降低25.2%的疾病侵袭、复发或死亡风险,3年iDFS绝对获益达3.3%。
绝经前激素受体阳性乳腺癌辅助卵巢功能抑制(OFS)
Adjuvant Ovarian Function Suppression in Premenopausal Hormone Receptor-Positive Breast Cancer.
PMID: 38477918 【JAMA Network Open, IF=13.8, JCR: Q1】
背景
激素受体阳性(HR+)乳腺癌是最常见的乳腺癌亚型,对于绝经前的这部分患者,卵巢功能抑制(OFS)是常用的辅助治疗手段,已被证实可提高这类患者的生存率。目前,OFS辅助治疗的研究大部分都是随机对照实验,很少有研究对辅助OFS在真实世界中的有效性进行评估。目标试验模拟越来越多地被用于估计观察组群的治疗效果。描述激素治疗和 OFS 治疗模式(目的 1),研究在他莫昔芬(TAM)或芳香化酶抑制剂(AI)基础上加用 OFS 与存活率之间的关系(目的 2),研究激素治疗(TAM 或 AI)加OFS(H-OFS)的持续时间与存活率之间的关系(目的 3)。
目的
探讨激素治疗和OFS治疗模式(目的 1);他莫昔芬(TAM)或芳香化酶抑制剂(AI)基础上加用OFS与生存率之间的关系(目的 2);激素治疗(TAM或AI)加上OFS(H-OFS)的持续时间与生存率之间的关系(目的 3)。
方法
这项基于人群的队列研究纳入了加拿大艾伯塔省2010年至2020年间所有绝经前早期乳腺癌患者病例,进行目标试验模拟。纳入标准参照SOFT和TEXT试验的入排标准。最长随访时间为5年。数据分析时间为2022年7月至2023年3月。对于目的 2,受试者在2年内接受以下基线治疗:AI+OFS(AI-OFS)、TAM+OFS(T-OFS)和单独TAM。对于目的 3,受试者为接受2年、2年以上和2年以下的H-OFS治疗。主要研究终点是无复发生存期(RFS)。在对基线和时变混杂变量进行调整后,采用反概率处理和加权剔除的边际结构Cox模型来估算危险比(HRs)。
结果
在3434名绝经前早期乳腺癌的患者(中位年龄[IQR]为45 [40-48]岁)中,有2647人符合SOFT和TEXT的纳入标准。入组患者中,2260名患者起始接受TAM治疗,232名患者起始接受T-OFS治疗,155名患者起始接受AI-OFS治疗;192名患者接受了2年或2年以上的H-OFS治疗,195名患者接受了不到2年的H-OFS治疗。TAM、T-OFS 和AI-OFS患者5年累积复发率分别为27.7% (95%CI, 23.6%-31.2%), 23.3% (95%CI, 18.0%-36.6%)和21.4% (95%CI, 11.8%-33.5%)。与TAM组相比,AI-OFS组(HR,0.76;95% CI,0.38-1.33)和T-OFS组(HR,0.87;95% CI,0.50-1.45)的5年复发风险没有明显降低。
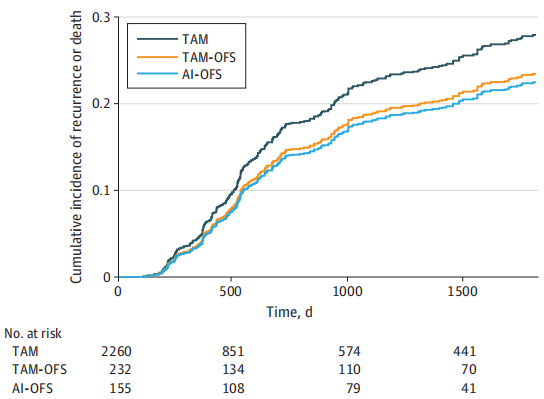
不同治疗模式患者累积复发风险
与接受H-OFS少于2年的患者相比,接受H-OFS持续2年或2年以上的患者5年无复发风险降低31%(HR,0.69;95% CI,0.54-0.90)。
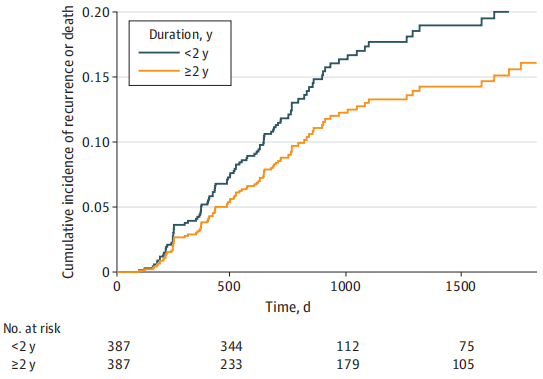
基于治疗时间分层的累积复发风险
结论
该研究发现,尽管在随机对照实验中OFS显示出患者的获益,但是在真实世界中,与单独使用TAM相比,AI-OFS和T-OFS的复发风险没有明显降低。持续至少2年的H-OFS与无复发风险的显著降低有关。
卵巢功能抑制(OFS)对乳腺癌患者的影响2
Ovarian Suppression: Early Menopause and Late Effects
PMID: 38305992【Current Oncology Reports, IF=4.7, JCR: Q2】
摘要
大约90%的乳腺癌在早期就被诊断出来,其中大约70%是激素受体阳性(HR+)乳腺癌患者。内分泌治疗是早期HR+乳腺癌辅助治疗的基石,根据疾病分期、肿瘤的生物学特征、患者的合并症、偏好和年龄量身定制。对于绝经前HR+乳腺癌患者,卵巢功能抑制(OFS)是内分泌辅助治疗的重要组成部分,可与芳香化酶抑制剂或他莫昔芬联合使用。此外,OFS可以在化疗期间作为标准策略用于所有亚型乳腺癌患者的卵巢功能保护。在转移患者中,所有绝经前HR+乳腺癌患者都应采用OFS治疗,以达到绝经后状态。尽管OFS具有一定疗效,但如果处理不当,可能会导致多种副作用,对患者的生活质量产生重大负面影响(如潮热、抑郁、认知障碍、骨质疏松症、性功能障碍、体重增加)。临床医生有必要深入了解OFS的副作用。应将这方面的正确咨询和积极管理视为患者护理的基本组成部分,以提高治疗依从性和患者的生活质量。
微调早期乳腺癌的辅助内分泌治疗:未来研究的开放性问题专家共识
Fine-Tuning Adjuvant Endocrine Therapy for Early-Stage Breast Cancer: An Expert Consensus on Open Issues for Future Research
PMID: 37906083 【Clinical cancer research, IF=11.5, JCR: Q1】
摘要
经过几十年的研究,提高早期乳腺癌辅助内分泌疗法(ET)的疗效变得越来越困难。除了技术上的突破和新药的出现,进一步提高辅助内分泌治疗的疗效还需要在研究不足的领域采用严谨的研究方法。在此,批判性地讨论了一些关键原则,这些原则应贯穿于未来提高ET疗效的研究中,包括确定可从升阶梯或降阶梯方法中获益的特定亚组患者、针对不同临床情况优化现有的和新的治疗策略,以及剖析治疗干预措施的直接和间接生物效应。与辅助ET有关的四个主要问题被确定为相关领域,在这些领域更好地应用这些原则可在不久的将来取得积极成果:(i)调整辅助ET的最佳持续时间,(ii)优化绝经前妇女的卵巢功能抑制,(iii)剖析雌激素受体操作的生物效应,以及(iv)完善治疗升阶梯候选患者的选择。
1. Slamon D, Lipatov O, Nowecki Z, et al. Ribociclib plus Endocrine Therapy in Early Breast Cancer. N Engl J Med. 2024;390(12):1080-1091. doi:10.1056/NEJMoa2305488.
2. Basmadjian RB, Lupichuk S, Xu Y, Quan ML, Cheung WY, Brenner DR. Adjuvant Ovarian Function Suppression in Premenopausal Hormone Receptor–Positive Breast Cancer. JAMA Netw Open. 2024;7(3): e242082. doi:10.1001/jamanetworkopen.2024.2082.
3. Goldberg C, Greenberg MR, Noveihed A, et al. Ovarian Suppression: Early Menopause, Late Effects. Curr Oncol Rep. 2024; 1-12. doi:10.1007/s11912-023-01491-5.
4. Conforti F, Pala L, De Pas T, et al. Fine-Tuning Adjuvant Endocrine Therapy for Early-Stage Breast Cancer: An Expert Consensus on Open Issues for Future Research. Clin Cancer Res. 2024;30(6):1093-1103. doi:10.1158/1078-0432.CCR-23-1836.
排版编辑:肿瘤资讯-momo











 苏公网安备32059002004080号
苏公网安备32059002004080号


