2024年AACR年会如火如荼,而奥希替尼一直是各大肿瘤学年会的常客,那么本届AACR都有哪些奥希替尼相关的研究结果公布呢,小编为您梳理了以下4篇重要的摘要,包括两篇FLAURA2研究的探索性分析、一篇奥希替尼联合赛沃替尼相比赛沃替尼单药的小样本随机对照研究以及一篇奥希替尼潜在疗效预测因子的探索性分析。
CT017 - FLAURA2: exploratory analysis of baseline (BL) and on-treatment plasma EGFRm dynamics in patients (pts) with EGFRm advanced NSCLC treated with first-line (1L) osimertinib (osi) ± platinum-pemetrexed1
研究背景
FLAURA2研究显示,奥希替尼联合含铂双药化疗相比奥希替尼单药一线治疗EGFR敏感突变(19外显子缺失突变或21外显子L858R突变,19Del/L858R)阳性晚期NSCLC患者有显著的PFS获益(研究者评估的中位PFS分别为25.5个月和16.7个月,HR=0.62,P<0.0001,BICR评估的中位PFS为29.4个月和19.9个月,HR=0.62,P=0.0002)。既往FLAURA研究显示,基线(BL)可检测到血浆EGFR突变是潜在的预后因素,血浆EGFR突变早期清除与预后较好有潜在的相关性。探索FLAURA2研究基线(BL)是否可检测到血浆EGFR突变以及血浆EGFR突变清除与PFS的相关性,识别可从奥希替尼联合化疗中获益的患者。
研究方法
将EGFR敏感突变阳性晚期NSCLC随机分为奥希替尼联合化疗治疗组和奥希替尼单药治疗组,使用ddPCR对基线(BL)和第3周/第6周时的血浆EGFR突变进行检测。血浆EGFR突变清除的定义为:基线可检测到血浆ctDNA EGFR突变,第3周/第6周时无法检测到血浆ctDNA EGFR突变。
研究结果
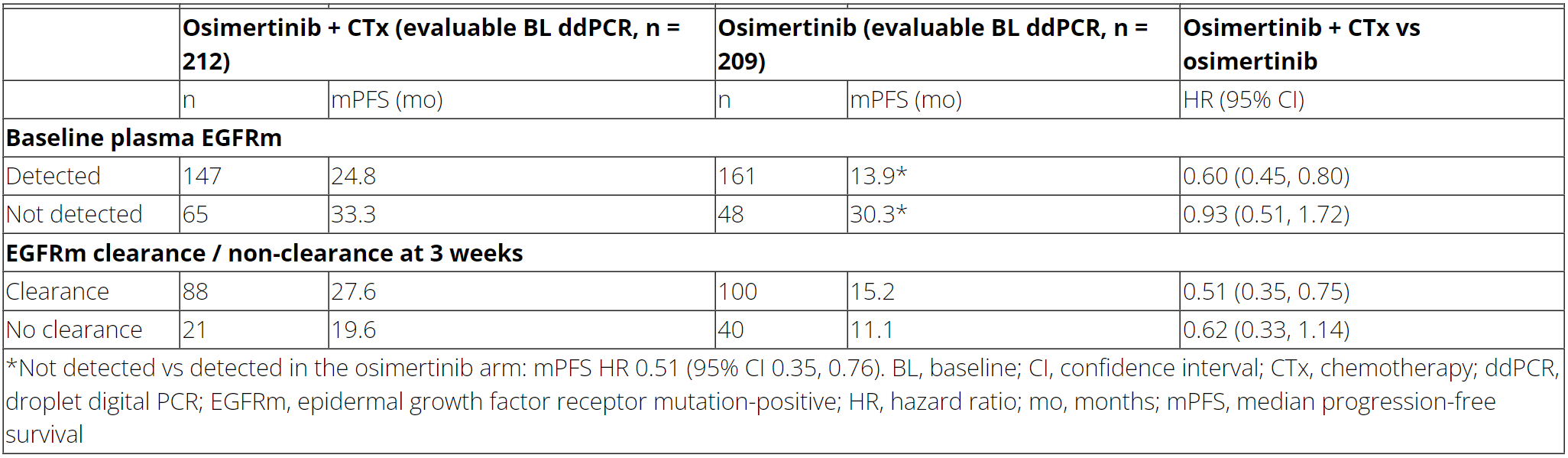
557例患者中有421例患者有可评估的基线血浆ddPCR结果,其中308例患者在基线时可检测到血浆EGFR突变。在奥希替尼单药治疗组中观察到,相比基线可检测到血浆EGFR突变的患者,基线无法检测到血浆EGFR突变患者的PFS更长。在基线和第3周/第6周时均有可评估的血浆ddPCR结果的患者中,奥希替尼联合化疗治疗组和奥希替尼单药治疗组,第3周/第6周时可检测到血浆EGFR突变的患者分别为19/12%和29/11%。
研究结论
在这项探索性分析中观察到,基线血浆EGFR突变是潜在的预后指标,可预测奥希替尼联合化疗和奥希替尼单药治疗的临床获益。基线是否可检测到EGFR突变或可帮助识别奥希替尼联合化疗治疗潜在获益最大的亚组。此外,在两个治疗组中均观察到第三周时血浆EGFR突变清除率与PFS获益有潜在的相关性,且两组的获益趋势一致,提示治疗阶段血浆EGFR突变清除率可能只是预后指标。
LB277 / 22 - Exposure response and safety analysis of osimertinib in combination with pemetrexed and platinum-based chemotherapy for the first-line treatment of locally advanced or metastatic NSCLC patients with EGFRm (FLAURA2)2
研究背景
奥希替尼是一种高效的且具有CNS活性的第三代EGFR-TKI,可同时抑制EGFR敏感突变(19外显子缺失突变或21外显子L858R突变,19Del/L858R)和EGFR T790M耐药突变。目前已在国内获批二线治疗既往EGFR-TKI治疗失败且有EGFR T790M突变阳性晚期非小细胞肺癌(NSCLC)患者、一线治疗EGFR敏感突变阳性晚期NSCLC患者、辅助治疗既往接受过或未接受过辅助化疗且接受过手术完全切除的IB-IIIA期NSCLC患者。
研究方法
FLAURA2研究是一项全球多中心开放标签随机对照III期临床研究,旨在评估奥希替尼联合化疗相比奥希替尼单药一线治疗EGFR敏感突变阳性晚期NSCLC患者的有效性和安全性。研究还在进行中,本次分析的目包括:(1)评估FLAURA2研究奥希替尼联合化疗组(n=244)患者群体PK模型衍生的奥希替尼暴露指标(AUCss、Cmaxss、Cminss)和PFS之间的暴露与疗效相关性;(2)评估奥希替尼暴露标准与关键安全性终点之间的相关性。
研究结果
研究对FLAURA2研究奥希替尼联合化疗组患者奥希替尼的暴露与PFS之间的暴露应答(ER)关系进行了分析,虽然观察到当AUCss四分位数达到最高值时PFS获益有降低的趋势,但ER相关性并不显著。逐步Cox比例风险模型显示,奥希替尼的暴露与PFS没有显著的相关性,但培美曲塞的治疗周期数可能与PFS有潜在的相关性。此外,研究还对奥希替尼暴露指标与奥希替尼治疗相关的≥3级不良事件(AE)以及特别关注的不良事件(AESI)之间的相关性进行了分析,结果显示,奥希替尼暴露与奥希替尼治疗相关≥3级AE发生率、导致奥希替尼剂量中断/下调/终止的AE以及AESI(包括≥3级血液学AE、心脏毒性、左室射血分数下降和≥1级间质性肺病)没有显著的统计学相关性。
研究结论
在FLAURA2研究中未观察到奥希替尼暴露与疗效之间有显著的统计学相关性,研究进一步支持奥希替尼每天80mg作为推荐剂量,如观察到不可耐受的毒性,则可将剂量下调至每天40mg。
CT251 / 10 - Savolitinib (savo) + osimertinib (osi) vs savo + placebo (PBO) in patients (pts) with EGFR-mutated (EGFRm), MET-amplified advanced NSCLC with progression on osi3
研究背景
奥希替尼是EGFR敏感突变阳性晚期NSCLC患者的一线优选治疗方案,但耐药不可避免,MET扩增是奥希替尼最为常见的耐药机制之一。既往一项使用奥希替尼联合赛沃替尼(一种MET-TKI)治疗EGFR敏感突变阳性且MET扩增阳性NSCLC患者的研究中,双通路抑制策略显示出了令人鼓舞的抗肿瘤活性。在此通过一项II期双盲随机对照临床研究来评估联合治疗中赛沃替尼的单药贡献。
研究方法
将EGFR敏感突变阳性且MET扩增(中心实验室通过FISH明确MET基因拷贝数≥5或MET/CEP7比值≥2)的既往接受过至少一线治疗(包括奥希替尼一线治疗)的晚期NSCLC患者随机分为赛沃替尼(300mg)联合奥希替尼组和赛沃替尼(300mg)联合安慰剂组,治疗直至发生疾病进展、不可耐受毒性或达到其他规定的停药标准。主要研究终点为研究者基于RECIST v1.1评估的ORR,探索性终点包括≥90%的肿瘤细胞染色3+(IHC90+)和/或MET基因拷贝数≥10(FISH10+)。收集血浆标本进行探索性分析。
研究结果
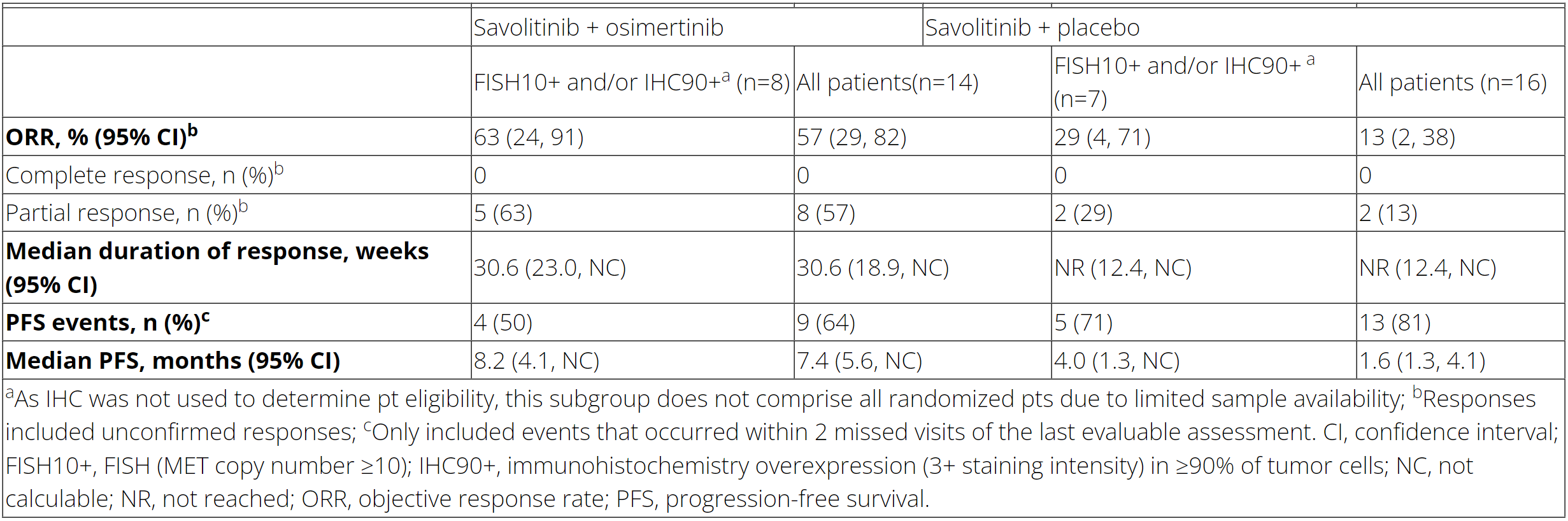
共有30例患者接受随机,其中赛沃替尼联合奥希替尼组14例,赛沃替尼联合安慰剂组16例。有3例接受赛沃替尼联合奥希替尼治疗的患者出现≥3级不良事件(≥3级AE:21%),有4例接受赛沃替尼联合奥希替尼治疗的患者出现严重不良事件(SAE:29%)。有5例接受赛沃替尼联合安慰剂治疗的患者出现≥3级不良事件(≥3级AE:31%),有3例接受赛沃替尼联合奥希替尼治疗的患者出现严重不良事件(SAE:19%)。与赛沃替尼联合安慰剂组相比,赛沃替尼联合奥希替尼组最常见的任何级别的AE是恶心(50% vs 19%)、周围水肿(36% vs 25%)和呕吐(21% vs 31%)。
研究结论
赛沃替尼联合奥希替尼相比赛沃替尼联合安慰剂,有更好的临床活性。在MET界值更高的患者中也观察到很好的临床活性。但由于样本量较小,需谨慎解读以上研究数据。安全性与联合治疗组每个药物单药治疗已知的不良事件谱一致。由于SAVANNAH研究已使用不同的赛沃替尼给药方案和更高的MET扩增界值来评估赛沃替尼联合奥希替尼相比赛沃替尼单药治疗的有效性和安全性,因此本研究提前终止。
964 / 5 - Updated results of a prospective observational multicenter study on resistance mechanisms to osimertinib using circulating tumor DNA analyses in EGFR-mutated non-small cell lung cancer patients (ELUCIDATOR study)4
研究背景
奥希替尼是EGFR敏感突变(19外显子缺失突变或21外显子L858R突变,19Del/L858R)阳性晚期NSCLC患者的一线标准治疗方案。但耐药依旧不可避免,因此了解奥希替尼的耐药机制并识别疗效不佳的患者对后续治疗策略的制定至关重要。这是一项前瞻性观察性多中心研究,旨在分析连续收集的ctDNA信息与临床结局之间的相关性;
研究方法
纳入计划一线接受奥希替尼治疗的EGFR敏感突变阳性且组织或细胞学明确的非鳞状NSCLC患者,以上患者还可提供血浆标本。收集奥希替尼治疗前基线(BL)和进展时收集的配对血浆DNA样本进行NGS检测以分析奥希替尼的潜在耐药机制。此外还会分析ctDNA与临床结局(PFS和OS)之间的相关性。中位随访33.1个月。
研究结果
2019年5月至2021年1月期间,共纳入188例患者,其中125例(66%)女性患者,96例(51%)19Del突变阳性患者,109名(58%)无吸烟史患者。共178例患者纳入分析,收集到111例疾病进展(PD)事件。与既往报告一致,患者的中位PFS和中位OS分别为19.1个月和36.0个月。奥希替尼治疗19Del突变阳性患者和L858R突变阳性患者的PFS和OS有差异,中位PFS分别为23.3个月和17.2个月,HR为1.56(95% CI:1.08-2.26),中位OS分别为40.3个月对30.4个月,HR为1.54(95% CI:0.98-2.45),有显著差异。单变量分析显示,基线合并TP53突变和MET扩增是PFS和OS预后不佳的潜在疗效预测因子。多因素分析显示,基线合并TP53突变是PFS和OS预后不佳的潜在疗效预测因子。85例患者的血浆样本可用于ctDNA分析,结果显示:耐药突变包括3例PIK3CA突变、4例MET扩增、4例TP53突变、2例BRIMP3突变、1例APC突变和2例BRAF突变、还有1例获得性EGFR C797S突变。
研究结论
基线合并TP53突变或可提示奥希替尼一线治疗预后不佳,MET扩增和PIK3CA是常见的获得性耐药机制,继发性EGFR耐药突变的发生率低于既往报道。
1. P. A. Jänne, et al. 2024 AACR, CT017
2. J. Yang, et al. AACR 2024, LB277/22
3. J.-H. Yang, et al. AACR 2024, CT251/10
4. M. Osuga, et al. AACR 2024, 964/5
责任编辑:肿瘤资讯-Nydia
排版编辑:肿瘤资讯-Wendy











 苏公网安备32059002004080号
苏公网安备32059002004080号


