第65届美国血液学会(ASH)年会于2023年12月9~12日在美国圣地亚哥(San Diego)以线下结合线上的方式举行。ASH年会是全球血液学领域最大最全面的涵盖恶性与非恶性血液疾病的国际盛会,每年都会公布和发表世界各国的最前沿的研究进展和突破性临床数据。
弥漫性大B细胞淋巴瘤(DLBCL)是最常见的非霍奇金淋巴瘤亚型。大多数患者通过一线治疗方案可治愈,但仍有30%~40%的患者会面临复发或难治(R/R),此时可选择的方案十分有限。随着维泊妥珠单抗(Polatuzumab vedotin,简称Pola)的问世,DLBCL患者治疗疗效获得历史性突破。本次ASH大会期间展示了一项基于Pola的方案在R/R DLBCL中国患者中的真实世界研究2年更新结果[1]。【肿瘤资讯】特邀研究者——江苏省肿瘤医院冯继锋教授和吴剑秋教授对研究进行解读以及分享治疗观点,以供参考。
观看视频,查看更多精彩内容
江苏省肿瘤医院/南京医科大学附属肿瘤医院党委书记
江苏省肿瘤质控中心主任
国家卫生健康委合理用药专家委员会委员
中国医师协会肿瘤分会副会长
中国抗癌协会常务理事
中国抗癌协会肿瘤临床化疗专委会主任委员
中国抗癌协会淋巴瘤专委会候任主委
中国临床肿瘤学会常务理事、淋巴瘤专委会常委
江苏省抗癌协会淋巴瘤专委会主委
江苏省医学会肿瘤化疗与生物治疗分会候任主委
江苏省预防医学会肿瘤学分会主任委员
江苏省肿瘤医院肿瘤内科-副主任
江苏省抗癌协会淋巴瘤专业委员会副主任委员
江苏省肿瘤防治联盟淋巴瘤专家委员会主任委员
江苏省研究型医院学会淋巴瘤专业委员会副主任委员
中国抗癌协会肿瘤临床化疗专业委员会委员
中国抗癌协会淋巴瘤专业委员会委员
中国老年保健协会淋巴瘤专业委员会常委
中华医学会肿瘤分会康复支持治疗分会委员
中华医学会肿瘤分会转化医学分会委员
南京医学会血液分会委员
DLBCL临床治疗中面临的主要困境有哪些?
DLBCL是最常见的非霍奇金淋巴瘤亚型,占所有NHL的30%~40%。尽管以CD20单抗为基础的R-CHOP免疫化疗方案可显著改善DLBCL的临床结局,但仍约40%的患者无法达到临床缓解[1]。DLBCL的主要治疗困境包括:
复发或难治性:在一线治疗后出现疾病进展和复发的患者,预后都会相对较差,R/R DLBCL患者接受现有的挽救化疗方案联合自体造血干细胞移植(ASCT)巩固治疗仅有10%的治愈率,不适合行ASCT或ASCT后复发患者的预后更差,中位生存期仅6~12个月左右[2]。另外,DLBCL具有高度异质性,预后具有很大差异,侵犯中枢、睾丸等部位的以及很多高危亚型预后更差。
患者年龄和身体状况:研究显示,年龄>60岁的DLBCL患者通常具有更高的肿瘤负荷,重要脏器储备状况较差,导致治疗难度增加。这部分患者更易出现治疗相关的不良事件,如感染、心衰、呼衰以及免疫治疗相关不良反应。国内外指南均将>60岁列为DLBCL治疗的不良预后因素。特别是我国近年来平均寿命延长,目前>60岁患者占比增高。
有限的治疗选择:对于复发或难治的DLBCL患者,可选择的能克服化疗耐药的治疗方案相对有限。近年来,虽然嵌合抗原受体T(CAR-T)细胞治疗的出现使部分R/R DLBCL患者获得持久缓解与长期生存,但CAR-T细胞治疗费用较高、制备周期较长、特殊的不良反应等诸多因素限制了其在临床中的广泛应用[2]。
随着新型药物的不断发展,ADC、单克隆抗体和双特异性抗体等抗体类新药的研发与应用为R/R DLBCL的治疗打开了新局面,特别是抗体药物偶联物(ADC)药物可能成为攻破DLBCL治疗困境的关键:现如今,DLBCL的标准疗法已由单一化疗转变为个体化综合治疗。
如何评价Pola为基石的方案在R/R DLBCL患者中的获益?
ADC是一类通过特异性的单克隆抗体与杀伤性的细胞毒性药物偶联起来的靶向生物制剂,以单抗为载体将小分子细胞毒性药物高效地运输至目标肿瘤细胞。ADC药物结合了靶向性、选择性强的抗体和抗肿瘤活性细胞毒性药物的优势,在保留小分子细胞毒性药物肿瘤杀伤特性的同时,降低小分子细胞毒性药物的脱靶不良反应,提高了抗肿瘤治疗的获益风险比。其中,维泊妥珠单抗(简称Pola)作为一种新兴的ADC药物,可靶向广泛表达于B淋巴瘤细胞表面的CD79b,精准释放细胞毒性药物,具有精确打击DLBCL的能力。近年来,基于维泊妥珠单抗的综合治疗方案,为血液肿瘤患者带来了新的希望。
我们在此次ASH大会上展示了基于Pola的方案在中国R/R DLBCL患者中的真实世界应用结果[3]。
· 通过回顾性研究分析了来自中国4家三级医院开展的同情用药项目的研究数据,共纳入了39例R/R DLBCL患者,治疗方案包括Pola联合利妥昔单抗(Pola+R)或联合苯达莫司汀加利妥昔单抗(Pola+BR),共给药6个周期,每个周期持续21天。
· 结果显示,治疗结束时ORR为38.5%(15/39),中位无进展生存期(PFS)和总生存期(OS)分别为6.6个月(95%CI:3.7~9.6)和15.6个月(95%CI: 3.4~27.9)。需要注意的是,与未完成全部(6个)周期治疗的患者相比,完成6个周期治疗的患者观察到更长的PFS(12.1 vs 3.5个月,P=0.006)和OS(18.8 vs 6.3个月, P=0.001)。
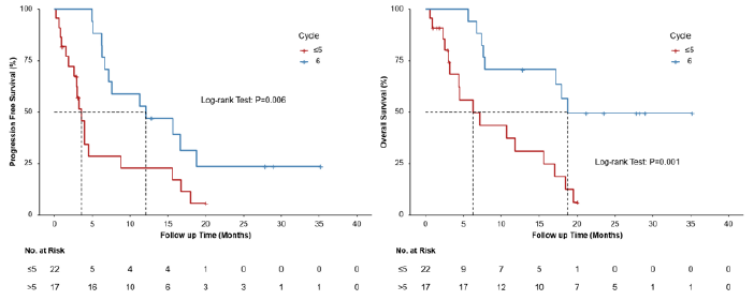 图1 完成与未完成6个治疗周期治疗患者的PFS(左)及OS(右)结果
图1 完成与未完成6个治疗周期治疗患者的PFS(左)及OS(右)结果
2年随访分析显示了基于Pola方案在R/R DLBCL患者中持续的PFS和OS获益,没有新的安全性信号。研究提示基于Pola的完整周期治疗方案可能有助于提高真实世界人群的疗效。我们中心从同情用药项目开始就有患者陆续参加,用药经验相对比较丰富,能看到我们的患者能通过Pola的治疗获得长期生存。综上所述,我们认为Pola为基石的方案在R/R DLBCL患者中具有显著的获益,可为患者提供更多新的治疗选择。
Pola自上市后在国内的应用情况如何?
中国DLBCL患者临床治疗现况[4]:DLBCL是最常见的淋巴瘤亚型,占所有淋巴瘤将近40%。随着规范化治疗的推广和新药的不断研发,DLBCL患者的生存获得了很大的改善。中国DLBCL患者的5年OS率达到38.4%,其中一线接受利妥昔单抗联合含蒽环类药物化疗方案患者5年、10年OS率分别为69%、55.6%,接近欧美国家水平。约60%的DLBCL患者可通过R-CHOP免疫化疗方案治愈,但仍有将近40%的患者面临复发难治。R/R DLBCL患者接受现有的挽救化疗方案联合自体造血干细胞移植(ASCT)巩固治疗10%可以达到治愈,还有很多患者不适合行ASCT,这类患者预后更差,中位生存期仅0.5~1年。近年来, ADC、单克隆抗体和双特异性抗体等抗体类新药的研发与应用改善了这类患者的预后,带来了生存获益。
真实诊疗环境下,Pola在中国DLBCL患者中的临床表现如何?
通过EAP临床试验项目,中国患者在上市前得到了使用维泊妥珠单抗的机会。在真实世界的临床中,Pola治疗中国DLBCL患者观察到较长的生存期。根据我们团队在ASH大会上展示的研究结果,Pola为基础的方案在中国R/R DLBCL患者中的应用已经取得了令人鼓舞的进展。在2年的随访期内,我们观察到了显著的总生存期延长、无进展生存期延长以及较高的完全缓解率。这些结果进一步证实了Pola在真实世界中的疗效和安全性。通过回顾性研究分析了来自中国4家三级医院开展的同情用药项目的研究数据,共纳入了39例复发/难治性(R/R)患者,治疗方案包括维泊妥珠单抗联合利妥昔单抗(Pola+R)或联合苯达莫司汀加利妥昔单抗(Pola+BR),共给药6个周期,每个周期持续21天。结果显示,治疗结束时ORR为38.5%(15/39),中位无进展生存期(PFS)和总生存期(OS)分别为6.6个月(95%CI:3.7~9.6)和15.6个月(95%CI: 3.4~27.9)。如图1所示,与未完成6个周期治疗的患者相比,完成6个周期治疗的患者观察到更长的PFS(12.1 vs 3.5个月,P=0.006)和OS(18.8 vs 6.3个月, P=0.001)。在接受Pola+R的16例患者和接受Pola+BR的23例患者中,完成全部6个治疗周期的患者比例分别为56.3%和34.8%。可以看到,Pola+R依从性更好,完成全部治疗周期患者的比例更高。
一般而言,相较于临床试验,真实世界研究纳入的患者身体机能状态欠佳,既往治疗线数偏多。真实世界研究表明,即使在这类基线较差的患者人群中,基于Pola的治疗方案仍具有良好的有效性和安全性,能改善患者生存。2年随访分析显示了持续的PFS和OS获益,没有新的安全性信号。研究提示基于维泊妥珠单抗的完整周期治疗方案可能为患者带来更好的临床获益。
Pola为基础的方案在DLBCL患者治疗中具有怎样的应用优势?
Pola为基础的方案在DLBCL患者治疗中具有多重优势[4]。
机制优势:Pola是一种ADC药物,将抗CD79b单克隆抗体通过蛋白酶可裂解的连接子与微管抑制剂单甲基奥瑞他汀E(MMAE)偶联,杀伤B细胞淋巴瘤的靶向性更强。CD79b作为B细胞受体复合物的成分,是B细胞NHL的治疗靶标。作为一款靶向CD79b的ADC药物,Pola具有精确的靶向杀伤作用,能够选择性地作用于恶性B淋巴瘤细胞,减少对正常细胞的损伤。
临床应用优势: Pola在临床研究中取得了显著的疗效,并在真实世界的临床实践中得到了充分证实。此外,Pola的用药经验也在不断积累,为临床医生提供了更多的治疗选择和指导。
未来探索: POLARIX研究已证实Pola-R-CHP方案在一线DLBCL患者中的PFS超越R-CHOP标准治疗,这是前所未有的突破。因此,Pola在一线治疗中具有广阔的前景。Pola在中国已上市,并且在指南中也被推荐为优选方案。在预后不好的患者中,特别是那些分期晚期的患者,Pola的应用可能会发挥更大的作用。对于早期患者,是否将Pola纳入一线治疗中,需要根据患者自身的经济条件来考虑。就疗效而言,临床研究和真实世界研究都显示,Pola在DLBCL患者中具有显著的疗效,并且耐受性良好。
对于Pola这款新药,我们需要进行更长时间的观察,以获得更多有益的经验。令人欣喜的是,目前已经有关于Pola与双抗联合治疗方案的临床实验注册启动。我们希望通过强强联合的治疗方式,达到更好的治疗效果和生存改善。随着不断的应用,Pola在临床上的地位将逐渐巩固,将为广大患者提供更多治疗选择,改善DLBCL患者的生存。
Pola在DLBCL中的应用前景及未来探索方向有哪些?
临床试验显示,无论是初治还是R/R DLBCL患者,应用Pola联合方案,均可有效降低疾病进展或死亡的风险,与现有治疗相比,其治疗效果可谓显著。我们对Pola在DLBCL的应用前景充满信心。未来的探索方向和应用前景包括:
· 一线治疗: Pola在初治人群中可以更好地提升一线治疗的疗效,减少疾病复发与进展可能,降低疾病后续治疗负担,同时改善预后。在POLARIX研究中,维泊妥珠单抗联合方案(Pola-R-CHP)一线治疗DLBCL患者较R-CHOP方案显示出PFS方面显著获益[4],因此,早期应用Pola治疗或可帮助控制疾病的进展,提高患者的治疗效果和生存期。Pola未来也可以作为一线治疗方案的基石在不同DLBCL人群中进行更多的探索。
· 联合治疗:Pola可以与其他治疗方法联合应用,以进一步提高治疗效果。例如,与免疫疗法、化疗、靶向治疗方法或其他新机制药物的联合应用可能会产生协同效应,提高患者的缓解率和生存期。2023 ASH大会也发布了一项基于Pola的联合治疗方案,研究显示,Pola与BTK抑制剂如泽布替尼和利妥昔单抗联合组成的ZPR方案在治疗DLBCL方面显示出很好的临床应用潜力[1]。
· 个体化治疗:根据患者的基因型和表型特征,可以探索将Pola个体化治疗应用于DLBCL患者。通过对患者的基因组学和免疫组学特征进行分析,可以预测患者对Pola的敏感性和耐药性,从而实现精准治疗。在2023 ASH会议上报道的POLARIX研究基因亚型的深度分析,显示了EZB亚型和MCD亚型患者中,Pola-R-CHP显示了更优的2年PFS获益趋势[4]。GCB型患者中,一部分具有暗区基因表达特征(DZsig +)患者从Pola-R-CHP治疗中显著获益(HR 0.47,95%CI:0.24~0.95)。因此,COO以外的分子分析可识别可能对Pola-R-CHP有良好反应的DLBCL不同分子亚群,进而达到精准治疗的目的,未来还需要前瞻性临床研究进一步验证。
综上,Pola在DLBCL的应用前景广阔,未来的探索方向包括一线治疗、联合治疗、个体化治疗等。通过不断的研究和临床实践,我们可以进一步提高DLBCL患者的治疗效果和生存期,满足临床需求,造福广大的淋巴瘤患者。
[1] Yuhong Ren, et al. Polatuzumab Vedotin, Zanubrutinib and Rituximab Achieved Rapid and Deep Response in Previously Untreated Frail and Elderly Diffuse Large B-Cell Lymphoma Patients [J]. ASH, 2023.
[2] Pengpeng XU, et al. [Current researches and progresses on new antibody drugs in the treatment of relapsed/refractory diffuse large B-cell lymphoma] [J]. Zhonghua Xue Ye Xue Za Zhi, 2023, 44(3): 259-64.
[3] Jianqiu Wu, et al. Real-World Study of Polatuzumab Vedotin-Based Regimen for Relapsed or Refractory Diffuse Large B-Cell Lymphoma in Chinese Cohort: Updated Results of 2-Year Follow-up [J]. Blood, 2023, 142(Supplement 1): 6265-.
[4] MORSCHHAUSER F, et al. Deciphering the Clinical Benefit of Pola-R-CHP versus R-CHOP in Different Genetic Subtypes Beyond Cell of Origin in the POLARIX Study [J]. Blood, 2023, 142: 3000.
“淋”航之声往期精彩回顾:
【1】【2023 ASH速递】“氏”界新格局——创新药多点布局 引领血液肿瘤治愈之路
【2】【2023 ASH】王黎教授,张薇教授:POLARIX研究深度解析,维泊妥珠单抗赋能一线DLBCL精准治疗
【3】【2023 ASH】刘艳艳教授、邹立群教授:刺破黑暗,照亮新生——双特异性抗体助力B细胞淋巴瘤患者长期生存
【4】【2023 ASH】许贞书教授:奥妥珠单抗联合方案为CLL治疗精准破局,增益深度缓解和长期生存
【5】【2023 ASH】李志铭教授、张会来教授:冲云破雾,突破瓶颈——格菲妥单抗有望成为DLBCL一线治疗的重要利器
【6】【2023 ASH】张曦教授、黄文荣教授:奥妥珠单抗成为惰性淋巴瘤治疗基石药物,扬帆引领治疗新格局
【7】【2023 ASH】刘澎教授团队:曙光已现——Pola-ZR方案助力老年虚弱DLBCL患者打破生存困境
【8】【2023 ASH】白鸥教授、赵杨祉教授:真实世界研究显示,奥妥珠单抗治疗中国非霍奇金B细胞淋巴瘤安全有效
【9】【2023 ASH】金正明教授,邹德慧教授:Pola-R-CHP联合小分子靶向药一线治疗DLBCL强力出击!
【10】【2023 ASH】陶荣教授、王亮教授:策略优化,获益升级——双特异性抗体相关CRS临床管理经验分享
【11】【2023 ASH】周辉教授、张旭东教授:打破局限,持久缓解——双抗Mosunetuzumab治疗侵袭性淋巴瘤彰显潜力
【12】【2023 ASH】景红梅教授、杨萍教授:奥妥珠单抗联合泊马度胺和BTKi治疗TP53突变MCL患者的疗效可期!
【13】【2023 ASH】沈建箴教授、苏丽萍教授:多项探索,全面获益——双抗Mosunetuzumab治疗惰性淋巴瘤彰显实
【14】【2023 ASH】独特靶点,创新机制——罗氏双抗和通用型CAR-T在多发性骨髓瘤的前沿治疗探索!
排版编辑:肿瘤资讯-tong











 苏公网安备32059002004080号
苏公网安备32059002004080号


