慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)是一种具有特异性免疫表型的成熟 B 淋巴细胞克隆性增殖性肿瘤。其主要特点是淋巴细胞在外周血、骨髓、淋巴结和脾脏中聚集,患者多为中老年人。CLL是一种高度异质性疾病。在过去二十年中,药理学家主要聚焦于B细胞受体(BCR)传递信号与CLL的关系。一些相关的靶向药物已被批准用于CLL 患者,其中包括布鲁顿酪氨酸激酶(BTK)抑制剂。一项荟萃分析探讨了新一代BTKi对慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)的疗效和安全性。【肿瘤资讯】特邀山西白求恩医院肿瘤中心的张巧花教授针对该研究结果1进行点评,详情如下。
研究背景
CLL/SLL作为西方国家较为常见的成人白血病,约占美国所有白血病患者的25%~35%。这种疾病在美国白人中更为常见,且以男性为主。患者确诊时的中位年龄约为72岁。
伊布替尼是第一代与BTK不可逆结合的BTKi。在美国,伊布替尼已获批用于治疗CLL。然而,随着研究的不断深入,出血、腹泻和心血管毒性等与治疗相关的不良事件(AE)引起了人们的关注。伊布替尼与其他激酶(如 EGFR、TEC、ITK)的脱靶结合可能是导致这些副作用的原因之一。而新一代BTKi在体内和临床前模型中表现出更强的特异性和持续作用。目前用于治疗CLL的新一代BTKi(如泽布替尼,阿可替尼)具有更高的选择性,且对非靶点激酶的抑制作用较低或无抑制作用。
在本项荟萃分析中,研究者全面检索了与新一代BTKi治疗CLL相关的研究,并分析了其疗效和安全性数据。此外,研究者还通过亚组分析进一步评估了BTKi治疗的疗效,旨在为更合理、有效地应用BTKi提供有力的证据。
研究方法
该系统综述方案已在PROSPERO上注册,注册号为 CRD42023398266。研究者使用主题词与自由词相结合,仔细检索PubMed、Embase、Cochrane Library和 ClinicalTrials.gov,以找出截至2023 年1月31日前发表的相关研究。检索的主题词是“白血病、淋巴细胞、慢性、B细胞”和“BTKi、阿可替尼、泽布替尼、奥布替尼、Tirabrutinib”。
本研究的纳入标准包括纳入标准:
(1) 前瞻性临床研究(包括单臂研究和随机对照试验);
(2) 包括确诊为CLL/SLL患者的研究;
(3) 涉及患者接受新一代 BTKi治疗的研究,包括单药治疗和与其他药物联合治疗;
(4) 同时报告疗效和安全性终点的研究,包括总缓解率(ORR)、完全缓解率(CR)和AEs;
(5) 以英文发表且与人体临床试验相关的研究。而存在“分配给患者的剂量有差异”、“统计方法或实验设计存在重大缺陷”、“重复发表或类似研究”、“文章类型:会议摘要、评论、信件、综述和病例报告”、“报告的信息不完整”、“细胞或动物研究”或“报告了一代BTKi的治疗结果”等问题的研究则被排除。
此外,ORR的定义是CR、CR伴血液学不完全恢复、结节性部分缓解 (PR)、伴有淋巴细胞增高的PR或达到PR患者的比例。CR率包括CR和CR伴血液学不完全恢复。PFS定义为从随机分配日期到患者出现疾病进展或因任何原因死亡的时间,OS定义为为从随机分配日期到因任何原因死亡的时间。
研究结果
通过一系列的筛选和排除,最终有15项研究入选并进行荟萃分析。本项荟萃分析评估了新一代BTKi 对2066例CLL/SLL 患者的疗效和安全性,其中涉及10项单臂研究和5项随机研究。由于部分研究有不止一种疾病状态或干预措施,研究者将其分为20项研究(表1)。
表1.入选研究的基线特征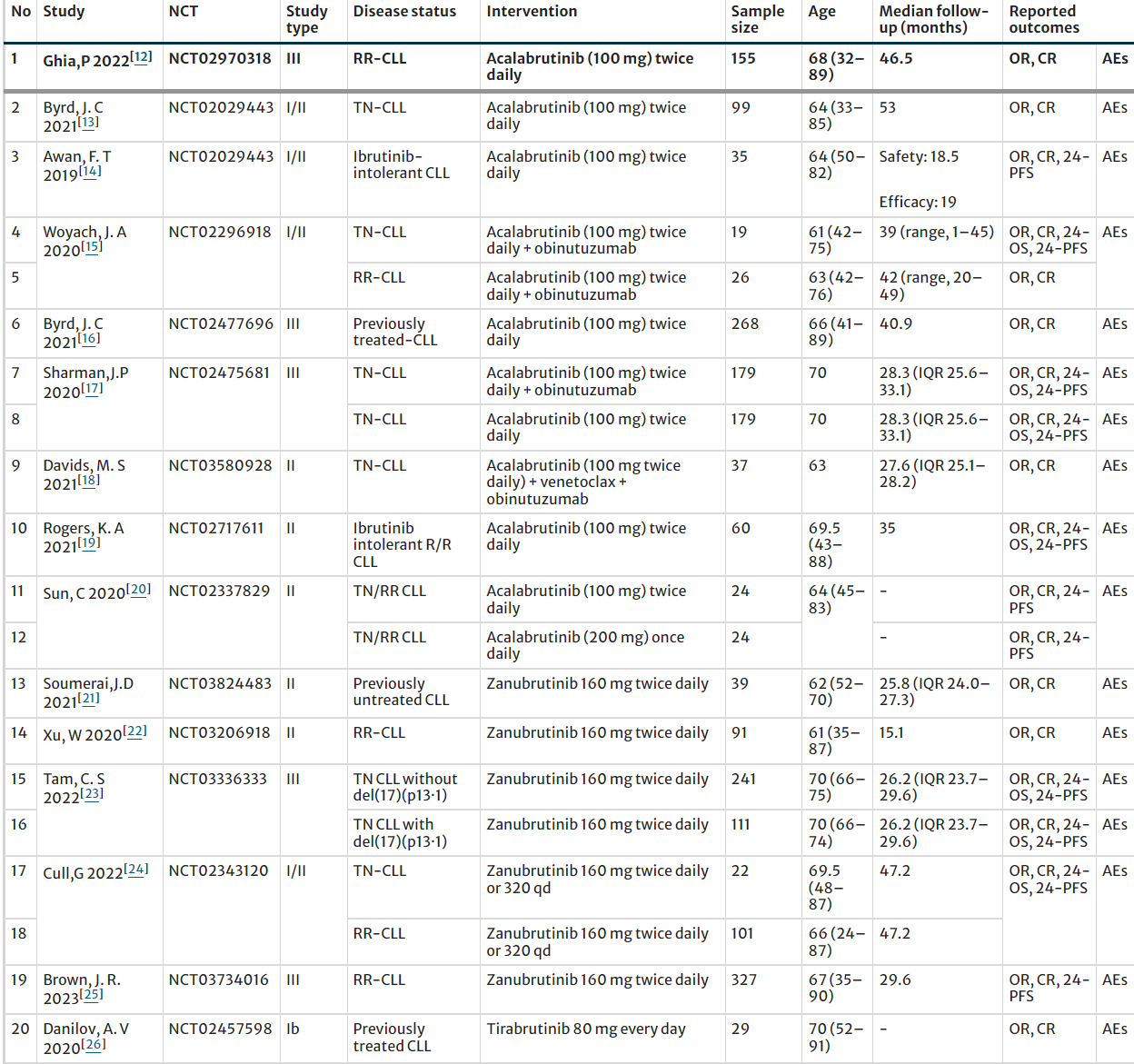
疗效结果
所有入选项研究都将ORR和CR率作为临床结果进行了报告。新一代BTKi的汇总ORR为 92%(95% CI,89%~95%,I2 = 80.68%,P = 0.00),而汇总CR率为 10%(95% CI,6%~14%,I2 = 88.11%,P = 0.00)(图1)。研究者通过随机效应模型进行的分析证实,新一代BTKi治疗CLL的疗效显著。
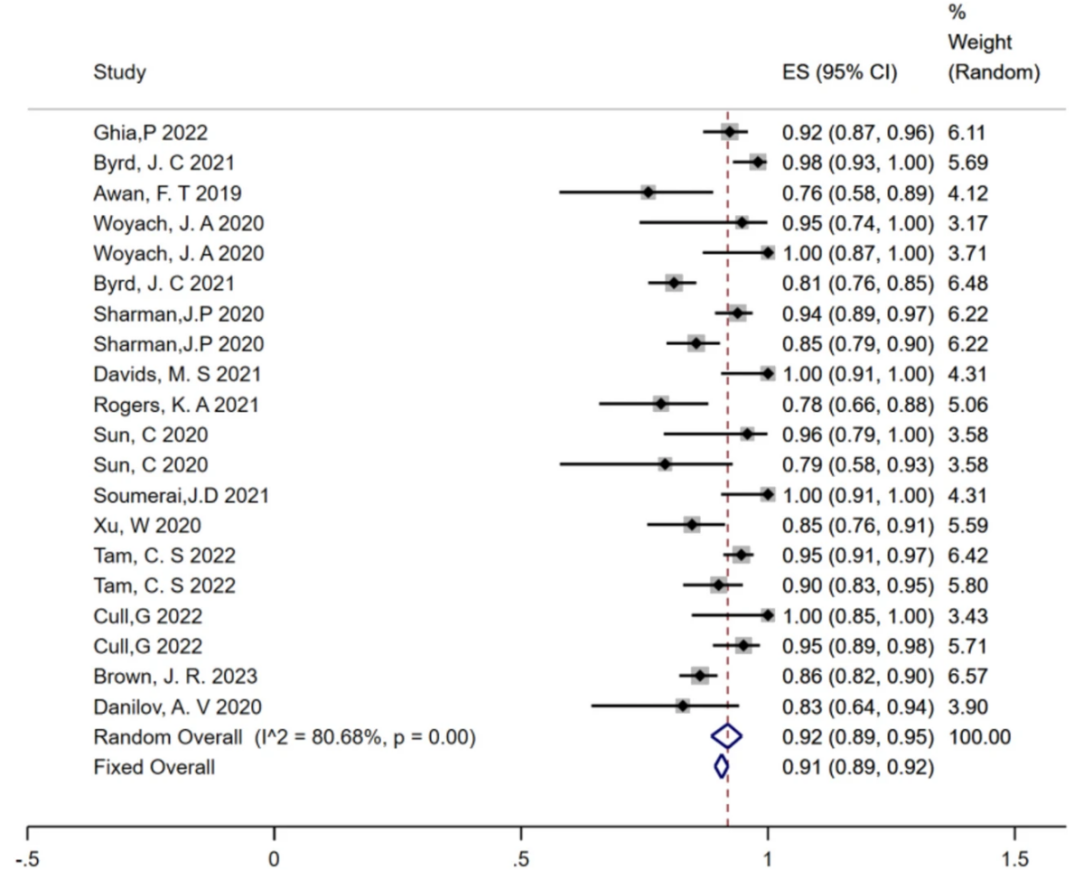 图1.所有研究汇总的总缓解率(随机效应模型)
图1.所有研究汇总的总缓解率(随机效应模型)
基于患者年龄的分析
所有研究均评估了不同年龄组患者的ORR和CR率。研究结果显示,年轻患者(< 65 岁)的ORR(95%,95% CI,88%~99%)似乎高于老年患者(≥ 65 岁)(90%,95% CI,86%~93%)。由于两组患者均表现出异质性,研究者采用随机效应模型进行分析。年轻组患者和老年组患者的CR 率分别为16% (95% CI, 5%~30%, I2 = 90.03%, P = 0.00) 和 6% (95% CI, 4%~10%, I2 = 82.97%, P = 0.00)。汇总结果显示,年轻组患者接受治疗后的疗效结果更好。
基于疾病状态的分析
此外,所有研究均按患者疾病状态(初治CLL vs 复发难治性CLL)列出了BTKi疗法的ORR和CR率。汇总分析结果显示,初治CLL组患者接受治疗后的结果更优(ORR:96% vs 90%,CR率:16% vs 7%)。
基于治疗策略的分析
新一代BTKi与不同治疗措施相结合的亚组分析表明,患者接受不同策略治疗后的总ORR和CR率各不相同。16项研究采用了BTKi单药治疗,汇总ORR为90%。8项研究采用阿可替尼单药治疗,汇总ORR为87%,而7项研究使用泽布替尼单药治疗,汇总的ORR为93%。BTKi单药治疗的汇总CR率为7%,在阿可替尼和泽布替尼亚组中分别为3%和13%。仅有一项研究对Tirabrutinib进行了评估,汇总的ORR为83%,而汇总的CR率为7%。
此外,还有4项研究对261例接受BTKi联合疗法的患者进行评估,汇总ORR为97%,汇总CR率为22%。12项研究报告接受以阿可替尼为基础治疗方案的患者汇总ORR和CR率分别为91%和8%(图2、图3)。
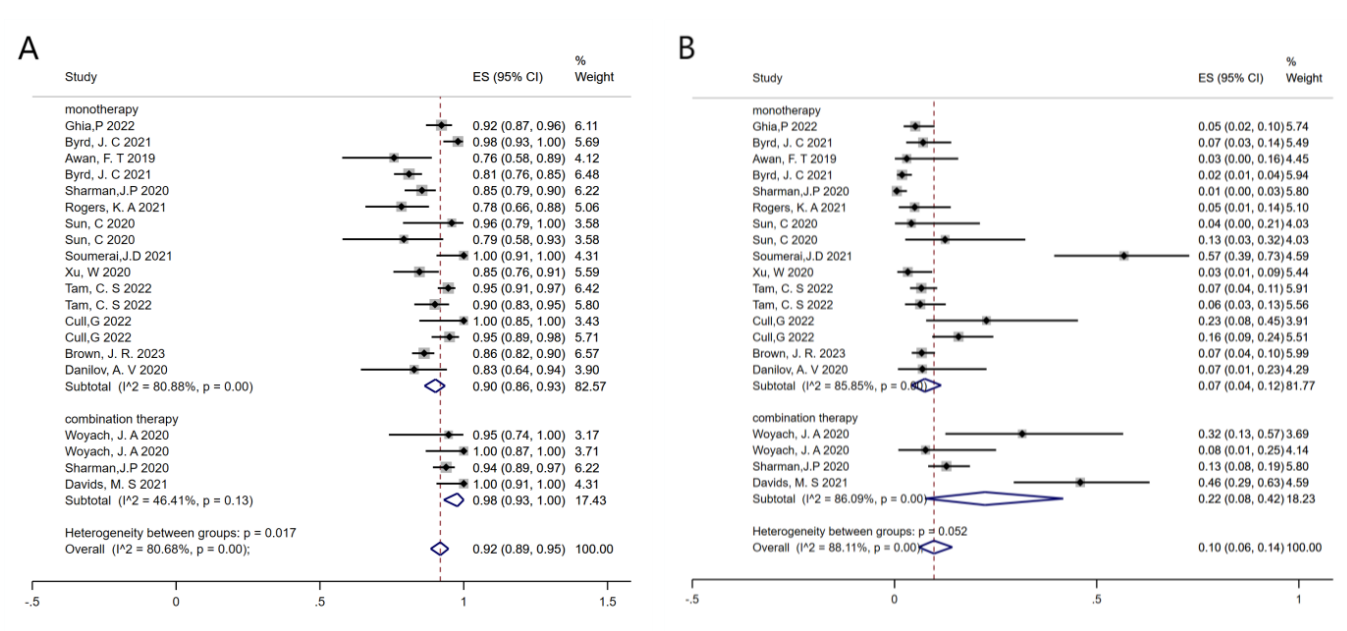 图2.评估不同治疗策略(BTKi单药与 BTKi联合疗法)对(A)ORR和(B)CRR影响的森林图
图2.评估不同治疗策略(BTKi单药与 BTKi联合疗法)对(A)ORR和(B)CRR影响的森林图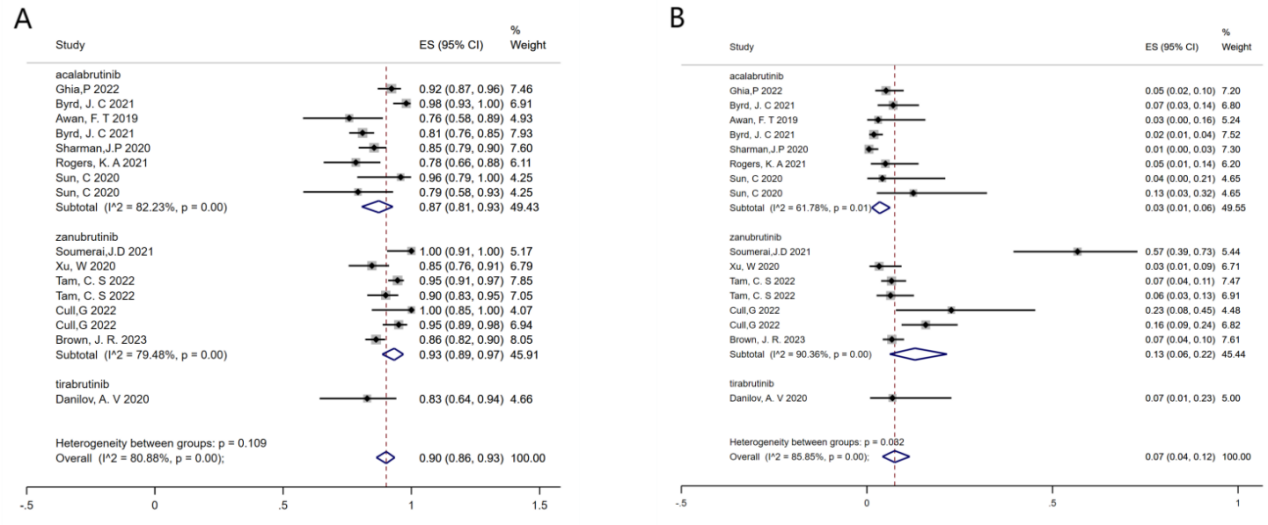 图3.评估不同治疗策略(阿可替尼单药与泽布替尼单药)对(A)ORR;(B)CRR影响的森林图
图3.评估不同治疗策略(阿可替尼单药与泽布替尼单药)对(A)ORR;(B)CRR影响的森林图
生存结果
多项研究报告了患者24个月OS率和24个月PFS率的数据。接受BTKi治疗CLL患者的24个月总OS率为94%(95% CI,92%~97%,I2 = 51.32%,P = 0.06),而24个月PFS汇总率为86%(95% CI,82%~90%,I2 = 72.16%,P = 0.00)。对阿可替尼单药治疗和泽布替尼单药治疗的亚组分析显示,汇总的24个月OS率分别为92%(95% CI,89%~96%,I2 = 0.00%)和95%(95% CI,92%~96%,I2 = 0.00%,P = 0.72)(图4)。而两组24个月的总PFS率分别为83%(95% CI,75%~90%,I2 = 57.74%,P = 0.05)和86%(95% CI,80%~91%,I2 = 77.84%,P = 0.00)(图5)。
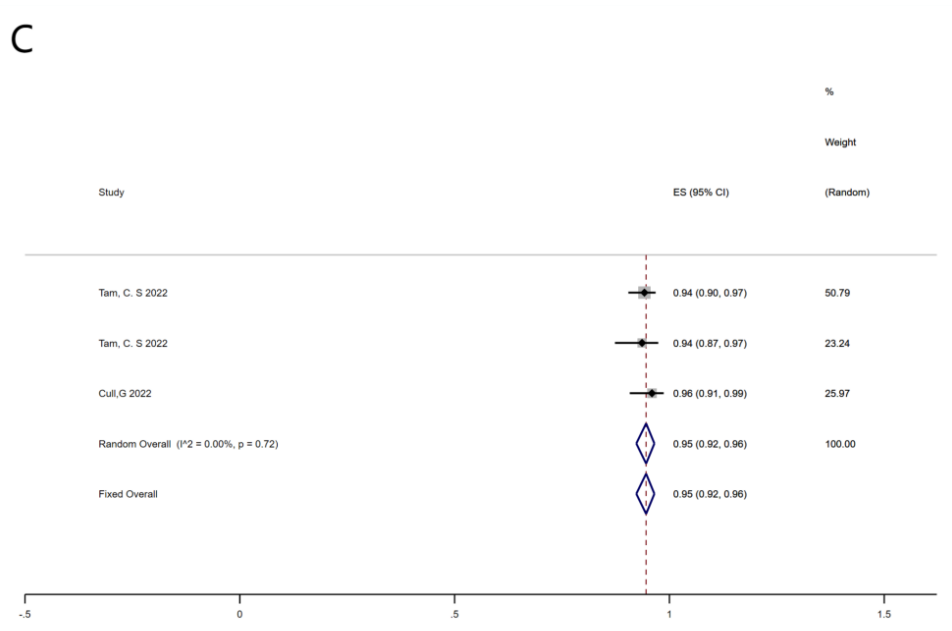
 图4.评估患者24个月OS的森林图(B)阿可替尼单药治疗;(C)泽布单药治疗
图4.评估患者24个月OS的森林图(B)阿可替尼单药治疗;(C)泽布单药治疗

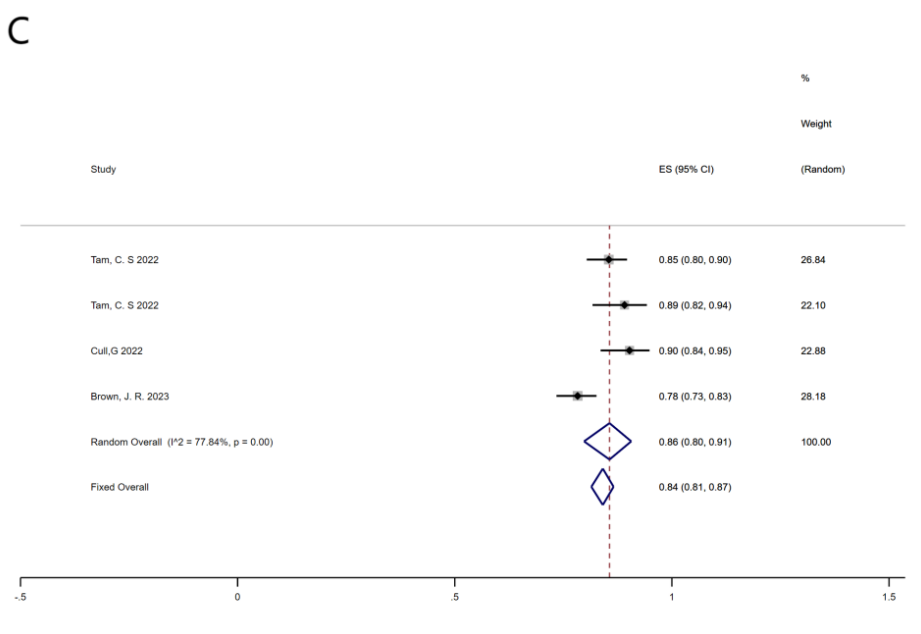 图5.评估患者24个月PFS的森林图(B)阿可替尼单药治疗;(C)泽布单药治疗
图5.评估患者24个月PFS的森林图(B)阿可替尼单药治疗;(C)泽布单药治疗
接受BTKi联合疗法和BTKi单药治疗的亚组24个月的总OS率分别为96%(95% CI,93%~99%,I2 = 0.00%)和93%(95% CI,90%~96%,I2 = 61.88%,P = 0.03),24个月PFS率分别为94%(95% CI,90%~97%,I2 = 0.00%)和85%(95% CI,80%~89%,I2 = 65.28%,P = 0.00)。此外,与复发难治性患者相比,初治患者的24个月总OS率(95% vs. 82%)和24个月PFS率(89% vs. 77%)更高。
安全性结果
所有研究均报告了AEs,而中性粒细胞减少、贫血和血小板减少是主要的血液学AE。严重的非血液学AEs主要包括腹泻、疲劳、上呼吸道感染、心房颤动和高血压。在BTKi单药治疗和BTKi联合治疗的研究中,≥3级上呼吸道感染和心房颤动的合计发生率均为1%。与BTKi联合疗法相比,BTKi单药疗法中≥3级高血压的汇总发生率更高(5% vs 2%)。而BTKi单药疗法研究中其他≥3级AEs的汇总发生率一直较低。
阿可替尼单药治疗亚组的≥3级中性粒细胞减少症、贫血和血小板减少症的汇总发生率分别为14%、7%和5%,而泽布替尼单药治疗亚组中≥3级中性粒细胞减少、贫血和血小板减少的汇总发生率分别为19%、2%和4%。泽布替尼单药治疗亚组的≥3级上呼吸道感染(2% vs 1%)和≥3级高血压的汇总发生率(6% vs 4%)与阿可替尼单药治疗相似,而其他≥3级AE的汇总率均为1%。
研究结论
本项荟萃分析表明,新一代BTKi治疗CLL的总ORR和CR率分别为92%和10%,证实了其良好的疗效。然而,ORR和CR率的I2值分别为80.68%和88.73%,存在较大的异质性。同时,亚组分析结果异质性并没有降低的原因可能是各研究的样本量和个体异质性存在显著差异。根据分析结果,年龄小于65岁患者亚组、TN-CLL患者亚组和BTKi联合疗法亚组的生存结果更佳。亚组分析显示,泽布替尼单药治疗的疗效更好,表明泽布替尼可能是CLL单药治疗的优选。然而,仍需进行头对头研究进一步比较泽布替尼单药治疗和阿可替尼单药治疗的疗效。
山西医学科学院山西白求恩医院肿瘤三科(淋巴瘤科)
省学科带头人,享受国务院特殊津贴
国家科学技术奖励委员会评审专家
中国老年协会淋巴瘤专业委员会副主任委员
中国女医师协会血液肿瘤专业副主任委员
中华中医药学会血液病分会常委
中国血液病精准治疗专委会常委
中国临床肿瘤学会(CSCO)淋巴瘤联盟委员
中国抗癌协会淋巴瘤专业委员
中国抗癌协会血液肿瘤专业委员
山西省抗癌协会淋巴瘤专业主任委员
山西女医师协会淋巴瘤专业主任委员
《白血病·淋巴瘤》杂志编委
历年获山西省科技进步一、二、三等奖共八项。编写论著四部。2008年获中国女医师协会“五洲女子科技奖” 。擅长淋巴瘤、骨髓瘤及白血病的治疗,在“EBV相关的淋巴增殖性疾病”的治疗方面积累了丰富的经验。
张巧花教授:慢性淋巴细胞性白血病(CLL)是一种B细胞恶性肿瘤,其特征是患者的骨髓和外周血中CD5 +和 CD19 + B细胞的克隆聚集。CLL患者的预后差异很大,有些患者病程惰性,终生无需治疗,而有些患者病程迁延,显示出早期治疗指征。虽然异基因造血干细胞移植可以帮助部分CLL患者达到痊愈,但大多数患者并不适合移植,只能通过药物控制病情和症状。
BCR信号通路是CLL发病机制中重要一环,其对于维持CLL细胞的存活、增殖和发展至关重要。通过药物抑制参与BCR通路的激酶(特别是BTK)是目前治疗CLL的标准疗法。虽然一代BTK抑制剂在部分CLL患者中展现出显著的疗效,但其心脏相关的安全性问题不容忽视。而泽布替尼、阿可替尼等新一代共价BTKi对BTK具有更高的选择性和安全性也更佳。既往研究结果显示,与其他疗法相比,新一代BTKi可以为患者带来更为优越的疗效和安全性。
该项荟萃分析进一步证实,新一代BTKi治疗CLL的卓越疗效和安全性。BTKi联合疗法的疗效优于BTKi单药疗法,但其不良事件发生率高于单药疗法。多种药物联合使用可能会增加药物相互作用和副作用的风险。因此,探索更安全的联合治疗策略有望成为未来的研究重点之一。
而对于新一代BTKi单药治疗,泽布替尼可能是CLL单药治疗的更优选择。但在2种新一代BTKi单药治疗期间,患者的心房颤动发生率都很低。未来研究还需要确认采用BTKi治疗CLL的最佳时间。
Yin, S., Zheng, X., Zhang, W. et al. Efficacy and safety of new-generation Bruton tyrosine kinase inhibitors in chronic lymphocytic leukemia/small lymphocytic lymphoma: a systematic review and meta-analysis. Ann Hematol (2023). https://doi.org/10.1007/s00277-023-05486-x
排版编辑:guangli











 苏公网安备32059002004080号
苏公网安备32059002004080号


