BTK 抑制剂的问世,改变了慢性淋巴细胞白血病(CLL)的治疗和管理模式。多个 BTK 抑制剂相继问世,不同共价 BTK 抑制剂疗效基本相当,但由于靶点选择性的差异,安全性特征存在一定的差别。随着 CLL 进入慢病化管理时代,针对不同人群,如何选择合适的 BTK 抑制剂以获得最佳获益-风险比,是临床医生和者共同关注的话题。特别是房颤、高血压、感染、出血等事件,是 BTK 抑制剂需要特别关注和可能导致严重后果的不良反应。阿可替尼在经治 CLL 患者中开展的一项头对头对比一代 BTK 抑制剂的 III 期研究对这个问题给出了部分答案。
【肿瘤资讯】特邀无锡市人民医院周新教授对研究内容进行解读及点评。
阿可替尼对比伊布替尼用于经治 CLL:首个 BTK 抑制剂头对头的 III 期随机对照研究结果
BTK 抑制剂使得 CLL 患者的治疗由传统免疫化疗时代步入了无化疗时代。然而,小分子靶向治疗相对免疫化疗延长 PFS、改善生活质量的同时,也带来了需长期服药的弊端,其长期用药的安全性显著影响患者依从性。此外,对于 CLL 患者而言,中位发病年龄超过 65 岁,多数患者为老年患者,自身合并基础病较多,靶向药的不良事件可能与自身基础病叠加或加重 基础病,也影响患者长期用药依从性。因此,从临床价值出发,在不影响疗效的同时选择更具安全性的 BTK 抑制剂很有必要。
研究背景
布鲁顿酪氨酸激酶(BTK)在 CLL 患者恶性 B 淋巴细胞的存活、增殖和迁移中发挥重要作用,BTK 抑制剂的问世改变了 CLL 患者的治疗格局。一代 BTK 抑制剂在初治或复发/难治性 CLL 患者中均显示了突出的疗效,但随访 5 年因不良反应停药率达 21%,房颤发生率超过 10%,高血压发生率超过 20%,长期用药安全性仍有待提高[1]。BTK 抑制剂导致心血管事件可能与其抑制心肌细胞的 EGFR 以及抑制 PI3K-Akt 信号通路(tec 蛋白酪氨酸激酶途径)[2]或 C 末端 Src 激酶有关[3]。此外,对 BTK 的选择性较低,nm 级别下与 Src 不可逆结合、抑制非 BTK 激酶半胱氨酸残基,导致了其他靶点相关不良事件的发生[4]。
在阿可替尼治疗 R/R CLL 的 II 期研究中,中位随访 53 和 41 个月,AZ 相关导致终止治疗发生率为 6%和 11%,表明阿可替尼在 R/R CLL 患者中具有良好的长期用药安全性。因此,为了验证阿可替尼能否在实现无进展生存期(PFS)非劣于一代 BTK 抑制剂的前提下提高耐受性,开展了 III 期 ELEVATE-RR 研究,以期头对头对比阿可替尼和一代 BTK 抑制剂在经治 CLL 患者中的有效性和安全性。
研究方法
该研究是一项开放、随机、多中心、III 期、非劣研究。主要入选标准包括:1)年龄≥18 岁;2)按照国际 CLL 工作组(iwCLL)标准需要治疗的经治 CLL;3)ECOG 0-2 分;4)存在经中心实验室确认的 del(17)(p13.1)和/或 del(11)(q22.3)。主要排除标准包括:1)患有 严重心血管疾病;2)合并使用华法林或维生素 K 拮抗剂治疗;3)既往接受过 BTK 或 BCL-2 抑制剂治疗;4)需要接受质子泵抑制剂(PPI)治疗。符合入选标准的患者按 1:1 随机分 配至阿可替尼组或伊布替尼组,分别接受阿可替尼 100mg BID 或伊布替尼 420mg QD 治疗直至疾病进展或毒性不能耐受。随机分层因素包括 del(17)(p13.1)状态(有 vs 无)、ECOG 评分(2 vs 0-1)和既往治疗线数(1-3 vs ≥4)。研究期间不允许组间交叉。
主要终点为独立评审委员会(IRC)评估的 PFS,采用 iwCLL2008 标准进行疗效评估,治疗相关淋巴细胞增多缺乏其他进展证据时不视为疾病进展(PD)。次要终点包括任何级别 房颤发生率、≥3 级感染发生率、Richter 转化发生率以及总生存期(OS)。非劣效界值为 30%,HR 界值 1.429。在入组完成和 IRC 评估达 250 个 PFS 事件时进行主要分析。针对主要终点 IRC 评估的 PFS,首先进行非劣分析,采用门控策略将主要终点和次要终点多重检验的总 I 类错误率控制在 0.05。如果首次分析显示阿可替尼非劣于伊布替尼(HR 双侧 95%CI 上限<1.429),在双侧 0.05 水平按下列预设顺序检验阿可替尼的优效性:1)任何级别房颤发生率;2)≥3 级感染发生率;3)Richter 转化发生率;4)OS。如果主要终点未达到非劣或某一次要终点未达到优效,后续终点的 P 值仅作描述性分析。
研究结果
自 2015 年 10 月至 2017 年 11 月,共筛选 808 例患者,15 个国家 124 家中心的 533 例患者随机分配至阿可替尼组(n=268)或伊布替尼组(n=265)。入组患者中位年龄 66 岁(范围:28-89),241 例(45.2%)存在 del(17)(p13.1),342 例(64.2%)存在 del(11)(q22.3)。两组既往中位治疗线数均为 2 线。截至 2020 年 9 月 15 日,阿可替尼组和伊布替尼组分别仍有124 例(46.3%)和 109 例(41.4%)接受治疗。中位随访 40.9 个月(范围:0.0-59.1),达到预设的非劣标准。IRC 评估的两组中位 PFS 均为 38.4 个月(阿可替尼组 95%CI:33.0-38.6;伊布替尼组 95%CI:33.0-41.6;HR 1.00;95%CI:0.79-1.27),包括del(17)(p13.1)、del(11)(q22.3) 以及既往治疗线数在内的特定亚组两组 PFS 均可比。两组中位 OS 均未达到,阿可替尼组和伊布替尼组的死亡事件数分别为 63(23.5%)和 73(27.5%)(HR 0.82;95%CI:0.59-1.15); IRC 评估的客观缓解率(ORR)分别为 81.0%(95%CI:75.8-85.2)和 77.0%(95%CI:71.5-81.6)。两组研究者评估的 PFS、IRC 和研究者评估的无事件生存期(EFS)以及研究者评估的 ORR 均基本相当。
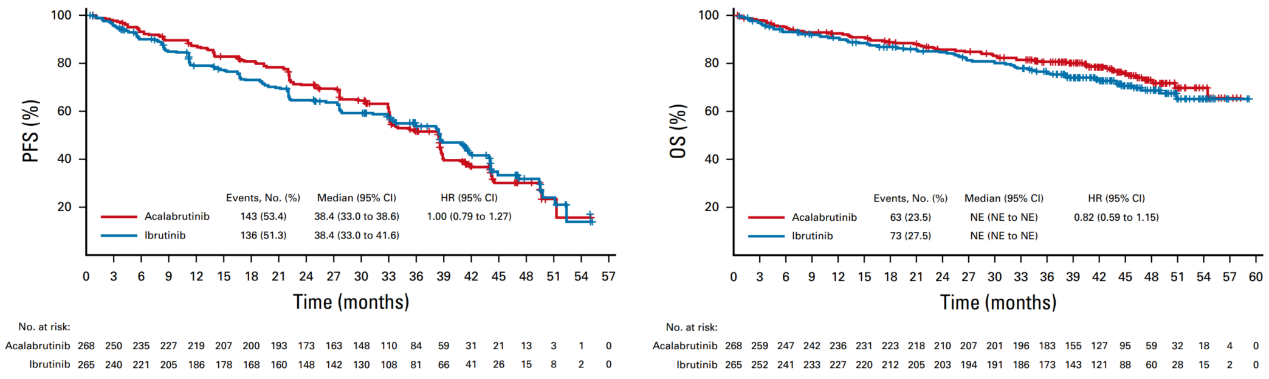 图1 阿可替尼组和对照组 PFS(左)和 OS(右)
图1 阿可替尼组和对照组 PFS(左)和 OS(右)
阿可替尼组和对照组的中位暴露时长分别为 38.3 个月和 35.5 个月,两组≥10%的任何级别常见不良事件(AE)均包括腹泻、头痛、咳嗽、关节痛、便秘、房颤、高血压、泌尿道感染、背痛、肌痉挛和呼吸困难。阿可替尼组和对照组≥3级AE发生率分别为68.8%和74.9%,两组≥5%的≥3 级 AE 均包括血细胞减少症、肺炎和高血压;≥5%的严重不良事件(SAE)均为肺炎(阿可替尼组:10.2%;对照组:9.9%)、贫血(阿可替尼组:5.3%;对照组:4.9%)和房颤(阿可替尼组:2.3%;对照组:5.3%);AE 导致停药率分别为 14.7%和 21.3%。
阿可替尼组任何级别房颤或房扑的发生率明显低于对照组(9.4% vs 16.0%;P=0.02),两组房颤或房扑患者中,分别有 10 例(40.0%)和 5 例(11.9%)既往有房颤病史;15 例(60.0%)和 23 例(54.8%)既往有高血压病史。既往无房颤或房扑病史患者中,阿可替尼组和对照组房颤或房扑的发生率分别为 6.2%和 14.9%。两组房颤导致终止治疗发生率分别为 0 和 2.7%。阿可替尼组总体心脏事件发生率(24.1% vs 30.0%)和高血压(9.4% vs 23.2%)发生率均低于对照组。房颤或房扑累计事件率显示阿可替尼组对比对照组的HR为0.52(95%CI:0.32-0.86), 高血压累计事件率的 HR 为 0.34(95%CI:0.21-0.54),总体心脏事件累计事件率的 HR 为 0.72(95%CI:0.52-1.0)。
阿可替尼组和对照组≥3 级感染的发生率分别为30.8%和 30.0%,Richter 转化发生率分别为3.8%和4.9%[5]。
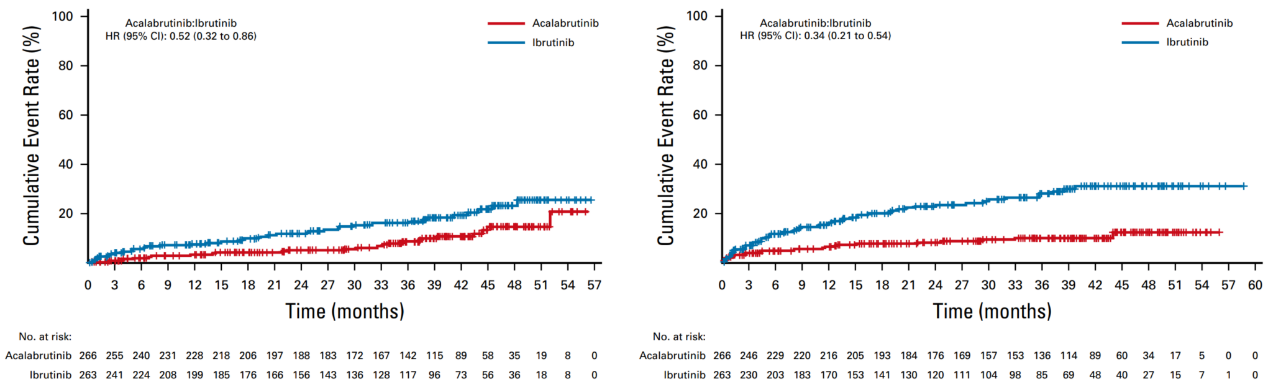 图2 阿可替尼组和对照组房颤(左)和高血压(右)的累计发生率
图2 阿可替尼组和对照组房颤(左)和高血压(右)的累计发生率
研究结论
首个 BTK 抑制剂的头对头研究显示,更高选择性的阿可替尼在 CLL 患者中 PFS 非劣于 一代 BTK 抑制剂,且心血管不良事件发生率显著降低[5]。
专家点评
周新 教授
无锡市人民医院血液科 主任医师
南京医科大学副教授
无锡市血液质控中心主任
CLL 患者多数年龄较大,合并症较多,小分子靶向药物持续用药的治疗模式带来 PFS 获益的同时,也提高了对长期用药耐受性和依从性的要求。我们知道,房颤和高血压可能增加老年人群中风和其他心脏合并症的发病率,导致心血管事件死亡率和全因死亡率增加。不同共价 BTK 抑制剂疗效基本相当,但由于靶点选择性的差异,安全性特征存在一定的差别。在经治 CLL 人群中阿可替尼对比一代 BTK 抑制剂的研究显示,阿可替尼房颤和高血压的发生率都明显降低,或许可以成为这部分 CLL 患者人群在选择 BTK 抑制剂时作为一大参考。在其他选定的次要终点中,3 级或更高级别感染(30.8% vs30. 0%)和 Richter 转化(3.8% vs 4.9%)在两组间具有可比性,两组的中位 OS 均未达到,其中阿可替尼组死亡 63 例(23.5%),对照组死亡 73 例(27.5%)。另外,阿可替尼组 14.7%的患者和对照组 21.3%的患者因不良事件而中断治疗。从目前现有数据来看,阿可替尼与一代 BTK 抑制剂之间的安全性各有千秋。比如,阿可替尼可能会使患者发生头痛、咳嗽,而一代 BTK 抑制剂在腹泻、关节痛、便秘等 AE 方面发生率可能更高。在实际临床工作中,具体治疗选择需要结合患者疾病状态、已有基础疾病、不良反应类型和严重级别以及疾病进展风险等综合评估。
总之,随着 BTK 抑制剂的问世,CLL 的管理模式发生了重大变化,进入慢病管理模式,需要像管理高血压、糖尿病一样进行个体化、长期、综合管理,以延长患者生存,提高患者生活质量。
[1] Jan A Burger, Paul M Barr, Tadeusz Robak, et al. Long-term efficacy and safety of first-line ibrutinib treatment for patients with CLL/SLL: 5 years of follow-up from the phase 3 RESONATE-2 study. Leukemia. 2020 Mar;34(3):787-798. doi: 10.1038/s41375-019-0602-x. [2] Julie R McMullen, Esther J H Boey, Jenny Y Y Ooi, et al. Ibrutinib increases the risk of atrial fibrillation, potentially through inhibition of cardiac PI3K-Akt signaling. Blood. 2014 Dec 11;124(25):3829-30. doi: 10.1182/blood-2014-10-604272.
[3] Ling Xiao, Joe-Elie Salem, Sebastian Clauss, et al. Ibrutinib-Mediated Atrial Fibrillation Attributable to Inhibition of C-Terminal Src Kinase. Circulation. 2020 Dec 22;142(25):2443- 2455. doi: 10.1161/CIRCULATIONAHA.120.049210.
本材料由阿斯利康支持,仅供医疗卫生专业人士参考
审批编号:CN-126640
排版编辑:肿瘤资讯-张钰晴











 苏公网安备32059002004080号
苏公网安备32059002004080号


