乳腺癌是危害我国女性健康的主要恶性肿瘤,其发病率以每年2%的速度增长[1]。2020年,我国新发乳腺癌40万,其中约60%为激素受体(HR)阳性和人表皮生长因子受体2(HER2)阴性[2]。当前HR+晚期乳腺癌的治疗以靶向联合内分泌治疗(ET),特别是细胞周期蛋白依赖性激酶4/6抑制剂(CDK4/6i)联合ET为主[3]。但治疗后的耐药问题是晚期乳腺癌患者普遍面临的困局[4]。
抗体偶联药物(ADC)等靶向药物的出现,为临床提供了新的解决思路。其中德曲妥珠单抗(T-DXd)值得关注,DESTINY-Breast04研究证实T-DXd能够为HER2低表达(包括HR+及HR-)晚期乳腺癌患者带来突破性生存获益[5],使其成为首个在FDA及中国获批用于HER2低表达晚期乳腺癌的ADC[6,7]。另一靶向人滋养细胞表面抗原2(Trop-2)的ADC戈沙妥珠单抗(SG)也在FDA获批了HR+晚期乳腺癌适应证[8]。ADC有望从众多靶向药物中脱颖而出,改变HR+晚期乳腺癌治疗格局,为更多患者带来获益。
CDK4/6i+ET:HR+晚期乳腺癌一线标准治疗
CDK4/6i通过选择性抑制CDK4/6的功能,阻断肿瘤细胞从G1期过渡到S期,进而发挥抗肿瘤作用[9]。PALOMA-3、MONARCH2、DAWNA-1、MONALEESA-3等临床研究确定了CDK4/6i+ET在治疗HR+晚期乳腺癌患者中的地位和作用,基于此,2023CSCO乳腺癌指南推荐「CDK4/6i联合内分泌治疗作为HR+/HER2-晚期乳腺癌患者的一线治疗选择」[10]。
但几乎所有晚期乳腺癌患者在接受CDK4/6i+ET治疗后均会产生耐药,导致疾病进展[4],临床亟需新的治疗策略,以解决后续治疗难题。
后CDK4/6i时代:积极探索多种靶向药物
MAINTAIN研究表明,经CDK4/6i(87%哌柏西利)+ET治疗进展后的HR+/HER2-晚期乳腺癌患者,跨线应用瑞波西利中位无进展生存期(PFS)为5.29个月(对照组:2.76个月),获益具有统计学显著性[11]。而PALMIRA研究则发现,在哌柏西利+ET治疗进展后再次跨线使用哌柏西利+另一种ET二线治疗HR+/HER2-晚期乳腺癌患者,中位PFS为4.9个月(对照组:3.6个月),但该结果无统计学显著性[12]。两项研究的结果提示CDK4/6i+ET进展后再使用CDK4/6i跨线治疗的疗效有限,且获益与否存在争议,不同作用机制的靶向药物或许能为临床提供新的解题思路。
PI3K-AKT-mTOR信号通路异常是介导ET和CDK4/6i耐药的重要原因[4]。TRINITI-1研究证实,对于CDK4/6i治疗进展的HR+/HER2-晚期乳腺癌,mTOR抑制剂依维莫司+依西美坦+瑞波西利方案治疗的24周临床获益率(CBR)为41.1%,满足预先设定的研究终点(10%)[13],靶向PI3K-AKT-mTOR信号通路可能是解决CDK4/6i+ET耐药的潜在策略之一。此外,另一种PI3K抑制剂Alpelisib也在开发中,目前该药在国内暂不可及[4]。
EMERALD研究证实,对于CDK4/6i治疗进展的HR+/HER2-晚期乳腺癌患者,新型内分泌药物——口服选择性雌激素受体降解剂(oral SERD)elacestrant较标准内分泌单药治疗显著延长ESR1突变患者PFS[14],但其适应证在国内暂未获批。
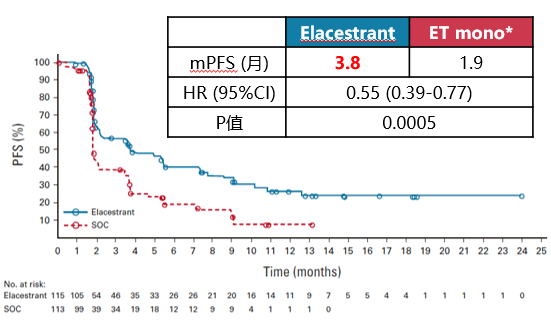 图1:EMERALD研究ESR1突变患者的PFS Kaplan-Meier图[14]
图1:EMERALD研究ESR1突变患者的PFS Kaplan-Meier图[14]
组蛋白去乙酰化酶(HDAC)也是抗肿瘤药物设计的重要靶点[3]。ACE研究表明,对于既往他莫昔芬和/或非甾体芳香酶抑制剂(NSAI)治疗失败的HR+/HER2-晚期乳腺癌患者,HDAC抑制剂西达本胺联合依西美坦较依西美坦单药可显著延长PFS,但ACE研究设计未覆盖CDK4/6i经治患者[15]。后续一项真实世界研究纳入24%的CDK4/6i经治的HR+/HER2-晚期乳腺癌,研究发现西达本胺后线治疗的中位PFS为6.4个月[16]。HDAC抑制剂为克服HR+晚期乳腺癌CDK4/6i+ET治疗后耐药提供了可行路径,但仍需更多循证证据支持。
ADC助力HR+晚期乳腺癌突破耐药屏障
ADC是一类新型肿瘤治疗靶向药物,由单克隆抗体、连接子和细胞毒药物3部分组成,兼具了传统化疗药物对肿瘤细胞的强大杀伤作用以及抗体药物的精准靶向性[17],已发表的关于ADC治疗CDK4/6i经治HR+晚期乳腺癌患者的研究结果十分亮眼。
随机、开放标签、多中心、Ⅲ期临床研究——DESTINY-Breast04(NCT03734029)纳入557例HER2低表达(IHC1+或IHC2+/ISH-),且既往接受过1~2线化疗的不可切除和/或转移性乳腺癌(mBC)患者,其中约70%为CDK4/6i经治HR+患者,以2:1比例随机接受T-DXd(5.4mg/kg,Q3W)或医生选择化疗(TPC)治疗。主要终点为盲法独立中心审查(BICR)评估的HR+队列PFS;关键次要终点为BICR评估的所有患者PFS,以及HR+队列和所有患者的总生存期(OS)[5]。
已发表在《NEJM》的首次分析结果表明,在HR+队列中,T-DXd组和TPC组的中位PFS分别为10.1个月和5.4个月,T-DXd组的死亡风险较TPC组降低36%(23.9个月 vs 17.5个月,HR=0.64)[18]。其中位随访32个月的数据于2023年欧洲肿瘤内科学会(ESMO)年会公布。针对HR+队列的分析结果表明,中位OS与首次分析结果一致,T-DXd组的死亡风险较TPC组降低31%(23.9个月 vs 17.6个月,HR=0.69),T-DXd组的24个月和36个月OS率均高于TPC组(49.0% vs 35.1%;26.5% vs 16.9%),证实T-DXd能够为HR+/HER2低表达晚期乳腺癌患者带来持续生存获益。进一步亚组分析结果证实,对于CDK4/6i经治的HR+晚期乳腺癌患者,T-DXd组的死亡风险较TPC组降低39%(22.3个月 vs 16.8个月,HR=0.71),与HR+整体队列疗效一致[5]。
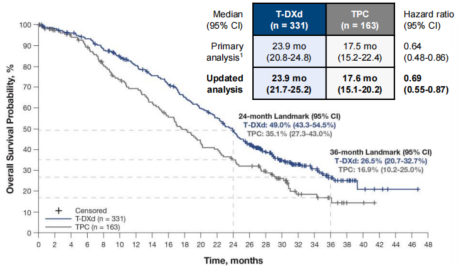 图2:DESTINY-Breast04研究HR+队列的OS Kaplan-Meier图[5]
图2:DESTINY-Breast04研究HR+队列的OS Kaplan-Meier图[5]
靶向Trop-2 ADC SG用于CDK4/6i+ET进展的HR+/HER2-晚期乳腺癌患者的TROPiCS-02研究生存结果近日在《Lancet》发表,与化疗组相比,SG组的疾病进展或死亡风险降低34%(中位PFS:5.5个月 vs 4.0个月,HR:0.66,P=0.0003);SG组的6个月和12个月PFS率均高于TPC组(46% vs 30%;21% vs 7%);与化疗组相比,SG组的中位OS也显著改善(14.4个月 vs 11.2个月,HR=0.79,P=0.020),SG组的12个月、18个月和24个月OS率均高于TPC组(61% vs 47%;39% vs 32%;25% vs 21%)[19,20]。
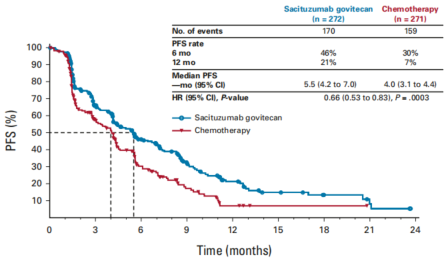 图3:TROPiCS-02研究PFS结果[19]
图3:TROPiCS-02研究PFS结果[19]
总结
目前CDK4/6i+ET仍是HR+晚期乳腺癌的一线标准治疗选择,但其长期应用存在普遍耐药风险,临床正积极寻找新的靶向治疗策略,以优化HR+晚期乳腺癌的后续治疗。众多新型靶向药物中,T-DXd、SG等ADC脱颖而出。值得注意的是,既往被归类为HER阴性的乳腺癌中约60%实际上为HER低表达[5],越来越受到临床的重视,为此2023 ESMO晚期乳腺癌在线指南新增HER2低表达患者分型[21],新近发布的《乳腺癌HER2低表达专家共识2023》也对HER2低表达的定义、诊断和治疗给出了具体意见[22],关注HER2低表达人群,可能为进一步解决HR+晚期乳腺癌耐药提供新的方向。
[1] 张帆,等.CDK4/6 抑制剂治疗 HR 阳性和 HER2 阴性晚期乳腺癌的作用机制研究进展[J].医学综述,2021,27(12):2349-2353.
[2] 初钊辉.老年 HR 阳性/HER2 阴性晚期乳腺癌患者在氟维司群耐药后应用西达本胺治疗的临床观察[J].老年医学与保健,2023,29(04):828-832.
[3] 王佳妮,等.组蛋白去乙酰化酶抑制剂在 HR 阳性 HER-2 阴性晚期乳腺癌的研究进展[J].中国肿瘤临床,2023,50(17):897-900.
[4] 郑秋帆,等.晚期乳腺癌 CDK4/6 抑制剂耐药后的治疗策略与探讨[J].中华医学杂志,2023,103(34):2652-2656.
[5] Shanu Modi, et al. Trastuzumab Deruxtecan (T-DXd) Versus Treatment of Physician’s Choice (TPC) in Patients With HER2-Low Unresectable and/or Metastatic Breast Cancer: Updated Survival Results of the Randomized, Phase 3 DESTINY-Breast04 Study. 2023 ESMO, abstract 376O.
[6] https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-fam-trastuzumab-deruxtecan-nxki-her2-low-breast-cancer
[7] https://www.nmpa.gov.cn/
[8] https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-sacituzumab-govitecan-hziy-hr-positive-breast-cancer
[9] 姜丹丹,等.HR+/HER2+晚期乳腺癌药物治疗方案选择的研究进展[J].中国肿瘤外科杂志,2021,13(6):546-551.
[10] 中国临床肿瘤学会指南工作委员会.乳腺癌诊疗指南 2023[M].人民卫生出版社,北京,2023.
[11] Kevin Kalinsky, Melissa Kate Accordino, Codruta Chiuzan, et al. A randomized, phase II trial of fulvestrant or exemestane with or without ribociclib after progression on anti-estrogen therapy plus cyclin-dependent kinase 4/6 inhibition (CDK 4/6i) in patients (pts) with unresectable or hormone receptor–positive (HR+), HER2-negative metastatic breast cancer (MBC): MAINTAIN trial. J Clin Oncol 40, 2022 (suppl 17; abstr LBA1004).
[12] Antonio Llombart-Cussac, Catherine Harper-Wynne, Antonia Perello, et al. Second-line endocrine therapy (ET) with or without palbociclib (P) maintenance in patients (pts) with hormone receptor-positive (HR[+])/human epidermal growth factor receptor 2-negative (HER2[-]) advanced breast cancer (ABC): PALMIRA trial. 2023 ASCO abstr OA1001.
[13] Bardia A, et al. Phase I/II Trial of Exemestane, Ribociclib, and Everolimus in Women with HR +/HER2 - Advanced Breast Cancer after Progression on CDK4/6 Inhibitors (TRINITI-1). Clin Cancer Res. 2021;27(15):4177-4185.
[14] Bidard FC, et al. Elacestrant (oral selective estrogen receptor degrader) Versus Standard Endocrine Therapy for Estrogen Receptor-Positive, Human Epidermal Growth Factor Receptor 2-Negative Advanced Breast Cancer: Results From the Randomized Phase III EMERALD Trial [published correction appears in J Clin Oncol. 2023 Aug 10;41(23):3962]. J Clin Oncol. 2022;40(28):3246-3256.
[15] Jiang Z, Li W, Hu X, et al. Tucidinostat plus exemestane for postmenopausal patients with advanced, hormone receptor-positive breast cancer (ACE): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol. 2019;20(6):806-815.
[16] 孙正魁,江泽飞. 2022版《中国临床肿瘤学会乳腺癌诊疗指南》更新解读 [J]. 中国肿瘤外科杂志, 2022, 14 (03): 212-218.
[17] 中国药学会医院药学专业委员会,等.抗体偶联药物安全性跨学科管理中国专家共识[J].中国医院药学杂志,2023,43(01):1-10+60.
[18] Modi S, Jacot W, Yamashita T, et al. Trastuzumab Deruxtecan in Previously Treated HER2-Low Advanced Breast Cancer. N Engl J Med. 2022;387(1):9-20.
[19] Rugo HS, Bardia A, Marmé F, et al. Sacituzumab Govitecan in Hormone Receptor-Positive/Human Epidermal Growth Factor Receptor 2-Negative Metastatic Breast Cancer. J Clin Oncol. 2022;40(29):3365-3376.
[20] Rugo HS, et al. Overall survival with sacituzumab govitecan in hormone receptor-positive and human epidermal growth factor receptor 2-negative metastatic breast cancer (TROPiCS-02): a randomised, open-label, multicentre, phase 3 trial. Lancet. 2023;402(10411):1423-1433.
[21] https://www.esmo.org/living-guidelines/esmo-metastatic-breast-cancer-living-guideline
[22] Tarantino P, et al. ESMO expert consensus statements (ECS) on the definition, diagnosis, and management of HER2-low breast cancer. Ann Oncol. 2023;34(8):645-659.
声明:本文材料由阿斯利康提供支持,仅供医疗卫生专业人士参考
审批编号:CN-126185
排版编辑:肿瘤资讯-高惠











 苏公网安备32059002004080号
苏公网安备32059002004080号


