 【丁培荣教授讲难治性肠癌】系肿瘤资讯于2023年8月开展的专栏,本专栏将具有代表性的难治性肠癌病例讨论部分搬到网络进行连载,旨在为全国肿瘤医生提供一个学习平台,深化对难治性肠癌诊断和治疗的理解,将最新的科学研究和临床证据结合到日常实践中,最终造福为广大的肿瘤患者。
【丁培荣教授讲难治性肠癌】系肿瘤资讯于2023年8月开展的专栏,本专栏将具有代表性的难治性肠癌病例讨论部分搬到网络进行连载,旨在为全国肿瘤医生提供一个学习平台,深化对难治性肠癌诊断和治疗的理解,将最新的科学研究和临床证据结合到日常实践中,最终造福为广大的肿瘤患者。
导读
1)病例简介:本文报告一例RAS野生型乙状结肠癌侵犯左侧附件、输尿管及左盆壁和腹膜后,并肝、肺、腹膜后淋巴结多器官转移的患者,通过多学科综合治疗,获得R0切除的机会,最终达NED状态。
病史简介
1)病史摘要:
a) 初诊时间:2022年1月
b) X患者,女,46岁。
c) 患者7月前因“便血2天”就诊于当地医院,肠镜检查示:乙状结肠肿物,病理提示中分化腺癌;腹部增强CT提示:乙状结肠癌侵犯左侧附件、输尿管并腹膜后淋巴结转移。后进一步于当地医院行PET-CT检查示:乙状结肠癌,肿瘤突破浆膜面并向周围浸润,邻近左输尿管受累致左肾积水;肠系膜淋巴结转移,左侧附件区转移瘤,肝转移瘤。现患者为进一步治疗至我院就诊。
d) 既往史:无特殊。
e) 家族史:患者母亲有结肠癌,因心脏病去世,余无特殊。
f) 查体:KPS 70分,浅表淋巴结(-),腹软,无压痛、反跳痛,无肌紧张。未触及腹部包块。肝脾肋下未触及。肠鸣音4次/分,肛门指检(-)。
2)初诊印象:
乙状结肠癌侵犯左侧附件、输尿管、左盆壁和腹膜后,并肝、腹膜后淋巴结多发转移
完善检查
1)实验室检查
2022-01-19肿瘤标志物:CEA 8.07ng/mL; CA199 20.60 U/mL
2)肠镜检查
a) 2022-01-14 本院肠镜:乙状结肠肿物,病理中分化腺癌(图1)
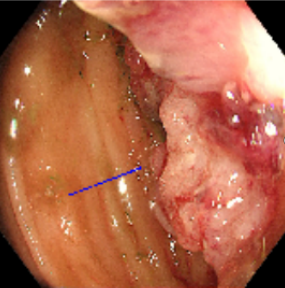
图1. 肠镜提示乙状结肠肿物,堵塞肠腔,内镜无法通过
3)影像学检查
a) 2022-01-14 本院MR:乙状结肠肠壁明显增厚,符合结肠癌,侵犯肠周脂肪间隙,累及左侧输尿管下段,累及左侧卵巢、左侧盆壁、左侧腰大肌及左髂血管。右侧附件区囊实性病灶,考虑转移可能性大。腹腔结节,考虑转移可能性大。结肠系膜区、左侧髂血管旁多发肿大淋巴结,考虑转移瘤。盆腔少量积液。肝多发转移瘤。左肾盂、输尿管明显扩张(图2)。
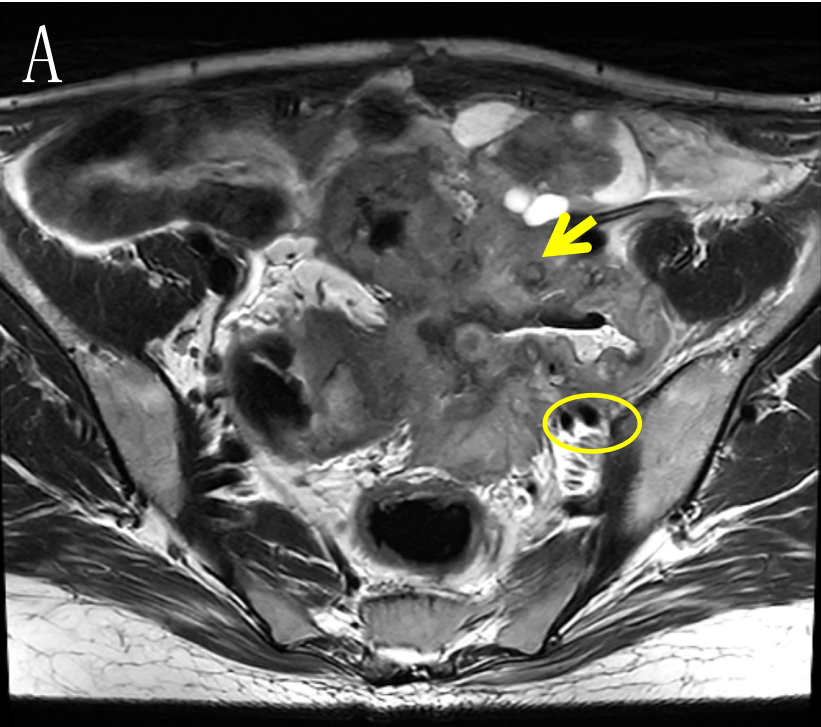
图2 A.乙状结肠肠壁明显增厚,病变累及左侧腰大肌,箭头(→)示左侧输尿管下段受累,圆圈(○)示左髂血管受累
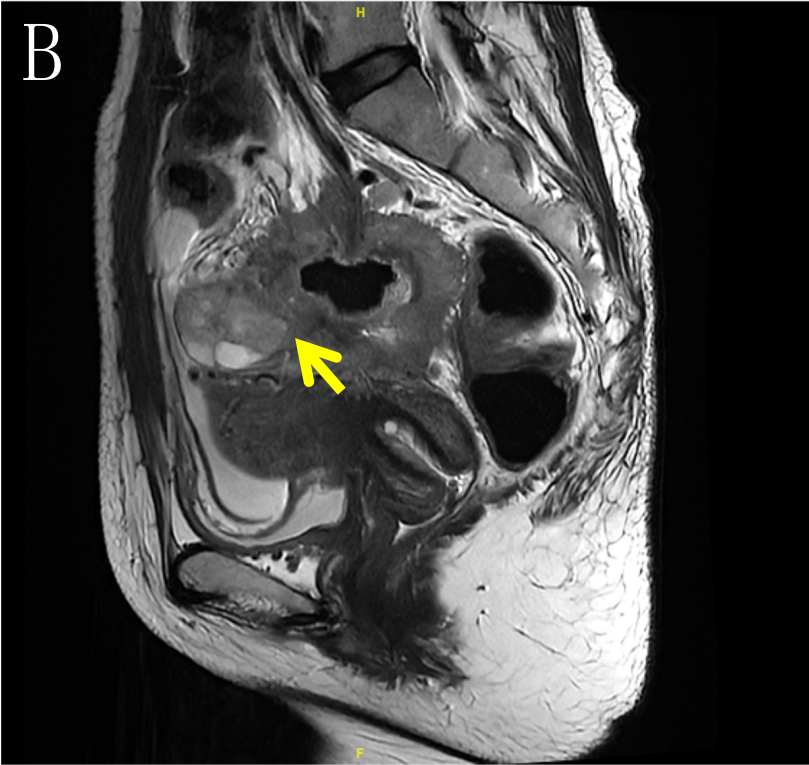
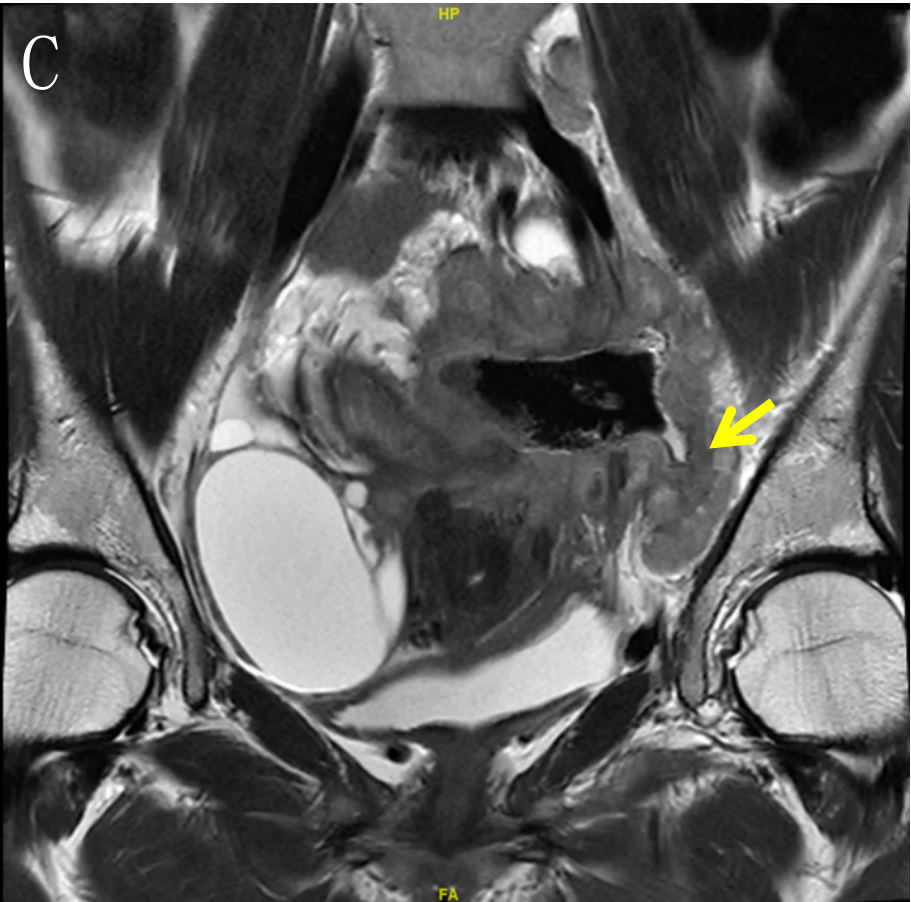
图2 B、C.箭头(→)示病变累及左侧附件
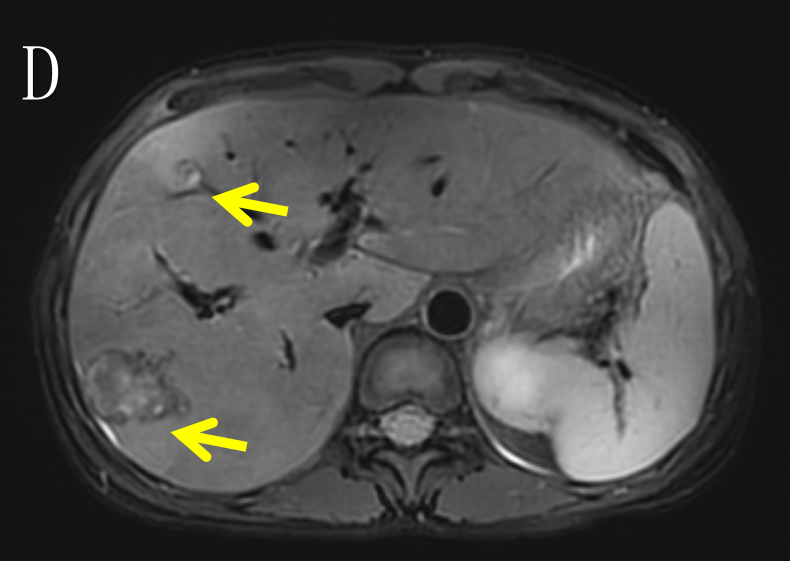
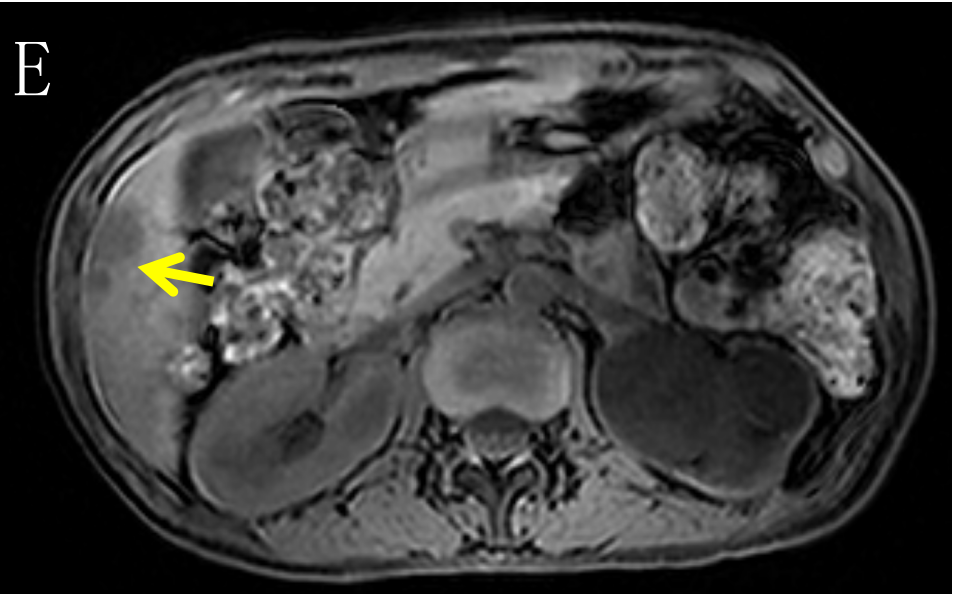
图2 D、E. 箭头(→)示肝多发转移瘤
4)基因检查
2022-01-14 本院二代测序检测结果:肿瘤突变负荷低(TMB-L,9.6 Muts/Mb) 微卫星稳定(MSS);KRAS、NRAS 及 BRAF 为野生型;RNF43 p.Q422Nfs*80 84.6%。
诊断
1)乙状结肠癌侵犯左侧附件、输尿管、左侧盆壁、左侧腰大肌及左髂血管,并腹膜后淋巴结、肝、腹腔种植多发转移 cT4bN+M1c IVc期MSS TMB-L
丁培荣教授查房分析1
1) 意见:
a) 仔细阅片,原发灶侵犯子宫膀胱及左侧盆壁、左卵巢、左输尿管、左侧盆壁、左侧腰大肌及左髂血管,目前无法 R0 切除;肝及腹膜后淋巴结相对局限有机会达到NED。拟采用高强度化疗方案,控制全身肿瘤,降低肿瘤负荷,再争取局部治疗机会。
b) 患者的基因检测结果,KRAS、NRAS 和BRAF 基因都为野生型,MSS,TMB-L;患者身体状况较差,无法耐受三药方案,因此考虑采用FOLFOX两药方案联合西妥昔单抗行转化治疗。
初始治疗
1)一线治疗方案选择:
a) 2022-01-20至2022-06 予FOLFOX(氟尿嘧啶3.25g d1+奥沙利铂110mg d1)+西妥昔单抗680mg d1方案化疗共8程。
2)一线治疗评价:
a) 2022-03-24本院MR(4程后):乙状结肠癌化疗后,对比2022-01-12 MR:乙状结肠肠壁明显增厚,符合结肠癌,范围较前缩小,侵犯肠周脂肪间隙,累及左侧卵巢及左侧盆壁,累及左侧输尿管下段;左肾盂、输尿管扩张积液较前稍加重,积气较前新见。右侧附件区囊实性病灶,考虑卵巢转移瘤可能,较前缩小。盆腔结节,考虑种植转移可能性大,较前缩小。结肠系膜区、左侧髂血管旁多发肿大淋巴结,考虑转移瘤,较前缩小。肝多发转移瘤,肝S4/8囊性病灶较前稍增大,余病灶大部分较前缩小(图3)。
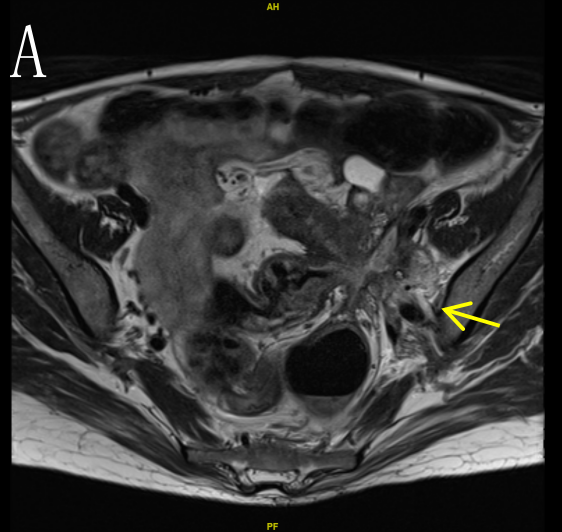
图3 A.箭头(→)示乙状结肠肠壁明显增厚,范围较前缩小
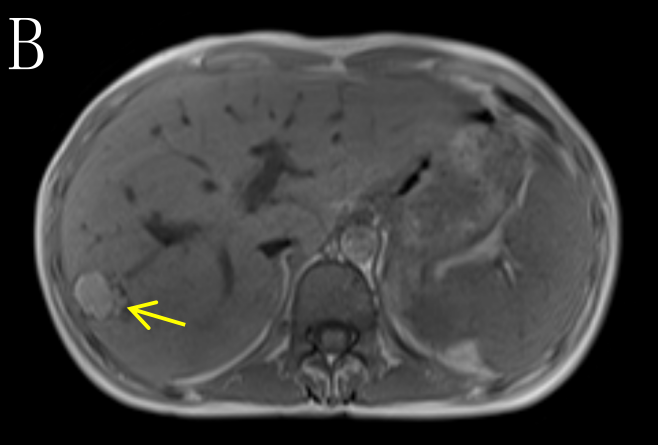
图3 B.箭头(→)示肝转移瘤较前缩小
2022-05-23本院CT(6程后):乙状结肠癌化疗后,乙状结肠病灶,侵犯肠周脂肪间隙,累及左侧卵巢及左侧盆壁,累及左侧输尿管下段,范围较前相仿,符合结肠癌,侵犯周围并感染。左下腹壁脓肿形成,与结肠病变见瘘道形成。左侧上段输尿管壁增厚,左侧输尿管、左肾盂、输尿管扩张、积液、积气,考虑感染。右侧附件区囊实性病灶,考虑卵巢转移瘤可能,较前缩小。结肠系膜区、左侧髂血管旁多发肿大淋巴结,考虑转移瘤,较前相仿。左侧输尿管旁多发淋巴结,转移与炎性相鉴别。肝多发转移瘤,大致相仿(图4)。
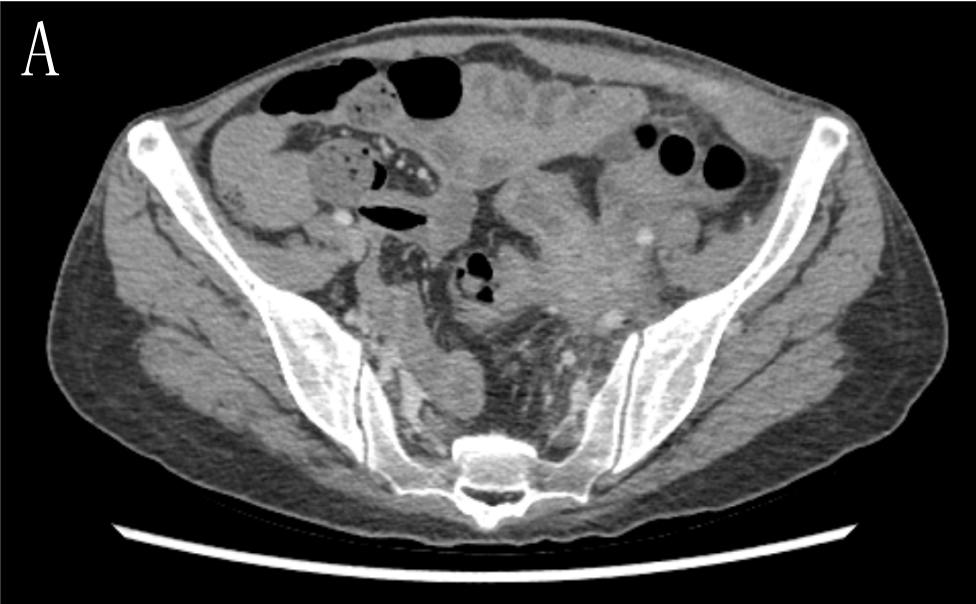
图4 A.原发灶范围较前相仿
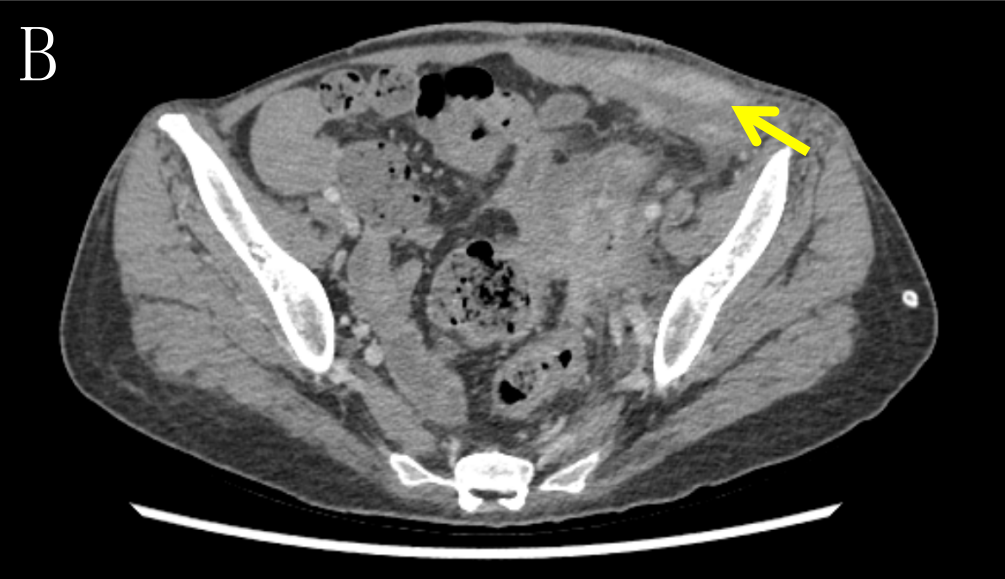
图4 B.箭头(→)示左下腹壁脓肿形成,与结肠病变见瘘道形成
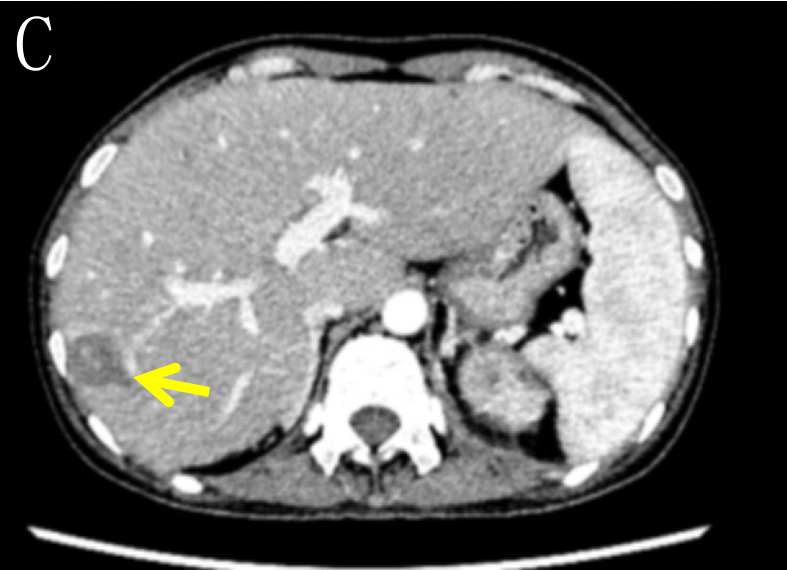
图4 C.箭头(→)示肝转移瘤,较前大致相仿
b) 肿瘤标志物变化及主要毒副反应:CEA持续下降,C4后降至正常,CA199在正常范围内呈波动变化(图5);出现奥沙利铂过敏。主要毒副作用为1-2级手足综合征及3级口腔溃疡。
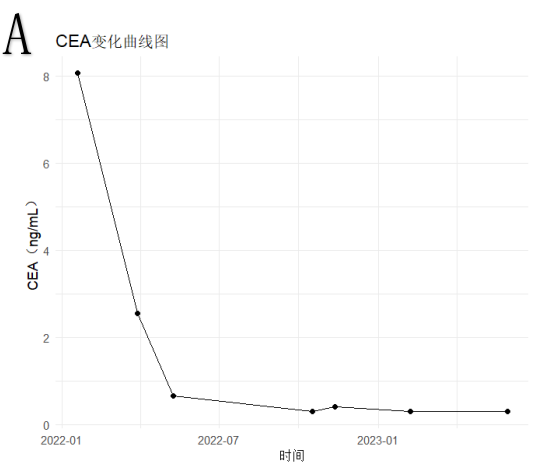
图5 A.CEA持续下降,C4后降至正常
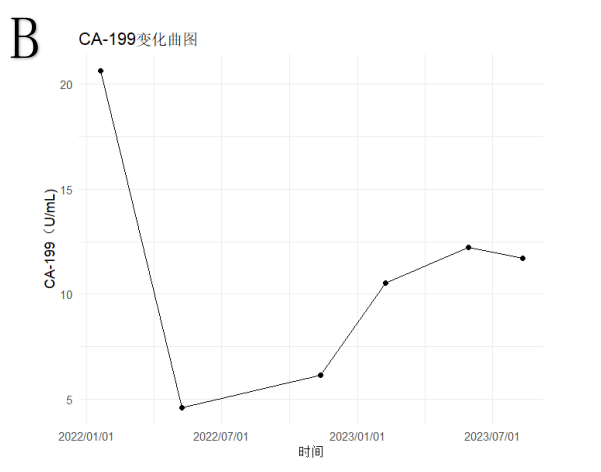
图5 B.CA199在正常范围内呈波动变化
丁培荣教授查房分析2
意见:患者已行8程化疗,总体耐受良好。复查提示原发灶、肝转移灶、左侧髂血管旁多发肿大淋巴结、卵巢可疑转移瘤均较前逐渐明显缩小及减少。患者手术意愿强烈,考虑目前肿瘤仍为T4b,外侵明显,与患者家属充分沟通后,建议原发灶放疗后再行手术治疗,争取NED。
后续治疗
1) 放疗:
患者于2022-6-22 至 2022-7-25 放疗 25 次。治疗期间因发现左侧腰大肌包块,CT检查提示肠癌累及并穿孔,形成局部巨大脓肿,予脓肿穿刺引流后缓解。
于2022-9-20本院 MR,结果示:乙状结肠肠壁明显增厚,肠壁较前稍肿胀,侵犯肠周脂肪间隙,累及左侧卵巢及左侧盆壁,累及左侧输尿管下段,并形成膀胱瘘,膀胱壁肿胀;左肾盂、输尿管扩张积液。原左下腹壁脓肿明显缩小。盆腔腹膜增厚。盆腔积液。结肠系膜区、左侧髂血管旁多发肿大淋巴结,考虑转移瘤,大致同前。肝多发转移瘤,大部分较前缩小(图6)。临床疗效评估:PR,结合患者意愿,争取手术达到NED。
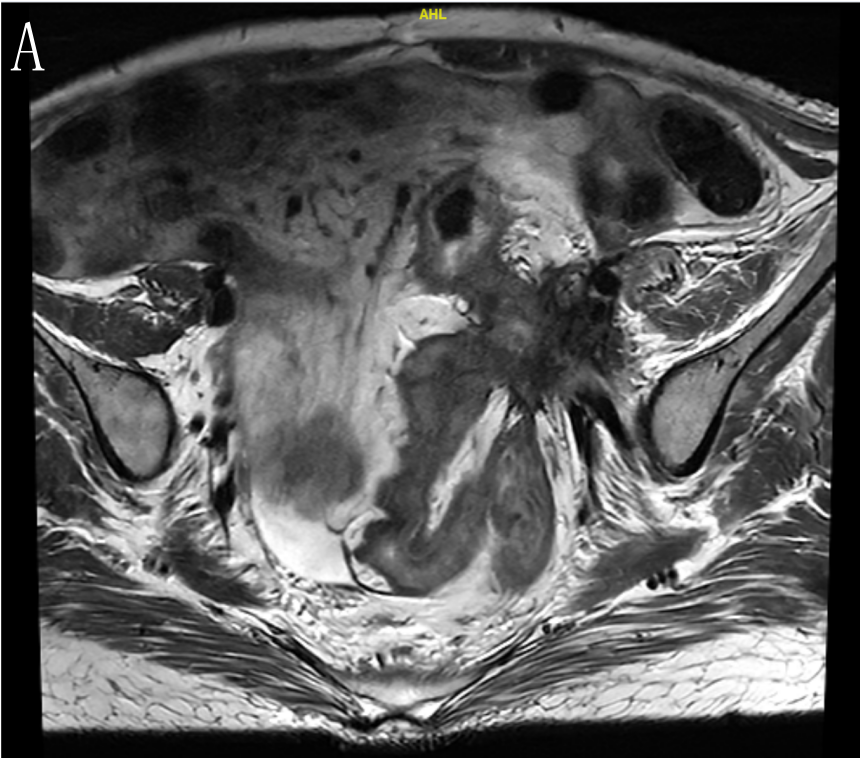
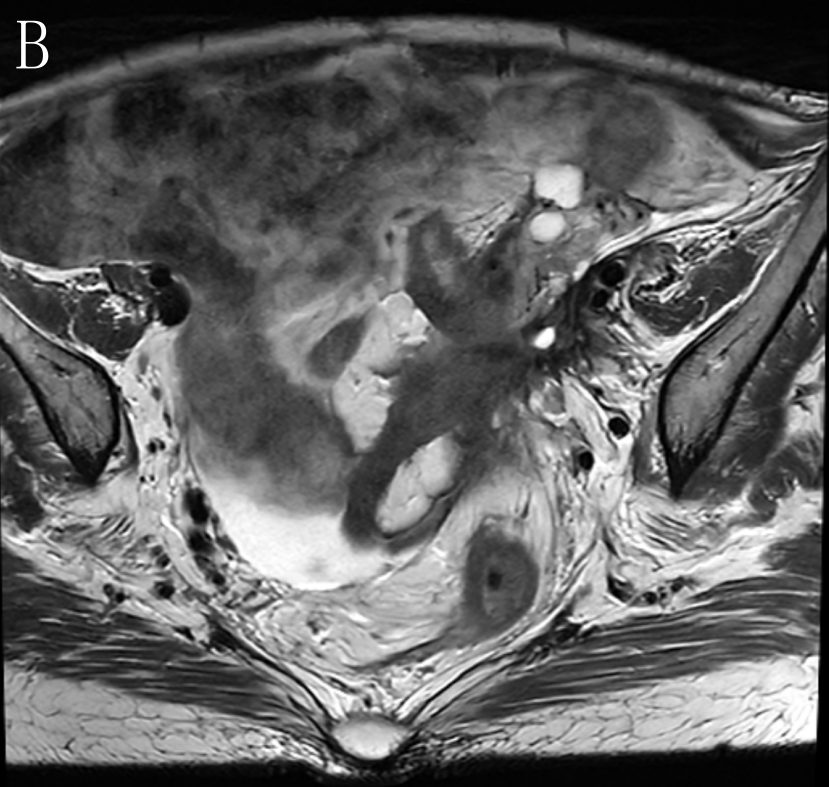
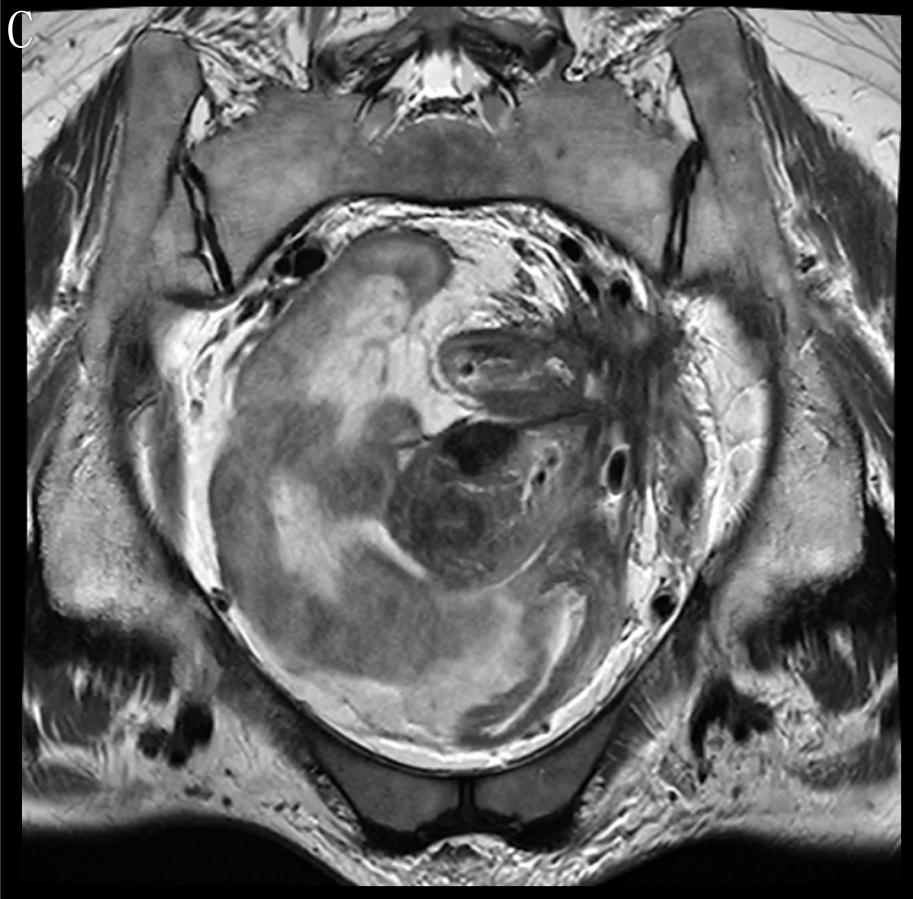
图6 A、B、C.示病灶较前明显退缩
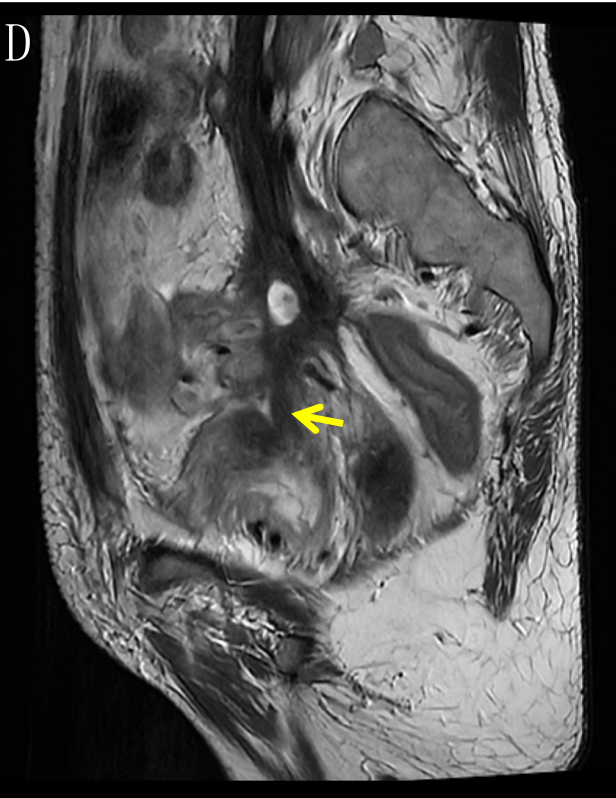
图6 D.箭头(→)示病灶侵犯膀胱并形成膀胱瘘
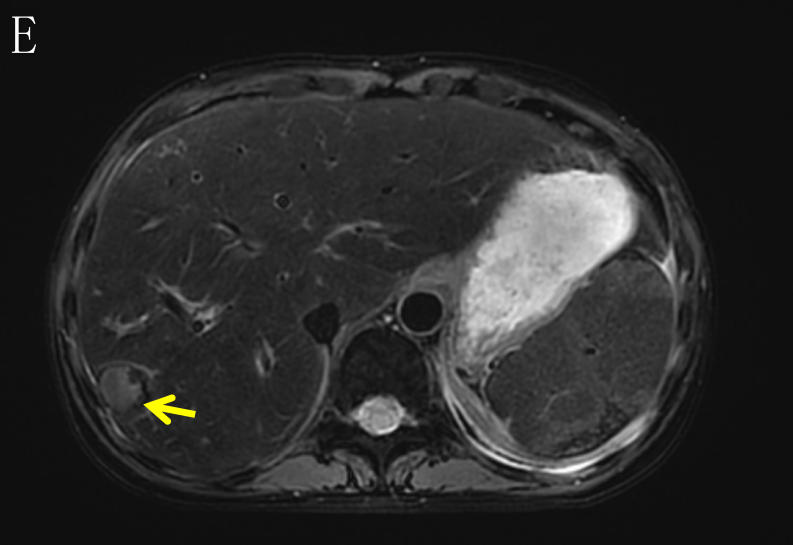
图6 E.箭头(→)示肝转移瘤,较前缩小
2) 手术:
a) 2022-11-09行Dixon术+全子宫双附件切除术+左肾切除术+膀胱部分切除术+左侧髂内血管离断术++回肠造瘘术。术后又行FOLFOX+西妥昔单抗 2程。
术后病理:(乙状结肠及子宫双附件、部分膀胱肿瘤大体)镜下:肠壁肌层及外膜层见少许异型细胞散在分布,结合免疫组化结果,符合肠中分化腺癌伴治疗后改变,累及外膜层;未见明确脉管及神经束侵犯;局灶伴纤维组织增生、组织细胞、淋巴细胞、浆细胞等炎症细胞浸润,可见钙盐沉积及胆固醇结晶形成,符合治疗后改变,未见癌残留,TRG 1级,淋巴结(0/7)。左侧输尿管、双侧附件、膀胱、子宫均未见癌。
b) 2023-02-08行肝转移瘤切除+肝囊肿开窗+腹腔粘连松解+肝肿物微波消融+回肠造口回纳术
肝转移瘤术后病理结果:1(S5段肝转移瘤)、2(肝S6段转移瘤)镜下:肝组织中见中分化腺癌浸润,结合病史及免疫组化结果,符合肠中分化腺癌肝转移。3(回肠造瘘口)镜下见肠壁及皮肤组织,伴慢性炎症细胞浸润,结合临床,符合造口组织,未见癌。
c) 2023-05-29本院复查胸部CT,提示:右肺下叶背段见实性结节,考虑转移可能性大,故于2023-06-12行单孔胸腔镜下右下肺叶楔形切除+肺门,纵隔淋巴结采样术
肺结节术后病理结果:冰冻后石蜡(右下肺结节)镜下:肺组织中见中分化腺癌浸润,倾向为肠腺癌肺转移,可见管内癌栓,未见明确脉神经束侵犯、气道内播散及肺膜累及;楔形切缘未见癌。淋巴结(0/6)。
术后治疗
患者肠癌术后行 FOLFOX+西妥昔单抗治疗 2 程,共行10程FOLFOX+西妥昔单抗方案,总体耐受良好,嘱3个月后复查CT,密切随访。
最近一次复查
2023-8-14 本院CT,结果示:结肠术后改变,子宫及双侧附件术后缺如,局部未见残留或复发征象(图7)。
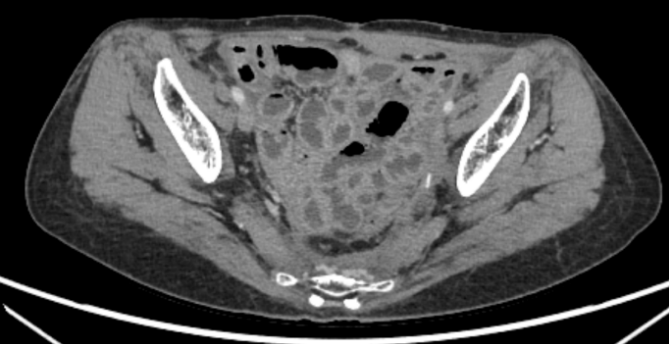
图7.最近一次复查盆腔CT
病例小结
1)诊疗时间轴(图8)

图8. 诊疗时间轴。
2) 诊治心得:
本病例初诊时为晚期乙状结肠癌,侵犯左侧附件、输尿管及左盆壁和腹膜后,并肝、肺、腹膜后多发转移的患者,采用FOLFOX+西妥昔单抗行转化治疗,多次不同部位手术后达到NED,目前患者生存良好,无肿瘤复发转移征象。
本例患者来诊时疾病状态严重,但合理的治疗布局、有效的全身治疗和适时的局部放疗为患者最终获得手术的机会和NED的结果。在治疗过程中,我们也重视对并发症的对症支持治疗。患者治疗过程中多次出现感染、脓肿、无法进食,及时的抗感染、引流、营养支持为其获得后继治疗的机会。如此种种有赖于多学科团队的紧密合作。此外,我们也需要让患者意识到治疗的长期性和复杂性以及家庭社会支持的重要性。
肝转移是结直肠癌患者最主要的死亡原因,未经治疗的肝转移患者的中位生存期仅6.9个月,无法切除患者的5年生存率低于5%,而肝转移灶能完全切除患者的中位生存期为35个月,5年生存率可达30%~57%,本例患者肝转移瘤初始可切除,在肠癌术后接受2程化疗,肝转移瘤进一步缩小,手术得以实现R0切除,大大延长了患者的生存时间。此外,本例患者针对肺转移也适时进行了手术。可以看到,对于多器官转移的患者,有效的全身治疗基础上积极的局部治疗也能让他们获得长期生存的机会。
排版编辑:肿瘤资讯-HYC











 苏公网安备32059002004080号
苏公网安备32059002004080号


