近年来,随着新药或新治疗方案不断涌现,淋巴瘤的远期生存得到明显的提高。为了使淋巴瘤专科医生及时、快速和高效地掌握淋巴瘤领域最关键的新进展,【肿瘤资讯】特邀中山大学附属肿瘤医院黄慧强教授淋巴瘤团队重磅推出【黄慧强 | 淋巴瘤】专栏,欢迎订阅。每月1期,慧强教授与您不见不散!

中山大学附属肿瘤医院大内科副主任
现任中国老年健康协会淋巴瘤专业委员会主任委员
中国CSCO抗淋巴瘤联盟副主席
中国抗癌协会淋巴瘤专业委员会常委
中国抗癌协会淋巴瘤专业委员会青年委员会主委
广东省抗癌协会血液肿瘤专业委员会主任委员
CSCO甲状腺癌专家组组长
NO.1 《英国血液学杂志》(Br J Haematol)初始治疗后第30个月疗效评估为完全缓解的滤泡型淋巴瘤患者预期寿命与西班牙健康人群相似
Magnano L, Alonso-Alvarez S, Alcoceba M,et al.
背景
免疫化疗的应用提高了滤泡型淋巴瘤(FL)患者的生存。近期,初始治疗后第30个月的完全缓解率(CR30)被建议作为无进展生存率的替代指标,本研究对比分析了根据初始治疗后第30个月疗效分组的FL患者与性别、年龄匹配的西班牙一般人群的预期寿命[相对生存率(RS)]。
结果
研究队列包含263例在10年内被诊断为FL、需要接受治疗并接受含利妥昔单抗方案治疗的FL患者,独立验证队列包含693例来自西班牙淋巴瘤和自体造血干细胞移植组(GELTAMO)的FL患者。在研究队列中,188例患者获得CR30,非CR30患者和CR30患者的10年总生存率分别为53%和87%,10年相对生存率分别为73%和100%。CR30患者未表现出预期寿命的缩短。多因素分析表明,FLIPI预后指数是在CR30亚组中预测总生存率最重要的指标。CR30状态对相对生存率的影响在独立的GELTAMO队列中被确证。
结论
接受免疫化疗、第30个月疗效评估为CR的滤泡型淋巴瘤患者与性别、年龄匹配的西班牙一般人群有相似的生存率。
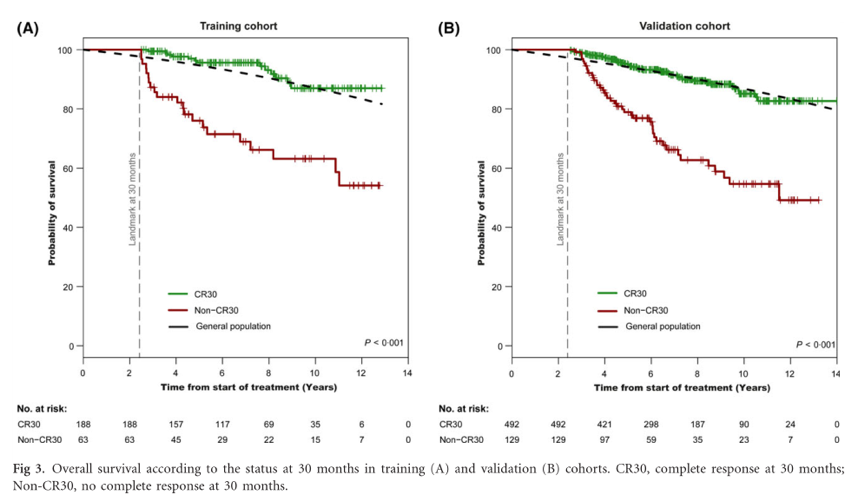
图1. 30个月时的总体生存率:(A)研究队列;(B)验证队列
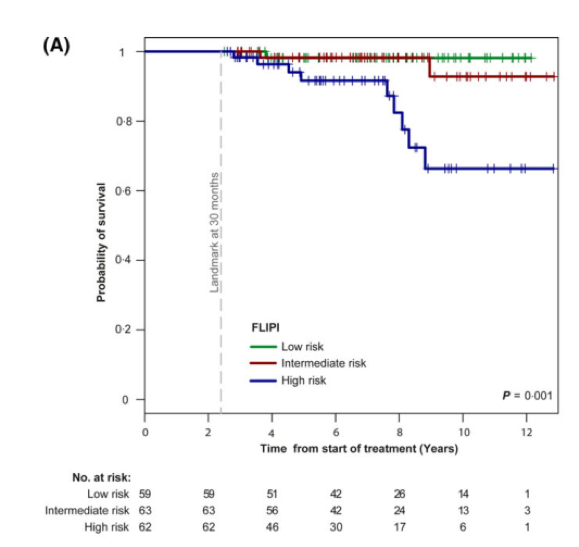
图2. 根据FLIPI评分区分CR30患者的总生存期
翻译:张宇辰;校正:白冰
Br J Haematol. 2019 Feb 22. doi: 10.1111/
NO.2 《英国血液学杂志》(Br J Haematol)转化滤泡性淋巴瘤的预后随着转化的时间和既往治疗的次数而恶化:一项来自意大利林弗米基金会的多中心回顾性研究
Rusconi C, Anastasia A, Chiarenza A, et al
转化滤泡性淋巴瘤(tFL)的最佳治疗尚未完全确定。本研究回顾性分析176例经活检证实的tFL的临床特点和治疗对其术后预后的影响。52%的患者(第1组)在初诊时发生了转化,48%的患者(第二组)在确诊后发生了FL。第1组患者5年总体生存率为84%,第2组患者为51% (P < 0.001)。在第1组中,利妥昔单抗维持治疗后5年无进展生存率优于单纯观察组(94% vs. 53%, P = 0.024)。在第2组中,患者存活率与转化前治疗线数目较多和转化时间较短呈相反趋势。
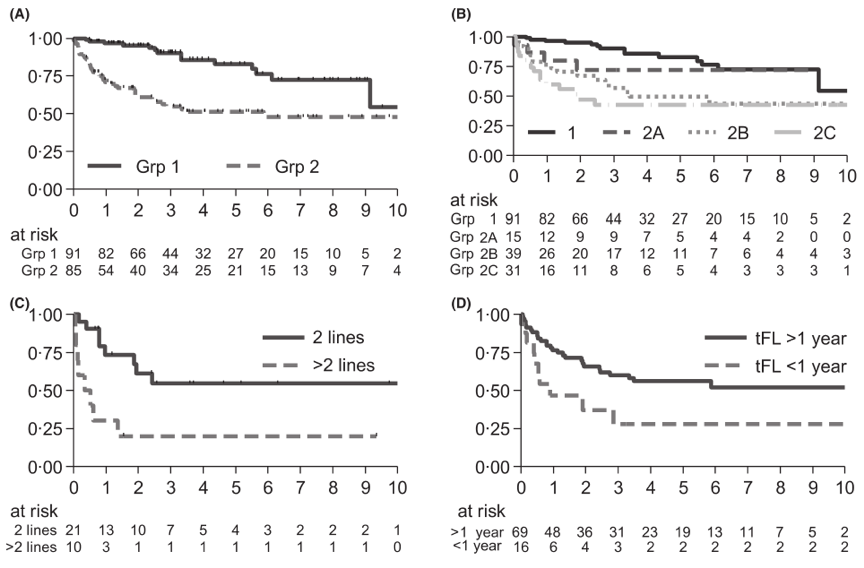
图1 (A)总生存第1组:84%;第二组:51% (P < 0.001); (B)第1组:84%;2A组:72% (P = 0.310);2B组:50% (P = 0.001);2C组:42% (P < 0.001)。(C) 2C组中二线转化:52%;2C组肿二线后转化:20% (P = 0.004);(D) 2A组和2B组患者>转化时间为12个月:56%;2A和2B患者转化时间≤12个月:29% (P = 0.023)。
Br J Haematol. 2019 Feb 21. doi: 10.1111/bjh.15816.
NO.3 《美国医学会杂志·肿瘤学》(JAMA Oncol)自体移植后何杰金和非何杰金淋巴瘤的维持治疗:ASBMT、CIBMTR和EBMT淋巴瘤工作组的共识
Kanate AS, Kumar A, Dreger P, et al
重要性
通常将维持治疗作为淋巴瘤患者自体造血干细胞移植(auto-HCT)后的治疗策略,以减少疾病复发的风险。随着治疗方式不断的发展,维持治疗的新型药物越发在治疗策略中向治疗早期移动,目前缺乏对该治疗方式的具有证据性的指导共识。美国血液和骨髓移植协会(ASBMT),国际血液和骨髓移植研究中心(CIBMTR)和欧洲血液和骨髓移植协会(EBMT)联合召集了一个具有不同专业背景和不同地域代表的专家小组,以对淋巴瘤患者auto-HCT后维持、巩固治疗制定共识。
意见
专家讨论结果遵循德尔菲法,75%投票率以上的项目被视为共识。该过程包括由专家主持的3次独立调查。该专家共识所达成的治疗推荐/建议共22项,涉及的疾病领域包括了霍奇金淋巴瘤(HL)、套细胞淋巴瘤(MCL)、弥漫大B细胞淋巴瘤(DLBCL)及滤泡淋巴瘤(FL)。 A级建议包括:(1)brentuximab vedotin(BV)可作为高危HL维持或联合治疗;(2)在一线治疗后接受auto-HCT治疗的MCL患者推荐利妥昔单抗维持;(3) FL中的建议利妥昔单抗维持;(4)DLBCL中不建议auto-HCT后进行维持治疗。
结论和相关性
在缺乏基于证据的治疗指导方式的情况下,专家组利用德尔菲法有效地提供了一个严格的框架,为淋巴瘤患者auto-HCT治疗后续的维持、巩固治疗提出共识建议。
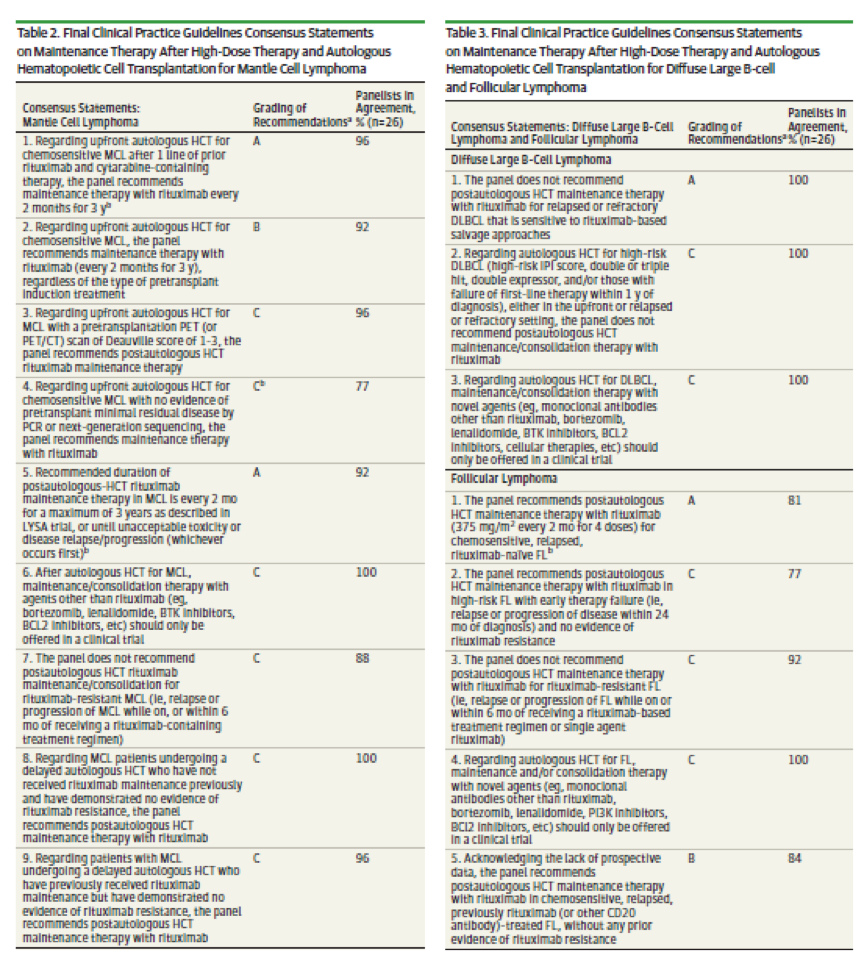
表1.霍奇金淋巴瘤维持治疗共识
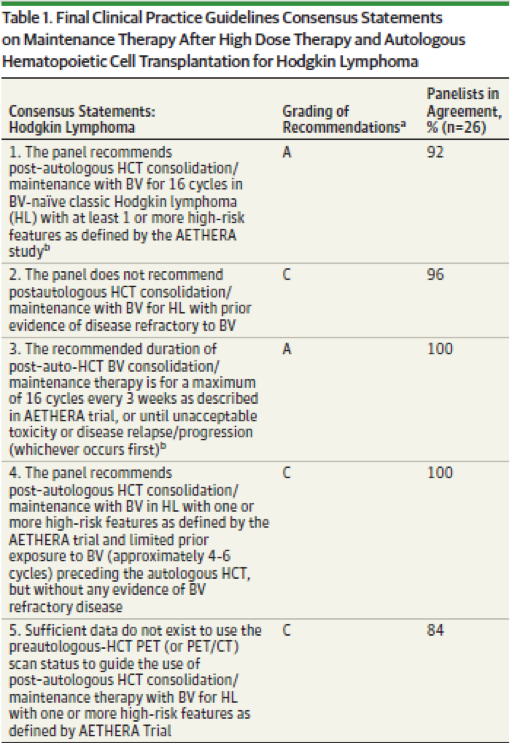
表2 .套细胞淋巴瘤维持治疗共识;表3 .弥漫大B细胞淋巴瘤维持治疗共识
JAMA Oncol. 2019 Feb 28. doi: 10.1001/https://www.ncbi.nlm.nih.gov/pubmed/30816957
NO.4 《美国医学会杂志·网络开放版》(JAMA Netw Open)早期NK/T细胞淋巴瘤放疗后的风险依赖条件生存和失败危险
Liu X, Wu T, Zhu SY, et al
意义
早期结外NK/T细胞淋巴瘤(NKTCL)的预后通常在诊断时被估计和分层,但对于治愈后存活的患者,预后如何随着时间的推移而发展仍是未知的。
目标
根据风险类别、既往存活率和治疗情况,评估条件存活率和随时间推移的失败风险。
研究设计,分组和研究对象
本回顾性队列研究回顾了2000年1月1日至2015年12月31日在中国淋巴瘤协作组多中心数据库中的2015例早期NKTCL接受放疗的患者的临床资料。根据先前建立的预后模型,患者被分为低、中、高风险组。存活患者的中位随访时间为61个月。数据分析时间为2017年12月1日至2018年1月30日。
治疗
所有患者均接受放疗加或不加化疗。
主要研究指标
条件存活率定义为生存概率,患者在规定的时间内存活,并将年度危险率定义为年度事件发生率。
结果
本研究共纳入2015例患者(平均值[标准差]岁,43.3[14.6]岁;1414例(70.2%)男性;1628例(80.8%)患者行放疗加化疗,387例(19.2%)患者行放疗加化疗。5年条件总生存率从治疗开始时的69.1% (95% CI, 66.6%~71.4%)上升到第3年的85.3% (95% CI, 81.7%~88.2%),无失败生存率从治疗开始时的60.9% (95% CI, 58.3%~63.3%)上升到第3年的84.4% (95% CI, 80.6%~87.6%)。治疗开始时,病死率为13.7% (95% CI, 13.0%~14.3%)和治疗失败风险为22.1% (95% CI, 21.0%~23.1%) 3年后分别下降到不到5%(病死率:范围,0%~3.9% [95% CI, 3.7%~4.2%];治疗失败风险:1.2%(95%CI,1.0%~1.4%)4.2%(95%CI 3.9%~4.6%)。
治疗开始时的死亡率在中危患者为(11.4% [95%CI,10.5%~12.3%])和高危患者为(21.6% [95% CI, 20.0%~23.2%]),但3年后死亡率均显著降低(<6%,范围:0%~5.9% [95% CI, 5.2%~6.7%]),而低危患者的死亡率持续低于5%(范围:0%~4.8%);95%CI,4.4%~5.3%)。
高危患者中,放疗联合非蒽环类药物治疗方案与高剂量相关与蒽环类药物治疗方案相比,第3年前的有条件总生存率(:死亡风险比 [HR],1.49; 95%CI,1.13~1.95; P =0.004(初始治疗时);HR,1.60; 95%CI,1.07~2.39; P=0.02(1年时);HR,1.77; 95%CI,0.94~3.33; P=0 .07(2年时)或单独放疗(HR,2.42; 95%CI,1.73~3.39;治疗时P <0.001; HR,1.82; 95%CI,1.05~3.17; 1年时P = 0.03 ;和HR,2.69; 95%CI,1.23~5.90; 2年时P = 0.01)。
结论和相关性
通过这种风险依赖性的方式评估放疗后早期NKTCL患者,其生存概率增加,而失败危害下降。这些动态数据似乎提供了有关疾病过程和持续生存的准确信息,因此其可能有助于研究人员设计其他前瞻性临床试验并制定风险适应性治疗和监测策略。
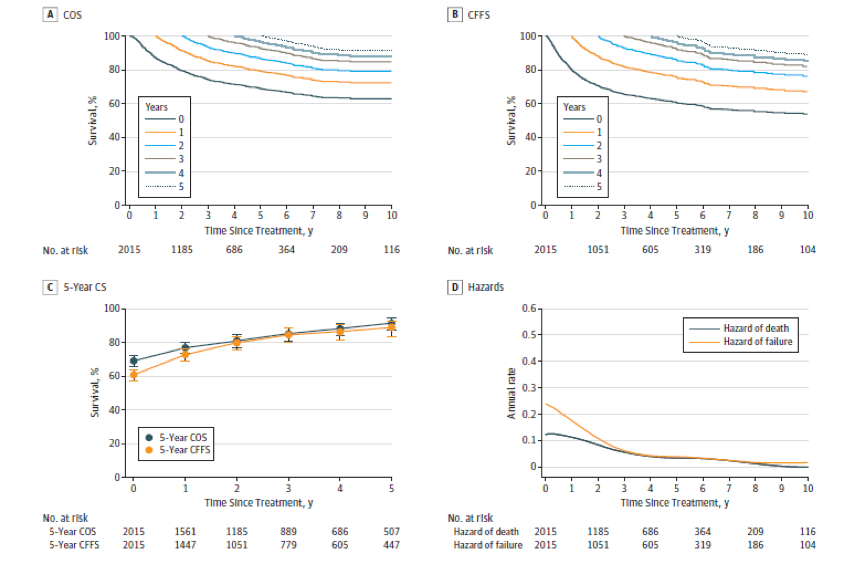
图1.放射治疗早期NK/T细胞淋巴瘤患者的条件生存和每年死亡和失败的危险
JAMA Netw Open. 2019 Mar 1;2(3):e190194. doi: 10.1001
NO.5 《柳叶刀杂志·HIV》(Lancet HIV)免疫抑制和HIV病毒血症与非霍奇金淋巴瘤罹患风险的总体和亚型关系: 在加拿大和美国HIV感染者中开展的一项多中心队列研究
Hernández-Ramírez RU, Qin L, Lin H, et al
背景
非霍奇金淋巴瘤是艾滋病患者的一种常见癌症,为了更好地了解免疫抑制和HIV病毒血症与患非霍奇金淋巴瘤风险之间的关系,我们开展了此项研究,其目标是确定CD4细胞计数和HIV RNA(病毒载量)对预测非霍奇金淋巴瘤总体上和亚型风险的作用。
方法
我们研究了1996至2014年期间加拿大和美国21个参加北美艾滋病研究与设计协作组的艾滋病患者。为了确定关键的独立非霍奇金淋巴瘤预测因素,我们用人口统计学调整后的人口统计学方法、按时间分层的Cox模型,评估了最近、过去、累积和最低值(或最高值)的CD4计数和病毒载量峰值的相关性,并使用赤池信息量准则比较了模型的效能。
结果
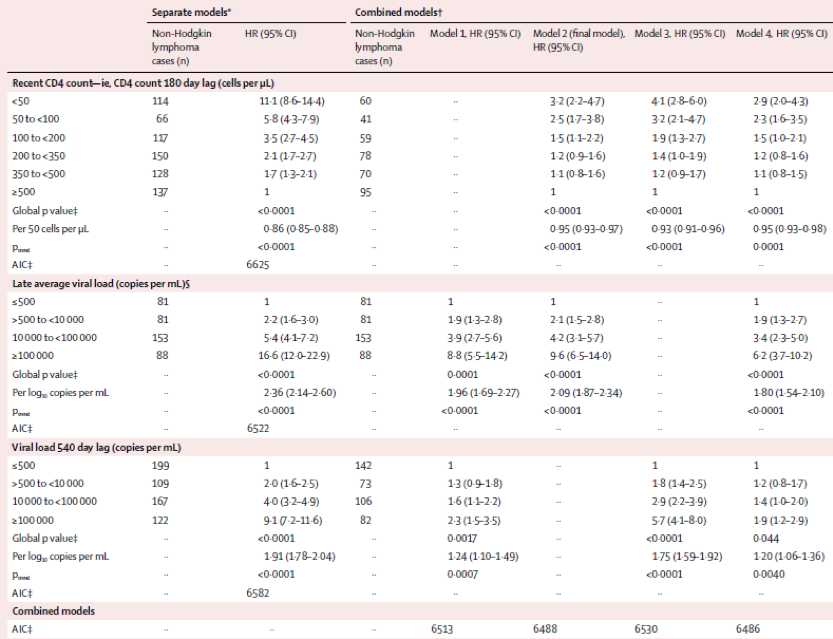
在研究期间中,共有102131人患有艾滋病,其中712人罹患非霍奇金淋巴瘤。预测整体非霍奇金淋巴瘤风险的主要独立预测因素是最近的CD4计数(如:滞后6个月;<50细胞/μL vs. ≥500细胞/μL,危险比为3.2,95%CI 2.2~4.7)。3年的平均病毒载量滞后6个月(累积数≥10万拷贝/mL vs. ≤500拷贝/mL,HR 9·6,95%CI 6.5~14.0)。这些指标也是弥漫性大B细胞淋巴瘤风险的主要预测因素(最近的CD4计数<50细胞/μL vs. ≥500细胞/μL,HR 2.4,95%CI 1.4 ~4.2;平均病毒载量≥10万拷贝 vs. ≤500拷贝/mL,HR 7.5,95%CI 4.5~12.7)。然而,最近的CD4计数是CNS非霍奇金淋巴瘤的唯一危险因素(<50细胞/μL vs. ≥500细胞/μL,HR 426.3,95%CI 58.1~3126.4),在3年窗口时间病毒载量(累积数)比例大于500拷贝/mL是Burkitt淋巴瘤的唯一主要预测指标(100% vs. 0%,HR 41.1,95%CI 9.1~186.6)。
结论
近期的免疫抑制和长期的HIV病毒血症都在非霍奇金淋巴瘤的发展中具有重要的独立作用,并可能存在亚型异质性。早期和持续的抗逆转录病毒治疗减少HIV复制、抑制B细胞活化,以及恢复整体免疫功能是预防非霍奇金淋巴瘤的关键。
表1. 总体非霍奇金淋巴瘤的最佳CD4计数和病毒载量风险预测因子和最终模型
Lancet HIV. 2019 Feb 27. pii: S2352-3018(18)30360-6.
NO.6 《临床肿瘤学杂志》(J Clin Oncol)放疗或自体干细胞移植治疗60岁及以下原发性中枢神经系统淋巴瘤:ANOCEF-GOELAMS组间随机II期PRECIS研究结果
Houillier C, Taillandier L, Dureau S, et al.
目的
化学免疫治疗后接受全脑放疗(WBRT)或大剂量化疗联合自体干细胞移植(ASCT)是原发性中枢神经系统淋巴瘤(PCNSL)的一线治疗方案,本研究的研究目的为明确两种方案的有效性和毒性。
研究对象和方法
将初治且具有正常免疫活性的PCNSL患者(18~60岁)随机分配至诱导化疗后接受WBRT治疗组或联合ASCT治疗组,诱导化疗为 R-MBVP方案(利妥昔单抗 375mg/m2 第1天,甲氨蝶呤3g/m2 第1、15天;VP-16 100mg/m2 第2天; BCNU 100 mg/m2 第3天,泼尼松60mg/kg/kg 第1-5天),随后接受2程的R-AraC方案(利妥昔单抗 375 mg/m2 第1天;阿糖胞苷3g/m2第1至2天)。大剂量化疗包括噻替派(250 mg/m2/d,第-7至-9天),白消安(8mg/kg,第-4至-6天)和环磷酰胺(60 mg/kg/d,第-2至-3天)。WBRT剂量为40 Gy(2 Gy/次)。主要终点为2年无进展生存期。认知程度是主要的次要终点。意向处理分析在非比较的II期阶段试验中进行。
结果
从2008年10月至2014年2月,23个法国中心共招募了140名患者。WBRT和ASCT均达到预定的阈值(每组前38例患者中至少有24例患者在随访2年时处于存活以及无疾病状态)。WBRT组和ASCT组的2年无进展生存率分别为63%(95%CI,49%~81%)和87%(95%CI,77%~98%)。毒性相关死亡WBRT组中1例,ASCT组5例。在认知功能方面,WBRT组中的患者受到损害,而ASCT组未变化或改善。
结论
WBRT和ASCT是治疗60岁及以下PCNSL患者的有效巩固治疗方法。而ASCT组倾向于有更佳的疗效终点。两种治疗模式的具体风险都应充分考虑。
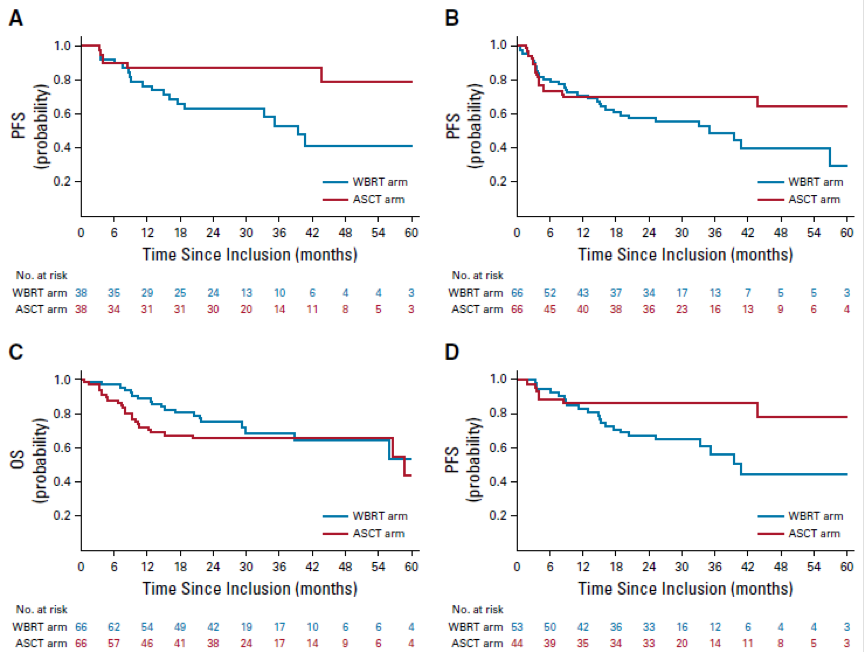
图1. (A)按合并组主要终点人群PFS;(B)ITT人群的PFS;(C) ITT人群的OS;(D) PP人群的PFS
J Clin Oncol. 2019 Feb 20:JCO1800306.
NO.7 《临床肿瘤学杂志》(J Clin Oncol)利妥昔单抗联合苯达莫司汀(BR)对比RCHOP或RCVP在惰性非霍奇金淋巴瘤或套细胞淋巴瘤的一线治疗:在BRIGHT研究的五年生存随访结果
Flinn IW, van der Jagt R, Kahl B, et al.
背景
BRIGHT研究(NCT00877006)旨在比较苯达莫司汀联合利妥昔单抗(BR)与利妥昔单抗联合环磷酰胺、阿霉素、长春新碱、强的松(R-CHOP)或利妥昔单抗联合环磷酰胺、长春新碱、强的松(R-CVP)在治疗初治惰性非霍奇金淋巴瘤或套细胞淋巴瘤患者的有效性和安全性。本文发表了此研究的长期随访数据。
研究对象和研究方法
所有病人治疗结束后的随访时间至少5年,研究者评估并统计研究终点事件的发生时间,包括PFS(无疾病进展生存期)、EFS(无事件生存期)、DOR(持续缓解时间)、OS(总生存期)。
结果
在完成研究时,无论是使用BR、RCHOP/R-CVP的治疗组患者无事件发生时间均未达到中位时间。在BR治疗组的五年PFS为65.5%,而在RCHOP/R-CVP治疗组中为55.8%。两组有显著差异,BR治疗组相比其他两种方案风险比下降(95%CI, 0.45~0.85; P=0.0025,HR 0.61)。在EFS和DOR的评估中,BR方案同样优于RCHOP/R-CVP方案(P=0.0020;P=0.0134),但是两个治疗组之间的五年OS无显著差异。在安全性方面,总体安全性均可预估,在长期随访过程中并无新增的安全性数据。在BR治疗组中发现更高的第二恶性肿瘤发生率。
结论
总而言之,对比RCHOP/R-CVP方案,BR方案作为惰性非霍奇金或套细胞淋巴瘤的一线治疗方案具有更高的远期生存率和疾病控制率。
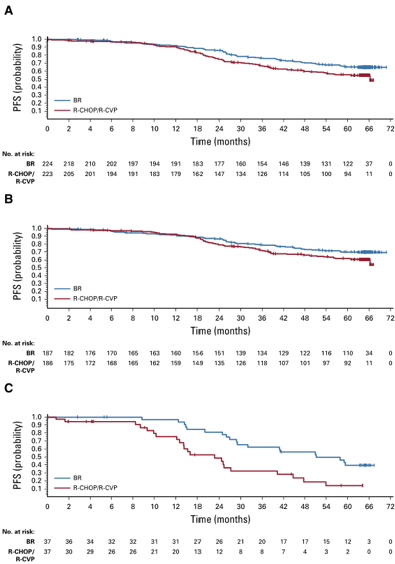
图1. PFS :(A)所有患者;(B)惰性非霍奇金淋巴瘤患者;(C)套细胞淋巴瘤患者
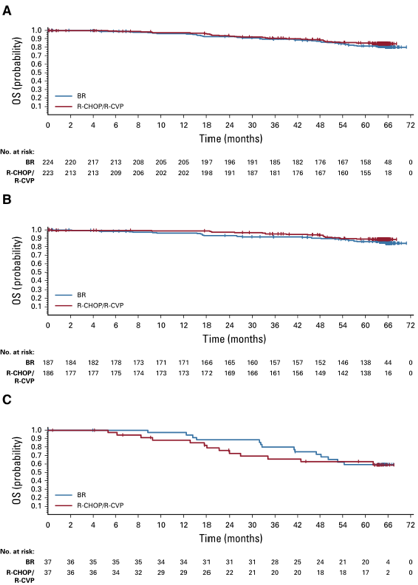
图2. OS (A)所有患者;(B)惰性非霍奇金淋巴瘤患者;(C)套细胞淋巴瘤患者
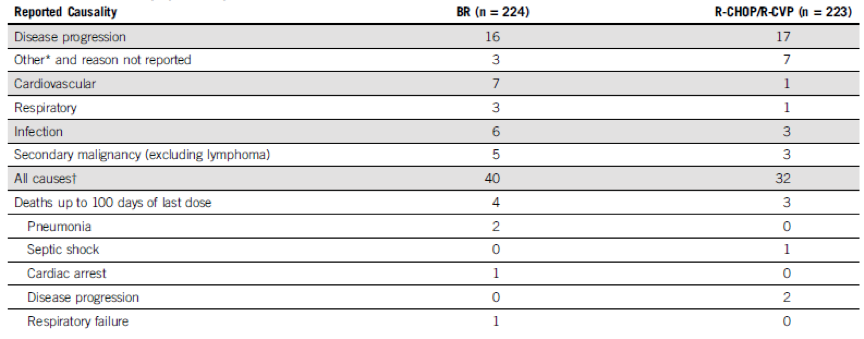
表1.患者死亡原因分析
J Clin Oncol. 2019 Feb 27:JCO1800605.
NO.8 《血液》(Blood)CD19嵌合抗原受体T细胞治疗(CD19 CAR-T)治疗侵袭性非霍奇金淋巴瘤时,机体对淋巴细胞耗竭的反应情况可影响PFS
Hirayama AV, Gauthier J, Hay KA, et al.
研究背景
目前在CD19 CAR-T治疗侵袭性B细胞非霍奇金淋巴瘤(NHL)后,与肿瘤持续缓解的相关因素尚未确定。
研究方法
本研究报道了在侵袭性非霍奇金淋巴瘤患者中应用环磷酰胺和氟达拉滨(Cy/Flu)进行清除淋巴细胞的预处理后应用2x106cells/kg的CD19 CAR-T细胞治疗,分析并报道了可能存在的影响CAR-T细胞治疗疗效和患者PFS的多因素分析结果。
结果
最佳总体有效率(ORR)为51%,40%的病人达到完全缓解(CR)。达到CR的侵袭性B细胞NHL患者的中位PFS为20个月(中位随访时间26.9个月)。在CD19 CAR-T细胞治疗后,研究者对这些患者的临床和治疗特点、血清生物标志物、CAR-T细胞生产和药代动力学数据进行多因素分析显示,较低的淋巴细胞耗竭前的血清LDH和良好的细胞因子谱与PFS相关,可获得更好的PFS。良好的细胞因子谱定义为第0天的血清MCP-1和峰值浓度超过中位数的IL-7。在采用普通淋巴细胞耗竭后或更高强度的Cy/Flu进行淋巴细胞删减后MCP-1 和 IL-7浓度的升高,使良好的细胞因子谱发生的可能性增加。接受了高强度淋巴细胞删减后获得良好的细胞因子谱的患者的PFS优于接受普通强度淋巴细胞删减后未获得良好的细胞因子谱的患者。尽管在淋巴细胞删减前的血清LDH高于正常值的高危患者中,淋巴细胞删减后获得良好的细胞因子谱的患者发生疾病进展的风险也更低。
结论
在CD19 CAR-T细胞治疗应用于侵袭性B细胞NHL患者中,增加淋巴细胞删减后的细胞因子反应的策略值得进一步去研究。
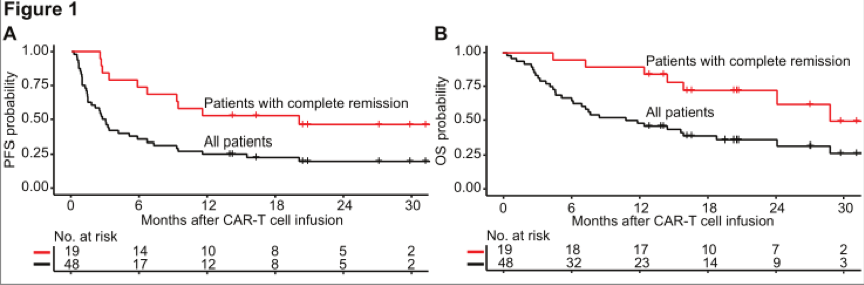
图1. PFS和OS
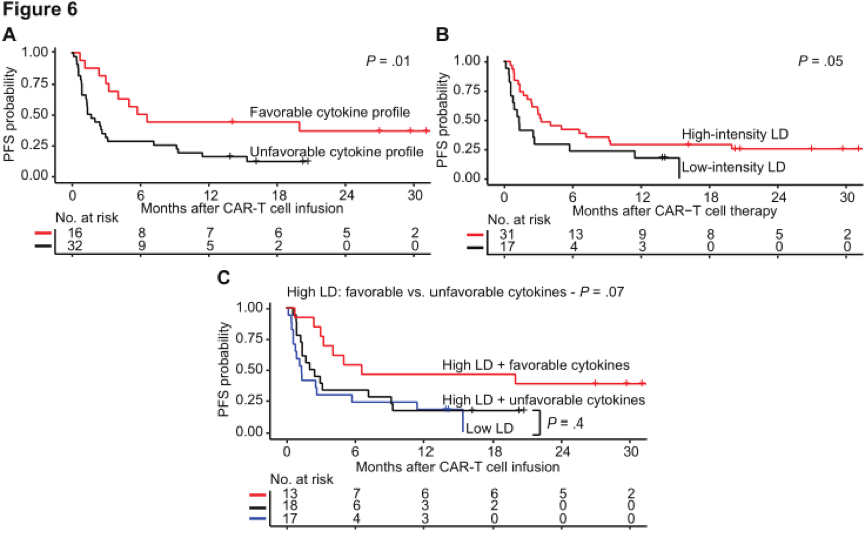
图6.血清MCP-1、IL-7及淋巴耗竭强度对无进展生存(PFS) 的影响。
Blood. 2019 Feb 19. pii: blood-2018-11-887067.
欲了解更多血液肿瘤、淋巴瘤相关资讯,与全国各地血液肿瘤、淋巴瘤医生交流讨论,请扫描以下二维码,备注“血液肿瘤”,添加【肿瘤资讯-娜小编】微信!















 苏公网安备32059002004080号
苏公网安备32059002004080号


