复发/难治性大B细胞淋巴瘤(R/R LBCL)是临床极具挑战的血液恶性肿瘤,一线治疗失败后,传统挽救化疗联合自体造血干细胞移植(ASCT)疗效有限,长期生存率不足20%,原发耐药或早期复发患者预后更差。以CD19为靶点的CAR-T细胞治疗已在三线治疗中展现突破性疗效,近年逐步向二线推进,但长期生存获益、安全性及真实世界适用性仍存争议。
近期,Cancer杂志发表的一项系统评价与荟萃分析,整合了3项随机对照试验(ZUMA-7、TRANSFORM、BELINDA)与1项大型真实世界对比研究,覆盖1199例患者,系统评估了二线CAR-T对比标准治疗(SOC)的长期疗效与安全性,为LBCL二线治疗策略提供高级别循证依据。【肿瘤资讯】特别邀请到江苏省人民医院范磊教授对该研究进行深度解读,以期为临床实践提供参考。
江苏省人民医院血液科 主任
主任医师、教授、博士研究生导师
中国抗癌协会血液肿瘤专委会 副主任委员
中华医学会血液分会淋巴细胞疾病学组 副组长
中国医师协会血液分会 委员
江苏省医师协会淋巴瘤专委会 主任委员
南京医学会血液分会 副主任委员
美国纽约哥伦比亚和康奈尔大学附属纽约长老会医院博士后
研究方向为淋巴肿瘤的精确诊疗

研究背景:从三线突破到二线探索,关键问题亟待解答
LBCL是最常见的非霍奇金淋巴瘤亚型,其中弥漫性大B细胞淋巴瘤(DLBCL)为常见亚型。对于一线治疗后复发或难治的患者,传统标准治疗方案为挽救性化疗免疫治疗,随后对化疗敏感者进行ASCT。然而,约半数患者对挽救治疗反应不佳,尤其是原发性难治或早期复发的患者,长期生存率仅约20%。
以阿基仑赛(axi-cel)、lisocabtagene maraleucel(liso-cel)、tisagenlecleucel(tisa-cel)为代表的CD19靶向CAR-T疗法,已在三线治疗中显示出卓越疗效。随后,ZUMA-7(axi-cel)、TRANSFORM(liso-cel)和BELINDA(tisa-cel)三项关键Ⅲ期临床试验,将CAR-T推向了二线治疗的前沿。然而,这些研究结果并不完全一致:ZUMA-7和TRANSFORM显示出显著的无事件生存(EFS)获益,而BELINDA未达到主要终点。此外,长期总生存(OS)优势、真实世界中的可推广性以及长期安全性等问题,仍待进一步明确。
为此,该项系统综述与荟萃分析旨在整合最新随访数据与真实世界证据,系统评估二线CAR-T相较于SOC的长期疗效与安全性,为临床治疗决策提供更充分、更可靠的依据。
研究方法:循证严谨设计,覆盖随机与真实世界数据
该研究系统检索了MEDLINE、Embase、Web of Science数据库,时间截至2025年8月,纳入标准包括:① 成人R/R LBCL患者;② 接受FDA批准的CAR-T产品(axi-cel、liso-cel、tisa-cel)作为二线治疗;③ 对照组为传统化疗免疫治疗(±ASCT);④ 报告OS、无进展生存期(PFS)、无事件生存期(EFS)或安全性数据;⑤ 包括Ⅲ期随机对照试验及非随机对照研究。
最终纳入三项随机对照试验(ZUMA-7、TRANSFORM、BELINDA)及一项高质量真实世界比较研究(Ghosh et al., 2025),共计1199例患者。研究采用固定效应或随机效应模型进行荟萃分析,并通过IPDfromKM算法对Kaplan-Meier曲线进行个体患者数据(IPD)重建,生成合并生存曲线。同时,研究对EFS进行了预设亚组分析,评估不同年龄、亚型、IPI评分及复发状态下的疗效一致性。
表1.纳入研究的特征
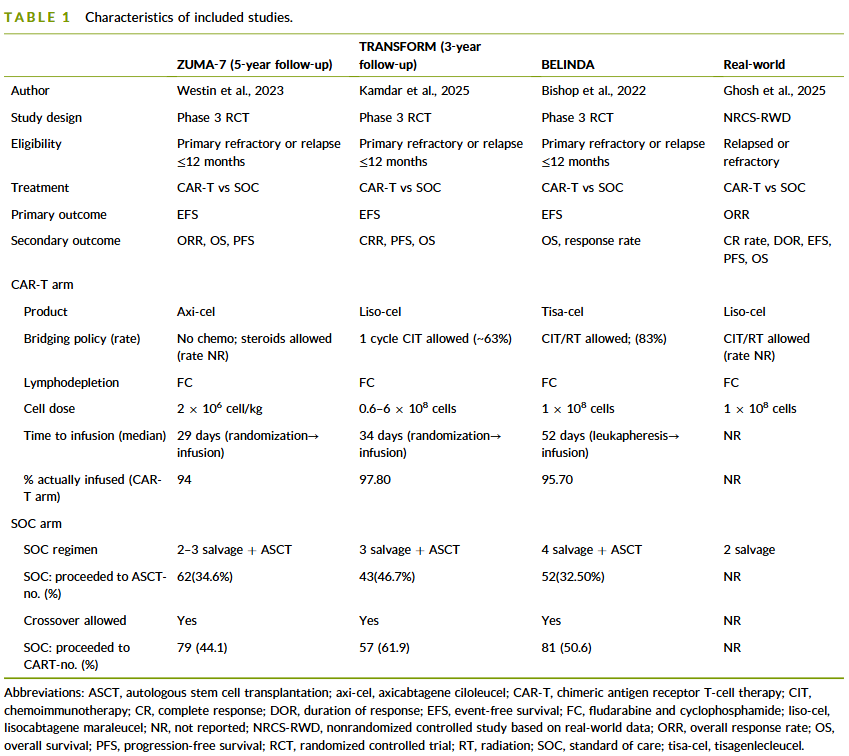
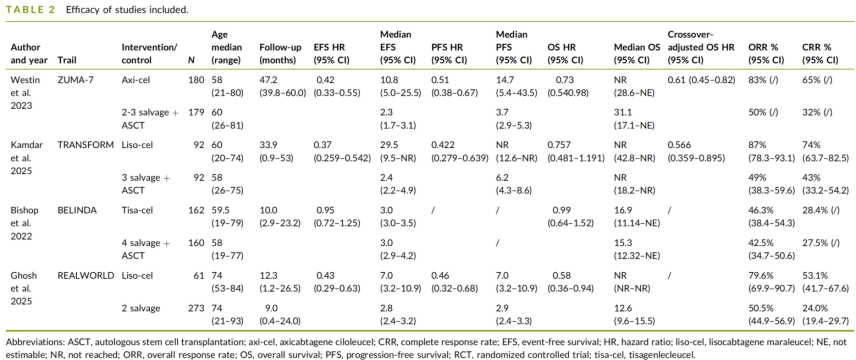
研究结果:CAR-T显著提升长期生存,疗效一致性强
生存结局:OS、EFS、PFS显著改善
汇总分析显示,二线CAR-T治疗在三个关键疗效指标上均显著优于标准治疗:
OS:合并HR=0.75(95%CI:0.62-0.92,P<0.001),死亡风险降低25%;基于重建的个体患者数据,CAR-T组3年OS率为53.59%,标准治疗组仅41.46%,CAR-T组中位OS未达到,标准组为18.1个月
PFS:合并HR=0.47(95%CI:0.39-0.58,P<0.001),进展/死亡风险降低53%(注:BELINDA研究未报告PFS,故该分析基于其余三项研究);CAR-T组3年PFS率为44.08%,标准治疗组仅17.82%,中位PFS分别为15.5个月 vs 3.5 个月
EFS:合并HR=0.51(95%CI:0.33-0.78),但研究间存在较高异质性(I²=86.71%),主要由BELINDA研究的无效应结果驱动。敏感性分析显示,排除BELINDA后,合并EFS HR改善至0.41(95%CI:0.34-0.49),异质性消失(I²=0%)。3年EFS率分别为32.56%和12.88%。
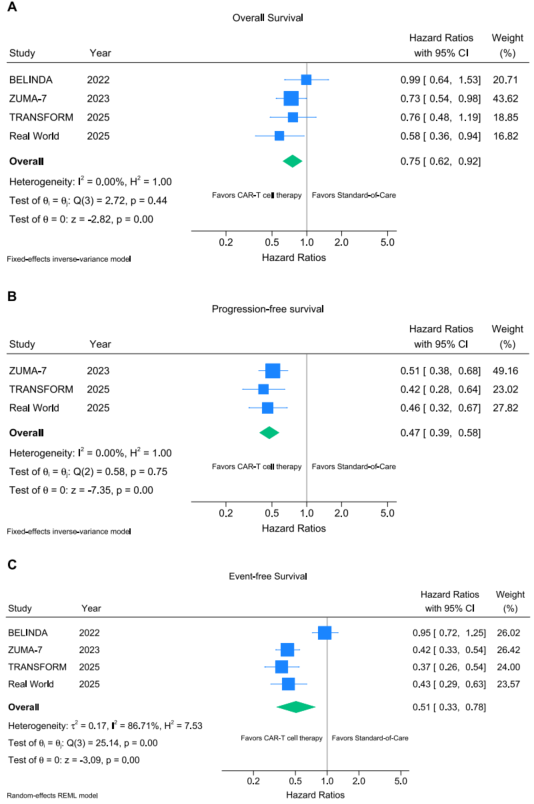
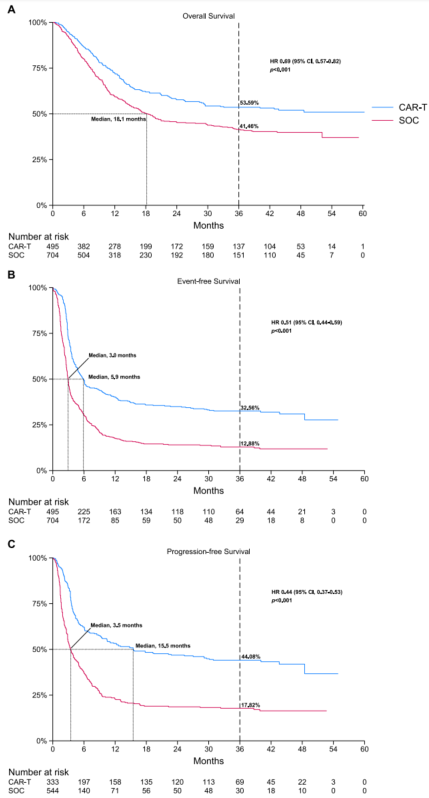
亚组分析:各高危人群均一致获益
基于ZUMA-7和TRANSFORM研究的详细亚组数据,研究者进行了预设的亚组分析,结果令人鼓舞:
病理亚型:无论是de novo DLBCL(HR=0.41)还是高级别B细胞淋巴瘤(HR=0.36),CAR-T均显示显著EFS获益;
年龄因素:<65岁患者(HR=0.44)和≥65岁老年患者(HR=0.29)均显著获益;
疾病状态:原发难治性疾病(HR=0.41)和12个月内早期复发(HR=0.34)患者均获益;
IPI评分:低危(IPI 0-1分,HR=0.40)和中高危(IPI 2-3分,HR=0.38)患者均显示一致获益。
尽管部分亚组样本量有限,但趋势一致,提示CAR-T在广泛高危人群中均具优势。
长期安全性:第二肿瘤风险相当,低丙种球蛋白血症需监测
第二原发恶性肿瘤发生率两组无显著差异,长期无额外致癌风险;
低丙种球蛋白血症(IgG<500 mg/dL)为特征性长期毒性,ZUMA-7研究显示11%的接受CAR-T治疗的患者仍存在低丙种球蛋白血症(IgG<500 mg/dL),TRANSFORM研究中30%的≥3年生存患者存在IgG<500 mg/dL;
3级及以上急性不良事件发生率两组相当,无新增安全信号。
总结
该项系统综述与荟萃分析首次整合了成熟的随机对照试验与真实世界数据,证实了CAR-T二线治疗在R/R LBCL患者中显著改善OS、PFS与EFS,且疗效在关键亚组中一致,长期安全性可控。研究结果表明,二线CAR-T有望成为高危LBCL患者的新型标准治疗策略,同时也凸显了治疗及时性与长期随访的重要性。
随着CAR-T疗法在临床应用日益广泛,未来仍需关注以下问题:① 如何优化桥接治疗策略以降低疾病进展风险;② 如何在化疗敏感人群中权衡CAR-T与ASCT的选择;③ 如何在成本效益与临床获益间取得平衡。该研究的证据为临床决策提供了坚实支持,也为后续研究指明了方向。
排版编辑:肿瘤资讯-Zika
Tang L, Cai D, Yan X, et al. Second‐line chimeric antigen receptor T‐cell therapy versus standard of care in relapsed or refractory large B‐cell lymphoma: A systematic review and meta‐analysis[J]. Cancer, 2026, 132(4): e70317.











 苏公网安备32059002004080号
苏公网安备32059002004080号


