神经内分泌肿瘤(NET)的诊疗近年来显著进展,多模式治疗策略不断完善,而以生长抑素类似物(SSA)为代表的内科药物治疗在整个管理过程中始终占据基础而关键的地位。作为一种长效释放制剂,奥曲肽不仅实现了靶向递送,显著降低了治疗相关毒副反应,还为患者带来了“活得好、活得长”的治疗获益,体现了当前神经内分泌肿瘤治疗从控制肿瘤向改善生存质量转变的趋势。这也标志着神经内分泌肿瘤治疗正朝着更加精准、安全和个体化的方向发展。
本期病例全面展示了胰腺及胆囊神经内分泌肿瘤在不同疾病阶段的系统管理策略及最新诊疗进展,体现了手术、系统治疗、介入与核医学的有机组合。这些病例有望为更多临床医生提供实践经验及诊疗思路,并进一步促进神经内分泌肿瘤综合治疗体系的规范化与发展。
Section 1
病例汇报:
杨茜教授 四川大学华西医院
病例点评:
郭敬教授 厦门大学附属第一医院
李敏教授 柳州市人民医院
彭渝教授 陆军军医大学第一附属医院
肿瘤学博士、副教授、硕士研究生导师
曾前往美国MD安德森癌症中心交流学习
任四川省抗癌协会委员
四川省医学科技创新研究会委员
主要研究领域为肿瘤综合治疗,新型免疫药物和新型药物递送系统
主持国家自然科学青年基金、四川省面上基金、四川省青年科学基金和博士后面上基金等项目
现已发表SCI学术论文30余篇
病例介绍
患者基本情况
患者男性,55岁,主因“胰腺神经内分泌瘤术后3+年,确诊肝转移1+月”就诊。
既往史:高血压病史10余年,长期口服非洛地平5 mg qd,血压控制良好。
一般情况:ECOG PS 0分,无皮肤潮红、皮疹、水肿或肢端肥大。
诊疗经过
2019年7月随访腹部增强CT显示肝脏多发动脉期强化结节,并伴肠系膜及肠系膜上动脉旁淋巴结增大。穿刺病理确诊为NET肝转移,SSTR2阳性、Ki-67约2%。MDT诊断为“胰腺NET术后(G2,pT3N1M0 IIIB)伴肝多发转移(IV期)”。
•一线治疗:生长抑素类似物(SSA) + TAE/TACE
2019年起给予奥曲肽微球30 mg q4w,并联合5次TAE/TACE。治疗后病情长期稳定,肝病灶缓慢增大,但未见严重不良反应。2022年8月MRI显示肝病灶增多增大,评估为PD,停止SSA治疗。
•二线治疗:索凡替尼
2022年9月起口服索凡替尼300 mg qd。主要不良反应为蛋白尿、贫血及大便隐血阳性。2023年MRI评估为SD,但患者出现间断解黑便。68Ga-DOTATATE PET/CT显示部分病灶SSTR阴性,未能进入177Lu临床研究。2024年1月患者因小肠溃疡再度解暗红色血便,停止索凡替尼治疗。
•三线治疗:依维莫司
2024年1月起给予依维莫司10 mg qd。2024年4月CT显示肝病灶部分缓解(PR)。但2024年7月因再次出现小肠溃疡及出血暂停治疗。对症处理后改为依维莫司5 mg qd,随后两次复查(2024-10、2025-01)均显示SD。MDT建议后续可考虑与SSA联合治疗。
•四线治疗:临床研究(高剂量SSA)
2025年2月PET-CT显示肝转移灶数量及摄取水平较前明显增加。患者随机进入临床研究对照组,开始醋酸奥曲肽微球60 mg q4w。至最新随访(2025年11月)疗效评估为SD。
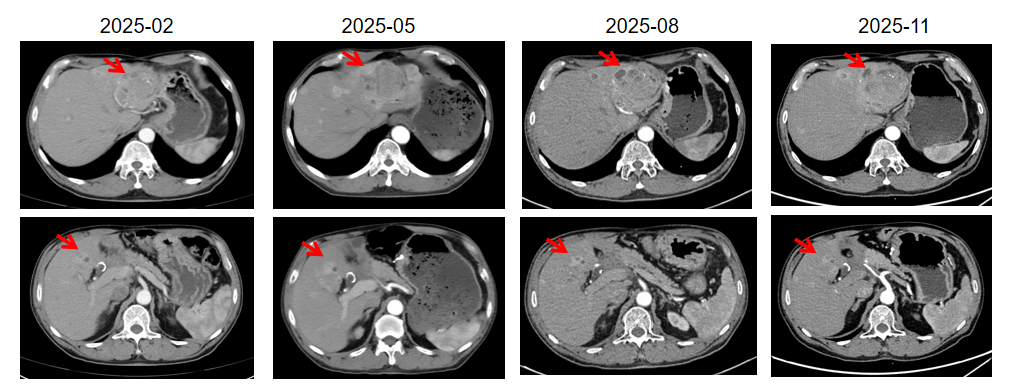
病例小结
本例为pNET术后复发并多发肝转移的患者,经多线系统治疗及介入治疗后达到长期带瘤生存。病例展示了pNET长期管理中对多模式治疗策略的灵活应用,包括SSA、靶向治疗、介入治疗及核素治疗筛选。治疗过程中肿瘤进展、SSTR表达变化及消化道不良反应均影响治疗路径,是制定个体化治疗策略的关键因素。基于此病例的经验可以为类似的pNET患者长期管理提供参考。
Section 2
病例汇报:
林鹭萍教授 福建省肿瘤医院
病例点评:
王莉教授 广西医科大学第二附属医院
王美清教授 海南省肿瘤医院
郑红教授 达州市达川区人民医院
腹部内科 主治医师
福建省医学会内科学分会青年学组委员
福建省海医会胆道疾病专委会委员
第一届福建省神经内分泌肿瘤专委会秘书
主持省级课题1项,参与省级课题4项,厅级课题2项
以第一作者发表SCI论文2篇
专注消化道肿瘤的综合治疗
病例介绍
患者基本情况
患者女性,29岁,ECOG评分0分。2023年8月因腹痛行腹部超声检查提示肝内及胆囊占位性病变。
术前MRI显示:肝方叶占位(5.1×3.5×3.5 cm),提示外周型胆管细胞癌可能;胆囊壁受累;肝S5段结节,考虑转移性病变。

诊疗经过
患者在全麻下接受胆囊切除+肝部分切除+8、12、13组淋巴结清扫+右肝转移灶射频消融。
术后病理诊断为:胆囊浸润性癌,小细胞神经内分泌癌约80%,腺癌约20%;肿瘤突破胆囊壁并侵犯肝组织;脉管癌栓及神经侵犯;送检“13组淋巴结”1/5(腺癌)。免疫组化示小细胞成分Syn、CD56阳性,CgA部分阳性,Ki-67约80%;腺癌CK、CK7阳性;PD-L1 TPS < 1%。术后1个月复查MRI即提示肝术区及S5/S6段出现多发新发可疑转移灶。
• 一线治疗:EP化疗
患者术后接受一线EP化疗(依托泊苷 + 顺铂)5周期,疗效评估为疾病稳定(SD),PFS约6个月。2024转诊至我院。会诊病理提示小细胞神经内分泌癌成分比例进一步升高至约90%,腺癌成分约10%,周围肝组织可见转移灶(成分为小细胞神经内分泌癌),PD-L1 CPS=0,SSTR2阳性。患者拒绝再次肝穿刺活检。
•二线治疗:III期临床研究
患者入组“评价索凡替尼联合特瑞普利单抗对比FOLFIRI作为晚期神经内分泌癌二线治疗的疗效和安全性的随机、开放多中心III期临床研究”,2024年5月起接受FOLFIRI治疗12周期,后因乏力与3级腹泻改为氟尿嘧啶3周期。此阶段最佳疗效为部分缓解(PR),PFS约7个月。随后因肝S8新发病灶提示疾病进展。
•三线治疗:ZG006三特异性抗体
患者之后进入三特异性T细胞衔接器ZG006的I/II期研究,自2024年12月至2025年4月共接受9周期治疗。C1-C2期间出现2级细胞因子释放综合征,经托珠单抗干预后缓解。该阶段患者肿瘤缩小:C2后达PR,C4后达完全缓解(CR)。但至C6时在肝门区出现新发淋巴结病灶,评估为进展(PD),PFS约4个月。
•四线治疗:LBL-024免疫治疗
其后患者入组LBL-024的I/II期研究,接受2周期免疫治疗,但肝内及肝门区淋巴结进展,PFS约6周。2025年7月行肝穿刺活检,提示小细胞神经内分泌癌浸润,Ki-67高达90%,并检测到TP53外显子7的移码突变,TMB为1 muts/Mb。
•五线治疗:贝伐珠单抗+白蛋白紫杉醇
综合MDT讨论后,2025年7月起给予“贝伐珠单抗+白蛋白紫杉醇”方案(C1D1-C5D8),患者获得部分缓解(PR),为当前有效治疗方案。
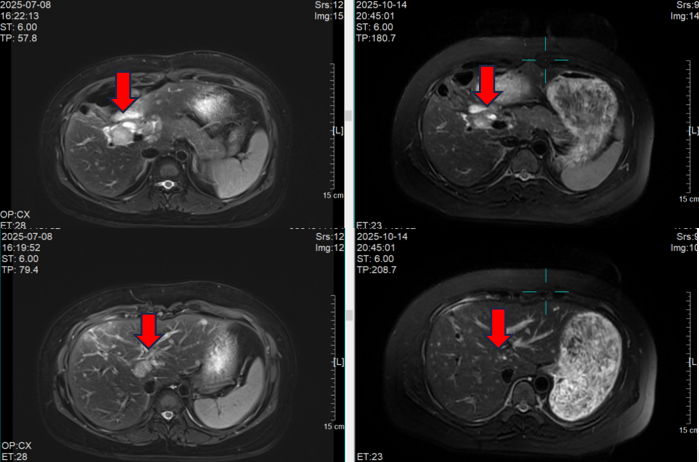
病例小结
本例患者为29岁女性,罕见的以小细胞神经内分泌癌为主的胆囊浸润性癌,初诊即伴肝转移,术后复发,先后接受EP化疗、FOLFIRI、ZG006、LBL-024免疫治疗及抗血管联合化疗等多线治疗,部分方案获得显著疗效(包括CR)。目前贝伐珠单抗+白蛋白紫杉醇治疗下疾病获得再次控制。病例反映了胆囊小细胞神经内分泌癌的高度侵袭性、生物学复杂性,亦展示了多线治疗、临床试验药物在此类罕见肿瘤中的潜在价值。
Section 3
病例汇报:
林春城教授 泉州市第一医院
病例点评:
许声江教授 海南省肿瘤医院
顾雨林教授 玉林市红十字会医院
张友才教授 德阳市人民医院
副主任医师、硕士研究生
福建省中西医结合学会普外科分会委员
福建省中西医结合学会普外科分会肝胆胰外科学组委员
泉州医学会快速康复学会委员
擅长肝胆胰及腹腔镜微创外科疾病的诊治
病例介绍
患者基本情况
患者男性,57岁。于2024年1月因“发现胰腺肿物1周”入院。
现病史:患者自觉近期体重下降,影像提示胰腺肿物后前来就诊。
入院后行腹部增强CT,显示明显脂肪肝,同时肝脏多发富血供结节,胰体尾可见约2-3 cm的不规则强化肿块,提示胰腺肿瘤伴多发肝转移。因影像呈富血供特征,无法完全排除神经内分泌肿瘤(NET),遂行超声引导穿刺活检。活检病理提示胰腺神经内分泌肿瘤(NET G2)。PET/CT示胰体尾病灶高摄取,肝脏多发高代谢结节,肾上腺亦见增厚但代谢未见明显异常,无法明确是否为转移。结合肿瘤生物学特征,诊断为胰体尾NET G2,伴多发肝转移(III型)。
诊疗经过
经MDT讨论,由于病灶位于胰体尾,手术不涉及消化道重建,且肿瘤体积较大、有压迫门静脉风险,同时多发肝转移仍具减瘤价值,因此决定实施胰体尾切除+脾切除+肝部分转移灶切除,其他深部小转移灶计划术后射频消融处理。术后病理提示NET G3,伴脉管及神经侵犯,肝多发灶均证实为转移。
术后1个月复查提示肝脏转移明显较术前增多,呈密集富血供结节,提示进展。患者随后接受肝动脉介入栓塞(TACE),以及卡培他滨联合替莫唑胺(CAPTEM)+索凡替尼的系统治疗策略。术后3个月复查,患者肝脏多发病灶几乎全部消失,肾上腺及腹膜结节显著缩小,继续接受化疗6周期后改为索凡替尼维持。随访一年时,肝脏及腹膜病灶持续完全消退,肾上腺结节亦进一步缩小。由于经济原因及病灶控制良好,患者逐步“降阶梯”,由索凡替尼转换为奥曲肽维持。
病例小结
该病例显示即使NET G3伴多发远处转移,依然可通过有效的减瘤手术、TACE、靶向治疗联合CAPTEM化疗、奥曲肽维持的综合模式获得长期生存。其中,索凡替尼及奥曲肽均具有良好的安全性,为长期管理提供可能。
总结
以上病例提示我们,神经内分泌肿瘤的管理绝不仅是单一科室能够完成的工作,而是需要多学科团队(MDT)全程参与的过程。综合评估后的决策,往往才能帮助患者获得真正的长期获益。无论是靶向、化疗、放疗还是内分泌治疗,规范化的指南与循证证据始终是我们制定治疗方案的基础,而最终目标都是让患者获得尽可能长久、尽可能高质量的生存。
排版编辑:肿瘤资讯-Sally











 苏公网安备32059002004080号
苏公网安备32059002004080号


