尽管早期认为自体造血干细胞移植(ASCT)是适合移植套细胞淋巴瘤(MCL)年轻患者的标准治疗策略之一,但目前尚无随机对照试验(RCT)明确证实其在现代治疗背景下能够显著改善患者的无进展生存期(PFS)和总生存期(OS)。值得注意的是,对于基线存在TP53突变的高风险MCL患者,即使接受强化化学免疫治疗后再进行ASCT,预后仍然较差[1]。因此,在当前临床实践中,对于MCL年轻患者早期接受ASCT治疗的风险与获益比仍需进一步探索和权衡。
此外,随着新药时代的到来,越来越多的新型药物,如BTK抑制剂(BTKi)等被应用于临床,这使得ASCT在MCL年轻患者治疗中的地位受到更多挑战和质疑。近期的多项国际大会中,针对MCL年轻患者的治疗是否需要ASCT这一热点问题,也引发了广泛关注。【肿瘤资讯】特别遴选了多篇具有代表性的研究,并邀请中山大学肿瘤防治中心黄慧强教授对主要研究结果及其临床意义进行深入点评,相关内容详见下文。
突破传统移植模式:BTKi方案或能为MCL年轻患者带来更多可能
TRIANGLE研究
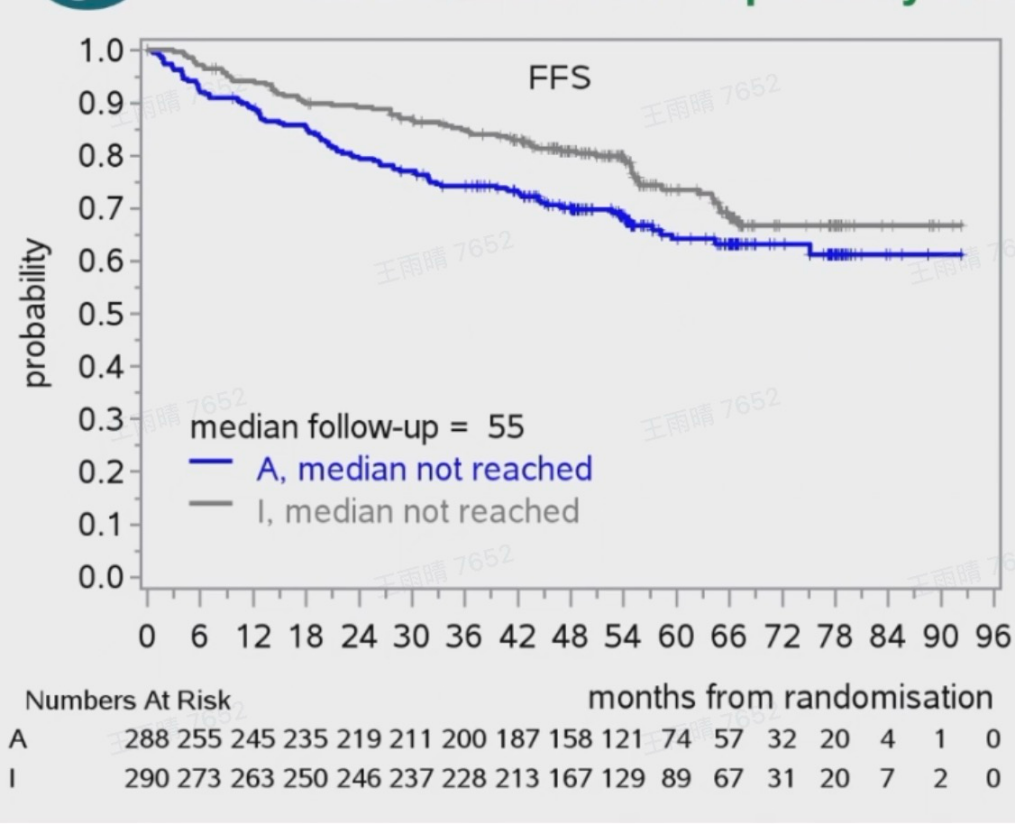
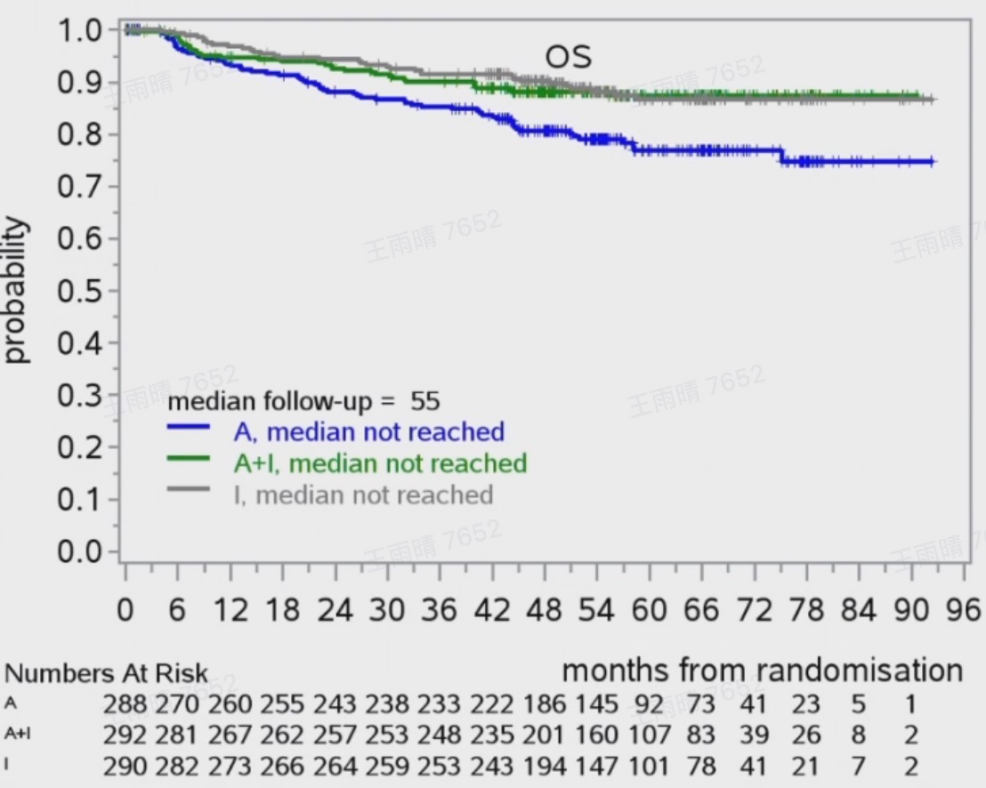
TRIANGLE研究聚焦于ASCT对接受一代BTKi伊布替尼治疗的MCL患者生存预后的影响。中位随访55个月的结果显示,A+I组和I组的4年无失败生存(FFS)率均优于A组(A+I组vs A组:82%vs70%,P=0.0026;I组vs A组:81%vs70%,P=0.0208)。而I组和A+I组之间的FFS并无显著差异,这表明总体上ASCT并未带来额外的益处。在高风险患者群体中,如母细胞样亚型、p53高表达或Ki-67大于30%的高危MCL患者,生存获益趋势相似。在总生存期(OS)方面,A+I组和I组均优于A组,4年OS率分别为88%、90%和81%(A组vs I组:P=0.0019;A组vs A+I组:P=0.0036)。目前,A+I组与I组之间的OS比较还在进一步分析中。
安全性方面,A+I组的血液和淋巴系统异常发生率较高(54%),感染发生率也显著增高(34%)。而BTKi单药组安全性相对更好。
研究结论:TRIANGLE研究结果显示,在中位随访期间,含一代BTK抑制剂的治疗方案(无论是否联合ASCT)在FFS和OS方面均显著优于单纯ASCT治疗。然而,进一步分析表明,在现代治疗背景下,ASCT联合一代BTK抑制剂并未显著改善患者的生存获益,且联合ASCT可能增加不良事件风险[2]。
BRIDGE研究
本中心开展的与TRIANGLE研究异曲同工之妙的II期BRIDGE研究旨在探索以新一代BTKi泽布替尼为基础的诱导和维持方案治疗初治年轻MCL患者的疗效和安全性。入组患者将交替接受泽布替尼联合R-CHOP和R-DHAOx诱导治疗6个周期。共入组7例患者,中位年龄56.3岁,基线时骨髓(BM)和外周血(PB)微小残留病(MRD)检测均呈阳性。经过6个周期的泽布替尼联合R-CHOP和R-DHAOx诱导治疗后,患者BM和PB MRD阴性率达到100%(7/7)。其中,1例患者接受了ASCT。截至数据收集时,1例患者在第53周完成泽布替尼维持治疗后因疾病进展退出,其余6例患者仍在继续接受泽布替尼维持治疗并处于随访中。
中位随访25.9个月时,所有患者均表现出良好的耐受性。以泽布替尼为基础的治疗方案在诱导治疗期间未出现剂量调整、停药情况,也未发生与BTKi相关的不良事件(AE,如腹泻、高血压、出血和心房颤动/扑动)[3]。
研究结论:BRIDGE研究结果表明,以泽布替尼为基础的治疗方案在初治MCL年轻患者中具有显著的疗效和良好的安全性,为进一步优化MCL治疗模式提供了重要参考。
新希望,新选择:BTKi联合方案或能为高危MCL带来非移植治疗突破
OASIS系列研究
I/II期OASIS研究聚焦于BTKi伊布替尼联合奥妥珠单抗和维奈克拉在初治及复发/难治(R/R)MCL患者中的应用,分为三个队列,纳入不同特征的R/R MCL患者。队列A(n=9)和队列B(n=24)的总缓解率(ORR)分别为89%和71%,中位随访时间分别为72个月和58个月,6年PFS率分别为53%和40%。长期随访期间,两组未出现新的安全性信号,显示出良好的耐受性。针对高危MCL患者的队列C(n=15),所有患者均呈现中危或高危的MIPI。结果显示,ORR高达93%,其中87%的患者达到完全缓解(CR)。中位PFS和持续缓解时间(DOR)均未达到,估计的60个月PFS率和DOR率均为80%。尽管2例患者因早期疾病进展和不良事件提前终止治疗,且出现了一些严重的不良事件(AE,如心房颤动、急性心力衰竭和进行性多灶性白质脑病PML),但总体而言,5年OS率仍高达93%,表明该方案在高危MCL患者中具有显著的生存获益[4]。
研究结论:OASIS研究证实伊布替尼联合奥妥珠单抗和维奈克拉方案在复发/难治及高危MCL患者中展现出卓越的抗肿瘤活性和长期生存获益,为优化MCL治疗策略提供了重要循证依据。
基于OASIS研究的成功经验,II期OASIS-2研究进一步评估了BTKi伊布替尼联合CD20单抗(A组)及其基础上加用BCL-2抑制剂维奈克拉的三药联合疗法(B组)在初治MCL患者中的疗效和安全性。研究分为两组,A组共有46例患者完成诱导治疗,B组共有45例患者完成诱导治疗。两组的CD20单抗中位剂量强度均为100%。进一步分析显示,B组患者中伊布替尼剂量调整的发生率更高(28% vs 15.7%),且24%的患者需要至少一次维奈克拉剂量减低。在疗效方面,诱导治疗结束时,B组的CR率为64%,高于A组的56.9%。中位随访13.5个月和27个月,研究的1年PFS率和OS率分别为91%和95%;2年PFS率和OS率分别为87.9%和91.9%。此外,MRD评估显示,诱导结束时,A组的MRD阴性率提升至53.8%(基线为40.2%),而B组达到82.1%(基线为42.1%)。在安全性方面,B组的AE发生率较高,特别是3级中性粒细胞减少症的比例显著升高(34% vs. 11.8%)。此外,B组中AE、特别关注的AE(AESI)和≥3级AE的发生率均高于A组(分别为92% vs. 82.4%,82% vs. 52.9%,64% vs. 47.1%)。然而,两组的≥3级严重不良事件(SAE)发生率相似(32% vs. 31.4%)。综合来看,OASIS-2研究中,伊布替尼联合CD20单抗和维奈克拉的三联治疗在初治MCL患者中展现了显著的疗效。尽管三联治疗的AE发生率较高,但其安全性仍在可接受范围内[5]。
研究结论:综合来看,OASIS-2研究中,伊布替尼联合CD20单抗和维奈克拉的三联治疗在初治MCL患者中展现了显著的疗效。尽管三联治疗的AE发生率略高,但其安全性仍在可接受范围内。
BOVen方案研究
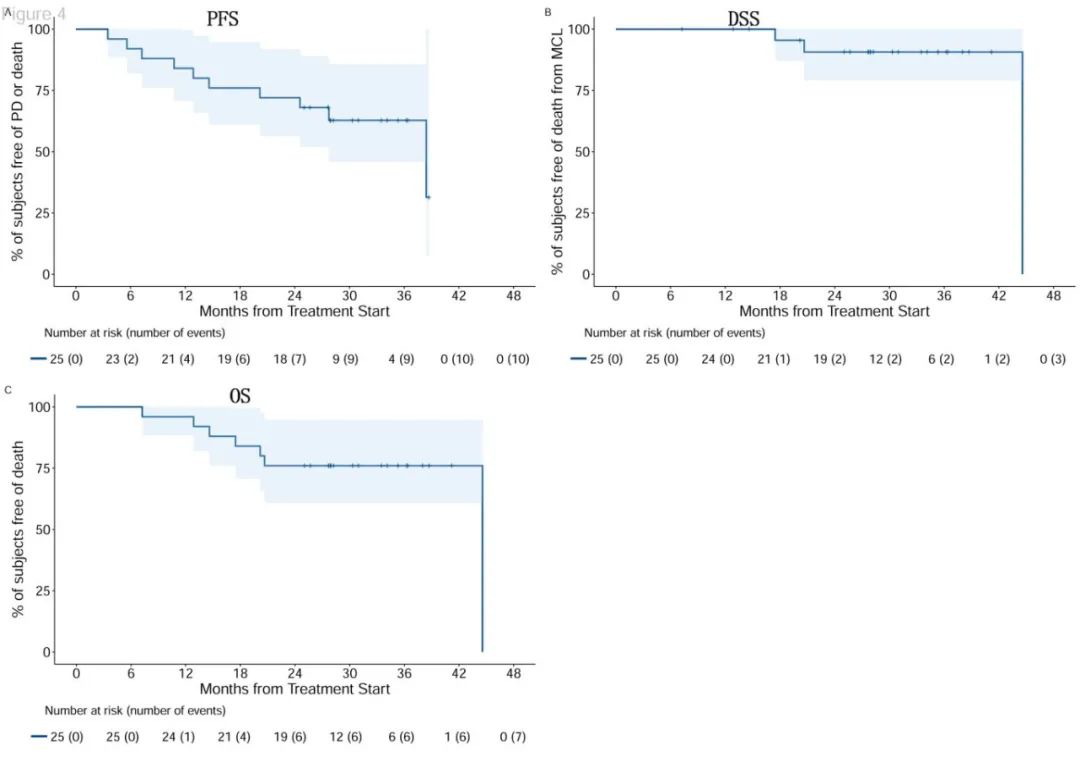
II期BOVen研究聚焦于评估新一代BTKi泽布替尼联合奥妥珠单抗和维奈克拉方案在一线治疗TP53突变MCL患者中的疗效与安全性。研究纳入25例患者,中位随访时间为28.2个月。结果显示,BOVen方案的ORR高达96%,其中CR率为88%。
生存分析方面,2年PFS率为72%,2年OS率为76%,而2年疾病特异性生存率(DSS)达到91%。值得注意的是,DSS优于OS的主要原因在于COVID-19相关死亡的影响。
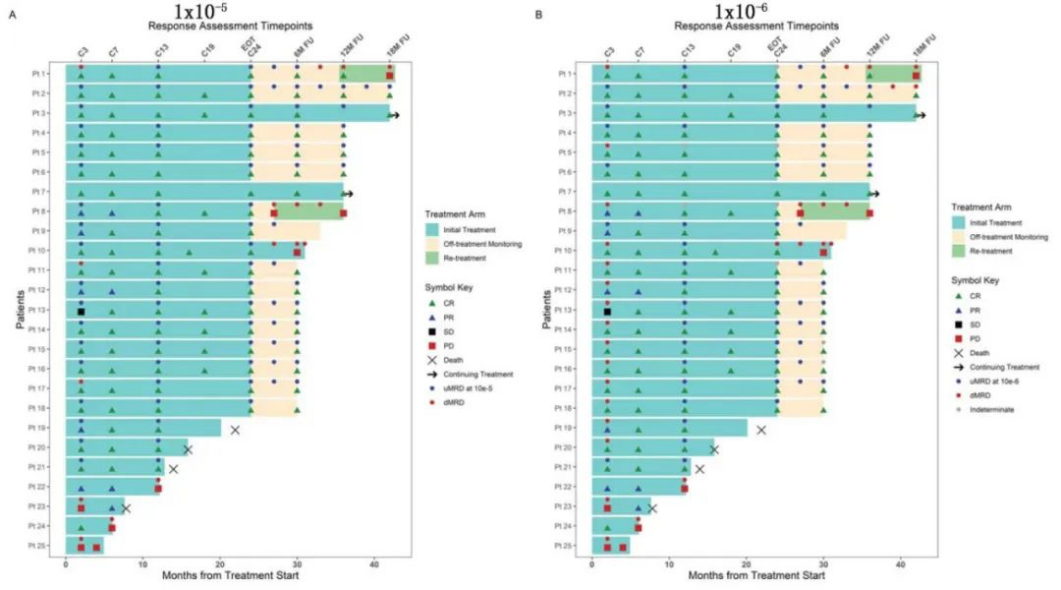
MRD评估显示,在第13周期时,外周血中uMRD5和uMRD6的比例分别为95%和84%。经过24个周期治疗后,在17例可评估的患者中,2例患者MRD可检测并继续治疗,而15例患者达到CR/uMRD,停止治疗。
安全性方面,常见副作用包括腹泻、COVID-19感染、中性粒细胞减少和输注相关反应,且多为低级别。
研究结论:总体而言,BOVen方案在TP53突变的高危MCL患者中展现出高缓解率和良好的2年PFS率,耐受性良好,安全性可控,为这一预后较差的患者群体提供了新的治疗选择[6]。
1.Kumar A. What is the role of up-front autologous stem cell transplantation in mantle cell lymphoma? Hematology Am Soc Hematol Educ Program. 2022 Dec 9;2022(1):155-162. doi: 10.1182/hematology.2022000333. PMID: 36485104; PMCID: PMC9820454.
2.Martin Dreyling, MD, et al. Role of Autologous Stem Cell Transplantation in the Context of Ibrutinib-Containing First-Line Treatment in Younger Patients with Mantle Cell Lymphoma: Results from the Randomized Triangle Trial By the European MCL Network. Presented at ASH 2024. December 7-10, 2024. San Diego, California. Abstract 240.
3. Gao Yan, Qingqing Cai, Zhiming Li, et, al. Mantle Cell, Follicular, and Other Indolent B Cell Lymphomas: Clinical and Epidemiological: Targeted Therapy. Blood (2023) 142 (Supplement 1): 6147. https://doi.org/10.1182/blood-2023-181619
4.Benoit Tessoulin et al.5-y Follow-up of Combination of Ibrutinib, Obinutuzumab and Venetoclax for Patients with Newly Diagnosed Mantle Cell Lymphoma, the Oasis Trial P1657
5.Steven Le Gouill et al,Ibrutinib, Venetoclax Plus CD20 Monoclonal Ab Provides Very High MRD Negativity in Previously Untreated MCL Patients, Initial Results of OASIS II, a Randomized Phase 2 Trial,O745
6.Anita Kumar, Jacob Soumerai, Jeremy S. Abramson, Jeffrey A. Barnes, Philip Caron, Shalini Chhabra, Maria Chabowska, Ahmet Dogan, Lorenzo Falchi, Clare Grieve, J. Erika Haydu, Patrick Connor Johnson, Ashlee Joseph, Hailey E. Kelly, Alyssa Labarre, Jennifer Kimberly Lue, Rosalba Martignetti, Joanna Mi, Alison Moskowitz, Colette Owens, Sean Plummer, Madeline Puccio, Gilles Salles, Venkatraman Seshan, Elizabeth Simkins, Natalie Slupe, Honglei Zhang, Andrew D. Zelenetz; Zanubrutinib, obinutuzumab, and venetoclax for first-line treatment of mantle cell lymphoma with a TP53 mutation. Blood 2025; 145 (5): 497–507. doi: https://doi.org/10.1182/blood.2024025563
排版编辑:肿瘤资讯-kk











 苏公网安备32059002004080号
苏公网安备32059002004080号


