多发性骨髓瘤(MM)是血液系统恶性肿瘤,约占肿瘤的1%,约占血液肿瘤的10%,中老年人多见,荧光原位杂交技术(FISH技术)迅速发展,1q21扩增检出率较高,新诊断MM患者的1q21扩增检出率为35%~45%。而且,越来越多的研究表明1q21扩增是MM预后不良因素之一。本文MM患者的FISH检测结果显示,1q21扩增为3个拷贝数,一线使用硼替佐米、脂质体阿霉素 、地塞米松(PAD方案)治疗后效果微小缓解(MR),二线选择含来那度胺和cd38单抗的DRD方案获得部分缓解(PR)的良好疗效。
广州医科大学附属第一医院
广东省医师协会血液分会委员
广东省医学会血液学分会青年委员
广东省健康教育协会血液学分会常委
广州市医学会血液分会副主任委员
广州地区医疗机构药品集团采购药事专家库专家
主要从事白血病、淋巴瘤、骨髓瘤、噬血细胞综合征等疾病的诊治
对化疗、造血干细胞移植及CART细胞免疫治疗等有较深的造诣
参与编写《血液系统疑难病例精析及诊断思路》一书,发表SCI论文3篇
国内核心期刊学术论文10余篇。参与国家及省市级科研项目多项
临床资料
病史介绍
患者,男,51岁,2020.10.29因“头晕乏力、骨痛1月余”入院。
既往史
患者于2020年10月份无明显诱因出现头晕,非天旋地转样,与体位变化无关,伴肢体乏力,心悸,伴活动后气促,伴肋骨疼痛,至澳门某医院就诊,查血常规:WBC 4.07*109/L,HB 61g/L,PLT 104*109/L。头颅CT:未见异常。未予处理。
至中山大学附属第五医院就诊,查血常规:WBC 3.2*109/L,HB54g/L,PLT 78*109/L;肌酐167umol/L,予输注血红细胞处理。
2月前当地医院就诊,骨髓检查示:骨髓增生重度减低,红系比例明显减低,未见巨核细胞,血小板单个散在分布,可见10%浆细胞(疑混入部分外周血)。
实验室检查(2020.10.30)
静脉血细胞分析(海印):白细胞3.23↓ 109/L,血红蛋白61↓g/L,血小板109 109/L
凝血五项(海印): 凝血酶原时间18.5↑秒,纤维蛋白原1.43↓g/L,活化部分凝血活酶时间55.4↑秒,D二聚体(免疫比浊法)0.38ug/mL FEU
CX3生化八项(20201030):钙 3.011↑mmol/L
免疫八项:免疫球蛋白G 2.15↓g/L,免疫球蛋白A 84.6↑g/L,免疫球蛋白M 0.0839↓g/L,β2-微球蛋白 8.37↑mg/L
肝功七项(海印)^生化六项(海印):总蛋白 124.5↑g/L,白蛋白 22.9↓g/L,乳酸脱氢酶 91↓U/L
葡萄糖6-磷酸脱氢酶活性检测:葡萄糖-6-磷酸脱氢酶活性(比值法) 0.38kU/L
免疫固定电泳(20201105): 免疫球蛋白A 阳性!,免疫球蛋白Kappa 阳性!

流式:骨髓检测可见异常表型单克隆浆细胞占有核细胞的4.34%,占浆细胞100%,其表cKappa、CD38、CD138、CD27、CD200、CD28,部分表达CD20。结论:可见异常表型单克隆浆细胞占骨髓有核细胞的4.34%,占浆细胞100%;成熟B淋巴细胞表型未见异常。
染色体,如下图所示: 
FISH,如下图所示:

NGS,如下图所示:
PET/CT 18F-FDG全身显像:
1.全身骨髓糖代谢弥漫性增高,CT于相应部位见骨质密度不均匀,局部见低密度影,结合骨穿检查结果,符合多发性骨髓瘤征象。
2.脾大,糖代谢未见增高。
3.双肺散在肺大泡;两下肺基底段少许慢性炎症/纤维灶;纵隔(2R、4R、4L组)多发淋巴结,糖代谢未见增高,考虑炎性增生;两侧少量胸腔积液;心腔密度减低,考虑贫血。
4.前列腺增生并钙化;腰椎退行性变;两侧第2、3前肋及右侧第12后肋骨折。
5.余全身PET/CT未见明确的异常糖代谢增高灶。
诊断与分型
1.多发性骨髓瘤IgA-κ RISS Ⅲ期 1q21(+三个拷贝数)
2.G-6-PD酶缺乏症
3.胆囊泥沙样结石
4.高血压2级 高危
治疗方案及疗效评估
患者符合HSCT
2020.11.3、2020.12.1、2020.12.29、2021.1.26分别予三程“硼替佐米2.1mg d1、d8、d15、d22+脂质体阿霉素40mg d3+地塞米松40mgd1-d4化疗”,过程顺利。
疗效评估:MR
2021.3.1拟造血干细胞采集予阿糖胞苷2.0g d1,d2+环磷酰胺2.0g d3,d4联合G-CSF,3-17,3-18予自体造血干细胞采集,过程顺利。
采集干细胞后IG-A上升。
二线治疗:2021.04.30、2021.5.7,2021.5.18,2021.5.25予达雷妥尤单抗注射液900mg QW+来那度胺25mg d1-21+地塞米松40mg qw化疗。
疗效评估:PR
下一步治疗计划
auto-HSCT
CAR-T
移植后强化
维持治疗? 伊沙左米?来那度胺
专家点评
多发性骨髓瘤(MM)是好发于老年人的恶性浆细胞疾病,具有高度异质性。多种因素可以影响MM治疗疗效及预后,其中细胞遗传学异常是MM最重要的预后因素,比如1q21扩增。1q21扩增比例在初治MM患者中占40%,而在复发难治MM患者中高达70%。目前新药如免疫调节剂、蛋白酶体抑制剂的应用,可延长患者的生存期,但对于1q21扩增的患者治疗反应差,且该扩增区域含有多种致病及耐药基因,如CKS1B、MCL1及PSMD4等[1]。有研究结果显示,伴1q21扩增初治MM患者应用含硼替佐米方案治疗,可提高深度缓解率,但并不改善PFS及OS。本文患者行一线治疗时应用PAD(硼替佐米+脂质体阿霉素+地塞米松)方案三疗程,疗效仅达微小缓解(MR),采集干细胞后IG-A上升明显。
对于首次复发患者,Mayo推荐含达雷妥尤单抗的方案;对于双重或多重耐药患者,可优选含CD38单抗的方案(图1-2)。
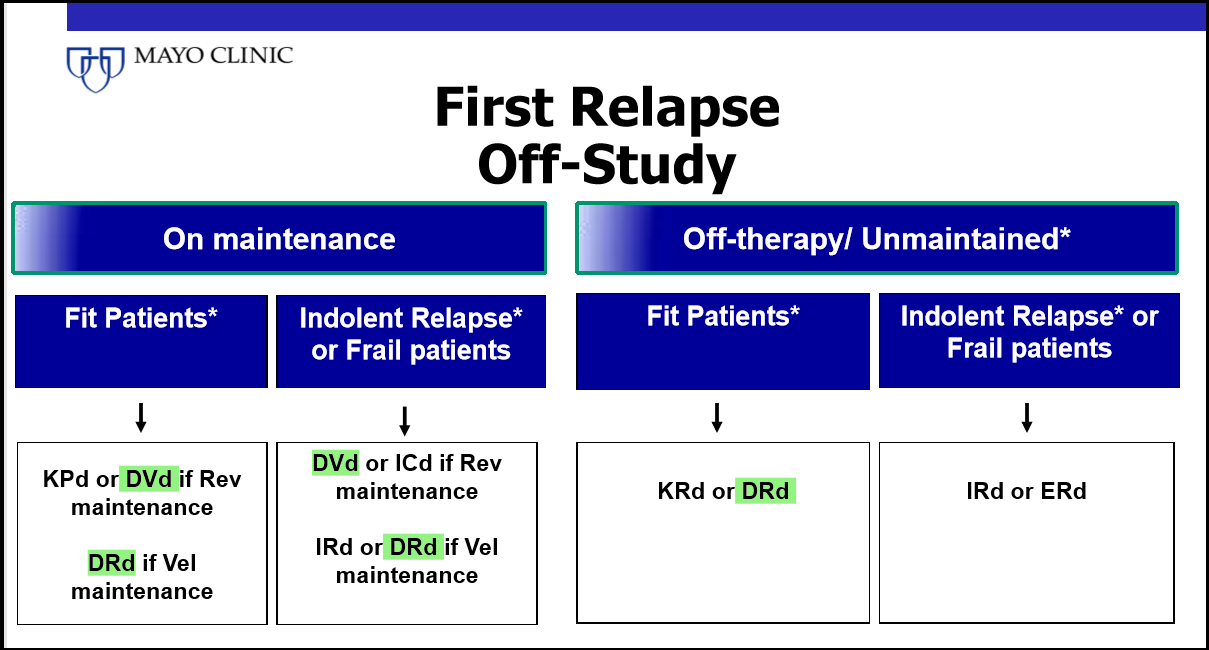
图1 首次复发患者治疗方案
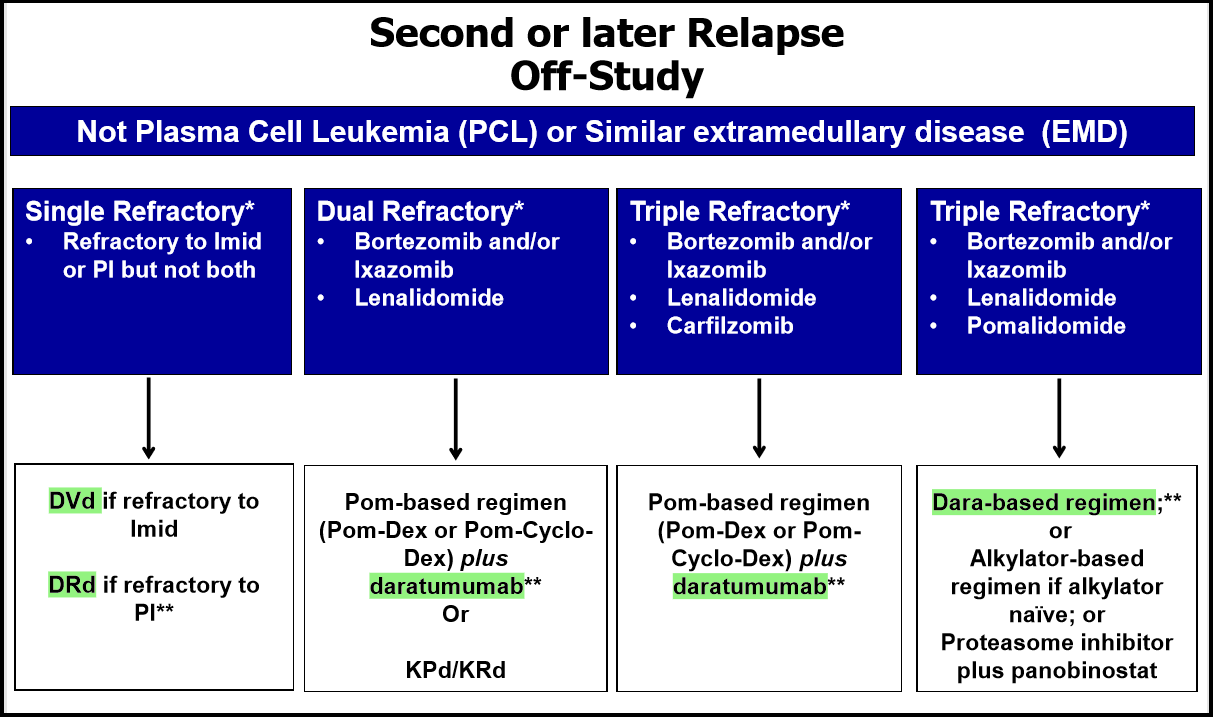
图2 双重或多重耐药患者的治疗方案
3期POLLUX试验[2]纳入了569名先前接受过一种或多种治疗的MM患者,随机分配接受来那度胺和地塞米松(RD)治疗组或联合CD38单抗(DRD)治疗组(图3)。

图3 POLLUX研究:Drd vs rd for RRMM实验设计
结果显示,中位随访时间13.5个月,DRD组12个月PFS率为83.2%,而RD组为60.1%;总体缓解率也显著高于对照组(92.9%vs.76.4%,P<0.001),其中完全缓解或疗效较好的患者比例也更高(43.1% vs.19.2%,P<0.001)。该研究表明,来那度胺与CD38单抗联合应用能带来更显著的疗效获益。
该患者二线接受了DRD(达雷妥尤单抗+来那度胺+地塞米松)方案治疗,很快获得PR的疗效(图4)。结合本病例,对于1q21+MM患者的治疗,应用来那度胺联合CD38单抗的治疗方案具有较好的疗效,为后续尽快行auto-HSCT治疗提供了机会。

图4 患者分别行PAD、DRD方案的IG-A前后变化
[1]王珊,伴1q21扩增的初治多发性骨髓瘤患者临床特点及预后分析
[2] Meletios A. Dimopoulos, M.D.,Albert Oriol, M.D.,Hareth Nahi, M.D., Daratumumab, Lenalidomide, and Dexamethasone for Multiple Myeloma, N Engl J Med 2016; 375:1319-1331;DOI: 10.1056/NEJMoa160775
排版编辑:guangli











 苏公网安备32059002004080号
苏公网安备32059002004080号


