受全球COVID-19疫情影响,美国癌症研究协会(AACR)今年决定不举办线下年会,改为两次AACR在线年会。美国东部时间2020年4月27-28日,AACR在线年会Ⅰ隆重召开。在肺癌靶向治疗专场,多项临床进展百花齐放。

CT081——Ⅱ期ZENITH20-1研究:Poziotinib对经治EGFR 20外显子突变NSCLC患者的疗效分析
研究简介和目的:目前而言,临床上尚没有疗效确定并批准用于治疗EGFR 20外显子突变非小细胞肺癌(NSCLC)的治疗方法。Poziotinib是针对EGFR 20外显子和HER2插入突变的酪氨酸激酶抑制剂(TKI)。在一项多队列、多中心、Ⅱ期ZENITH20-1研究中,研究者评估了Poziotinib在既往接受过治疗的EGFR 20外显子插入突变NSCLC患者中的临床疗效和安全性。
方法:Poziotinib治疗剂量为16 mg口服,一日一次,允许由于不良反应而调整Poziotinib治疗剂量,随访时间为24个月。主要研究终点是采用RECIST v1.1标准评估的客观缓解率(ORR)。如果治疗人群中95%CI的下限大于17%,则达到ORR终点。次要终点包括疾病控制率(DCR),缓解持续时间(DoR),无进展生存期(PFS)和安全性。安全性监测贯穿整个研究过程中。
结果:本研究共纳入115例患者,中位年龄为61岁(33~83岁)。患者既往接受过治疗并失败[中位治疗线数为2 (1~9)],大多数患者接受过化疗和免疫疗法。Poziotinib的中位相对剂量强度为72%(7%~100%),65%的患者剂量减量,10%的患者因相关不良反应(AE)停药。ORR为14.8%(95%CI 8.9%-22.6%),DCR为68.7%(95%CI 59.4%-77.0%)。17例患者疗效评估为确定的部分缓解(PR),5例患者为未确定的PR,62例(53.9%)患者稳定疾病(SD)。总体而言,75例(65%)患者的肿瘤缩小。中位DoR为7.4个月(95%CI 3.7-9.7),中位PFS为4.2个月(95%CI 3.7-6.6)。安全性与其他第二代TKI相似,最常见的治疗相关的3级及以上AE为皮疹(28%),腹泻(26%),口腔炎(9%)和甲沟炎(6%)。作为与TKI治疗相关的重要AE,Poziotinib治疗相关性肺炎的发生率为4%。
结论:尽管该研究未达到主要终点ORR,但Poziotinib治疗可以使大多数患者(65%)肿瘤体积缩小。肿瘤缩小与持久的缓解证明,Poziotinib在既往接受过治疗的EGFR 20外显子突变NSCLC患者中的抗肿瘤活性。研究者正在进一步优化治疗剂量和AE管理。
CT082——Ⅱ期GEOMETRY mono-1研究:Capmatinib在METex14突变(mut)晚期NSCLC中的应用,以及对伴脑转移(BM)患者的疗效分析
背景:Capmatinib是一种高选择性MET抑制剂,可穿越血脑屏障。在GEOMETRY mono-1研究中,Capmatinib在具有METex14跳跃突变的晚期NSCLC患者中显示出具有临床意义的缓解率,包括在基线伴脑转移(BM)患者中同样显示出抗肿瘤活性和可控的安全性。本研究旨在分享Capmatinib治疗的临床疗效和安全性数据,以及在METex14跳跃突变NSCLC伴基线BM患者的疗效分析。
方法:本项Ⅱ期、多队列、多中心GEOMETRY mono-1研究(NCT02414139)旨在评估Capmatinib在ECOG PS评分0~1、ALK和EGFR野生型、METex14突变/MET扩增的ⅢB/Ⅳ期NSCLC成年患者中,包括具有症状稳定/无症状BM患者的临床疗效。入组患者被分配至队列4(经治,2/3线)和队列5b(未接受治疗),并接受Capmatinib 400mg一日二次治疗。主要研究终点:根据RECIST v1.1标准,盲化独立评审委员会(BIRC)评估的ORR。关键次要研究终点为BIRC评估的DoR。基于改良的RECIST v1.1评价标准,BIRC神经放射学专家通过对队列4和5b中所有伴基线BM患者的脑转移灶进行回顾性分析。
结果:截至2019年4月15日,共有97例患者疗效可评估(队列4共有69例患者;队列5b共有28例患者)。BIRC评估的队列4和5b的结果分别为:(i)ORR(95%CI):40.6%(28.9-53.1)和67.9%(47.6-84.1);(ii)中位DoR(95%CI):9.72(5.55-12.98)和11.14(5.55-NE)月;(iii)中位PFS(95%CI):5.42(4.17-6.97)和9.69(5.52-13.86)月。BIRC确认的基线伴可评估BM患者为13例[平均每例患者3.3个脑转移病灶(范围1-8)]。13例患者中,7例(54%)患者颅内缓解,其中4例所有脑转移灶完全消退。其他3例患者:(i)共7个脑转移灶,其中3个完全消退,4个稳定(1个脑转移灶缩小~50%);(ii)共3个脑转移灶,其中2个完全消退,1个稳定;(iii)共4个脑转移灶,其中1个完全消退,3个稳定。在13例基线伴可评估BM患者中,颅内DCR为92.3%(12/13)。颅内反应与全身反应一样快。7例颅内缓解的患者中,3例曾接受过脑部放疗;5例在研究入组时出现已有脑转移灶疾病进展或新发BM的迹象。在所有队列(N=334)中,最常见的治疗相关不良事件(≥15%,所有级别)是周围性水肿(41.6%),恶心(33.2%),血中肌酐升高(19.5%)和呕吐(18.9%)。
结论:BIRC神经放射学专家对13例基线伴可评估BM患者的分析表明,Capmatinib在脑组织中具有抗肿瘤疗效。在METex14突变晚期NSCLC患者中,无论患者的治疗线数如何,Capmatinib均显示出持久深度的缓解作用和可控的安全性。
CT084——KEYNOTE-042研究中STK11和KEAP1突变状态与临床疗效之间的关系:一线帕博利珠单抗单药对比铂类化疗,对PD-L1阳性晚期NSCLC的临床疗效分析
背景:STK11(也称为LKB1)和KEAP1突变,被证实与化疗耐药和不良预后密切相关,在具有高肿瘤突变负荷(TMB)的PD-L1阴性肿瘤中更为常见。本研究对KEYNOTE-042研究(NCT02220894)进行了探索性分析,以评估STK11和KEAP1突变频率及其与临床疗效的关系。
方法:通过全外显子测序(WES)的方法评估肿瘤组织和匹配正常DNA中,STK11和KEAP1的状态以及TMB。用PD-L1 IHC 22C3 pharmDx方法分析评估PD-L1表达水平。通过描述性分析,评估STK11和KEAP1状态与TMB和PD-L1表达状态的相关性,以及STK11和KEAP1状态与疗效之间的关系。
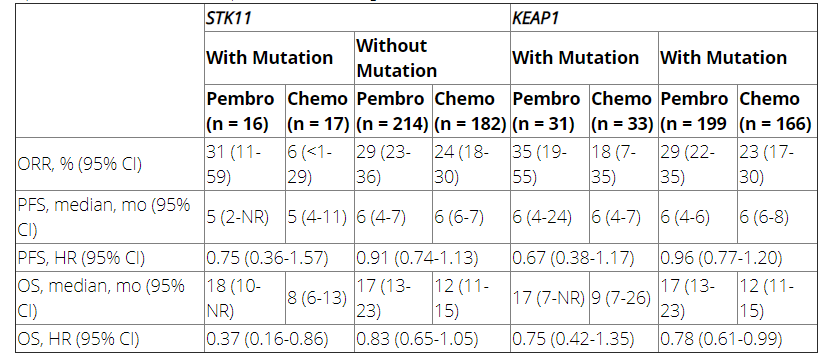
结果:429/1274例患者(34%)的肿瘤组织和正常DNA具有可评估的WES数据。STK11和KEAP1突变分别见于33例(8%)和64例(15%)患者。共有12例(3%)患者存在共突变。发生STK11突变的患者,PD-L1 TPS较未发生STK11突变的患者趋于更低(中位[IQR] 15%[3-50] vs 40%[10-80]);TPS在有或没有KEAP1突变的患者中趋于相似(40%[10-81] vs 40%[10-80])。相比于没有STK11或KEAP1突变的患者,存在STK11(中位[IQR] 191 [104-272] vs 146 [72-253])或KEAP1(183 [114-283] vs 142 [68-252])突变的患者的TMB水平往往更高。帕博利珠单抗治疗的ORR,PFS和OS,在有或无STK11、KEAP1突变的患者中相似;有STK11突变的患者与无STK11突变的患者相比,化疗的疗效较低。具体结果可见于下表。不论STK11或KEAP1的状态如何,帕博利珠单抗都比化疗有更好的预后。
结论:该探索性分析的结果表明,无论STK11或KEAP1的状态如何,都应将帕博利珠单抗单药治疗,视为PD-L1阳性晚期NSCLC的标准一线治疗选择。
CT085——KEYNOTE-189研究事后分析:培美曲塞(Pem)+铂类(Plat)联合帕博利珠单抗(Pembro)治疗转移性非鳞NSCLC的安全性分析
背景:Pem+Plat+Pembro可延长转移性非鳞NSCLC的OS和PFS。为了评估联合用药的安全性,本研究评估了接受Pem+Plat+Pembro或安慰剂治疗的患者,3~5级AE的发生和缓解时间,以及后续治疗中止情况。
方法:分析KEYNOTE-189研究中的所有被治疗者(ASaT)人群。数据截止日期为2017年11月8日。任何原因的AE均为MedDRA 20.1标识。本研究描述了中位和四分位间距的AE发生和缓解时间,以及因AE导致的治疗中止。
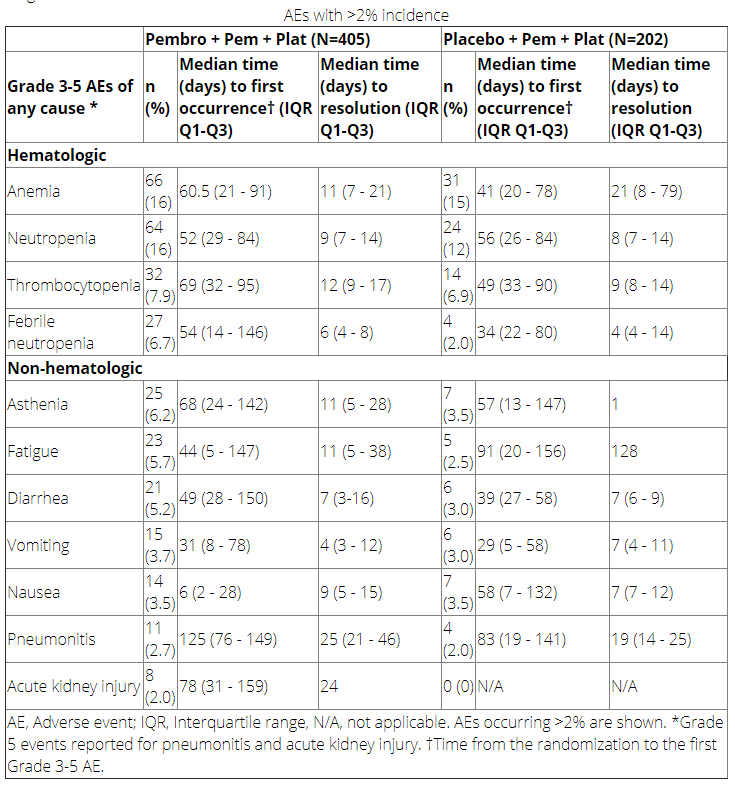
结果:研究中共包括607例患者(Pembro组 vs 安慰剂组:405 vs 202)。中位年龄为64岁,72%的患者接受卡铂治疗,18%的患者曾有基线脑转移病史。Pembro和安慰剂组的中位治疗时间分别为7.4和5.4个月。每组中分别有272例(67.2%)和133例(65.8%)患者发生3~5级AE。发生率>2%的AE发生和缓解时间情况可见于下表。其中,初次出现恶心的中位时间最短(6天),而发生肺炎的中位时间最长(125天)。从AE发生到缓解的中位时间从4天(呕吐)到25天(肺炎和贫血)不等。在两个治疗组中,分别有112(27.7%)和30(14.8%)例患者因AE导致治疗中止。在1~4周期中,因AE导致33%的患者停止Pem或40%的患者停止Pembro。当Pem与Pembro联合使用时,由于AE导致Pem停药的比例与安慰剂组相当(每个周期平均为2.0% vs 1.4%)。
结论:大多数AE首次发生在治疗后的3个月内,并在发病后2周内得到缓解。Pembro+Pem+Plat长期使用安全性可靠,毒性可控。
CT086——临床试验和真实世界中NSCLC接受免疫疗法或化疗的肺炎发生率分析
背景:肺炎是某些抗癌药物潜在的、威胁生命的不良事件。本研究在临床试验(CT)和真实世界数据(RWD)中,比较了有或无(+/-)既往肺炎病史的晚期NSCLC患者,接受免疫检查点抑制剂(ICI)或化疗(chemo)的治疗相关性肺炎(TAP)的发生情况。
方法:对8项ICI对比化疗治疗晚期NSCLC的临床试验,检索肺炎、急性间质性肺炎、化学性肺炎和间质性肺病发生情况。使用来自社区卫生系统的RWD,检索接受ICI(+/-化疗)或化疗(无同步放疗)的晚期NSCLC患者;肺炎使用ICD-9和ICD-10包括肺炎或统一医学用语系统中的相关概念定义。RWD患者使用CT的核心资格标准来选择。在CT和RWD中,计算4个亚组的肺炎发生比例:有或无(+/-)既往肺炎病史患者接受ICI vs 化疗发生的肺炎。评估肺炎诊断类型,包括放疗性肺炎。
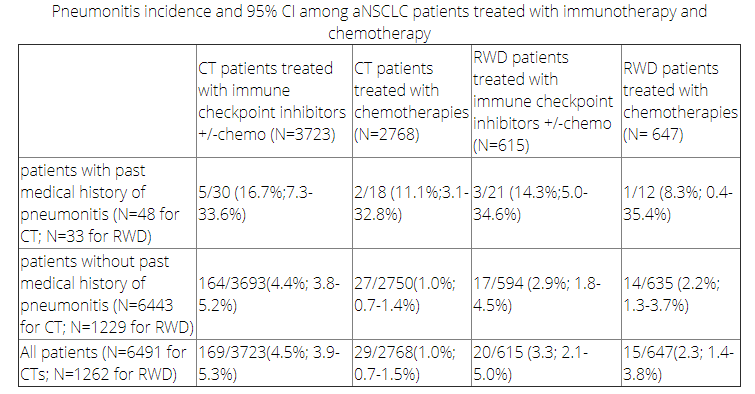
结果:在CT和RWD中,ICI组和化疗组中有既往肺炎病史的晚期NSCLC患者发生TAP的比例,均高于无既往肺炎病史的患者,见下表。CT中,没有既往肺炎病史的患者发生ICI相关肺炎比化疗相关肺炎更常见。CT和RWD中,TAP率类似。RWD中,ICI组和化疗组任何时间发生的肺炎都与放疗密切相关,所有诊断为肺炎的73%与放疗有关。
结论:在CT和RWD中,存在既往肺炎病史的晚期NSCLC患者接受ICI和化疗的TAP发生风险更高。RWD数据表明,放疗是导致肺炎的常见原因。仅在CT数据中,并且仅对于无既往肺炎病史的患者,ICI组与化疗组的TAP发生率有差异。必须进行进一步研究(例如包含使用TKI治疗的患者)以优化有既往肺炎病史的癌症患者的治疗。
1. Xiuning Le, Jonathan Goldman, Jeffrey Clarke, et al. Poziotinib activity and durability of responses in previously treated EGFR exon 20 NSCLC patients - a Phase 2 study[EB/OL].2020 AACR, abstract CT081.
2. Edward B. Garon, Rebecca S. Heist, Takashi Seto, et al. Capmatinib in METex14-mutated (mut) advanced non-small cell lung cancer (NSCLC): Results from the phase II GEOMETRY mono-1 study, including efficacy in patients (pts) with brain metastases (BM)[EB/OL].2020 AACR, abstract CT082.
3. Byoung Chul Cho, Gilberto Lopes, Dariusz M. Kowalski, et al. Relationship between STK11 and KEAP1 mutational status and efficacy in KEYNOTE-042: pembrolizumab monotherapy versus platinum-based chemotherapy as first-line therapy for PD-L1-positive advanced NSCLC[EB/OL].2020 AACR, abstract CT084.
4. Edward B. Garon, Fangfang Sun, Catherine E. Muehlenbein, et al. Safety of pemetrexed (Pem) plus platinum (Plat) in combination with pembrolizumab (Pembro) for metastatic nonsquamous NSCLC: A post hoc analysis of KEYNOTE-189[EB/OL].2020 AACR, abstract CT085.
5. Qi Liu, Chenan Zhang, Yutao Gong, et al. Pneumonitis incidence in patients with non-small cell lung cancer treated with immunotherapy or chemotherapy in clinical trials and real-world data[EB/OL].2020 AACR, abstract CT086.
排版编辑:MJ














 苏公网安备32059002004080号
苏公网安备32059002004080号


