塞瑞替尼,作为第二代ALK TKI药物,最初经ASCEND-1和ASCEND-4研究,确定了750mg空腹服用作为临床用药方案,但该方案胃肠道不良事件(AE)发生率较高。虽然大多数胃肠道AE为1~2级,但塞瑞替尼750mg空腹服用,患者的治疗依从性较差,导致剂量调整或治疗中断/延迟的比例较高,可能影响治疗效果。为解决这个问题,研究人员开展了ASCEND-8研究,探讨剂量和服用方式调整后塞瑞替尼的安全性和有效性,结果表明,塞瑞替尼450mg减量随餐服用不仅减少了胃肠道AE,疗效反而还有增加的趋势。 对此我们特邀解放军总医院第五医学中心刘晓晴教授为您介绍塞瑞替尼剂量调整的前世今生。


解放军总医院第五医学中心肺部肿瘤科
中国临床肿瘤学会(CSCO)理事会理事
CSCO小细胞肺癌专家委员会副主任委员
中国抗癌协会肺癌专业委员会委员
精准医学与肿瘤康复专业委员会副主任委员
中国老年肿瘤专业委员会肺癌分委会常委
中国抗癌协会化疗专业委员会委员
中国药学会抗肿瘤药物专业委员会委员
中国医疗保健国际交流促进会胸部肿瘤分会常委
全军放射肿瘤治疗学专业委员会委员
中央军委保健专家
抗癌药物剂量/服药方式调整可以提高药物生物利用度和降低不良反应
精准靶向治疗药物的问世,为肿瘤治疗带来了革命性的改变,随之而来的的问题是,最佳药物剂量是否依然应延续传统化疗药物的方案,采用最大耐受剂量用于临床治疗?是否在耐受范围内,剂量越高越好,more is better?其实,不尽如此。有诸多药物降低剂量改善用药方案后,通过提高生物利用度,维持药物疗效的案例。阿比特龙(abiraterone acetate)常规空腹以1000mg的剂量与泼尼松合用,用于治疗转移性去势抵抗性前列腺癌(mCRPC),一项研究表明,以常规剂量的1/4(250mg)随餐服用,在疗效及降低前列腺特异性抗原(PSA)水平方面,与常规剂量等效,不良反应同样相似。另一个用于HER2阳性乳腺癌的靶向治疗药物,拉帕替尼,常规用药方案为每天以1250mg早餐前或后一小时服用,但后续研究表明,随餐服用,低脂或高脂餐饮均可以显著提高其生物利用度,甚至有研究表明,以常规剂量的1/5(250mg)随餐或用果汁送服,可以维持原有药物疗效。二代EGFR TKI,诸如阿法替尼和达可替尼也都展现出less is better,减量不减效。
这一现象引起了人们对靶向治疗最适剂量的反思与探讨,药物的上市剂量究竟应推荐最大耐受剂量,还是推荐最适剂量?塞瑞替尼减量后,是不是也能保证疗效,甚至有更好的疗效?
塞瑞替尼是第二代高效、高选择性的口服小分子ALK TKI。体外研究显示,塞瑞替尼对ALK的亲和力是目前获批上市的ALK TKI中最高的,约为克唑替尼的20倍,阿来替尼的13倍,其临床前数据也展现出高效的肿瘤杀伤作用。
ASCEND-1研究表明,在系统治疗失败后进展的ALK阳性晚期NSCLC,后线塞瑞替尼干预均带来了可喜的疗效。于是,仅凭借亮眼的I期临床数据,美国食品药品监督管理局(FDA)就批准了塞瑞替尼的上市。在随后开展的ASCEND-4和ASCEND-5研究中,塞瑞替尼的疗效更是在ALK阳性晚期NSCLC患者的一线治疗和二线治疗中得到了验证。在2017年塞瑞替尼随即获批ALK阳性晚期NSCLC一线治疗适应证后,并被美国国立综合癌症网络(NCCN)指南作为一类推荐用药。在国家卫健委“新型肿瘤药物临床应用指导原则”(2019版)指出,在患者同意的情况下,可以选择塞瑞替尼作为一线治疗。
ASCEND-1和ASCEND-4研究在奠定塞瑞替尼治疗ALK阳性晚期NSCLC患者的重要地位的同时,也提示了塞瑞替尼在胃肠道不良反应发生率较高。该系列研究中,塞瑞替尼的给药方式为750mg空腹服用方案,56%~80%的患者出现1~2级的呕吐、恶心、腹泻等胃肠道AE,5%左右的患者出现3级胃肠道AE。ASCEND-4研究中,80%的患者由于AE不得不接受剂量调整,甚至中断/延迟治疗,这无疑会对塞瑞替尼的治疗疗效产生影响,同时影响患者的生活质量。胃肠道毒性较高成为塞瑞替尼临床应用中急需解决的问题。
那么能否通过改变用药方式增加生物利用度,从而降低用药浓度,在保证疗效的同时,减少毒副反应的发生呢?答案是肯定的。
在一项入组了健康成人的随机、开放标签、2阶段交叉食物效应研究中,探讨了随餐服用模式相对于空腹对塞瑞替尼(500 mg和750 mg)的安全性和生物利用度的影响。研究表明,500mg和750mg用药组,随餐(低脂餐,高脂餐或者小食)服用塞瑞替尼,对比空腹用药,Cmax及AUC均显著增加(500mg:AUC0-∞ 增加58% (低脂)和73%(高脂);Cmax增加43% (低脂)和41% (高脂);750 mg:AUC0-∞增加54% (低脂小食);Cmax增加45% (低脂小食))。随餐服用模式显著提高了塞瑞替尼的生物利用度。更重要的是,塞瑞替尼500mg随餐相较于750mg空腹有效减少了腹泻及恶心等胃肠道不良反应的发生。
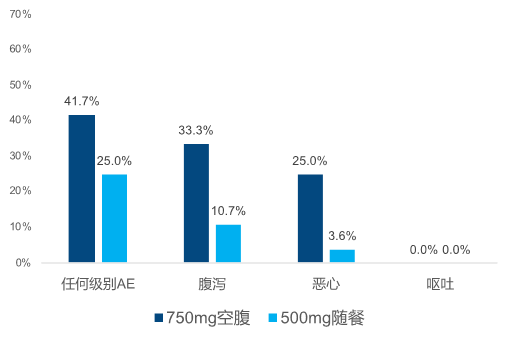
图1.塞瑞替尼500mg随餐较750mg空腹显著降低胃肠道不良反应
ASCEND-8及真实世界数据表明,塞瑞替尼450mg随餐服用方案更安全有效
有了前期调整剂量及给药方案的数据支持,提示我们通过降低用药剂量,随餐服用,低剂量塞瑞替尼依然能保证药物的有效生物学浓度并解决塞瑞替尼的胃肠道毒性问题。在此基础上,研究人员开展了随机、开放标签的I期ASCEND-8研究,评估塞瑞替尼450mg/600mg随餐服用对比750mg空腹服用在ALK阳性晚期NSCLC的疗效及安全性。2015年4月20日至2017年11月21日,ASCEND-8研究纳入来自24个国家87家中心共306患者。研究设计见图2。
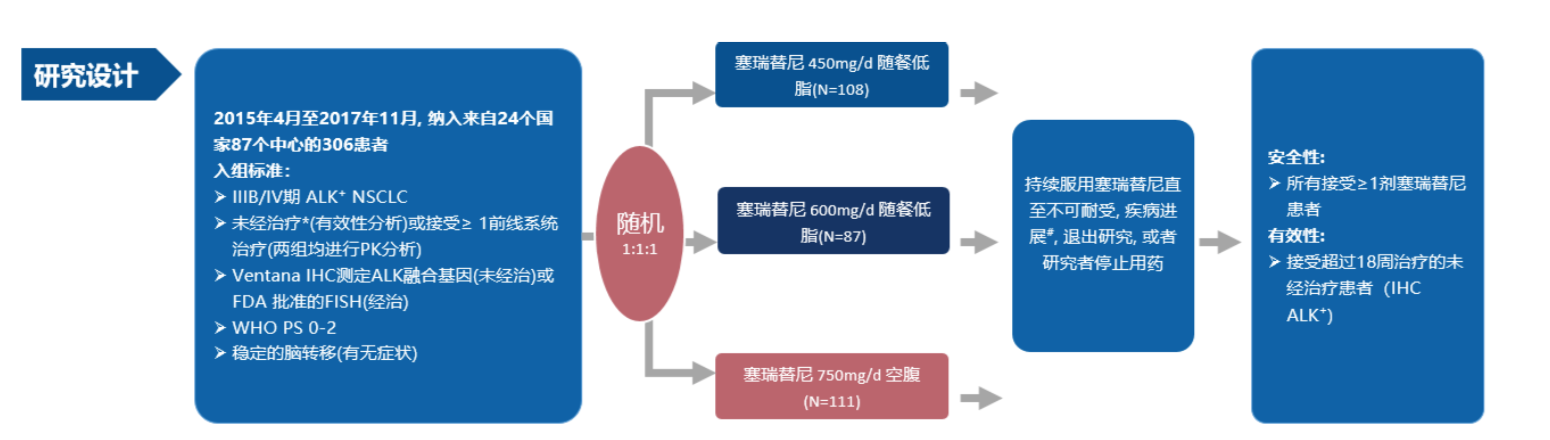
图2.ASCEND-8研究设计
药效动力学研究表明,塞瑞替尼450mg随餐相比750mg空腹,0~24小时血药浓度时间曲线下面积(AUC0-24h)和血药峰浓度(Cmax)均相当,有效浓度及药物代谢情况并无明显差异。
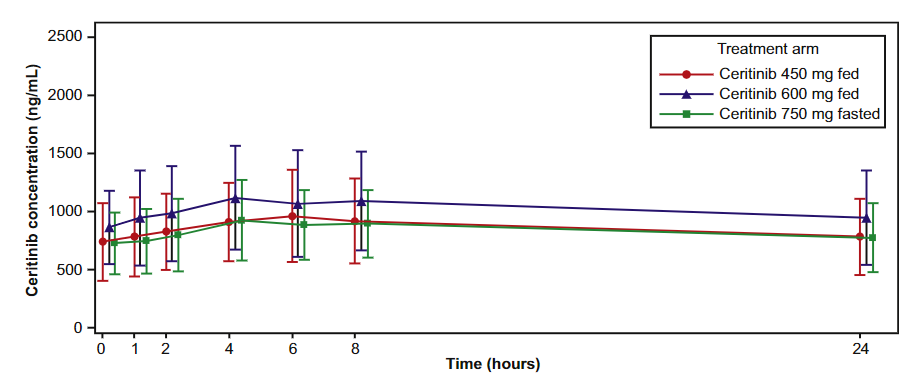
图3.塞瑞替尼450mg随餐相比750mg空腹,AUC0-24h和Cmax值相当
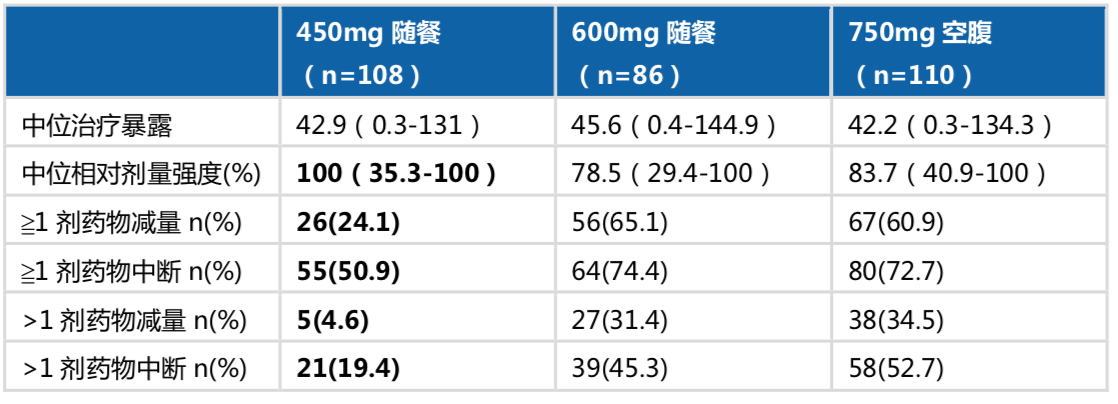
降低药物剂量和改变服用方式提高了患者的用药依从性,显著降低治疗中断及剂量调整等事件的发生,这从一定程度上为塞瑞替尼的足疗程应用提供了保障。
表1.塞瑞替尼450mg随餐组的依从性显著提高
 同时安全性分析表明,450mg随餐组相比750mg空腹组,胃肠道AE发生率明显下降,所有级别胃肠道AE分别为腹泻57.4% vs 79.1%,恶心41.7% vs 57.3%,呕吐38.9% vs 63.6%;胃肠道AE严重程度明显更低,主要为1级,极少发生3/4级。
同时安全性分析表明,450mg随餐组相比750mg空腹组,胃肠道AE发生率明显下降,所有级别胃肠道AE分别为腹泻57.4% vs 79.1%,恶心41.7% vs 57.3%,呕吐38.9% vs 63.6%;胃肠道AE严重程度明显更低,主要为1级,极少发生3/4级。

图4. ASCEND-8研究中,塞瑞替尼450mg随餐显著降低胃肠道不良反应
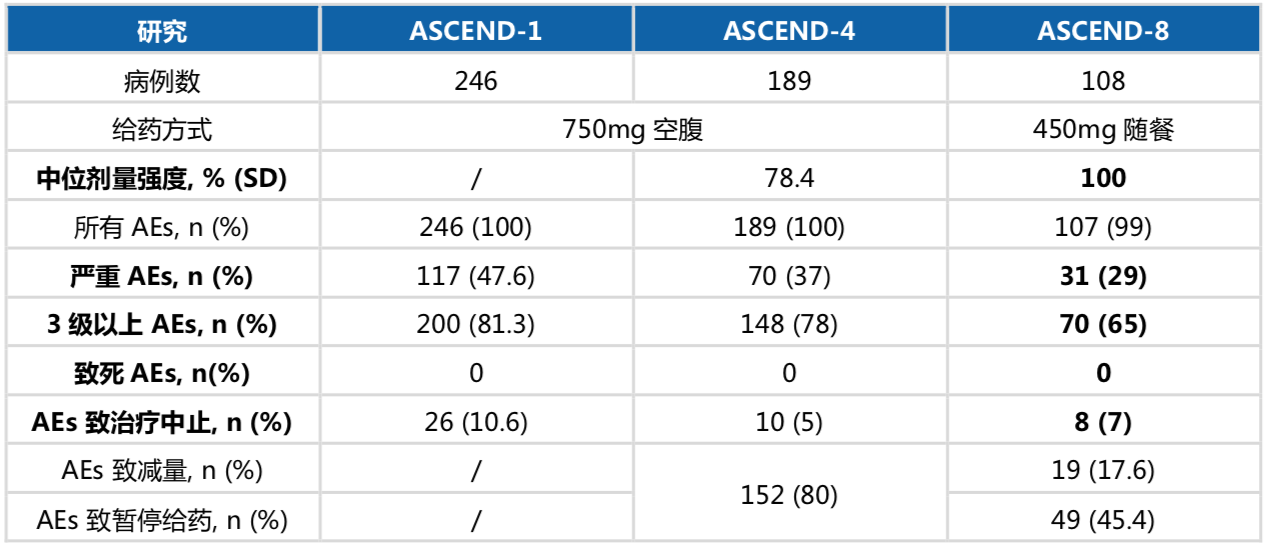
间接比较ASCEND-1,-4和-8研究、中位剂量强度在ASCEND-4研究中750mg空腹组只有78.4%,但是随着剂量调整为450mg随餐,中位剂量强度可达100%,得到明显改善。塞瑞替尼剂量调整后,3~4级不良反应发生率明显降低,其中严重不良反应发生率明显降低。塞瑞替尼没有致死性AE发生。
表2.ASCEND-1、4和8研究中,不同给药方式的安全性比较
 除了ASCEND-8研究,来自真实世界研究的数据也得到了同样的结果。在2019年世界肺癌大会(WCLC)上报道了一项真实世界研究,对使用塞瑞替尼450mg随餐服用方案治疗中国的ALK/ROS-1阳性NSCLC患者,进行安全性及近期疗效分析。51例入组患者中,在接受塞瑞替尼治疗之前,82.1%的患者接受了二线以上的治疗,23.5%的患者接受了三线以上的治疗。AE事件统计结果表明,仅个别患者出现3/4级胃肠道AE,胃肠道和其他主要AE的发生率都较低,与ASCEND-8研究结论一致。
除了ASCEND-8研究,来自真实世界研究的数据也得到了同样的结果。在2019年世界肺癌大会(WCLC)上报道了一项真实世界研究,对使用塞瑞替尼450mg随餐服用方案治疗中国的ALK/ROS-1阳性NSCLC患者,进行安全性及近期疗效分析。51例入组患者中,在接受塞瑞替尼治疗之前,82.1%的患者接受了二线以上的治疗,23.5%的患者接受了三线以上的治疗。AE事件统计结果表明,仅个别患者出现3/4级胃肠道AE,胃肠道和其他主要AE的发生率都较低,与ASCEND-8研究结论一致。
临床试验和真实世界数据都表明,塞瑞替尼450mg随餐服用方案的安全性更好,那么减少用药剂量是否会影响疗效呢?
Less is More,减量不减效
ASCEND-8研究显示,对塞瑞替尼450mg随餐组中位随访14.3个月,经第三方独立评审机构评估的中位PFS仍未达到,而750mg空腹组和600mg随餐组的中位PFS分别为12.2和17.0个月。从当前数据来看,显然降低剂量并没有显著影响塞瑞替尼的疗效。
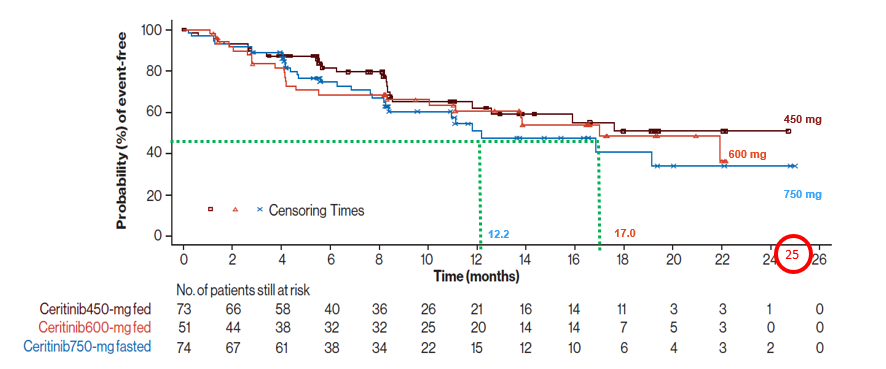
图5. 塞瑞替尼450mg随餐组的中位PFS最优,仍未达到
另一项来自中国台湾的真实世界研究中,共计入组48例初治的ALK阳性NSCLC患者,其中35例患者接受克唑替尼治疗(250mg,每日两次),13例患者接受塞瑞替尼治疗(750mg或450mg)。塞瑞替尼组获得了更长的PFS,中位PFS为45.0个月,克唑替尼的中位PFS为11.5个月(HR=0.18,P=0.010),塞瑞替尼显著降低82%的疾病进展风险。
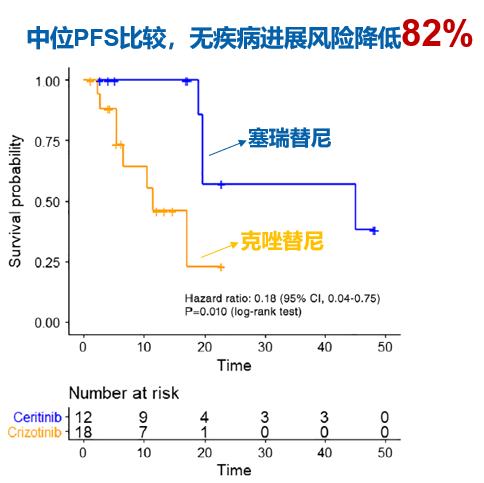
图6.对于初治的ALK阳性NSCLC,塞瑞替尼较克唑替尼显著降低82%的疾病进展风险
总之,无论是临床前数据、后续队列研究,还是真实世界研究,塞瑞替尼在ALK阳性NSCLC的一线/后线治疗中均展现出喜人的疗效,但起始确定的750mg空腹治疗方案面临胃肠道相关毒副作用大、难以耐受的困境。幸运的是,这个难题并非无解,临床使用时调整用药剂量和服用方式就可以克服。ASCEND-8研究表明,450mg随餐用药方案可以显著降低相关毒副作用的发生,真实世界的数据同样验证了这一结论。并且,塞瑞替尼减量用药并不会使疗效打折扣,多方面数据表明,450mg随餐用药方案在降低毒副作用的同时,可以有效保证或甚至增加塞瑞替尼的疗效。Less is more!
[1] Lau, Y. Y. et al. Effects of meal type on the oral bioavailability of the ALK inhibitor ceritinib in healthy adult subjects. J Clin Pharmacol 56, 559–566 (2016).
[2] D.-W. Kim et al., Activity and safety of ceritinib in patients with ALK -rearranged non-small-cell lung cancer (ASCEND-1): updated results from the multicentre, open-label, phase 1 trial. The Lancet Oncology. 17, 452–463 (2016).
[3] L. Crinò et al., Multicenter Phase II Study of Whole-Body and Intracranial Activity With Ceritinib in Patients With ALK-Rearranged Non-Small-Cell Lung Cancer Previously Treated With Chemotherapy and Crizotinib: Results From ASCEND-2. J. Clin. Oncol. 34, 2866–2873 (2016).
[4] J.-C. Soria et al., First-line ceritinib versus platinum-based chemotherapy in advanced ALK-rearranged non-small-cell lung cancer (ASCEND-4): a randomised, open-label, phase 3 study. Lancet. 389, 917–929 (2017).
[5]B. C. Cho et al., Efficacy and Safety of Ceritinib (450 mg/d or 600 mg/d) With Food Versus 750-mg/d Fasted in Patients With ALK Receptor Tyrosine Kinase (ALK)–Positive NSCLC: Primary Efficacy Results From the ASCEND-8 Study. Journal of Thoracic Oncology. 14, 1255–1265 (2019).
[6] S. H. Huang et al., Front‐line treatment of ceritinib improves efficacy over crizotinib for Asian patients with anaplastic lymphoma kinase fusion NSCLC: The role of systemic progression control. Thorac Cancer. 10, 2274–2281 (2019).
[7]F. Liang, D. Shen, EP1.14-02 Comparative Efficacy of First-Line Ceritinib at a Dose of 450mg with Food and Alectinib in Advanced ALK+ NSCLC. Journal of Thoracic Oncology. 14, S1032 (2019)..
MCC号ZYK2201854有效期2023-01-12,资料过期,视同作废。
排版编辑:Vicky














 苏公网安备32059002004080号
苏公网安备32059002004080号


