EGFR突变阳性晚期NSCLC具有高度异质性,肿瘤异质性和肿瘤细胞克隆演化会影响治疗选择和疗效。泛ErbB家族抑制剂阿法替尼能够提高T790M突变丰度,进而可能增加对序贯三代EGFR-TKI治疗的敏感性。随机对照研究以及真实世界数据均提示阿法替尼序贯三代EGFR-TKI能够带来更好的疗效。

北京大学第三医院 肿瘤化疗与放射病科北京市肿瘤治疗质量控制与改进中心委员会委员
北京抗癌协会中西医结合专业委员会委员
北京中西医结合学会呼吸专业委员会委员
《中华放射医学与防护学杂志》编委
《国际放射医学核医学杂志》编委
2011-2012年曾MD Anderson cancer center 学习与工作
背景
表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)是EGFR突变的晚期NSCLC的标准治疗。然而由于EGFR突变的晚期NSCLC具有高度异质性,可以通过多重分子机制促进耐药肿瘤细胞克隆增殖,所以从一代到三代药物都不可避免会发生获得性耐药。目前已上市的EGFR-TKI中,一代TKI如吉非替尼和厄洛替尼,仅能与EGFR可逆性结合;二代TKI代表药物阿法替尼的作用机制与一代药物不同,阿法替尼是一种泛ErbB家族受体阻滞剂,不可逆的与所有可能的ErbB同源或异源二聚体激酶域结合,阻断信号传导,且阻断效力更强;三代药物如奥希替尼则是与EGFR共价结合,针对性的与EGFR T790M特异性结合。
本文将对EGFR-TKI的耐药机制进行深入探讨,并从肿瘤异质性角度分析耐药的深层原因,探讨EGFR-TKI序贯用药的最佳顺序,从而进一步延长无进展生存时间(PFS)并提高患者生存获益。
克隆演化与肿瘤异质性影响治疗选择
首先,需要明确克隆演化与肿瘤异质性对于诊断、治疗及耐药性的影响。多项研究提示,EGFR突变阳性的肿瘤细胞是复杂且高度异质的[1]。肿瘤发生发展过程中的基因组不稳定性导致产生了一些“优势细胞群”,并在一定的微环境或治疗作用下,具有表型优势的克隆选择性生长,最终演化为特定亚克隆的细胞群[2-3]。随着二代测序平台和技术的普及,新型液体活检技术的应用,越来越多的耐药机制被揭示[4]。
了解“系统发育树”有助于进一步理解肿瘤异质性在耐药方面的意义[5-8]。“干枝性突变”及“分枝性突变”的概念其实大家并不陌生。通俗来说“干枝性突变”就是在某个体所患肿瘤中最“主要”的突变,其一般出现在肿瘤早期,并在大多数肿瘤细胞/组织中存在。在伴有EGFR突变的NSCLC中,针对“干枝性突变”的治疗在起初效果卓著。然而随着时间的推移,优势克隆细胞群会发生大幅变化,逐步出现“分枝性突变”(图1)。“分枝性突变”可浅显的理解为“相对次要”或“突变频率较低”的其他突变位点,(可以在诊断初期就存在,但多在治疗过程中逐步产生,并仅出现于某些肿瘤的区域,分布相对局限)。但值得注意的是,“分枝性突变”的出现虽然影响了药物前期的治疗效果,但对后续治疗药物的选择有了指导作用。
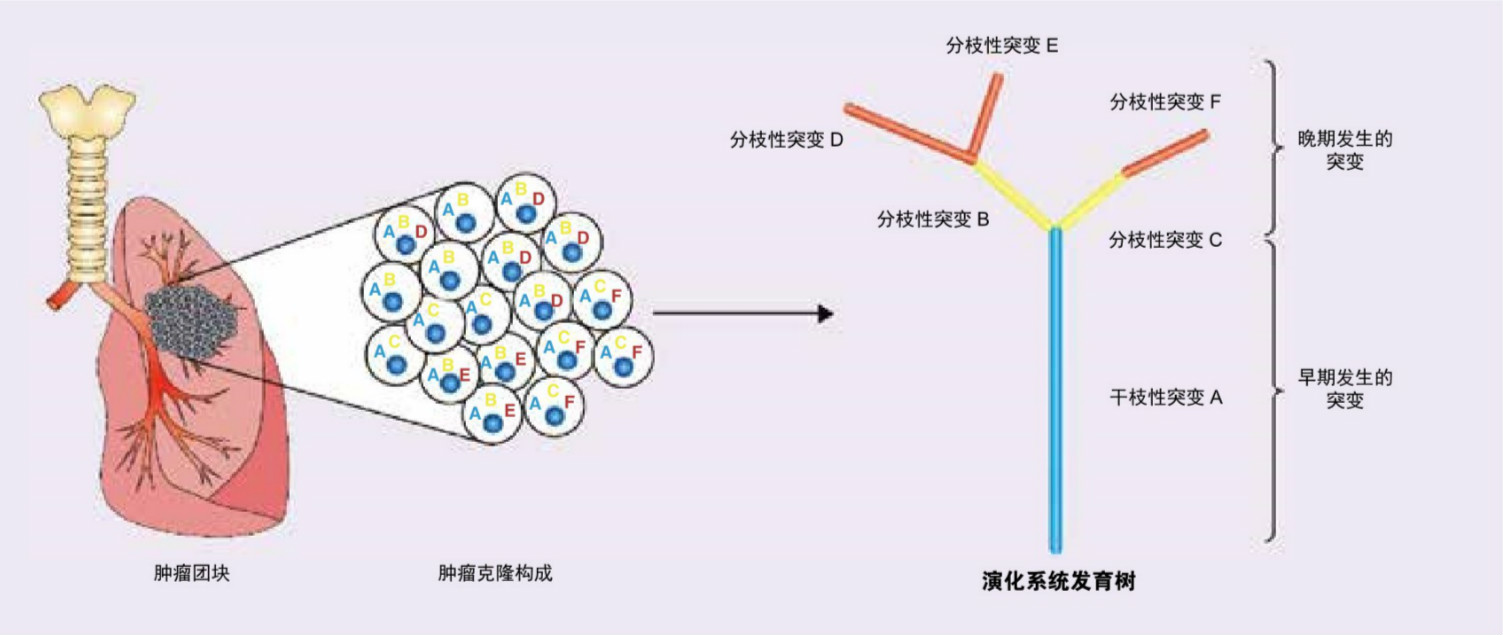
图1.系统发育树分析
阿法替尼提高T790M耐药突变的丰度
临床前研究提示[9],与一代和三代TKI相比,二代TKI有较广的ErbB抑制谱(图2)。一项评估NSCLC细胞耐药机制的基础研究[10]发现,EFGR Del19突变的NSCLC细胞经阿法替尼和厄洛替尼药物处理后大多数出现了T790M耐药突变,但经阿法替尼处理的细胞中T790M等位基因出现频率高于经厄洛替尼处理的细胞。这提示,阿法替尼处理后的T790M突变丰度更高,序贯奥希替尼可能获得更好的疗效(如图3所示:比较一二代TKI耐药所致T790M突变中甲硫氨酸与苏氨酸第2编码位的胸腺嘧啶与胞嘧啶比例来判断突变纯度)。
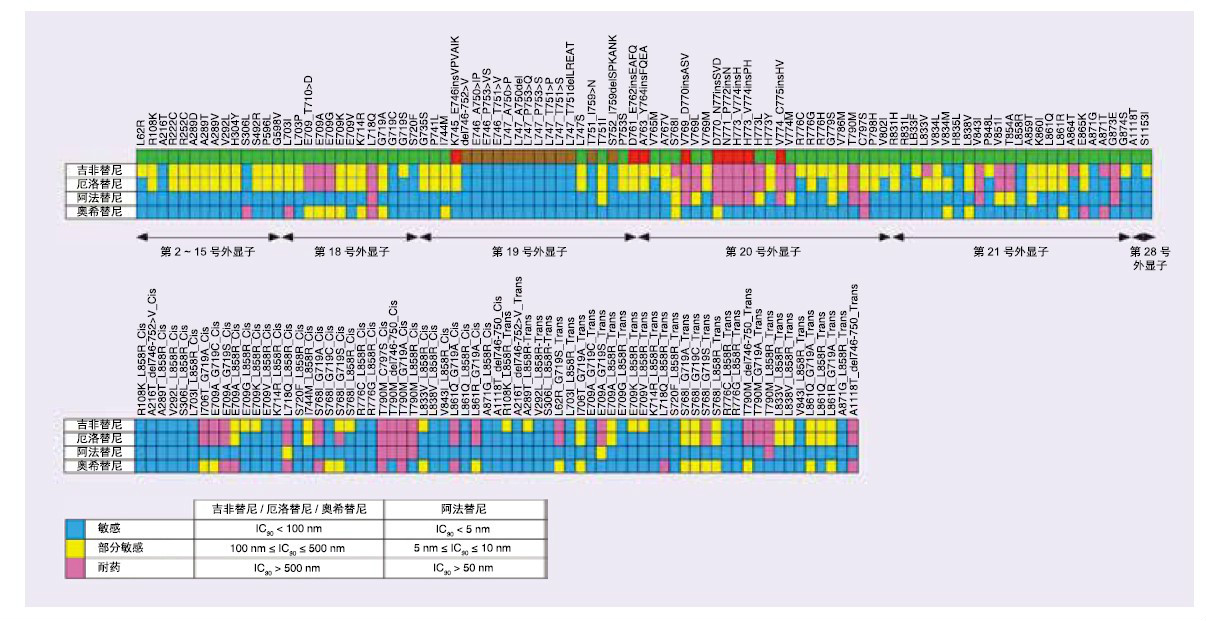
图2.在Ba/F3细胞中采用所有选定突变合一(mixed-all-nominated-mutants-in-one,MANO)分析法评估少见单一或复合EGFR突变的药物敏感性。

图3.对厄洛替尼和阿法替尼耐药的EGFR del19 Ba/F3 细胞中的T790M基因剂量。
阿法替尼序贯奥希替尼可能使患者最大化获益
在LUX-LUNG7研究[11]后续治疗随访中可见,一线治疗使用阿法替尼,后序贯使用奥希替尼的患者,3年总生存(OS)率≥90%。提示阿法替尼序贯奥希替尼,可作为一种序贯治疗的策略。
GioTag研究[12]是第一项国际多中心观察性研究,旨在评估患者接受一线阿法替尼序贯奥希替尼治疗的疗效。研究回顾性分析了真实世界中一线接受阿法替尼治疗,耐药后出现T790M突变,二线接受奥希替尼治疗的患者。结果显示,一线阿法替尼序贯二线奥希替尼的模式可以维持很长时间的临床获益,中位OS达到41.3个月(90%CI:36.8-46.3),且临床各个亚组的患者均可以从序贯治疗中获益,尤其是Del 19患者(中位OS 45.7个月)。值得强调的是,Giotag研究中,二线奥希替尼至治疗失败时间(TTF)为15.6个月,数值上较AURA3研究中10.1个月的无疾病进展生存时间(PFS)有所延长。这似乎也验证了前文提到的T790M突变丰度影响奥希替尼疗效的设想。
总结
EGFR-TKI的最佳用药方案仍在探索中。基于目前的证据,临床前研究表明阿法替尼耐药亚克隆(T790M)的同质性相对较高,可能在后续二线治疗对奥希替尼更敏感;GioTag研究表明,阿法替尼序贯奥希替尼治疗,能够提升二线奥希替尼疗效,最大程度延长患者 EGFR-TKI 治疗时间。同时日本的ABC研究也证实阿法替尼联合贝伐单抗可以诱导 T790M 阴性转阳性,考虑与激发“克隆选择”从而纯化了异质肿瘤中的 T790M 阳性细胞有关。上述研究为 EGFR 突变的 NSCLC 患者的治疗模式提供了新的思考方向。生物科学技术的进一步发展将有利于监测肿瘤细胞演化的过程,进一步探索肿瘤细胞异质性,并深入挖掘耐药机制,以期更好的指导 EGFR突变阳性 NSCLC 患者的最佳治疗策略。
[1] Aparicio S, Caldas C. The implications of clonal genome evolution for cancer medicine. N. Engl. J. Med. 368(9), 842–851 (2013).
[2] Nowell PC. The clonal evolution of tumor cell populations. Science 194(4260), 23–28 (1976).
[3] Burrell RA, McGranahan N, Bartek J et al. The causes and consequences of genetic heterogeneity in cancer evolution. Nature 501(7467),338–345 (2013).
[4] Rolfo C, Mack PC, Scagliotti GV et al. Liquid biopsy for advanced non-small cell lung cancer (NSCLC): a statement paper from the IASCL. J. Thorac. Oncol. 13(9), 1248–1268 (2018).
[5] Gerlinger M, Rowan AJ, Horswell S et al. Intratumor heterogeneity and branched evolution revealed by multiregion sequencing. N.
Engl. J. Med. 366(10), 883–892 (2012).
[6] de Bruin EC, McGranahan N, Mitter R et al. Spatial and temporal diversity in genomic instability processes defines lung cancer evolution. Science 346(6206), 251–256 (2014).
[7] Blakely CM, Watkins TBK, Wu W et al. Evolution and clinical impact of co-occurring genetic alterations in advanced-stage EGFR-mutant lung cancers. Nat. Genet. 49(12), 1693–1704 (2017).
[8] Hata AN, Niederst MJ, Archibald HL et al. Tumor cells can follow distinct evolutionary paths to become resistant to epidermal growth factor receptor inhibition. Nat. Med. 22(3), 262–269 (2016).
[9] Kobayashi Y, Mitsudomi T. Not all epidermal growth factor receptor mutations in lung cancer are created equal: perspectives for individualized treatment strategy. Cancer Sci. 107(9), 1179–1186 (2016).
[10] Kohsaka S, Nagano M, Ueno T et al. A method of high-throughput functional evaluation of EGFR gene variants of unknown significance in cancer. Sci. Transl. Med. 9(416), pii:eaan6566 (2017)
[11] Park K, Tan EH, O’Byrne K et al. Afatinib versus gefitinib as first-line treatment of patients with EGFR mutation-positive non-small-cell lung cancer (LUX-Lung 7): a Phase 2B, open-label, randomised controlled trial. Lancet Oncol. 17(5), 577–589 (2016).
[12] Hochmair M J, Morabito A, Hao D, et al. Sequential treatment with afatinib and osimertinib in patients with EGFR mutation-positive non-small-cell lung cancer: an observational study[J]. Future Oncology, 2018, 14(27): 2861-2874.
更多往期精彩文章请点击下方链接进行观看
第一期【勃学万象·文献精粹】EGFR-TKI靶向药物治疗:安全性≠耐受性
排版编辑:Raffle











 苏公网安备32059002004080号
苏公网安备32059002004080号


