新春伊始,疫情肆虐,全国人民携手抗击新型冠状病毒肺炎,共同谱写了一曲可歌可泣的战斗篇章。而在肺癌治疗领域,抗血管生成药物与免疫检查点抑制剂的携手联合,亦开创了肺癌治疗的新方向。
随着对血管生成在肿瘤的生长、复发和转移中关键作用的研究,抗血管生成药物通过抑制血管新生和使血管正常化等作用机制来改变肿瘤微环境,从而抑制肿瘤生长。目前,抗血管生成药物在肺癌领域的应用越来越广,从非鳞癌到选择性鳞癌到小细胞肺癌(SCLC),从三线到二线到一线和维持治疗,从大分子单抗到小分子多靶点酪氨酸激酶抑制剂(TKI),包括贝伐珠单抗、雷莫芦单抗、尼达尼布和安罗替尼在内的抗血管生成药物已经成为晚期肺癌治疗的重要手段。其中,安罗替尼是我国自主研发的小分子多靶点TKI,具有双通路作用机制,治疗晚期NSCLC和SCLC疗效显著,已经得到领域内专家的高度认可。
近年来,免疫检查点抑制剂(ICI)已经取得了相当大的成功,但是有效率有限。因此,为了提高疗效,各种联合疗法正在研究中。临床前研究数据表明促血管生成因子具有免疫抑制作用[1],为免疫检查点抑制剂和抗血管生成药物联合使用提供了合理的解释;临床数据亦显示,抗血管生成药物与免疫检查点抑制剂联合使用能够发挥更好的抗肿瘤作用,延缓耐药,且不良反应可控。
1、抗血管生成药物机制
20世纪70年代初,美国国家科学院院士Folkman教授[2]首次提出“恶性实体瘤的生长始终伴随新生血管生成”。随后的研究[3]也揭示,直径为1 ~ 2 mm的微小肿瘤在没有新生血管供血的情况下,往往处于“休眠”状态,不会发生增殖与转移。当肿瘤直径超过2 ~ 3 mm时,肿瘤细胞可以通过产生多种细胞因子,诱导新生血管生成,为肿瘤提供氧和营养物质,进而导致肿瘤的增殖和转移。由此提出,肿瘤血管生成相关通路可作为治疗包括NSCLC在内的多种实体瘤的重要靶点。
激活肿瘤内血管生成相关通路的关键刺激因素是一系列促血管生成因子的高表达,包括血管内皮生长因子(vascular endothelial growth factor,VEGF)、血小板源性生长因子(platelet-derived growth factor,PDGF)、成纤维细胞生长因子(fibroblast growth factor ,FGF)等,其中以VEGF的作用尤为重要。VEGF可通过结合其信号通路受体VEGFR,激活并调节通路下游细胞水平的生物学功能,例如内皮细胞生存、有丝分裂、移动和分化等,进而作用于病理性的血管生成过程[4]。VEGFR包括VEGFR 1-3,其中以VEGFR 1亲和力最高,但在肿瘤血管生成中发挥主要作用的是VEGF-VEGFR2信号转导通路,VEGF和VEGFR2的胞外区特异性结合,激活MAPK、PI3K、PKC、FAK等多条下游信号通路,参与了内皮细胞芽生、迁移、血管通透性、肿瘤细胞存活[5]。
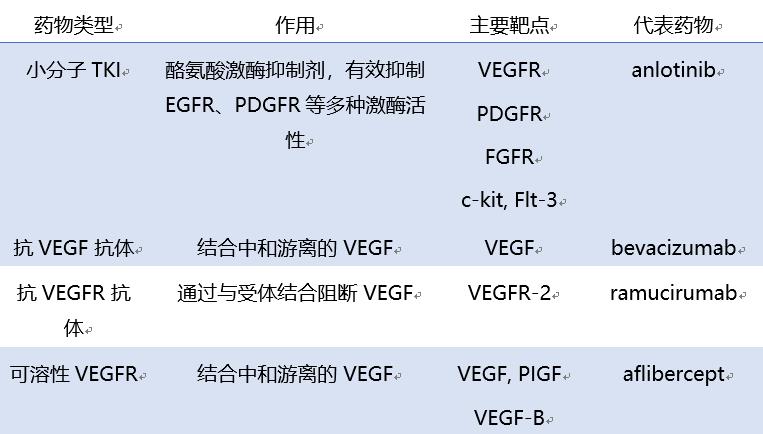
抗血管生成药物可分为:①小分子TKI,酪氨酸激酶抑制剂,主要靶点有VEGFR1、VEGFR2、PDGFR-ß、FGFR、c-kit和Flt-3,如安罗替尼(anlotinib)。②抗VEGFR单抗,通过与受体结合阻断VEGF起作用,主要靶点是VEGFR2,如雷莫芦单抗(ramucirumab)。③可溶性VEGFR药物,通过结合与中和VEGF起作用,主要靶点是VEGF、PIGF和VEGFB,如阿柏西普(aflibercept)。④抗VEGF单抗,通过结合和中和游离的VEGF起作用,主要靶点是VEGF,如贝伐珠单抗(bevacizumab)。(图1和表1)
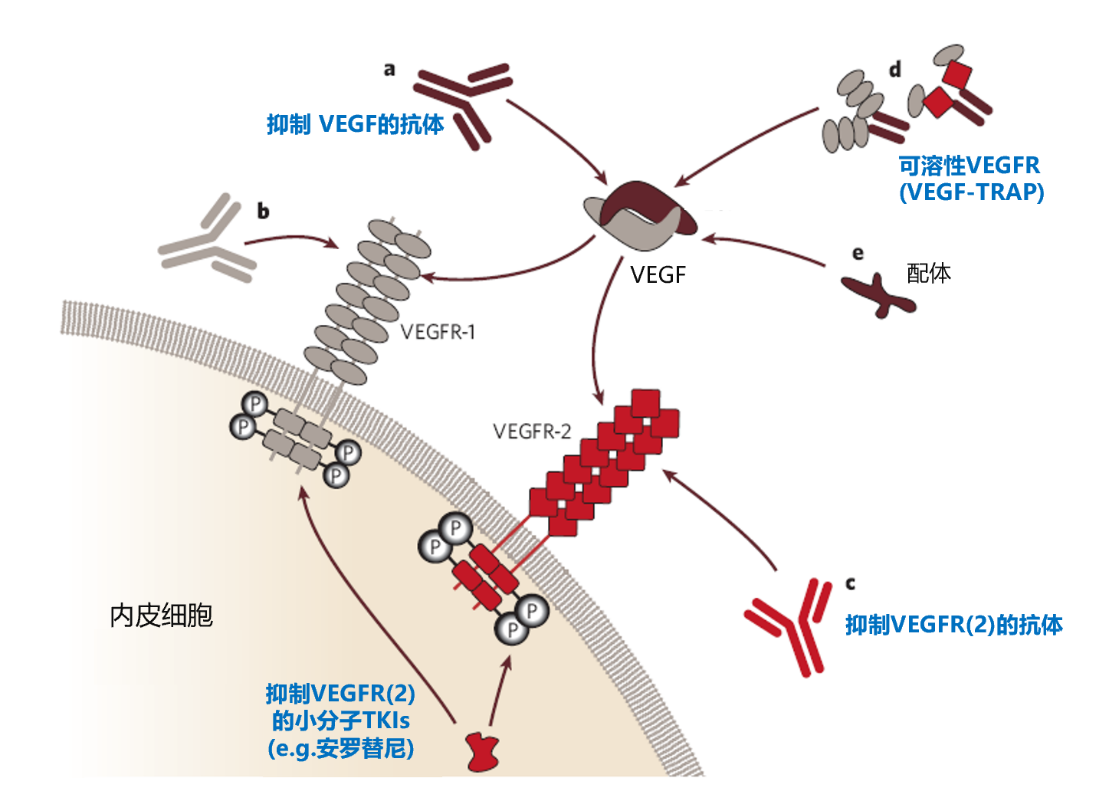
图1 抗血管生成药物作用机制
表1 抗血管生成主要药物
2、免疫治疗作用机制
广义的免疫治疗包括主动免疫和被动免疫,目前肺癌的免疫治疗是狭义的免疫治疗,即免疫检查点抑制剂。免疫检查点是通过调节免疫反应来维持自身耐受并保护周围组织的免疫抑制性通路,是人体免疫系统中起保护作用的分子,起类似刹车的作用,防止T细胞过度激活导致的炎症损伤等,对维持自身耐受、对调控生理性免疫应答的时间和强度至关重要,且将免疫应答对外周组织可能造成的损伤减少到最小。主要包括细胞毒性T淋巴细胞相关蛋白4(cytotoxic T-lymphocyte-associated proteint 4,CTLA-4)[6]和程序性死亡受体1(programmed cell death protein 1,PD-1)及其配体PD-L1通路[7]。CTLA-4是表达于活化的T细胞表面的一种跨膜蛋白,作用于免疫反应的启动阶段,其激活能够抑制T细胞免疫应答的启动,从而导致活化的T细胞减少并阻止记忆性T细胞的生成。肿瘤细胞能够激活CTLA-4,使活化的T细胞失去活性,从而实现了肿瘤的免疫逃逸。PD-1在免疫反应的效应阶段起作用,其表达于活化的T细胞、B细胞及髓系细胞,有两个配体分别为PD-L1和PD-L2。PD-L1/L2在抗原提呈细胞都表达,PD-L1在多种组织也有表达。PD-1与PD-L1的结合介导T细胞活化的共抑制信号,抑制T细胞的杀伤功能,对人体免疫应答起到负调节作用。但在机体肿瘤微环境中,肿瘤细胞高表达 PD-L1,与T细胞上的PD-1发生结合后,诱导T细胞的衰竭,抑制T细胞的功能,无法有效激活免疫系统,引起肿瘤细胞的免疫逃逸。
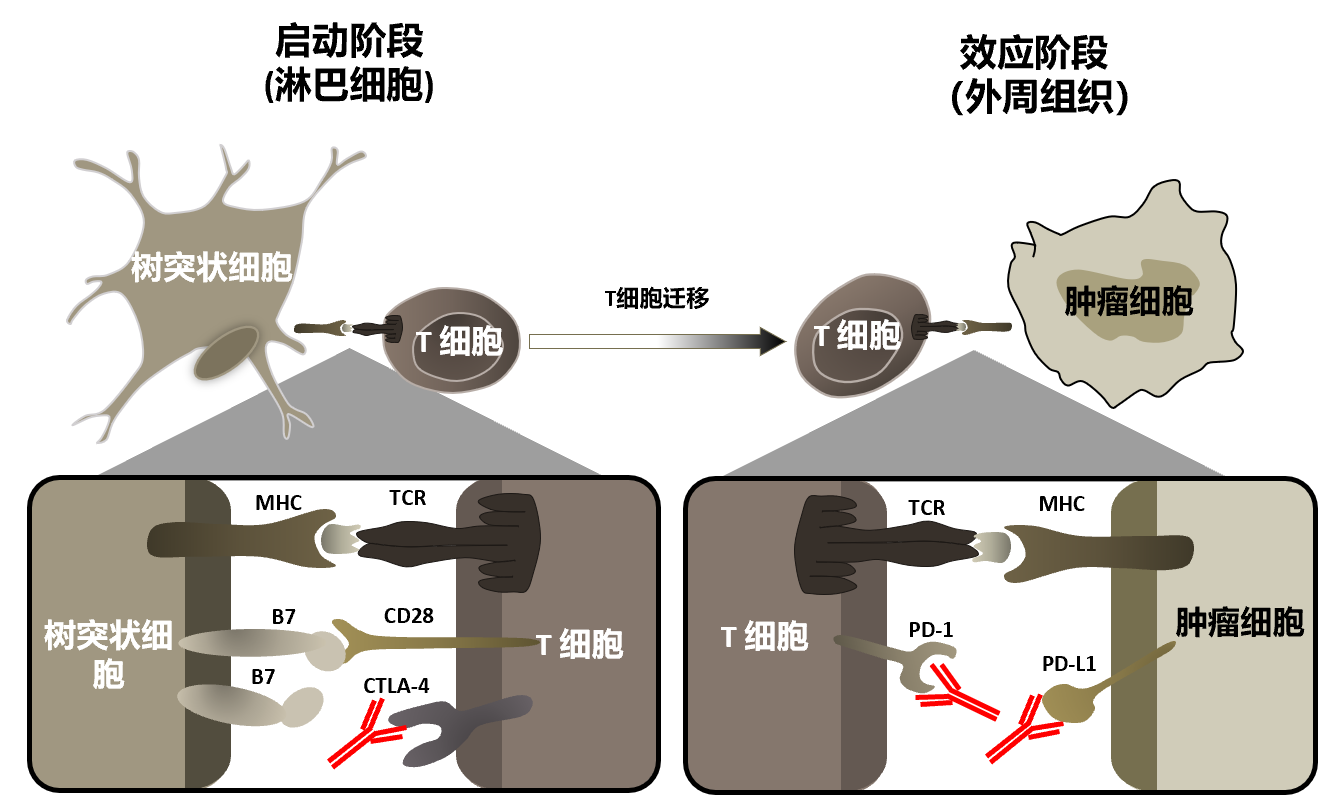
图2 免疫检查点抑制剂作用机制
配体/受体相互识别可启动很多免疫检查点通路,所以抗体或经修饰的配体/受体重组形式可以轻易将免疫检查点通路信号阻断。免疫检查点抑制剂通过与免疫检查点结合而抑制其活性(图2),释放肿瘤微环境中的免疫刹车,重新激活T细胞对肿瘤的免疫应答,从而达到抗肿瘤的作用,这也使其成为抗肿瘤的新武器。目前用于肺癌的免疫检查点抑制剂有抗CTLA-4抑制剂伊匹木单抗 (ipilimumab)和抗PD-1/PD-L1抑制剂,包括帕博利珠单抗(pembrolizumab)、纳武利尤单抗(nivolumab)、阿特珠单抗(atezolizumab)和德瓦鲁单抗(durvalumab)等。
3、抗血管生成药物联合免疫治疗的协同作用及临床研究进展
抗血管生成药物联合免疫治疗是如何相互作用的呢?首先,抗血管生成药物降低髓源性抑制细胞(myeloid-derived suppressor cell, MDSC)和调节性T细胞(T regulatory cells,Treg)的活性,重塑肿瘤微环境,从免疫抑制改变为免疫许可模式(重塑微环境),通过阻断VEGF介导的对树突状细胞成熟的抑制,使得结合肿瘤抗原的T细胞更有效地启动和活化(抗原识别),正常化肿瘤血管结构,促进T细胞浸润进入肿瘤(细胞招募),而免疫药物通过T细胞介导的肿瘤细胞杀伤进而恢复抗肿瘤免疫功能,进一步增强免疫功能恢复[8]。
抗血管生成治疗贯穿免疫治疗的多个步骤,同时激活免疫机制杀伤肿瘤细胞,两者联合具有协同作用,在多个临床研究中得到证实。
IMpower150研究[9]结果显示,化疗联合抗血管生成药物贝伐珠单抗联合PD-L1抑制剂atezolizumab可显著延长晚期野生型非鳞NSCLC患者的无进展生存期(progression-free survival,PFS)和总生存期(overall survival,OS),明显改善客观缓解率(objective response rate,ORR)和缓解持续时间(duration of response,DOR)。atezolizumab+贝伐珠单抗+卡铂+紫杉醇与贝伐珠单抗+卡铂+紫杉醇组的12个月PFS率分别为36.5%和18.0%,12个月PFS率翻倍,疾病进展风险降低38%(中位PFS:8.3个月 vs 6.8个月;HR 0.59;95%CI 0.52 ~ 0.74; P < 0.001),死亡风险降低22%(中位OS:19.2个月vs 14.7个月;HR 0.78;95%CI 0.64 ~ 0.96; P = 0.0164),同时未出现新的安全性事件。基于IMpower150研究结果,美国FDA批准了首个抗血管生成联合化疗联合免疫治疗方案用于晚期NSCLC一线治疗。
Ⅰ期JVDF研究[10]评估了雷莫芦单抗联合帕博利珠单抗治疗晚期初治NSCLC的疗效和安全性,入组初治的转移性/局部晚期不可切除的非鳞NSCLC患者,主要研究终点是安全性,次要研究终点是ORR(RECIST V1.1)、DCR、PFS、OS。结果显示雷莫芦单抗联合帕博利珠单抗一线治疗NSCLC安全性可控,联合治疗用于PD-L1 TPS ≥ 50%患者的一线治疗,临床获益最为显著。ITT人群的中位PFS为9.3个月(4.0,NR),PD-L1 TPS 1%~49%患者的中位PFS为4.2个月(1.2,NR),PD-L1 TPS ≥ 50%的患者中位PFS尚未达到。
贝伐珠单抗联合atezolizumab一线治疗肾细胞癌亦取得了成功[11]。此外,基于JAVELIN Renal 101研究[12]和KEYNOTE‑426研究[13],多靶点药物阿昔替尼(axitinib)与阿维单抗(avelumab)联合以及阿昔替尼(axitinib)与帕博利珠单抗(pembrolizumab)联合获美国FDA批准用于一线治疗肾细胞癌。
4、安罗替尼的作用机制及目前安罗替尼联合免疫治疗的研究
安罗替尼是一种多靶点抗血管生成药物,能全面抑制血管新生相关的VEGFR、PDGFR及FGFR所介导的下游信号通路,干预内皮细胞的增殖、迁移及形成管腔的能力,全面阻断肿瘤血管新生。此外,安罗替尼对于干细胞因子受体c-kit也显示出了很强的抑制活性,c-kit所介导的信号通路在多种恶性肿瘤的发生、发展以及复发的过程中扮演着重要角色,也是目前众多在研靶向药物的主要靶点。通过分子动力学模拟发现,安罗替尼主要结合在VEGFR2和c-kit激酶的ATP结合域,能够深入进入ATP结合位点的催化口袋,其结构中的吲哚环恰好位于天冬氨酸-苯丙氨酸-甘氨酸模段(DFG-motif)附近,而DFG motif对于激酶活性具有重要的调控作用,安罗替尼可能通过和DFG motif 发生相互作用而显示出极强的激酶抑制活性。因此,具有抗肿瘤血管生成和抑制肿瘤生长的双重作用(图3)。
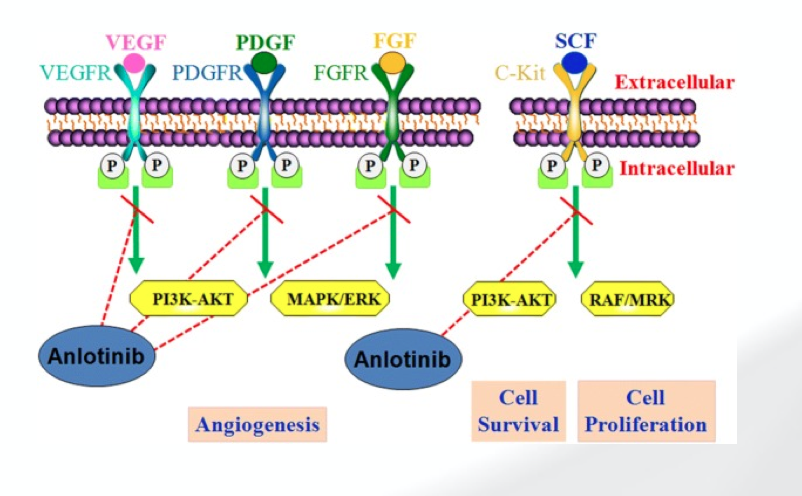
图3 安罗替尼的作用机制
安罗替尼一线联合信迪利单抗治疗晚期NSCLC的探索性研究[14]的初步结果提示,安罗替尼一线联合方案安全性较好,患者耐受性高。入组的22例患者中共计16例患者实现PR,6例患者实现SD,ORR为72.7%(49.8%, 89.3%),DCR 高达100%(84.6%, 100%),其中62.5%(10/16)的患者在首次肿瘤评估时即出现应答,81.8%(18/22)的患者在数据截止时仍接受治疗(图4~6,表2)。未来仍需要大样本临床研究验证。
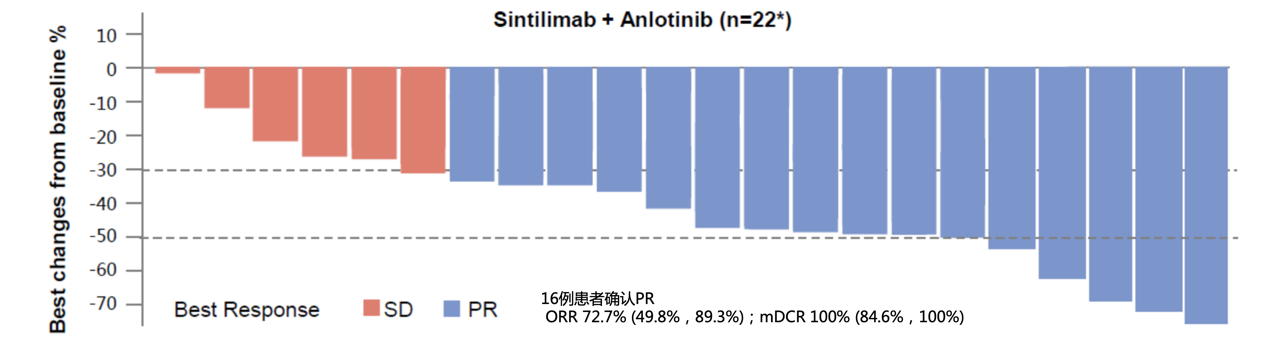
图4 安罗替尼联合信迪利单抗一线治疗晚期NSCLC患者,ORR达到72.7%
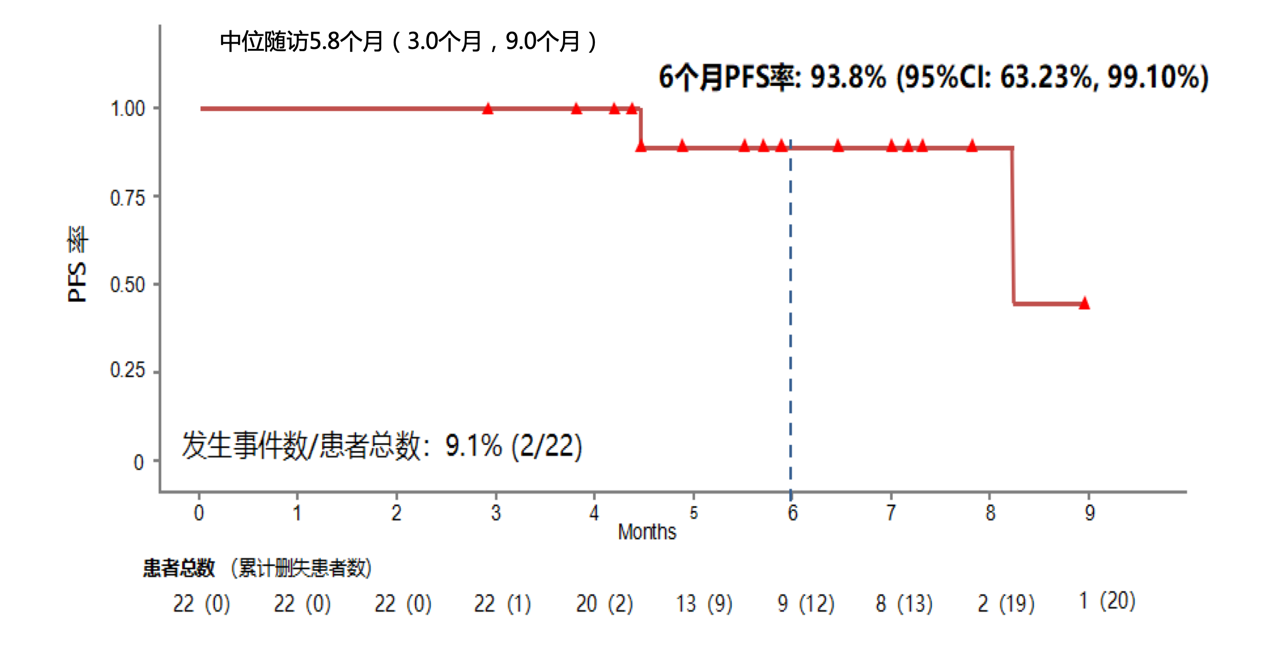
图5 安罗替尼联合信迪利单抗一线治疗晚期NSCLC患者,6个月PFS率达到93.8%
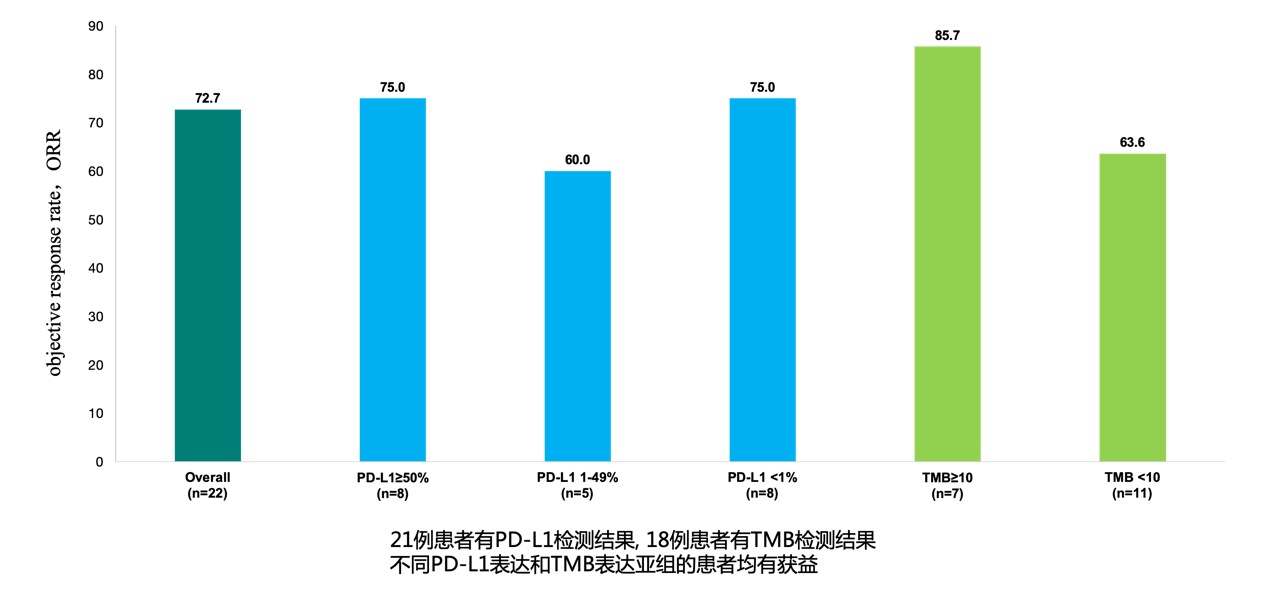
图6 安罗替尼联合信迪利单抗一线治疗晚期NSCLC患者,不同PD-L1/TMB亚组均能获益
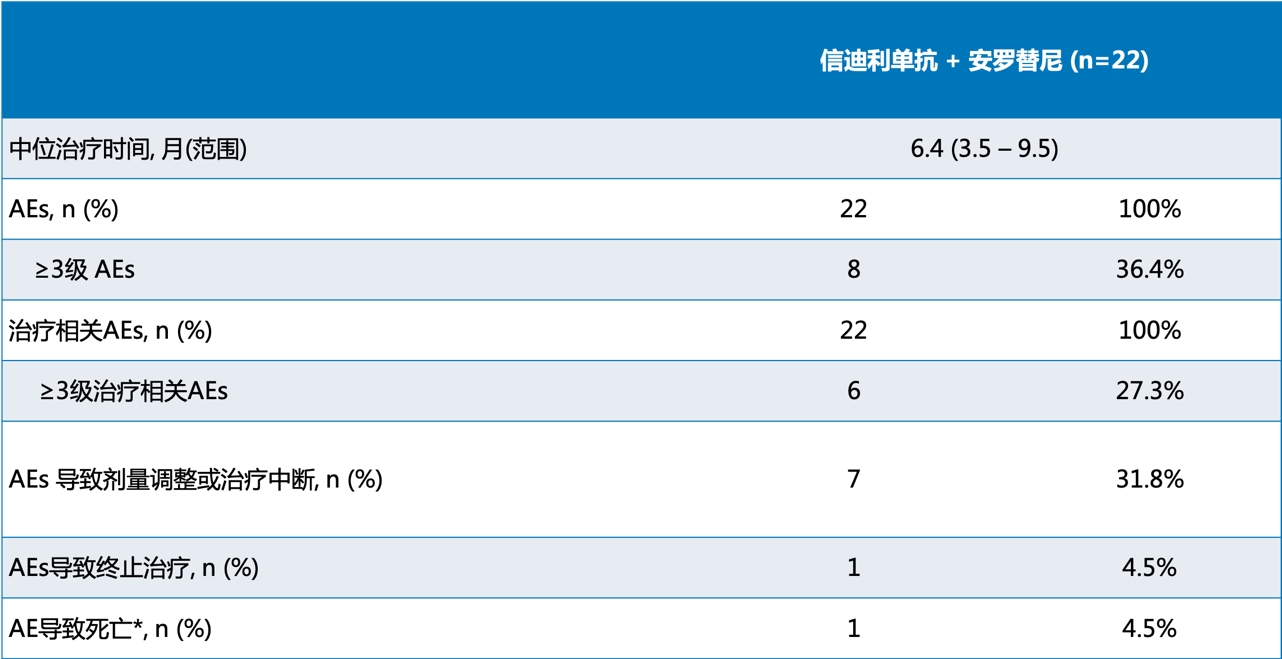
表2 安罗替尼联合信迪利单抗一线治疗晚期NSCLC患者耐受性良好没有新发生的不良反应
此外,多项评估安罗替尼联合免疫治疗的研究正在进行中,如安罗替尼联合PD-L1单抗TQB2450用于晚期NSCLC,安罗替尼联合PD-1单抗AK105用于肝细胞癌的安全性和有效性。期待这些研究的结果给安罗替尼联合免疫治疗带来新的证据。
5、展望
安罗替尼是我国具有自主知识产权的1.1类创新药,已经国家药品监督管理局(NMPA)批准单药用于治疗晚期NSCLC、SCLC和软组织肉瘤适应证,安罗替尼获批用于治疗SCLC和软组织肉瘤,是首个靶向药,也是晚期NSCLC抗血管生成靶向药物中唯一单药有效的药物。为了进一步提高疗效,联合治疗是王道,安罗替尼作为多靶点双通路的抗血管生成药物,从前期的应用基础和作用机制来看,联合免疫治疗具有很好的应用前景,期待未来能够有更多的临床试验成果给临床带来更多选择,让患者更多获益。
疫情之下,有很大一部分肿瘤患者无法到医院就诊,而疗效更为确切、不良反应更低等抗血管生成药物与免疫治疗的联合方案为肿瘤患者带来更多的守护。期待疫情早日结束,也期待肿瘤患者早日战胜癌症!
[1] Voron T, Colussi O, Marcheteau E, et al. VEGF-A modulates expression of inhibitory checkpoints of CD+8 T cells in tumors[J] .J. Exp. Med., 2015, 212, 2:139-48.
[2]Folkman J,Merler E,Abernathy C,et al. Isolation of a tumor factor responsible for angiogenesis[J] .J. Exp. Med., 1971, 133: 275-88.
[3]Hanahan D. Rethinking the war on cancer[J] .Lancet, 2014, 383: 558-63.
[4]Ferrara Na. VEGF and the quest for tumour angiogenesis factors[J] .Nat. Rev. Cancer, 2002, 2: 795-803.
[5]Wu Florence T H,Stefanini Marianne O,Mac Gabhann Feilim, et al. A systems biology perspective on sVEGFR1: its biological function, pathogenic role and therapeutic use[J] .J. Cell. Mol. Med., 2010,14: 528-52.
[6]Leach D R,Krummel M F,Allison J P. Enhancement of antitumor immunity by CTLA-4 blockade[J] .Science, 1996, 271: 1734-6.
[7]Dolan Dawn E,Gupta Shilpa. PD-1 pathway inhibitors: changing the landscape of cancer immunotherapy[J] .Cancer Control, 2014, 21: 231-7.
[8]Kwilas Anna R,Donahue Renee N,Tsang Kwong Y, et al. Immune consequences of tyrosine kinase inhibitors that synergize with cancer immunotherapy[J] .Cancer Cell Microenviron, 2015, 2(1).
[9]Socinski Mark A,Jotte Robert M,Cappuzzo Federico et al. Atezolizumab for First-Line Treatment of Metastatic Nonsquamous NSCLC[J] .N. Engl. J. Med., 2018, 378: 2288-2301.
[10]Herbst RS,Arkenau H,Bendell J,et al. Phase Ⅰ expansion cohort of ramucirumab plus pembrolizumab in advanced treatment-naïve non-small cell lung cancer(JVDF)[R]. 2019 WCLC Abstract MA14.07.
[11]Rini BI, Powles T, Atkins MB, et al. IMmotion151 Study Group. Atezolizumab plus bevacizumab versus sunitinib in patients with previously untreated metastatic renal cell carcinoma (IMmotion151): a multicentre, open-label, phase 3, randomised controlled trial[J]. Lancet,2019,393(10189):2404-2415.
[12]Motzer RJ, Penkov K, Haanen J, et al. Avelumab plus axitinib versus sunitinib for advanced renal-cell carcinoma[J] .N. Engl. J. Med., 2019,380:1103-15.
[13] Rini BI, Plimack ER, Stus, et al. Pembrolizumab plus axitinib versus sunitinib for advanced renal-cell carcinoma[J] .N. Engl. J. Med., 2019, 380: 1116-27.
[14]Han BH, Chu T, Zhong R, et al. Efficacy and safety of sintilimab with anlotinib as first-line therapy for advanced non-small cell lung cancer[R]. 2019 WCLC Abstract JCSE01.11.
排版编辑:肿瘤资讯-细胞田














 苏公网安备32059002004080号
苏公网安备32059002004080号


