
内分泌治疗对于激素受体阳性的乳腺癌患者无论是术后辅助还是晚期治疗都是非常重要。如何理解、掌握、应用合适的内分泌治疗手段,尽可能为激素受体阳性乳腺癌患者谋求更长生存,是临床医生致力实现的目标。本文分享一例激素受体阳性乳腺癌患者的治疗过程,探讨激素受体阳性乳腺癌的诊疗思路。

美国西达赛奈(Cedars-Sinai Medical Center)医院乳腺中心访问学者
湖北省抗癌协会乳腺癌专业委员会委员
湖北省抗癌协会乳腺癌专业委员会青年委员会委员
湖北省临床肿瘤学会乳腺癌专业委员会委员
湖北省临床肿瘤学会青年委员会常务委员
2019年度武汉市中青年医学骨干人才
获国家发明专利授权2项,实用新型专利授权1项,主持湖北省基金项目2项,发表学术论文10余篇。
基本病史
患者女性,57岁,绝经后。既往2014年因“冠状动脉粥样硬化型心脏病”行心脏支架植入术,术后规律口服阿司匹林, 阿托伐他汀钙片治疗;确诊糖尿病3年,规律口服格列吡嗪控释片,血糖控制尚可。否认传染病、遗传病史。
就诊及手术
2015年11月,患者因“无意中发现左乳腺肿块”就诊。专科查体示:左乳2点钟方向距乳头5cm处可扪及一大小约4.0cm×4.0cm质硬不规则肿块,边界欠清晰,活动度差,无触痛,左乳外上象限可见酒窝征,表皮及乳头乳晕未见异常。右乳、腋窝及双侧锁骨上淋巴结未及肿大。
辅助检查:①血肿瘤标记物CA153示:318.5 U/ml(参考值<30 U/ml);②乳腺钼靶示:左乳腺占位,符合BI-RADS V类,左腋下多发淋巴结肿大(图1);③乳腺超声示:双侧乳房切面形态轮廓正常,层次清楚,双侧乳腺组织回声增强,分布不均,呈粗大的光点光斑和蜂窝状低回声及无回声。左乳2点距离乳头5.3cm处可见一大小约3.14cm×1.86cm边界欠清晰形态不规则低回声光团,其内可见少许钙化点回声。左侧腋下可见数枚边界清晰形态规则的低回声光团,其中最大为1.78cm×0.77cm,右侧乳腺和腋下未见明显异常。余心脏超声、心电图、颅脑CT平扫未见明显异常。患者拒绝穿刺明确诊断后行新辅助治疗,要求尽快手术治疗。

图1 患者乳腺钼靶(2015年11月)
排除明显手术禁忌,于2015年12月行“左乳腺癌改良根治术”,术后病理示:(左)乳腺浸润性导管癌(invasive ductal carcinoma,IDC),SBR Ⅲ级,可见脉管癌栓,未见明确神经侵犯。乳头、皮肤及基底均净,残腔见癌组织。送检淋巴结见12/13枚转移癌,送检腋窝淋巴结镜下见淋巴结外的纤维脂肪组织中见癌组织广泛浸润。免疫组化(IHC):ER(3+,90%)、PR(2+,90%)、HER2(-)、 Ki-67(约60%)。
结合患者病史、手术病理,目前明确诊断为:①(左)乳腺浸润性导管癌伴腋窝淋巴结转移(pT2N3M0 Ⅲb期,分子分型:HR阳性/HER2阴性型);②冠心病 冠脉支架植入术后;③2型糖尿病。
术后治疗
患者术后于2015年12月起行多西他赛联合环磷酰胺(TC)方案化疗6周期。患者于第3周期骨扫描发现:①骨扫描ECT示:颅骨、右第11后肋、右肩胛内缘、第1腰椎、左髂前上棘、左骶髂关节、右髋臼等处骨骼可见异常放射性浓聚区,结合病史考虑乳腺癌转移可能性大;②腰椎CT示(图2):胸12椎体及左侧附件、腰1、腰2、腰4椎体异常信号影,血管瘤可能,转移瘤待排。结合患者目前情况,不排除骨转移可能。经与患者本人及家属沟通后,于第3周期TC方案开始时加用唑来膦酸治疗。2016年5月化疗结束后给予50Gy/25次局部放疗,同时口服阿那曲唑1mg/日联合唑来膦酸治疗。定期复查,肿瘤标记物CA153恢复正常范围,未见明显复发征象或转移征象。

图2腰椎CT(2015年7月)
第一次疾病进展
2017年8月患者定期复查:①胸部CT示(图3):胸椎及两侧肋骨异常密度结节影,考虑多发转移;②骨扫描示(图4):左肩胛骨下角、右第10后肋、第11、12胸椎,骶骨,左髂骨骨质代谢异常活跃,较前有部分新发,结合病史考虑转移;③血肿瘤标记物CA153示:294.8U/ml。结合患者相关实验室和影像学检查结果,综合疗效评估价为:病情进展(progressive disease,PD)。
予以氟维司群(fulvestrant )联合唑来膦酸治疗,治疗期间定期复查,未见明显复发征象或转移征象。

图3 胸部CT(2017年8月)
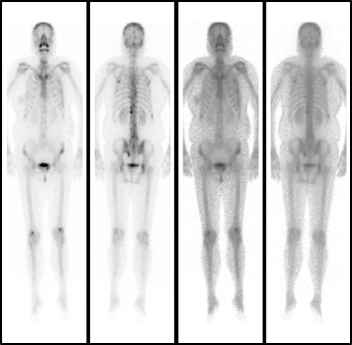
图4 骨扫描复查
再次疾病进展
2018年12月,患者无明显诱因下出现腰痛,复查:①腰椎CT示:所扫描胸椎、腰椎及附件、骶骨、两髂骨多发转移瘤,与既往比较有所进展。L1轻度压缩性骨折;②胸部CT示:胸椎、两侧肋骨、左侧肩胛骨骨质异常,范围较前无明显变化,部分病灶较前硬化;③颅脑CT示:两侧顶骨半片状高密度影,转移待排;④腹部MR示(图5):肝内多发转移瘤,肝内多发转移瘤,较大者范围约11.6cm×7.8cm;⑤血肿瘤标记物CA153示:540.1.8U/ml。结合患者相关实验室和影像学检查结果,综合疗效评估价为:病情进展(progressive disease,PD),其无进展生存期(progression-free survival, PFS)为16个月。

图5 腰椎CT、腹部MRI(2018年12月)
经与患者及家属商议,予以长春瑞滨+顺铂(NP)方案化疗,2周期后复查:腹部MR示(图6):肝转移癌化疗后,肝转移灶较前缩小,其中较大的为8.4cm x 5.5cm,较前明显缩小,余病灶稳定,综合疗效评价为:部分缓解(partial response,PR)。但因患者在治疗期间出现明显的骨髓抑制毒性,血小板最低为31×109/L,结合5.0版美国国立癌症研究所通用毒性反应标准(general toxicity criteria of the national cancer institute,NCI-CTC),评价为3级。且患者明确拒绝进一步化疗,故于2019年3月开始依西美坦联合CDK4/6抑制剂治疗。6月复查腹部MRI示(图6):肝转移癌治疗后,肝转移灶较前缩小,其中较大的为5.0cm x 3.6cm。综合疗效评价为:PR,现口服内分泌治疗至今,定期复查未见明显复发征象或转移征象。

图6 患者腹部MR(左: 2019年3月;右:2019年6月)

图7 患者治疗历程图

中国抗癌协会乳腺癌专业委员会常委
湖北省乳腺病防治研究中心主任
湖北省肿瘤医院乳腺科主任
湖北省抗癌协会乳腺癌专业委员会主任委员
武汉市医学会肿瘤学分会副主任委员
湖北省抗癌协会青年委员会常委
湖北省医学会肿瘤学分会委员兼秘书
患者中老年女性,已绝经。初诊为绝经后HR阳性转移性乳腺癌,病理分期: pT2N3M0 Ⅲb期。术后化疗时发现骨转移,结合化疗、内分泌治疗、放疗等治疗手段在20个月后出现疾病进展。疾病进展后首次治疗选择氟维司群内分泌治疗,获得约16个月的PFS,再次进展后选择了NP方案,因为化疗不耐受调整为AI+CDK4/6抑制剂治疗至今。
(1)患者术后治疗方案的选择
抗癌药物的选择、剂量和应用以及相关毒性的处理非常复杂,需要考虑毒性反应、个体差异、合并症等多种因素,临床需要根据患者危险度、耐受程度、患者意愿并结合临床试验的背景选择具体的用药方案。该患者术后病理提示:SBR Ⅲ级,可见脉管癌栓,送检淋巴结明确转移,淋巴结外的纤维脂肪组织中见癌组织广泛浸润, Ki-67(+,约60%)。多项证据提示该患者为高复发风险患者,临床予以TC方案化疗、放疗、阿那曲唑内分泌治疗,多管齐下,但患者仍然在20个月后出现疾病进展。
患者在内分泌治疗期间出现转移,需要考虑内分泌耐药的情况。内分泌治疗的耐药分为原发和继发两大类。原发性内分泌耐药指:辅助内分泌治疗时间小于2年复发,或晚期一线内分泌治疗小于6个月出现疾病进展。继发性内分泌耐药指:辅助内分泌治疗时间大于2年且于停药后1年内复发,或晚期一线内分泌治疗≥6个月出现疾病进展。综合考虑,该患者属于原发性内分泌耐药,针对原发性内分泌耐药的患者,后续治疗该如何选择?
(2)氟维司群给原发性内分泌耐药患者带来获益
在AI使用过程中,依赖配体的转录激活区(LBD)会出现ESR1突变,并且突变率会随着使用时间的延长而上升[1]。转移性乳腺癌中,ESR1突变比例较高,在11%~55%之间[2],突变后的ERs在没有雌激素的情况下可以自行启动转录,驱动肿瘤远处转移,加速肿瘤生长,因此会影响患者预后。针对ESR1突变的患者,如果继续使用其他AI类药物,疗效并不乐观。SoFEA研究显示非甾体类AI治疗进展的患者换用甾体类AI之后的PFS较低,仅2.6个月[3]。BOLERO-2研究显示,非甾体类AI治疗失败后换用甾体类AI依西美坦单药治疗的缓解率仅为0.4%[4]。SoFEA研究和EFFECT研究中的临床获益率虽然稍高,但是也仅约30%,分别为27%和31.5%[5,6]。由于AI使用过程中肿瘤细胞会累积ESR1突变,突变的ERs在没有雌激素的情况下依然能够激活转录,因此再次换用AI,即使降低雌激素水平可能也不会有明显的效果。因此,多项指南在内分泌解救治疗的选择及注意事项中提到,尽量不重复使用辅助治疗或一线治疗用过的药物。
氟维司群是一类雌激素受体下调剂类抗乳腺癌治疗药物。该药物不仅可以与雌激素受体竞争性结合,亲和力与雌二醇相似,还可以阻滞受体,抑制雌激素的结合并激发受体发生形态改变,降低ER浓度而损害肿瘤细胞。而0020/0021临床研究中证实了氟维司群250mg在抗雌激素治疗失败的患者疗效中与AI疗效等效。Global CONFIRM和China CONFIRM已经证实在经内分泌治疗的绝经后HR+乳腺癌患者中,氟维司群500mg的疗效优于250mg[7,8]。Ⅱ期的FIRST试验[9]也证实完成辅助TAM治疗停药>12个月以上复发的患者,使用氟维司群500mg优于阿那曲唑。Ⅲ期FALCON研究[10]亦证实了晚期未经内分泌治疗的患者氟维司群较第三代AI延长了无疾病进展时间,差异具有统计学意义。
基于多项临床试验结果,目前《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南》2019版已经将氟维司群作为未经内分泌治疗、TAM治疗失败及AI治疗失败的绝经后激素受体阳性晚期乳腺癌患者内分泌治疗策略中的Ⅰ级推荐。该患者作为高复发风险的激素受体阳性乳腺癌,在原发性内分泌治疗耐药的情况下使用氟维司群,获得PFS 16个月,与临床试验的获益基本相符。临床对于绝经后晚期/转移性乳腺癌患者经内分泌治疗失败的患者可以选择氟维司群单药,以求最大获益。
应用氟维司群之后进展的患者该如何选择治疗方案?该患者选择了NP方案,但是因为对化疗不耐受,更换为AI+CDK4/6抑制剂。期待通过内分泌联合方案给患者带来更长生存获益。目前已经有多项临床试验证实内分泌联合方案的疗效与安全性,内分泌联合方案也给患者带来更多选择。
[1] Schiavon G, Hrebien S,Garcia-Murillas I, et al. Analysis of ESR1 mutation in circulating tumor DNA demonstrates evolution during therapy for metastatic breast cancer.[J] .Sci Transl Med, 2015, 7: 313ra182.
[2]Clarke R, Tyson JJ, Dixon J M, et al. Endocrine resistance in breast cancer--An overview and update.[J] .Mol. Cell. Endocrinol., 2015, null: 220-34.
[3]Fribbens C, O'Leary B, Kilburn L, et al. Plasma ESR1 Mutations and the Treatment of Estrogen Receptor-Positive Advanced Breast Cancer.[J] .J. Clin. Oncol., 2016, 34: 2961-8.
[4]Baselga J, Campone M, Piccart M, et al. Everolimus in postmenopausal hormone-receptor-positive advanced breast cancer.[J] .N. Engl. J. Med., 2012, 366: 520-9.
[5]Johnston Stephen Rd,Kilburn Lucy S,Ellis Paul, et al. Fulvestrant plus anastrozole or placebo versus exemestane alone after progression on non-steroidal aromatase inhibitors in postmenopausal patients with hormone-receptor-positive locally advanced or metastatic breast cancer (SoFEA): a composite, multicentre, phase 3 randomised trial.[J] .Lancet Oncol., 2013, 14: 989-98.
[6]Chia S, Gradishar W, Mauriac L, et al. Double-blind, randomized placebo controlled trial of fulvestrant compared with exemestane after prior nonsteroidal aromatase inhibitor therapy in postmenopausal women with hormone receptor-positive, advanced breast cancer: results from EFECT.[J] .J. Clin. Oncol., 2008, 26: 1664-70.
[7]Robertson J F, Dixon J M, Sibbering D M, et al. A randomized trial to assess the biological activity of short-term (pre-surgical) fulvestrant 500 mg plus anastrozole versus fulvestrant 500 mg alone or anastrozole alone on primary breast cancer[J]. Breast Cancer Research, 2013, 15(2):R18.
[8] Leo A D, Jerusalem G, Petruzelka L, et al. Results of the CONFIRM Phase III Trial Comparing Fulvestrant 250 mg With Fulvestrant 500 mg in Postmenopausal Women With Estrogen Receptor–Positive Advanced Breast Cancer[J]. Journal of Clinical Oncology Official Journal of the American Society of Clinical Oncology, 2010, 28(30):4594.
[9] Ellis Matthew J, Llombart-Cussac A, Feltl D, et al. Fulvestrant 500 mg Versus Anastrozole 1 mg for the First-Line Treatment of Advanced Breast Cancer: Overall Survival Analysis From the Phase II FIRST Study.[J] .J. Clin. Oncol., 2015, 33: 3781-7.
[10] Robertson John F R, Bondarenko Igor M, Trishkina Ekaterina, et al. Fulvestrant 500 mg versus anastrozole 1 mg for hormone receptor-positive advanced breast cancer (FALCON): an international, randomised, double-blind, phase 3 trial.[J] .Lancet, 2016, 388: 2997-3005.











 苏公网安备32059002004080号
苏公网安备32059002004080号


