审校:天津医科大学肿瘤医院 张会来教授
2019年6月18日~22日,第15届国际淋巴瘤大会(ICML)在风光旖旎的瑞士·卢加诺(Lugano)隆重举行。目前ICML已成为全球淋巴瘤领域最具影响力的盛会,3500多名来自世界各地的淋巴瘤领域专家参加了这次学术盛会。 弥漫性大B细胞淋巴瘤(DLBCL)是一种具有高度侵袭性及异质性的疾病。R-CHOP是其标准治疗方案,如何进一步提高DLBCL的治疗效果是近年来的研究热点。在本次ICML大会上,DLBCL领域也有多个重要研究数据亮相。【肿瘤资讯】特邀天津医科大学肿瘤医院赵培起博士进行了筛选编译,并邀请张会来教授作了精彩点评,详情如下。

现任天津医科大学肿瘤医院医务处处长;淋巴瘤内科主任
主要研究方向:恶性淋巴瘤的分子诊断和个体化治疗
主要协会/学会任职:
中国抗癌协会(CACA)淋巴瘤专业委员会副主任委员
中国临床肿瘤学会(CSCO)抗淋巴瘤联盟常委
中国医疗保健国际交流促进会肿瘤内科分会副主任委员
中国老年保健协会淋巴瘤专业委员会副主任委员
中华医学会肿瘤分会淋巴瘤学组委员
天津市抗癌协会淋巴瘤专业委员会主任委员
中国老年肿瘤学会淋巴血液肿瘤专委会委员

天津医科大学肿瘤医院淋巴瘤内科,主治医师,肿瘤学博士;
主要从事淋巴瘤的内科诊治及基础、临床研究;
主持国家自然科学基金一项,参与多项国家及省部级课题,发表SCI文章十余篇;
获2017年天津医科大学肿瘤医院青年医师讲课大赛二等奖;
2018年淋巴瘤青年医师病例演讲大赛北区冠军,全国冠军;
2018年CSCO35位35岁以下最具潜力青年肿瘤医生。
Venetoclax联合利妥昔单抗、异环磷酰胺、卡铂和依托泊苷(VICER)治疗复发性DLBCL的安全性和有效性:来自I期临床研究的最终结果(ABS:277)
背景
DLBCL经一线免疫化疗后复发难治的患者预后欠佳。接受二线、含铂方案的ORR约为50%,CR为30%~40%。我们进行了一项Ⅰ期试验,评估venetoclax(VEN)联合RICE(利妥昔单抗、异环磷酰胺、卡铂和依托泊苷)方案治疗复发性DLBCL的安全性和有效性。
方法
研究纳入R/R DLBCL (≥18岁)。口服VEN,d1-10 q21d,共3个周期。按照3+3设计递增3个剂量水平(400、600和800 mg)。按标准剂量和时间表给予RICE方案。所有患者均在第1周期接受肿瘤溶解的预防治疗,每个周期后给予pegfilgrastim预防性升血。
结果
18例患者完成入组及随访。所有患者均接受含利妥昔单抗和蒽环类药物的一线方案化疗,其中4例二线治疗失败,6例难治。14例(78%)患者达到CR,2例(11%)患者PR (ORR=89%)。14/16例应答者成功采集干细胞。2例动员失败的患者年龄均在70岁以上,并拒绝了第二次采集。14例患者均行造血干细胞移植。中位随访12个月,5例患者复发,包括一名没有接受ASCT治疗的患者。1年PFS为55%。4例患者死亡,其中包括2例VICER无效患者,2例ASCT后复发患者。1年的OS为71%。在接受ASCT的患者中,1年PFS和OS分别为62%和77%。
结论
I期研究结果显示VICER方案在包括高危患者在内的R/R DLBCL中安全有效,CR为78%,移植率78%。VICER方案的PFS和OS优于报道的R-ICE和其他二线治疗方案。VICER的II期研究将在2019年中开始招募受试者。

Nivolumab联合brentuximab vedotin在R/R原发纵隔大B细胞淋巴瘤的疗效及安全性研究(ABS:108)
背景
原发纵隔B细胞淋巴瘤(PMBL)是一种少见但侵袭性的NHL,复发/难治性(R/R)患者预后较差。PD-L1过表达和CD30弱表达是PMBL的特点。PD-1抑制剂和brentuximab vedotin (BV) 在R/R PMBL中的ORR分别为41%和13%。Nivolumab与BV在R/R PMBL中可能具有协同作用。
方法
CheckMate 436是一个应用nivolumab联合BV治疗CD30+ NHL的开放标签的1/2期研究。患者接受每3周一次的nivolumab (240mg)和BV(1.8mg/Kg),直到疾病进展或不可接受的毒性。主要终点是ORR及安全性。
结果
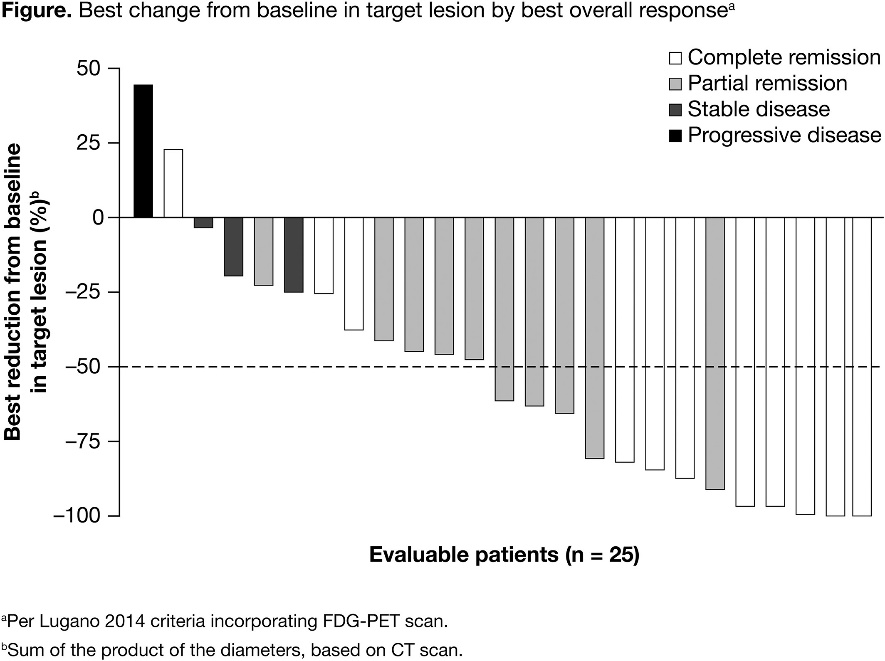
30例患者接受nivolumab + BV治疗,并纳入该初步分析。在基线时,中位年龄为35.5岁;患者接受过中位2线的全身治疗,4例(13%)先前接受了自体造血干细胞移植。中位随访时间为11.1个月,ORR为73%,11例患者(37%)达到CR;25例可评估患者中13例(52%)的靶病灶减少> 50% 。在数据截止时,22名应答者中有3人在开始后续治疗前已经进展或死亡;尚未达到中位DOR。25名(83%)患者报告了治疗相关的AE(TRAE)。最常见的TRAE是中性粒细胞减少症(30%),周围神经病变(27%),外周感觉神经病变,血小板减少症,皮疹和甲状腺功能亢进(各占13%)。
结论
在R/R PMBL患者中,nivolumab + BV显示出较高的有效率,ORR为73%,CR为37%。TRAE与单独nivolumab和BV治疗的安全性一致。Nivolumab+BV的组合在R/R PMBL中可以达到协同增效的效果。
Venetoclax(VEN)联合R-CHOP方案改善了BCL2阳性DLBCL的预后:来自CAVALLI研究的结果(ABS:089)
背景
BCL2、BCL2和MYC过表达,BCL2和MYC共易位(DHL)与DLBCL的不良预后相关。VEN是一种高选择性BCL2抑制剂,可能会增强目前利妥昔单抗(R)+ CHOP标准方案的效果。我们报告了CAVALLI研究的安全性,有效性和生物标志物分析(数据截止日期:2018年7月13日)。
方法
研究纳入初治DLBCL,年龄≥18岁,ECOG ≤2,IPI 2-5的患者。口服VEN 800mg d1-4,C1;d1-10,C2-C8联合R(8周期)和CHOP(6-8周期);21天1周期。主要终点是治疗结束时的PET完全缓解(PET-CR)。次要终点是PFS、OS和安全性。GOYA研究的R-CHOP对照组(564例患者,IPI 2-5)用作历史对照。生物标志物分析包括BCL2、MYC表达,BCL2和MYC易位和细胞来源。
结果
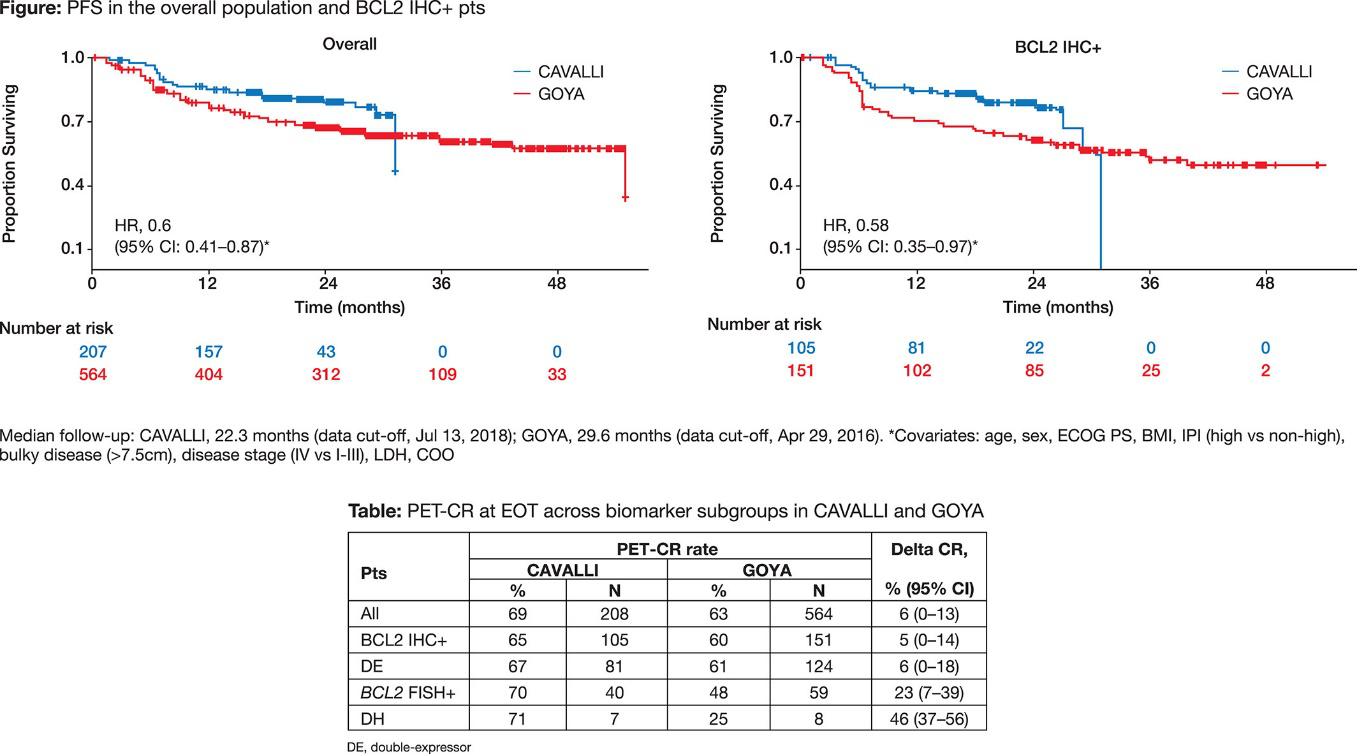
CAVALLI研究纳入了211例患者,208例接受了治疗,并进行了有效性和安全性分析。CAVALLI与GOYA研究的基线特征相似,但纳入了更多的IV期(65%对47%)和BCL2 IHC+(58%对49%)患者。在整体人群中,PET-CR相似(CAVALLI 69%; GOYA 63%),而CAVALLI研究中BCL2 FISH+和DHL患者的PET-CR更高。与GOYA研究相比,PFS在整体和BCL2 IHC+人群中有所改善; 在ABC和GCB 亚型中均能观察到BCL2 IHC+患者中的PFS获益。与GOYA相比,同样也有OS获益的证据。CAVALLI研究中有86%的患者发生3~4级AE,而GOYA研究为66%,主要是血细胞减少、FN和感染。在接受G-CSF预防的患者中观察到中性粒细胞减少和FN/感染发生率降低的趋势。多因素分析中,年龄<60岁是预测完成8个周期治疗的唯一因素(p = 0.002)。CAVALLI研究中有4例致死性AE(2%),GOYA有30例(5%),但GOYA的随访时间较长(29.6 vs 22.3个月)。
结论
与匹配的GOYA研究对照组相比,VEN联合RCHOP 可改善BCL-2 IHC+的初治DLBCL的疗效。与GOYA研究相比,CAVALLI研究有更高的血细胞减少、FN和感染,但是死亡的风险没有增加,化疗的相对剂量强度也是相似的。
CD20xCD3双特异性抗体REGN1979在R/R B-NHL患者中的临床活性研究(ABS:052)
背景
REGN1979是一种抗CD20和抗CD3双特异性IgG4单克隆抗体。本研究报告了既往经抗CD20单抗治疗的R/R B-NHL患者接受REGN1979治疗的1期研究的更新结果。主要目的是确定REGN1979的安全性、耐受性和剂量限制毒性(DLT)。其他目的包括评估其抗肿瘤活性,药代动力学和药效学。
方法
符合入组条件的R/R B-NHL患者必须接受过≥1次针对CD20的靶向治疗。治疗方案为静脉注射REGN1979,每周一次,共12次;随后每2周注射REGN1979 1次,共12次(共36周)。
结果
截至2018年12月6日,71例患者接受了REGN1979治疗,剂量为0.03~80mg,中位治疗次数为9,其中DLBCL 39例,FL 1-3a级17例,其它类型淋巴瘤15例。10例患者仍在治疗中,15例已完成治疗,46例中止治疗(29例因PD)。没有患者出现DLT。最常见的AEs为发热(n=56)、寒战(n=38)、CRS(n=37)。4例患者出现≥3级的CRS,通过优化预处理,即使REGN1979剂量进一步递增,CRS症状的严重程度也有所下降。最常见的≥3级的AEs为中性粒细胞减少(n=14)、淋巴细胞减少(n=14)、贫血(n=12)。癫痫发作和/或脑病未见报道。4例患者因AEs而中止治疗,分别是3级溶血、3级疲劳、3级肺炎和3级颈部脓肿各1例。9例患者在研究中死亡:6例PD、1例胃穿孔、1例心脏骤停、1例肺部感染。R/R FL 1-3a级在REGN1979 ≥5mg时显示出明显的疗效(ORR 100%;8/10 CR; 2/10 PR),而R/R DLBCL(及其他B-NHL)则随着剂量的递增也显示出治疗效果。值得一提的是,在R/R DLBCL患者中,2/11(18%)例在5-12mg剂量时出现治疗反应,6/11 (55%)例在18-40mg剂量时出现治疗反应,2/2(100%)例在80mg剂量时出现治疗反应,而且后2例患者均达到了CR。研究表明,CD20高表达和低表达患者均有效。有治疗反应的患者再复发主要见于维持治疗或CD20表达丢失时,提示存在抗原依赖和非抗原依赖的逃逸机制。
结论
REGN1979在R/R B-NHL患者中耐受性好,没有DLTs发生,也没有明显的神经毒性。R/R FL在≥5mg剂量水平时的表现令人印象深刻(ORR 100%)。随着治疗剂量的增加,R/R DLBCL同样也显示出临床获益。根据这些结果,未来计划在R/R FL 1-3a,R/R DLBCL和其他R/R B-NHL亚型进行2期研究。

ROBUST:来那度胺/R-CHOP(R2-CHOP)与安慰剂/R-CHOP在初治ABC亚型DLBCL中III期研究的首次报道(ABS:005)
背景
尽管努力提高R-CHOP组合方案的治疗效果,但ABC亚型DLBCL的生存仍然很差。II期研究结果显示,在R-CHOP方案中加入免疫调节剂来那度胺可改善ABC亚型DLBCL患者的不良预后,提高其治疗效果。
方法
ROBUST研究首次前瞻性对比来那度胺/R-CHOP (R2-CHOP)和安慰剂/R-CHOP治疗初治CD20+ABC亚型 DLBCL的疗效。入组患者Ⅱ-Ⅳ期,IPI≥2,ECOG≤2。采用NanoString淋巴瘤亚型检测技术,由中心病理确定肿瘤组织学和细胞类型 (Scott,Blood 2014)。ABC亚型DLBCL患者根据IPI评分(2分和≥3分)、大包块(<7cm和≥7cm)和年龄(<65岁和≥65岁)进行分层,患者1:1随机分入来那利度胺口服15 mg/d,d1-14/21+标准R-CHOP 21组和安慰剂/R-CHOP 21组,共6个周期,可根据当地惯例加用2次利妥昔单抗。主要研究终点是PFS。
结果
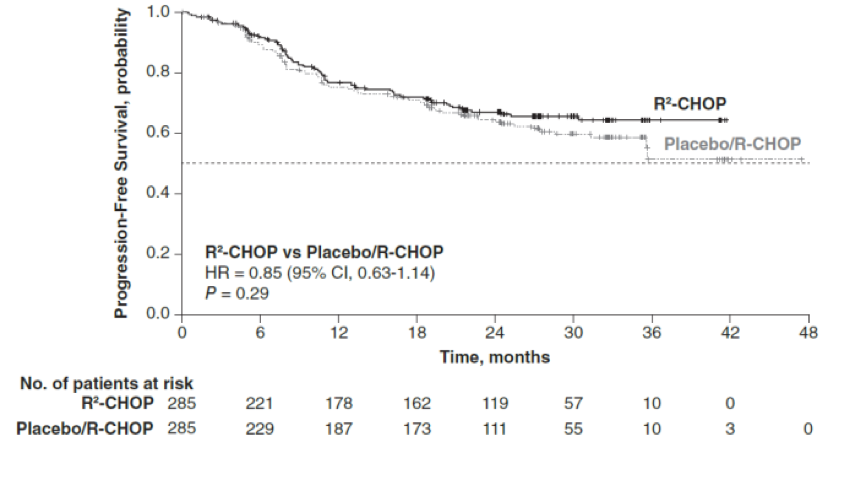
共计570例ABC亚型DLBCL患者符合ROBUST研究的入组标准 (每组285例)。两组患者的基线特征相似,中位年龄65岁(52%≥65岁);42%患者IPI 2;58% IPI≥3;88% Ⅲ/IV期;34%伴有大包块。主要研究终点PFS没有达到;两组的中位PFS也没有达到。Ⅲ/IV期和IPI≥3患者中观察到R2-CHOP组相较于安慰剂/R-CHOP组具有PFS获益趋势。两组均未达到中位EFS(P=0.73)。生存者中位随访27.1个月(0~47),R2-CHOP组的2年OS为79%,安慰剂/R-CHOP组为80%。两组的ORR均为91%,R2-CHOP和安慰剂/R-CHOP组的CR分别为69%和65%。74%的R2-CHOP组和84%的安慰剂/R-CHOP组患者完成了6个周期治疗。AEs(主要是中性粒细胞减少)是停止治疗的最常见原因。R2-CHOP与安慰剂/R-CHOP最常见的3/4级AEs (≥10%)为中性粒细胞减少(60%和48%)、贫血(22%和14%)、血小板减少(17%和11%)、白细胞减少(14%和15%)、发热性中性粒细胞减少(14%和9%)和淋巴细胞减少(11%和8%)。
结论
总体而言,在初治的ABC-DLBCL患者中,ROBUST研究并未达到主要研究终点,但是晚期和高危患者接受R2-CHOP治疗后显示出PFS获益趋势。R2-CHOP的安全性与个体药物一致,联合治疗后未产生新的安全性问题。
Selinexor在R/R DLBCL患者中的2B期临床研究(ABS:031)
背景
接受过至少2线治疗的R/R DLBCL患者(包括干细胞移植后进展或不适合干细胞移植患者)的治疗选择有限。需要具有不同作用机制的治疗方法来改善这些患者的生存。Selinexor是一种口服的选择性XPO1抑制剂,其可导致肿瘤抑制蛋白在细胞核内积累和活化。在1期研究中,单药selinexor治疗R/R DLBCL的ORR为25.6%,CR为9.3%。
方法
入组的R/R DLBCL患者既往接受过2-5线的治疗。通过亚型(GCB或non-GCB)对患者进行分层,selinexor 60mg,每周两次,28天为1周期。主要终点是ORR。次要终点包括DOR和安全性评估。
结果
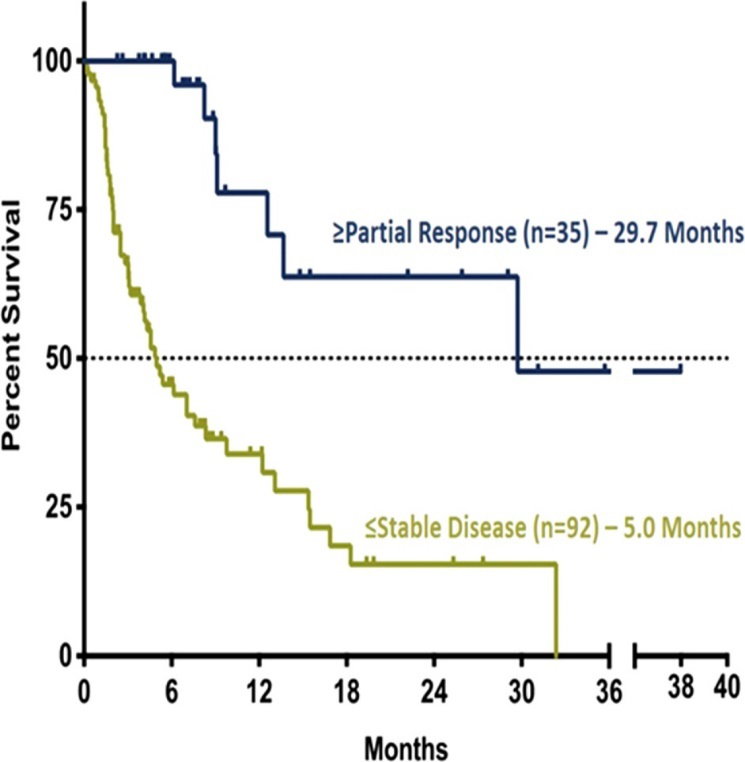
研究入组了129名患者。中位年龄为67岁(54%的患者>65岁)。先前治疗的中位数为2(1-6),34%的患者接受≥3线治疗,31%的患者先前接受干细胞移植治疗。21%的患者报告了与治疗相关的严重不良事件(SAE)。最常报告的治疗相关AE(3,4级)包括:恶心(6%,0%),血小板减少(24%,13%),疲劳(9%,0%),厌食(3%,0%)和贫血(13%,1%)。在停止治疗的85.8%的患者中,大多数是由于PD,9.3%是由于AE。 ORR为27.6%(14例CR和21例PR)。GCB亚型的ORR为32.2%,non-GCB亚型的ORR为20.6%。中位反应时间为57天(47-115天),中位DOR为8.4个月;CR患者的中位DOR为13.4个月。中位PFS为3.6个月,中位OS为9.1个月。≥PR患者的中位OS为29.7个月,显著长于≤稳定患者5.0个月的中位OS(p <0.0001)。
结论
单药selinexor在R/R DLBCL中表现出深度和持久的反应(ORR为27.6%,DOR为8.4个月)。没有发现新的安全性问题; 通过剂量调整和/或支持治疗来管理AE。 在GCB和non-GCB亚型中均观察到临床获益。这些结果强调了selinexor作为一种新疗法治疗R/R DLBCL的潜力
张会来教授点评
DLBCL是一组具有高度侵袭性及异质性的疾病。R-CHOP是其标准治疗方案,如何进一步提高DLBCL的治疗效果是近年来的研究热点。其中一种治疗策略是RCHOP+X方案,但是不论是硼替佐米、伊布替尼抑或是来那度胺均未能提高其治疗效果;而另一种治疗策略是RCHOP基础上的维持治疗,同样经历了利妥昔单抗、来那度胺、依维莫司以及enzastaurin的不断探索,但仍以失败告终。这些研究再次表明,R-CHOP方案仍然是DLBCL的一线标准治疗方案,即使在新药辈出的今天,其地位目前来看依然是不可撼动的。
本次ICML会议上,CAVALLI研究(ABS:089)证实VEN联合RCHOP 可改善BCL-2 IHC+的初治DLBCL的疗效。Smart Start研究也证实RLI这种无化疗方案对新诊断的DLBCL疗效显著,当然这也需要入组更多的患者以及更长时间随访的验证。此外,针对初治中高危或高危的DLBCL,目前有两项全球多中心的III期临床研究值得关注,分别为ENGINE(Abs: OT03)和POLARIX(Abs: OT02)。
虽然RCHOP方案可以使60%的DLBCL患者达到长期缓解,但仍有高达40%的患者最终会转变成复发、难治,除了少部分患者经过挽救治疗及移植巩固达到治愈,还有20%~30%的患者目前仍缺乏行之有效的治疗手段。SCHOLAR-1研究纳入了636例难治的DLBCL,接受化疗的ORR为26%,CR7%,而中位的OS只有6.3个月。CAR-T在R/RDLBCL展现出较好的疗效和前景,但CRS和神经毒性发生率较高,仍需开发更为高效低毒的产品。
近年来随着对DLBCL分子生物学特点的深入了解,根据分子表型制定个体化治疗是目前研究热点。靶向CD79b的polatuzumab vedotin、BCL-2抑制剂venetoclax、XPO1抑制剂selinexor、CD20和CD3双特异性抗体REGN1979等分子靶向和免疫治疗新药已经在R/R DLBCL患者中取得了一定效果。当然上述研究多为I/II期,仍需更多大样本、多中心、随机、对照的III期临床试验的验证。
1. https://onlinelibrary.wiley.com/toc/10991069/2019/37/S2
2.Crump M, Neelapu SS, Farooq U, et al. Outcomes in refractory diffuse large B-cell lymphoma: results from the international SCHOLAR-1 study Blood. 2017;130(16): 1800-1808.
3.Locke FL, Ghobadi A, Jacobson CA, et al. Long-term safety and activity of axicabtagene ciloleucel in refractory large B-cell lymphoma (ZUMA-1): a single-arm, multicentre, phase 1-2 trial. Lancet Oncol. 2019 Jan;20(1):31-42.
4.Schuster SJ, Bishop MR, Tam CS, et al. Tisagenlecleucel in adult relapsed or refractory diffuse large B-cell lymphoma. N Engl J Med 2019;380:45-56.
5. Tilly H, Morschhauser F, Bartlett NL, et al. Polatuzumab vedotin in combination with immunochemotherapy in patients with previously untreated diffuse large B-cell lymphoma: an open-label, non-randomised, phase 1b-2 study. Lancet Oncol. 2019 May 14. pii: S1470-2045(19)30091-9.











 苏公网安备32059002004080号
苏公网安备32059002004080号


