
第51例
乳腺癌中HER2阳性乳腺癌素来被称为“最凶险的乳腺癌”。在曲妥珠单抗问世前,HER2阳性乳腺癌可谓与三阴性乳腺癌“并驾齐驱”, 是乳腺癌中进展快、易复发转移且预后不良的一类。随着抗HER2治疗的问世,其疗效得到了极大的改善。因此对于HER2阳性的晚期乳腺癌患者,抗HER2治疗应尽早、全面和坚持不懈的持续治疗。

浙江大学医学院附属杭州市第一人民医院乳腺外科主任
浙江省抗癌协会乳腺癌专业委员会常委
浙江省医师协会乳腺肿瘤专业委员会副主任委员
浙江省抗癌联盟乳腺肿瘤专业委员会副主任委员
海峡两岸医药卫生交流协会肿瘤防治专家委员会常委
中国医药教育乳腺浙江分会常委
浙江省中西医结合学会乳腺病专业委员会常委
浙江省杭州市医学会肿瘤学分会乳腺癌学组组长

浙江大学医学院附属杭州市第一人民医院乳腺外科
浙江省抗癌协会乳腺癌专业委员会青年委员
中国医药教育协会乳腺疾病专业委员会浙江分会委员
浙江省杭州市医学会肿瘤分会乳腺肿瘤学组委员
基本情况
患者女性,51岁,平素月经规律。2017年1月,因“发现左乳肿块2年余,左腋下肿块1月余”入院。1年前曾有卵巢囊肿手术病史,高血压和糖尿病病史多年,否认其他疾病和传染病史。
检查及病理
▎体格检查:双侧乳腺外观正常,未见橘皮样变、乳头凹陷等。左乳外上象限可及大片增厚乳腺组织,大小约5.0cm×5.0cm,质硬,活动差,边界欠清。右乳11点方向可触及一约1.2cm×1.0cm的肿块,边界尚清,活动度欠佳。左侧腋窝可触及一约5.0cm× 6.0cm的肿块,质硬,边界尚清,活动度差,右侧腋窝未及明显肿大淋巴结,双侧锁骨上淋巴结未及肿大。
▎影像学及实验室检查:①乳腺超声:双乳大小对称,外形无殊,腺体回声不均,结构紊乱,以左乳为著。左乳腺12点位置可见一大小约1.2 cm×0.8 cm× 0.9cm的低回声结节,浅分叶状,内可见一点状强回声,未见血流信号。右乳内可见3~4个低回声结节,较大的3个分别位于9、10、11点钟位置,大小分别为0.7 cm×0.6 cm×0.7cm、1.4 cm×0.8 cm× 1.0 cm、1.2 cm×0.7 cm×0.8cm,CDFI未见明显血流信号。双侧腋下可见低回声结节,左侧较大为4.3 cm× 3.2cm,呈融合状,内可见少许血流信号,右侧较大为1.8 cm×1.0cm,内部结构清,皮质偏厚。左侧12点钟及右侧11点钟结节BI-RADS 4A类,余BI-RADS 3类。②乳腺钼靶示(图1):左乳腺体结构欠佳、乳头轻凹陷伴左腋下肿大淋巴结,考虑BI-RADS 4B类。③乳腺MRI示(图2):左乳上方可见斑片状异常信号灶,平扫T1WI呈等信号,T2WI呈混杂高低信号,DWI呈高信号,ADC值约0.8×103~1.1×103,增强后强化明显,强化欠均匀,时间信号强度曲线呈流出型为主。左乳上方占位,BI-RADS 4B 类,双乳腺病伴小结节,BI-RADS 2类,双侧腋下多发淋巴结,左侧部分增大、融合。④肺CT示:双肺未见明显异常病灶。⑤腹部MRI示:肝多发大小不等结节,转移瘤考虑,后腹膜多发淋巴结淋巴结,转移可能。⑥颅脑MRI及全身骨ECT未见明显异常。
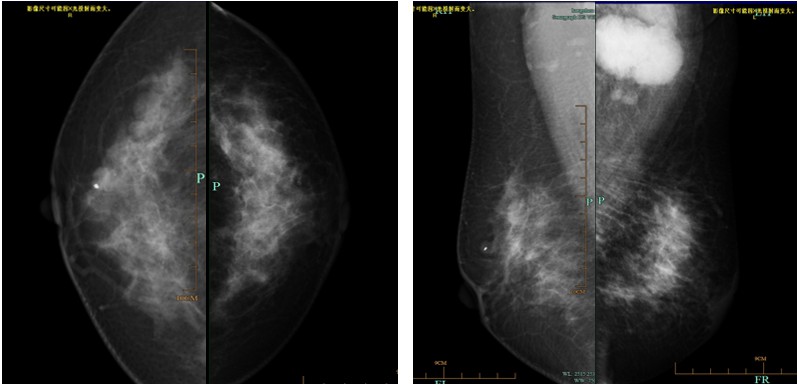
图1 患者入院时的乳腺钼靶
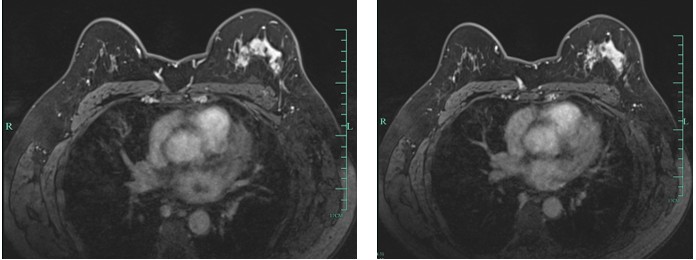
图2 患者入院时的乳腺MRI

图3 患者入院时的肝脏MRI
患者行超声引导下左乳肿物及左腋下淋巴结活检术,病理示:“左乳穿刺”脂肪及增生的纤维组织内见少数导管及明显异型细胞团,结合免疫组化结果考虑为癌组织,因病灶太少无法判断有无浸润性成分及具体分类分型。左腋下淋巴结穿刺见转移性癌。免疫组化(左腋窝)示:ER(个别+),PR(-),HER2(3+),Ki-67(+,30%)。结合患者病史、相关影像学和病理检查结果,目前诊断为:左乳浸润性癌(cT2N3M1,Ⅳ期),左腋窝淋巴结转移,肝转移。分子分型:HR阴性HER2阳性型。
治疗经过
1.化疗与靶向治疗
经与患者及其家属反复沟通交流,强调了乳腺癌治疗中抗HER2的重要性和必要性,建议一线治疗拟行多西他赛+环磷酰胺双药化疗联合曲妥珠单抗靶向治疗(TCH方案),于2017年1月开始,共8周期。
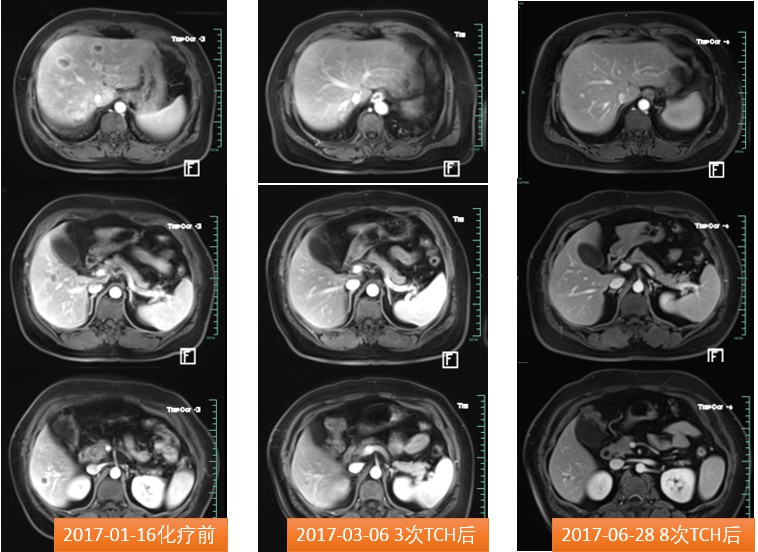
图4 患者影像学复查评估
8周期化疗后影像学显示:左侧乳腺类结节样影,与2017年1月6日检查对比,左侧腋窝淋巴结较前明显缩小,肝内多枚低密度灶较前明显缩小。综合疗效评价为完全缓解(complete response,CR)。
2.手术治疗
患者排除明显禁忌,于2017年7月行左乳癌姑息性单乳切除+左侧腋窝淋巴结清扫术,术后病理示:左乳腺高级别导管原位癌(最大径约1.8cm),可见多灶浸润性癌Ⅲ级,非特殊类型,最大浸润灶大小0.05cm~0.1cm,部分肿瘤细胞胞质空泡化,肿瘤间质纤维化,内见灶状淋巴细胞浸润,脉管内未见癌栓,肿瘤累及神经束,乳头下大导管未累及,基底切缘未累及,周围非肿瘤性乳腺组织基底膜和小叶硬化,腋窝淋巴结内见肿瘤转移(1/5)伴化疗后改变。纤维腺瘤伴间质胶原化(内有结节2个,最大径分别为0.6cm和1.0cm)。免疫组化示:ER(-),PR(-),HER2(3+),Ki-67(+,15%)。术后患者行局部放疗同时联合曲妥珠单抗靶向治疗1年。
3.复发与手术
2018年5月患者出现腰痛症状,影像学检查:①泌尿系CT平扫+增强(图5):左侧输尿管中段可疑结节影伴左肾盂输尿管扩张积水,周围脂肪间隙浑浊、多发小淋巴结影,提示需首先除外占位性病变,建议进一步检查。腹膜后及左侧盆壁淋巴结肿大。②泌尿系超声示:右输尿管中段异常增强区占位,大小约1.5cm×0.8cm。
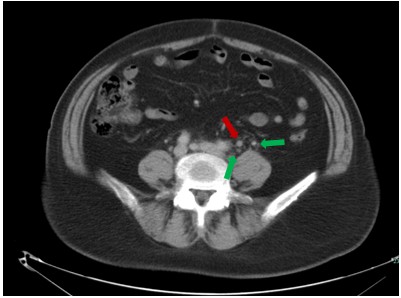
图5 患者泌尿系CT
患者于2018年7月6日在全麻下行左侧输尿管镜探查术+双J管置入术。术中见左输尿管开口上方约10cm处可见输尿管狭窄,上方输尿管扩张,于狭窄段取组织3块送检。术后病理:左输尿管纤维及平滑肌组织内见低分化癌浸润,结合免疫组化及临床病史考虑来源于乳腺。免疫组化示:ER(-),PR(-),HER2(3+),Ki-67(+,30%)。截至2018年5月,无进展生存期(progression-free survival, PFS)为11个月。
4.术后治疗
患者术后给予曲妥珠单抗联合紫杉醇(PH)周方案9周期联合治疗,后给予卡培他滨联合曲妥珠单抗(XH)方案6周期治疗,治疗结束后给予曲妥珠单抗维持治疗至今,患者目前定期复查,未见明显转移或复发征象。
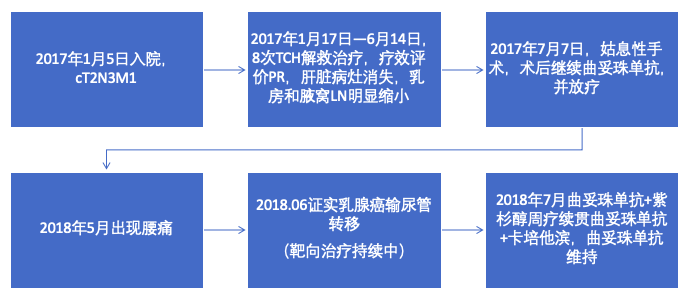
图6 患者治疗流程图
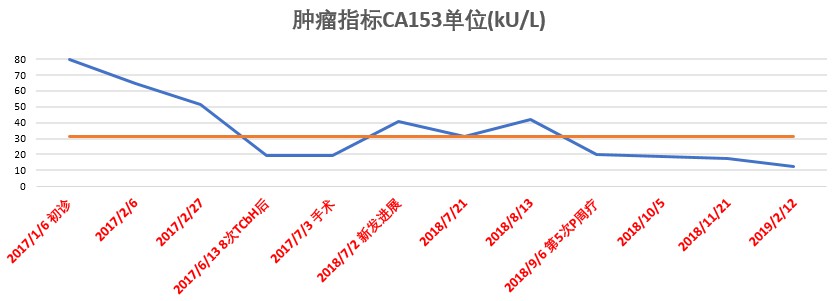
图7 患者肿瘤标记物CA15-3变化趋势图
点评专家

复旦大学附属肿瘤医院
中国临床肿瘤学会(CSCO)青委会副主任委员
中国研究型医院学会乳腺专业委员会常务委员
中国临床肿瘤学会乳腺癌专家委员会委员
中国女医师协会临床肿瘤学专业委员会委员
中国女医师协会乳腺疾病研究中心委员
上海抗癌协会癌症康复与姑息治疗专委会(CRPC)青委主任委员
上海抗癌协会癌症康复与姑息治疗专委会常委兼秘书长
上海市抗癌协会脑转移瘤专业委员会常务委员
上海市中西医结合学会乳腺病专业委员会常务委员
上海市抗癌协会乳腺癌专业委员会委员
上海市抗癌协会青年理事会常务理事
点评
患者为一位初治IV期的HER2阳性的中年女性,左乳癌伴肝淋巴结转移。一线接受多西他赛+环磷酰胺+曲妥珠单抗化疗8程(最佳疗效CR),接受原发灶切除手术后曲妥珠单抗治疗1年。二线接受曲妥珠单抗+紫杉醇方案治疗9周期(最佳疗效PR),后予以卡培他滨联合曲妥珠单抗方案6疗程,曲妥珠单抗单药维持。
该患者的治疗经过有以下几点值得思考:
1. HER2阳性患者的一线治疗:作为既往未接受过治疗的HER2阳性的转移性乳腺癌患者,NCCN(2019V1)乳腺癌指南提示其一线治疗选择为帕妥珠单抗与曲妥珠单抗双靶向联合紫杉类药物,包括紫杉醇以及多西他赛。考虑到当时帕妥珠单抗的不可及性,根据2017年中国抗癌协会指南以及2019年CSCO乳腺癌诊疗指南,曲妥珠单抗联合多西他赛+卡培他滨、多西他赛、长春瑞滨、卡培他滨以及紫杉醇±卡铂、都是中国患者可选择的一线方案。此例患者一线接受多西他赛+环磷酰胺+曲妥珠单抗的治疗达到了CR。多西他赛+环磷酰胺+曲妥珠单抗在HER2阳性患者的辅助治疗中有一定的证据,在单臂的II期临床研究中,4疗程多西他赛+环磷酰胺(q3w)联合曲妥珠单抗在I-II期早期乳腺癌患者中与含蒽环类的辅助化疗方案的疗效相似。但其作为晚期一线治疗的证据并无直接证据,以曲妥珠单抗及多西他赛为基础的治疗方案是HER2阳性转移性患者晚期一线的推荐方案。
2.对于初治IV期患者原发灶手术的意义:既往研究结果对于初治IV期患者是否接受手术存在矛盾,TATA研究前瞻性探索对于一线化疗获得缓解的Ⅳ期乳腺癌,原发灶切除手术对生存获益的影响。手术治疗组和非手术治疗组的OS时间无明显差异,提示手术不能带来生存改善。另一项土耳其研究者开展的前瞻性MF07-01研究,一组先局部手术再序贯全身治疗,另一组仅接受全身治疗,主要观察终点3年OS率为阴性结果,但是更长时间的随访发现手术序贯化疗组患者的中位OS得到显著延长。在孤立骨转移、年龄<55岁、ER/PR+及HER2-亚组患者中具有显著生存获益。中山大学孙逸仙纪念医院姚和瑞教授通过中国患者真实世界的多中心数据以及倾向性评分,比较初治IV乳腺癌患者接受原发灶手术与否的疗效后发现,手术患者和非手术患者的5年生存率分别为62.4%和60.3%,OS 无统计学差异,但在Ki67≥20%的亚组患者中接受原发灶手术可带来生存获益。同时对42 项回顾性研究的进行Meta分析,发现原发灶手术较非手术者存在OS的显著获益。与此相反,纳入的 5 项高质量前瞻性研究发现接受原发灶手术组与非手术组的 OS 无统计学差异。综上研究结果,未经选择的初治Ⅳ期乳腺癌患者不能手术治疗中获益,特定患者,包括孤立骨转移、年龄<55岁、ER/PR+、HER2-以及Ki67≥20%,可能能从手术治疗中获益。此例患者为初治IV期伴肝淋巴结多处转移,一线化疗联合抗HER2靶向治疗获得完全缓解,后接受原发灶切除手术,可能出于减少肿瘤负荷的考虑,但对于OS的获益可能并不大。
3. 曲妥珠单抗治疗进展后二线治疗方案的选择:既往研究证实在曲妥珠单抗治疗进展后,持续抑制HER2通路能够带来持续的生存获益。对于接受曲妥珠单抗治疗后进展的转移性乳腺癌患者,2019年CSCO乳腺癌诊疗指南提示拉帕替尼+卡培他滨、吡咯替尼+卡培他滨、T-DM1、酪氨酸激酶抑制剂+其他化疗药物(如长春瑞滨)、曲妥珠单抗+拉帕替尼、曲妥珠单抗+另一类化疗药物都是二线HER2阳性患者的可选方案。NCCN(2019V1)乳腺癌指南也提示,在转移后接受化疗+曲妥珠单抗治疗但未接受过帕妥珠单抗的患者可考虑曲妥珠单抗+帕妥珠单抗联合或不联合细胞毒药物(如长春瑞滨或紫杉烷)的治疗,随着帕妥珠单抗在中国上市,以及后续可能进入医保,可以考虑选择。该患者后续选择曲妥珠单抗单药维持,考虑到曲妥珠单抗相对有效、不良反应轻、经济可承受,使患者得到长期的病情控制,是个合理的选择。
1. NCCN guidelines for breast cancer version 1.2019. Available at:http://www.nccn.org/professionals/physician_gls/pdf/breast.pdf.
2. 中国抗癌协会乳腺癌专业委员会. 中国抗癌协会乳腺癌诊治指南与规范(2017年版)[J]. 中国癌症杂志, 2017,27(09):695-759.
3. R. Badwe, R. Hawaldar, N. Nair, R. Kaushik, V. Parmar, S. Siddique, A. Budrukkar, I. Mittra, S. Gupta. Locoregional treatment versus no treatment of the primary tumour in metastatic breast cancer: an open-label randomised controlled trial[J]. Lancet Oncol, 2015,16(13):1380-1388.
4. Soran A, Ozmen V, Ozbas S, et al. Randomized Trial Comparing Resection of Primary Tumor with No Surgery in Stage IV Breast Cancer at Presentation: Protocol MF07-01[J]. Ann Surg Oncol, 2018,25(11):3141-3149.
5. Yao H, Yu Y, Wang Y, et al. Overall survival following locoregional surgery of the primary tumor in de novo stage IV breast cancer patients.[J]. JOURNAL OF CLINICAL ONCOLOGY, 2018,36S(15).
6. Argolo D F S D, Smyth L M, Iyengar N M, et al. Trastuzumab and pertuzumab-based versus other therapy as second-line therapy in HER2-positive metastatic breast cancer: A retrospective study from single center[J]. JOURNAL OF CLINICAL ONCOLOGY, 2015,33S(15).
7. Baselga J, Gelmon K A, Verma S, et al. Phase II Trial of Pertuzumab and Trastuzumab in Patients With Human Epidermal Growth Factor Receptor 2-Positive Metastatic Breast Cancer That Progressed During Prior Trastuzumab Therapy[J]. JOURNAL OF CLINICAL ONCOLOGY, 2010,28(7):1138-1144.
8. Urruticoechea A, Rizwanullah M, Im S, et al. Final overall survival (OS) analysis of PHEREXA: A randomized phase III trial of trastuzumab (H) plus capecitabine (X) +/- pertuzumab (P) in patients with HER2-positive metastatic breast cancer (MBC) who experienced disease progression during or after H-based therapy[J]. JOURNAL OF CLINICAL ONCOLOGY, 2018,36S(15)
9.Verma S, Miles D, Gianni L, et al. Trastuzumab emtansine for HER2-positive advanced breast cancer.[J]. New England Journal of Medicine, 2013, 368(25):1783-91.
10.Extra J M, Antoine E C, Vincentsalomon A, et al. Efficacy of Trastuzumab in Routine Clinical Practice and After Progression for Metastatic Breast Cancer Patients: The Observational Hermine Study[J]. Oncologist, 2010, 15(8):799.
11.Minckwitz G V, Bois A D, Schmidt M, et al. Trastuzumab Beyond Progression in Human Epidermal Growth Factor Receptor 2–Positive Advanced Breast Cancer: A German Breast Group 26/Breast International Group 03-05 Study[J]. Journal of Clinical Oncology, 2009, 20(4):420-422.













 苏公网安备32059002004080号
苏公网安备32059002004080号


