
第47例
HER2阳性乳腺癌素来被称为“最凶险的乳腺癌”,是乳腺癌中进展快、易复发转移且预后不良的一类。因此,对于ER+/HER2+的晚期乳腺癌患者,抗HER2治疗应尽早、全面和坚持不懈。

辽宁省肿瘤医院乳腺四病区主任
中国医科大学及大连医科大学肿瘤外科研究生导师
中国抗癌协会乳腺癌专业委员会委员
中国医药教育协会常务理事
中国医药教育协会乳腺疾病专业委员会常委
中国医学促进会乳腺疾病分会常委
中华医学会肿瘤整形学组委员
辽宁省抗癌协会靶向治疗专业委员会副主任委员
中国医药教育协会乳腺疾病专业委员会沈阳学组副主任委员
辽宁省抗癌协会乳腺癌专业委员会常委
辽宁省“百千万⼈人才”百层⼈人才

辽宁省肿瘤医院乳腺外科
2007年9月-2010年7月 就读复旦大学
辽宁省细胞生物学学会乳腺肿瘤精准治疗与临床科研委员会委员
曾在国内外期刊发表多篇学术论文
参与多项国家及省部级课题
基本情况
患者女性,43岁,平素月经规律。2014年5月因“发现左乳肿块1周”就诊。既往体健,否认慢性病、传染病史。
初步检查与诊断
▎体格检查:双侧乳房对称,左乳房皮肤发红伴水肿。左乳头下方可触及直径约4cm肿块,边界不清,质硬,活动度差。左腋窝可及多枚肿大的淋巴结。右乳和右腋窝未触及明显异常。
▎辅助检查:①乳腺超声:左侧乳腺乳头下方腺体层内可探及一大小约34mm×43 mm×26mm不均质低回声区,形态不规则,边界不清楚,内见血流信号,测其中一条动脉,RI=0.89,结合临床表现考虑BI-RADS 5类。左侧腋下见大小约22 mm×11mm和14 mm×14mm的低回声区两处,形态尚规则,边界尚清晰,内未见明显血流信号。右侧腋下未探及明显肿大淋巴结。②乳腺MRI示(图1):左乳略肿大,腺体内多发结节状、斑片状及条状长T1或稍长T2信号影,增强后左乳可见区域性强化灶,大小约35 mm×43 mm×23mm强化曲线呈速升平台型。双乳另见点状强化灶。左腋下见肿大淋巴结,余项未见明显异常。③骨扫描未见异常。④肝胆脾彩超未见异常。⑤血肿瘤标志物未见异常。
患者行超声引导下左乳肿物及左腋下淋巴结穿刺活检术,病理示:左乳腺浸润性癌,左腋下穿刺淋巴结可见转移性癌,结合病史考虑乳腺来源。免疫组化(乳腺)示:ER(+,70%),PR(-),HER2(3+),Ki-67(+,50%)。
结合患者病史、相关影像学和病理检查结果,目前诊断为:左乳浸润性癌(pT4N2M0,ⅢB期),左腋窝淋巴结转移,分子分型:ER阳性HER2阳性型。
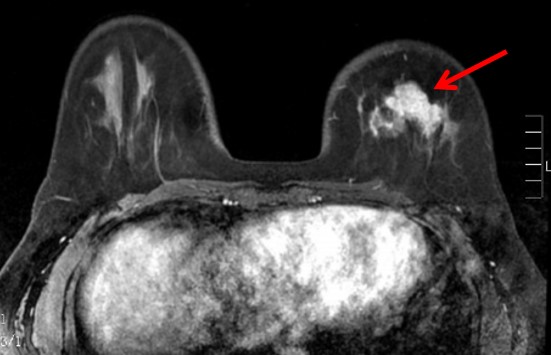
图1 乳腺MRI检查(2014年5月)
治疗经过
▎新辅助治疗:经与患者及其家属反复沟通交流,强调了乳腺癌治疗中抗HER2的重要性和必要性,建议一线治疗拟行多西他赛+卡铂双药化疗联合曲妥珠单抗靶向治疗(TCbH方案),于2014年6月开始,共使用7周期。
第2周期后影像学显示:左乳略肿大,腺体内多发结节状、斑片状及条状长T1或稍长T2信号影,增强后左乳可见区域性强化灶,大小约25 mm×14 mm×10mm,强化曲线呈速升平台型。双乳另见点状强化灶和左腋下见肿大淋巴结。与2014年5月片对比,左乳病变范围及左腋窝肿大淋巴结均缩小,综合疗效评价为部分缓解(partial response,PR)。第6周期后影像学显示:双侧乳房由不均质腺体组成,背景实质几乎不强化,双侧乳腺内未见确切异常信号影,双侧腋下未见肿大淋巴结。与2014年5月影像学对比,左乳肿块及左腋窝淋巴结均消失,综合疗效评价为完全缓解(complete response,CR)。
▎手术治疗:排除明显禁忌,于2014年9月26日行左乳癌改良根治术,术后病理示:左乳腺癌符合新辅助化疗后改变,G4,淋巴结见转移癌(4/21)。免疫组化示:ER(+,80%),PR(-),HER2(3+),Ki-67(+,40%)。术后患者行局部放疗同时联合曲妥珠单抗靶向治疗1年。后给予戈舍瑞林+来曲唑内分泌治疗。
▎疾病进展:2018年5月患者常规复查:①颈部超声:于左侧锁骨上可探及3枚大小约为22 mm×7.0mm、14 mm×8mm及 11 mm×8.5mm的低回声区,形态尚规则,边界尚清晰,内见少许血流信号.②胸部CT示(图2):纵隔居中,前纵隔多发肿大淋巴结影。与2017年10月30日影像学资料比较,前纵隔新发多个肿大淋巴结,余未见明显变化,建议进一步检查明确。
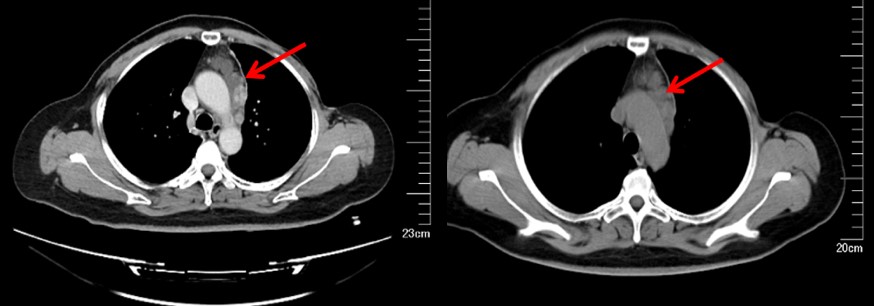
图2 患者胸部CT(2018年5月)
▎颈部肿物切除及化疗:患者于2018年5月行左颈部肿物切除术,病理示:左颈部淋巴结转移癌,结合病史考虑乳腺来源。免疫组化示:ER(+,70%),PR(-),HER2(3+),Ki-67(+,20%)。截至2018年5月,患者无病生存期(disease-free survival,DFS)为44个月。
术后患者行白蛋白紫杉醇+曲妥珠单抗联合治疗(PH方案)。2周期后复查超声示:左颈部可探及多枚淋巴结,较前略增大。综合疗效评价为:病情稳定(stable disease,SD)。后更改治疗方案,更换为白蛋白紫杉醇+曲妥珠单抗+拉帕替尼治疗,2周期治疗后综合疗效评价为PR。患者目前仍在继续原方案治疗中,其间定期复查,未见明显转移或复发征象。
点评专家

中国医科大学附属第一医院乳腺外科主任
辽宁省抗癌协会乳腺癌专业委员会主任委员
中国临床肿瘤学会(CSCO)理事会理事
中华医学会肿瘤分会乳腺肿瘤学组副组长
中国老年学学会乳腺癌分委会副主任委员
中国康复医学会修复重建美容外科分会常务委员
北京乳腺病防治学会外科专委会副主任委员
中国抗癌协会乳腺专业委员会常务委员
中华医学会外科分会乳腺癌学组委员
辽宁医学会外科分会乳腺外科学组组长
点评
患者青年女性,月经规律。既往穿刺病理提示为ⅢB期乳腺癌。多次化疗及手术治疗,手术前后自始至终贯穿并坚持抗HER2治疗,取得了较为成功的效果。分析患者年龄、既往治疗和手术病理等情况,结合NCCN乳腺癌指南2018 V3版和《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南》 2018 V1版分析,截至目前,患者未出现新的疾病进展,患者既往化疗、手术、内分泌及靶向治疗的序贯治疗是较为合适和有效的。
1. HER2阳性乳腺癌需要抗HER2治疗
乳腺癌中HER2阳性乳腺癌是一种凶险程度很高的乳腺癌类型,其绝大部分依赖于HER2通路来驱动肿瘤细胞的增殖,与肿瘤侵袭性强、复发率高有关。在乳腺癌的治疗中,无论处于治疗的什么阶段,对于有HER2阳性表达的肿瘤患者,抗HER2治疗是首要且需要持久进行的。曲妥珠单抗显著改变了HER2阳性乳腺癌的结局,其能显著提高HER2阳性早期乳腺癌的治愈机会,显著延长HER2阳性晚期乳腺癌患者的总生存期(overall survival,OS),显著降低复发和病死风险,是HER2阳性乳腺癌治疗的标准药物,已被各类指南的推荐和首选。
2. 抗HER2的新辅助治疗
在患者首次明确病情后,新辅助治疗首选TCbH方案是合理的。回顾术前积极地行新辅助治疗,结合指南分析,新辅助治疗需满足以下条件:①肿块较大(>5cm);②腋窝淋巴结转移;③HER2阳性;④三阴性乳腺癌;⑤有保乳意愿,但肿瘤大小与乳房体积比例大难以保乳者。其中大部分中国专家认同仅有HER2阳性或三阴性乳腺癌作为术前新辅助治疗的指征的选择标准时,肿瘤应大于2cm。既往临床研究证明HER2患者的新辅助治疗,曲妥珠单抗联合化疗与单用化疗相比能够显著提高pCR率,奠定了曲妥珠单抗在HER2阳性乳腺癌新辅助治疗中的标准地位[1~2]。目前AC-TH与TCbH方案均可作为新辅助治疗的推荐方案[3],但考虑到先用曲妥珠单抗可能达到快速缩瘤、防止肿瘤进展的作用,更倾向于TCbH方案,对于此患者的应用是合适的。如果不考虑药物可及性、患者经济承受能力等问题,亦可选择双靶联合化疗的新辅助治疗方案,以进一步提高pCR率。
3. 内分泌治疗
该患者相对年轻,就诊时肿瘤负荷较大,分期晚,化疗后未达到绝经状态,组化ER阳性,且呈高表达。对于此类术后复发转移的高危人群,手术后的放疗及序贯1年的靶向治疗是无可厚非的;而对于这类患者内分泌治疗方案的选择不用考虑HER2状态,OFS+AI是首选方案。
4. ER+/HER2+乳腺癌复发抗HER2治疗的选择
在患者发现转移时DFS为44个月,如此的DFS时间客观上也肯定了此前的治疗策略及效果。针对HER2阳性复发转移乳腺癌,晚期一线解救治疗的标准方案仍然是以抗HER2为基础的综合治疗,而治疗目的主要是延长PFS和OS、提高生活质量。既往H0648g和M77001的临床研究证实在以紫杉类基础上联合曲妥珠单抗治疗能够显著提高PFS和OS,确立了曲妥珠单抗联合紫杉类在一线标准治疗的地位[4~5]。目前,国际上对HER2阳性的晚期乳腺癌患者标准的一线治疗为曲妥珠单抗、帕妥珠单抗双靶联合多西他赛[6],帕妥珠单抗也已于2018年12月17日获得我国药品监督管理局的批准。结合患者当时出现左颈部淋巴结和纵隔多发淋巴结转移的情况,转移部位比较分散,同时由于药物可及性的局限性因素,选择PH方案治疗是较为合适的。
患者此时的治疗属于晚期治疗,一线应用白蛋白紫杉醇联合赫赛汀治疗2周期后因超声评估颈部淋巴结略有增大,综合评效为SD而加用拉帕替尼。按照RECIST标准,超声并不是评估疗效的标准手段。晚期治疗追求的是总体OS延长,治疗原则为细水长流,药尽其用。该患者一线治疗2周期后若根据RECIST评估标准获得了确切疾病进展(progressive disease, PD)证据,则该患者属于赫赛汀原发耐药,需要按照二线治疗进行选择;若为SD,需要坚持目前标准的一线治疗方案。
该患者属于HR阳性HER2阳性的双阳患者,常规做法是一线靶向联合化疗6~8周期后可考虑使用抗HER2靶向治疗联合内分泌治疗进行维持治疗,从而为患者争取到一定时间的化疗假期。如果一线化疗效果理想,副作用小也可以化疗联合靶向治疗持续应用至疾病进展。结合患者具体情况而言,其新辅助化疗至手术,术后及术后复发持久的抗HER2治疗是较为合理的,且取得了较为满意的临床获益。
该病例基于指南规范,同时又基于临床现实合理调整的成功病例,很有启示意义。对于HER2阳性型乳腺癌患者来说,强调了抗HER2治疗的必要性、重要性和长期性。在临床工作中应充分告知所有HER2阳性的乳腺癌患者,及时接受HER2靶向治疗的获益及必要性。
1.Buzdar AU, Ibrahim NK, Francis D, et al. Significantly higher pathologic complete remission rate after neoadjuvant therapy with trastuzumab, paclitaxel, and epirubicin chemotherapy: results of a randomized trial in human epidermal growth factor receptor 2-positive operable breast cancer.[J]. Journal of Clinical Oncology, 2005, 23(16):3676.
2.Gianni L, Eiermann W, Semiglazov V, et al. Neoadjuvant and adjuvant trastuzumab in patients with HER2-positive locally advanced breast cancer (NOAH): follow-up of a randomised controlled superiority trial with a parallel HER2-negative cohort.[J]. Lancet Oncology, 2014, 15(6):640-647.
3.Perez EA, Romond EH,Suman VJ, et al.Trastuzumab plus adjuvant chemotherapy for human epidermal growth factor receptor 2-positivebreast cancer: planned joint analysis of overall survival from NSABP B-31 and NCCTG N9831[J]. Journal of Clinical Oncology,2014,20;32(33):3744-3752.
4.Kataoka K, Tokunaga M, Mizusawa J, et al. A randomized phase II trial of systemic chemotherapy with and without trastuzumab followed by surgery in HER2-positive advanced gastric or esophagogastric junction adenocarcinoma with extensive lymph node metastasis: Japan Clinical Oncology Group study JCO[J]. Japanese Journal of Clinical Oncology, 2015, 45(11):1082-1086.
5.Slamon D J, Leylandjones B, Shak S, et al. Use of chemotherapy plus a monoclonal antibody against HER2 for metastatic breast cancer that overexpresses HER2[J]. N Engl J Med, 2001,15;344(11):783-792.
6.Swain S M, Baselga J, Kim S B, et al. Pertuzumab, trastuzumab, and docetaxel in HER2-positive metastatic breast cancer[J]. N Engl J Med, 2015, 372(8):724-734.













 苏公网安备32059002004080号
苏公网安备32059002004080号


