
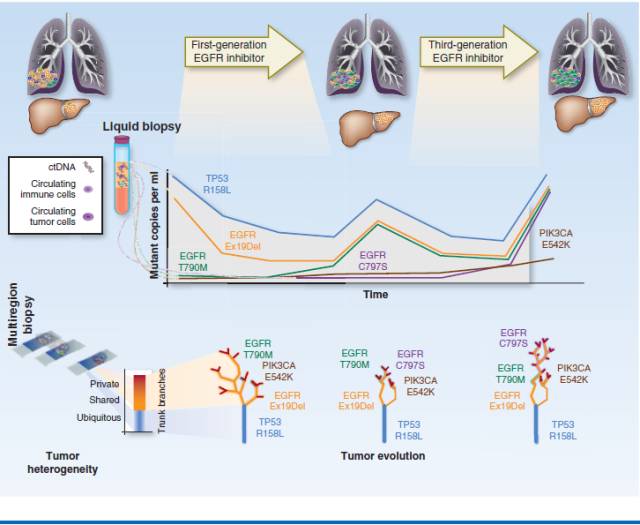
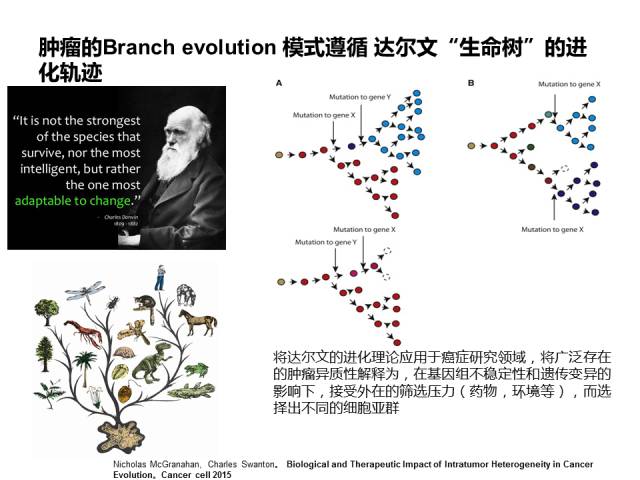
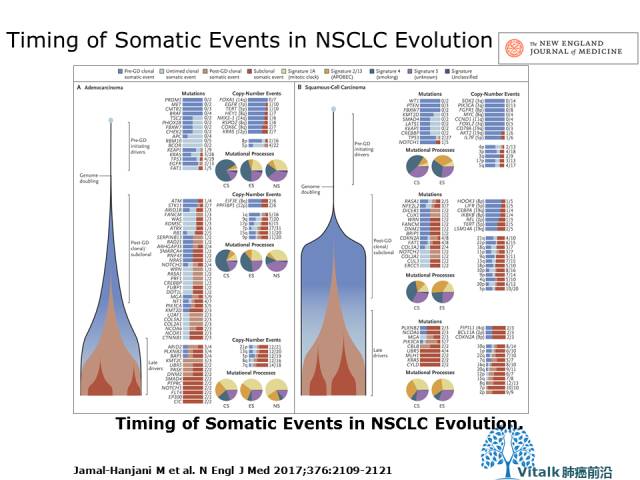
将达尔文的进化理论应用于癌症研究领域,将广泛存在的肿瘤异质性解释为,在基因组不稳定性和遗传变异的影响下,接受外在的筛选压力(药物,环境等),而选择出不同的细胞亚群
Nicholas McGranahan, Charles Swanton。 Biological and Therapeutic Impact of Intratumor Heterogeneity in Cancer Evolution。Cancer cell 2015
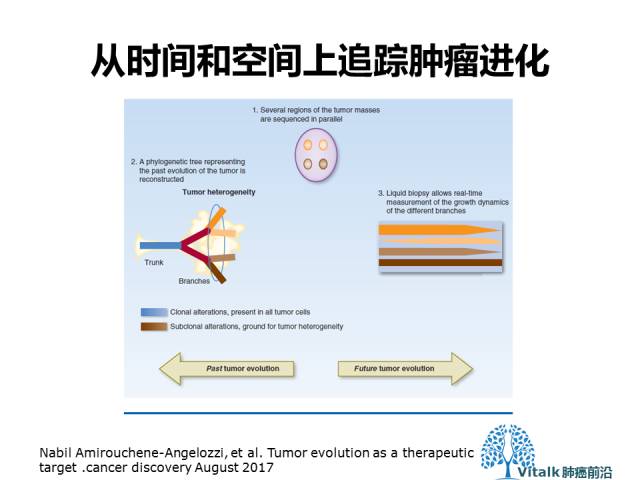
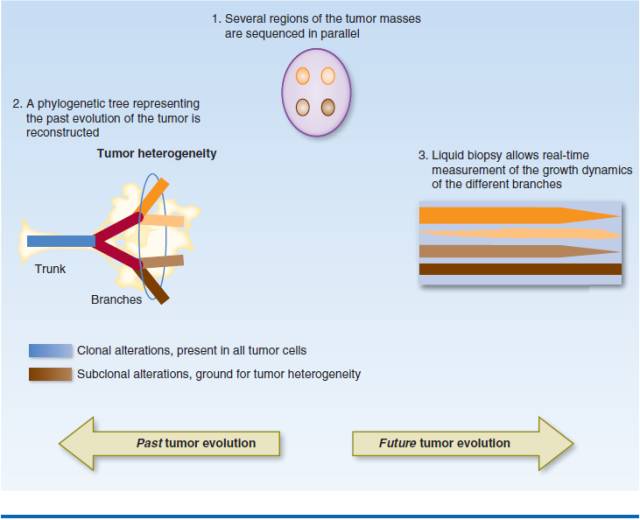
Multiregional biopsy 包括来自同一个肿块不同区域的组织的平行分析,也包括来自同一患者不同转移部位病变的分析(步骤1)。
通过评估他们在不同样本的变异发生,能够推导出个体的克隆性事件演变规律。在所有分析样本(蓝色)中存在的克隆变异可能代表“祖先”事件,
在肿瘤发生早期发生,因此被表示为肿瘤的系统发育“干”, 而异质(亚克隆)事件(棕色阴影)可能发生在后期,因此代表了系统发育树的“分支” 。亚克隆的演化是导致肿瘤异质性,对治疗产生适应性和癌症进化的基础(步骤2)。液体活检可以纵向评估不同克隆的动态变化,通过交叉比较突变的亚克隆等位基因的相对频率和(假设的)trunk 突变的“正常轨迹”,来推测未来的突变进化事件(步骤3)。
追踪肿瘤进化的方法:multiregional sequencing
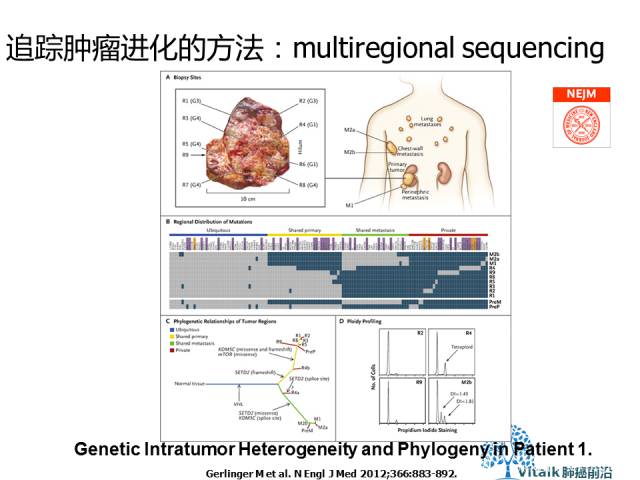
如图所示,从多区域活检获得的信息可以有效地使用以重建肿瘤进化动态(或“历史”),图形呈现为肿瘤进化树(phylogenetic tree ),存在于所有肿瘤细胞中的树干(trunk mutation)克隆变化代表祖先事件,而异质性遗传改变构成分支.
Gerlinger M et al. N Engl J Med 2012;366:883-892
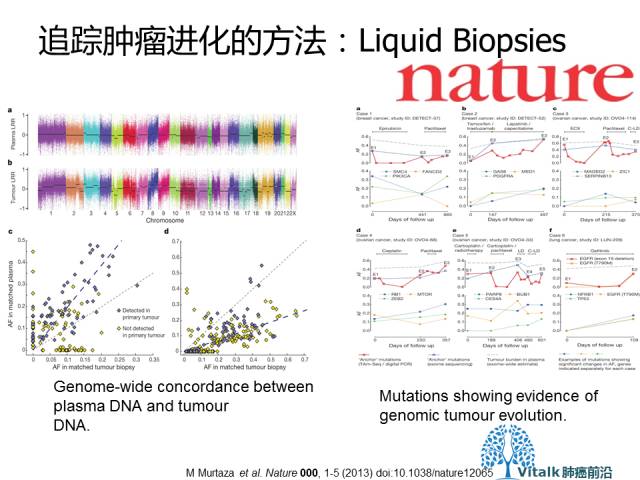
在这个proof of principle study中,我们证明了血浆ctDNA的外显子分析代表了新的非入侵性的肿瘤进化特征分析方法。 该实验数据表明,ctDNA中鉴定的CNA和体细胞突变是肿瘤基因组的广泛代表,并提供可以克服重复活检肿瘤取样的局限性的替代方法。
M Murtaza et al. Nature 000, 1-5 (2013)
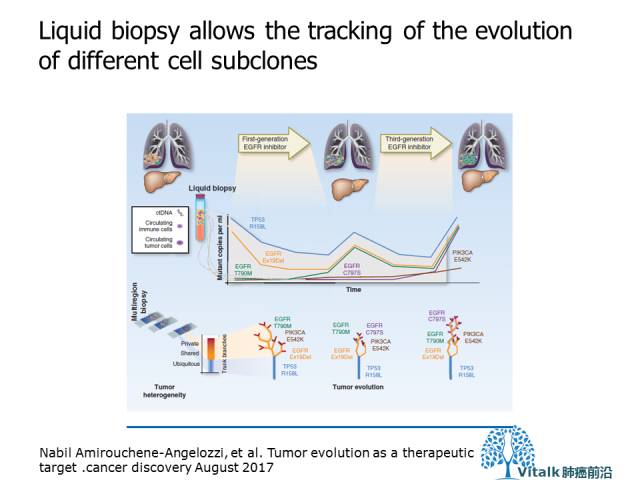 有效监测肿瘤进展要求临床医生仔细选择组织样本活检(具体目的是描绘肿瘤异质性),选择循环DNA检测的时间点,将分子情景senario与从“标准”技术获得的信息相结合,如成像诊断和蛋白质标记。 应用监测肿瘤进展的多项诊断技术治疗对肿瘤进化进行综合分析的研究,如TRACERx提供了证据验证这种方法的可行性。
有效监测肿瘤进展要求临床医生仔细选择组织样本活检(具体目的是描绘肿瘤异质性),选择循环DNA检测的时间点,将分子情景senario与从“标准”技术获得的信息相结合,如成像诊断和蛋白质标记。 应用监测肿瘤进展的多项诊断技术治疗对肿瘤进化进行综合分析的研究,如TRACERx提供了证据验证这种方法的可行性。
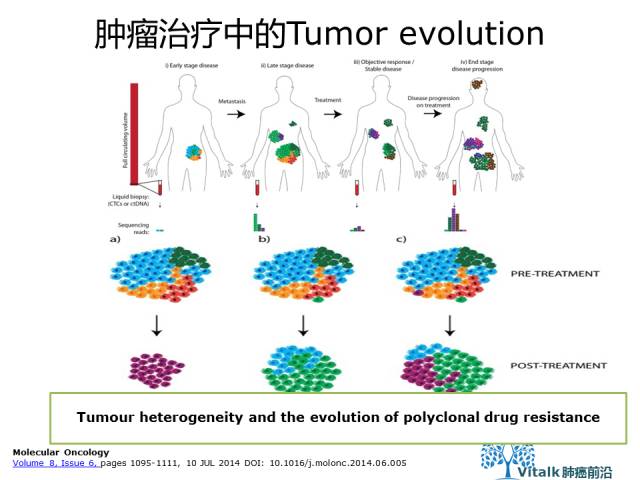
克隆进化和肿瘤耐药。 获得性耐药性可能由于以下选择性扩张的结果而出现:a)先前敏感的克隆产生耐药性(例如由于处理诱导的诱变或肿瘤内在的基因组不稳定性)b)预先存在的耐药克隆得以增殖 c)两种情况同时并存
Molecular Oncology volume 8, Issue 6, pages 1095-1111, 10 JUL 2014
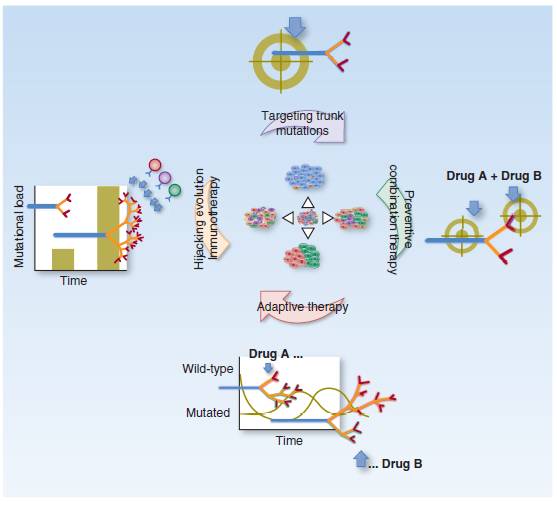
Targeting cancer evolution
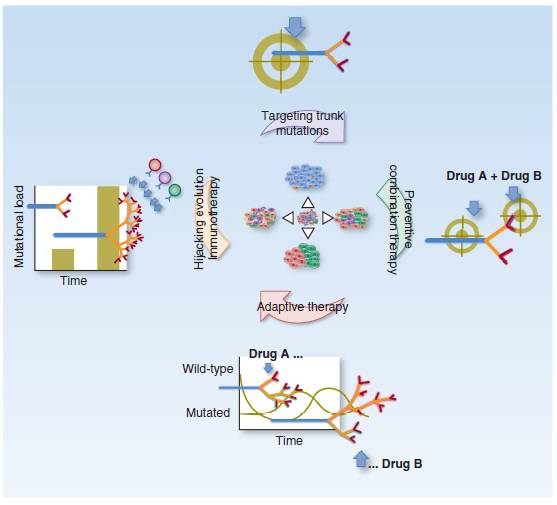
通过液体活检(和多功能活检)进行的进化的测量允许选择克隆并整合适当的策略来应对肿瘤进化:
识别可靶向的主干突变减少了缺乏可靶向目标的侧支变异克隆逃生的几率;
预防性联合治疗可能允许在出现耐药之前消灭抗性细胞;
适应性的抗肿瘤策略,如药物假期的交替管理和针对不同分支克隆的治疗,加上液体活检动态监测亚克隆生长比例,可以促进克隆竞争,并保持整体肿瘤生长的控制;
免疫疗法可以针对肿瘤进化进行治疗,免疫应答可以通过选择和输注针对trunk 克隆改变的肿瘤淋巴细胞来狙击肿瘤进化,通过增加新抗原的数量,来促发进化引起免疫反应
Nabil Amirouchene-Angelozzi, et al. Tumor evolution as a therapeutic target .cancer discovery August 2017
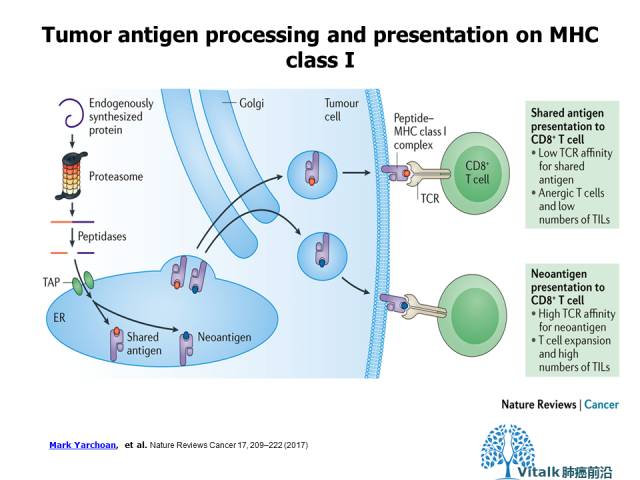
个性化疫苗或adaptive 细胞疗法。靶向多种新抗原的可能性会大大减少耐药产生的几率, 但由新抗原缺失(由于genetic or epigenetic mechanisms)引起的2例接受T细胞治疗的黑色素瘤观察到耐药现象。
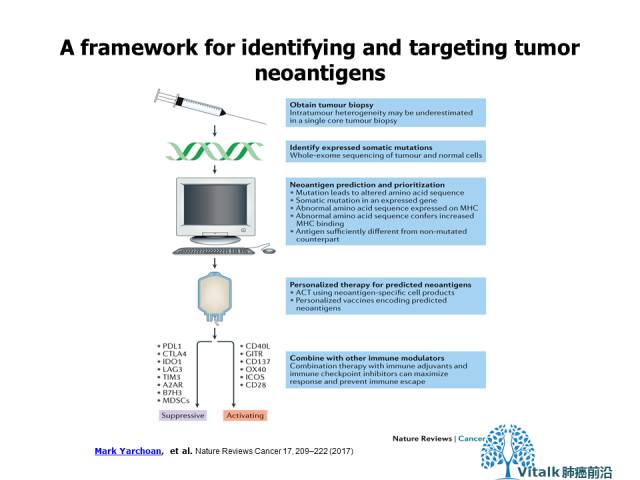
Mark Yarchoan, et al. Nature Reviews Cancer 17, 209–222 (2017)
Neoantigen clonal architecture and clinical benefit of immune checkpoint blockade
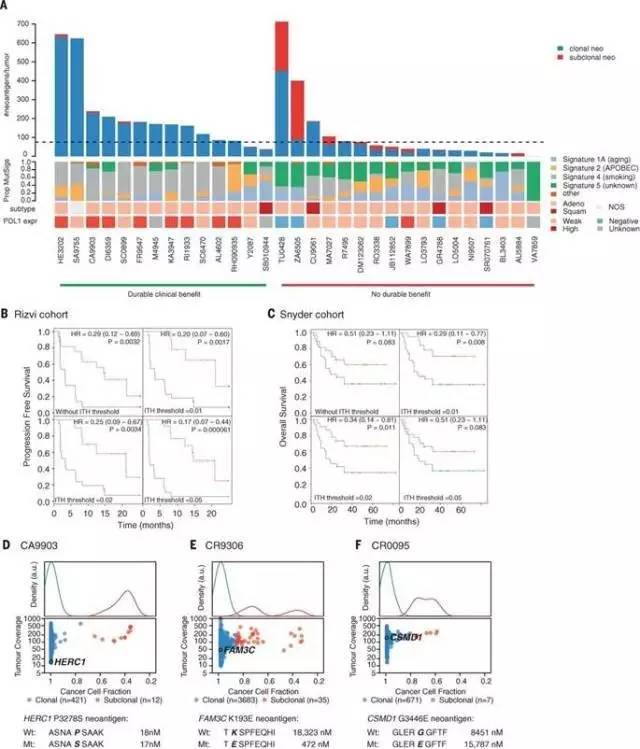
新抗原负荷与pembrolizumab的临床获益相关,高clonal neoantigen与改善的临床获益正相关。然而,与新抗原同样重要的是,PD-1阻断的临床疗效也与每个肿瘤的克隆结构相关(图4A),来源于病人标本分析发现,缺乏有效肿瘤应答的患者具有更高的neoantigen ITH(瘤内异质性),与具有显着高于具有持久临床益处的患者的肿瘤的新抗原ITH相比(P = 0.006)。几乎所有携带有低 neoantigen subclonal fraction(<5%亚克隆)和高突变负担(≥70,队列的中位克隆新抗原)的几乎每个肿瘤(13/13)都显示抗PD-1治疗具有持久的临床益处
Nicholas McGranahan et al. Science 2016;351:1463-1469
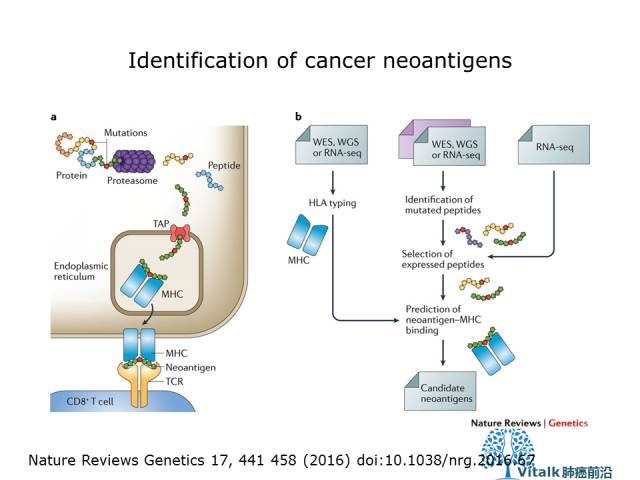
a |新抗原起源于癌细胞中表达的突变蛋白。突变的蛋白质被蛋白酶体切割成较短的肽,并通过与抗原加工(TAP)相关的转运蛋白转运到内质网,其中肽结合主要组织相容性复合物(MHC)分子。然后,肽-MHC复合物显示在抗原呈递细胞的细胞表面上,以被CD8 + T细胞的T细胞受体(TCR)识别。 b |基于测序(NGS)数据的新抗原识别需要实施若干计算任务:从全外切片测序(WES),全基因组测序(WGS)或RNA测序(RNA-seq)数据从匹配的肿瘤/正常组织样本中发现突变的短肽;通过整合肿瘤样本的RNA-seq数据来选择表达的肽;来自WES的人类白细胞抗原(HLA)分型,肿瘤样品的WGS或RNA-seq数据;并预测特异性HLA等位基因的肽-MHC结合。
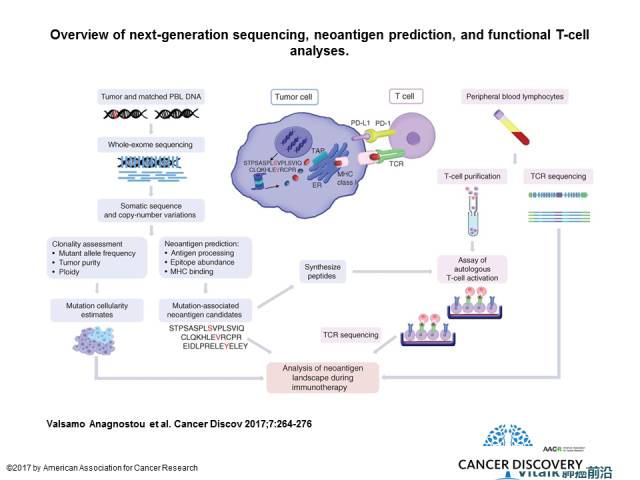
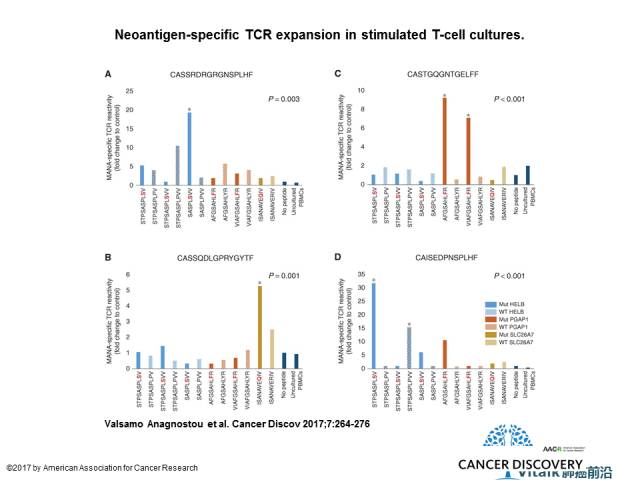
应用NGS技术进行新抗原预测和功能性T细胞分析,并在T细胞培养物中进行新抗原特异性TCR扩增。
Nature Reviews Genetics 17, 441 458 (2016)
Valsamo Anagnostou et al. Cancer Discov 2017;7:264-276
tumor evolution as a Therapeutic Target
对肿瘤细胞进行全部外显子测序,并与正常组织进行匹配,以鉴定在肿瘤细胞中表达的体细胞突变。设计用于预测主要组织相容性复合物(MHC)/人白细胞抗原(HLA)结合亲和力的软件算法然后被用于优先考虑哪种预测的新抗原对免疫靶向最有吸引力。列出了在选择新抗原靶点期间可能考虑的属性。接下来,使用新抗原疫苗或细胞疗法来靶向预测的新抗原。这些疗法应与免疫检查点抑制剂和其他基于免疫的疗法相结合,以克服抑制新生抗原特异性免疫反应的肿瘤微环境中的免疫抑制机制。











 苏公网安备32059002004080号
苏公网安备32059002004080号


