在人类与癌症博弈的漫长岁月中,自然界始终是不可或缺的“天然创新药库”。尽管近二十年来,单抗、ADC、双抗及免疫检查点抑制剂(ICI)占据了学术讨论的高地,但在肿瘤内科的处方单上,天然产物及其衍生物依然占据着不可动摇的“半壁江山”。
然而,受限于传播偏差,部分临床医生常将“植物源药物(Plant-derived drugs)”误等同于“缺乏机制的粗提取物”或“传统经验医学”的范畴。事实上,现代天然产物药理学(Natural Product Pharmacology)早已脱离了单纯的经验医学范畴。在分子克隆、化学生物学及多组学技术的赋能下,植物源药物正以精准、高效、多靶点的科学姿态,开启肿瘤治疗的全新发展阶段。
一、 奠定现代肿瘤化疗基石的植物源分子
回顾抗肿瘤药物的发展史,几乎每一次里程碑式的突破都深深植根于植物界。这些分子的发现,并非偶然的采撷,而是严谨的表型筛选与化学合成演进的结晶。
1. 生物碱的突破(1950s): 研究者从长春花(Catharanthus roseus)中分离出长春碱(Vinblastine)和长春新碱(Vincristine)。它们通过与微管蛋白(Tubulin)特异性结合,诱导微管解聚,从而将肿瘤细胞阻滞于M期。这一发现诞生了首批进入现代临床诊疗路径的高效、广谱植物源化疗药物,更深刻揭示了细胞有丝分裂的生物学机制。
2. 紫杉烷类的传奇(1960s~1970s): 美国国家癌症研究所(NCI)从太平洋紫杉(Taxus brevifolia)树皮中发现了紫杉醇(Paclitaxel),其通过“稳定微管”来阻止细胞分裂。这种独特的微管稳定机制,使其成为乳腺癌、卵巢癌等实体瘤化疗的基石药物。
3. 喜树碱及其衍生物(1970s):源自中国特有植物喜树(Camptotheca acuminata)中提取的喜树碱(Camptothecin),是人类发现的首个针对DNA拓扑异构酶I(Topoisomerase I)的抑制剂。其半合成衍生物伊立替康(Irinotecan)已成为转移性结直肠癌(mCRC)标准治疗方案(如FOLFIRI)的基石,通过诱导DNA单链断裂,特异性阻断肿瘤细胞复制,为晚期实体瘤患者带来了显著的生存获益。
根据Newman和Cragg在Journal of Natural Products上发布的统计数据,1981年至2019年间批准的所有抗肿瘤小分子药物中,仅有约25%是纯合成来源,其余75%均源于天然产物及其结构启发。
二、科学本质:从“经验方剂”到
“现代分子单体”的进阶
临床医生对植物来源药物的疑虑,多源于对“中草药”与“天然产物药物”定义的混淆。然而,现代植物源药物已完成了从模糊到精确的科学进化。
结构明确化与纯度标准化
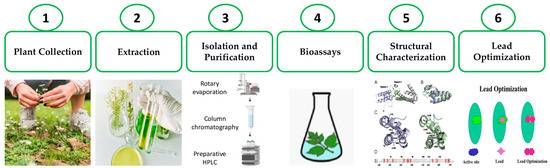
依托高效液相色谱(HPLC)、超临界流体萃取(SFE)及核磁共振(NMR)等精密工艺,现代制药已实现活性成分的单体级提取。无论是青蒿素(Artemisinin)、水飞蓟素(Silymarin),还是近年来备受关注的葫芦素(Cucurbitacins)、姜黄素(Curcumin)等,在进入临床应用前均需经过严格的成分鉴定与指纹图谱控制。其化学结构式明确,药理活性清晰,完全符合ICH(国际人用药品注册技术协调会)的质量标准。
药代动力学(PK)的精确测定
不同于成分复杂的原始煎剂,现代植物源药物单体具有明确的吸收、分布、代谢、排泄(ADME)特征。通过同位素标记与血药浓度监测,研究者可以精确绘制体内代谢曲线,指导临床给药剂量与频次,使其具备了进入现代循证医学临床路径(Clinical Pathways)的先决条件。例如,水飞蓟素单体在保肝治疗中的应用,不仅有明确的指纹图谱控制,更有大规模随机对照试验(RCT)研究证实其对化疗性肝损伤的防护作用。
分子机制的深度解析
现代植物药不再停留在宏观的“性味”描述,而是深入到信号转导通路。随着系统生物学和网络药理学的发展,科学界发现植物源药物在抗肿瘤方面具备“多靶点、多途径”的协同优势。例如,许多植物黄酮类、三萜化合物被证实能通过调节STAT3、NF-κB或PI3K/Akt等经典肿瘤信号通路发挥作用。
生产标准化与剂量一致性
现代植物提取药物(如水飞蓟素、葫芦素片等)通过严格的GMP生产标准,确保了活性成分的定量化,满足临床路径标准化应用要求。
循证医学证据的构建
现代植物药的临床准入标准与合成药物并无二致,其必须经过严谨的RCT,通过多中心、大样本的临床数据验证其在安全性、有效性及药效学(PK/PD)方面的优势。美国食品药品监督管理局(FDA)和欧洲药品管理局(EMA)对植物药(Botanical Drugs)的审批流程,均要求其在临床前研究中展示出清晰的毒理学概况和明确的剂量效应关系。这种基于证据的医学逻辑,将植物药从民俗疗法升级为循证抗肿瘤治疗的重要组成部分。
三、 科技赋能:天然产物的“老药新用”与精准筛选
随着高通量筛选(HTS)、合成生物学、多组学技术及计算机辅助药物设计(CADD)的应用,研究者们正在重新评估那些在民间应用已久、但缺乏深层机制研究的植物分子。
1. 攻克“难成药”靶点:许多植物来源的次生代谢产物具有人工合成难以模拟的复杂化学结构,这赋予了它们与复杂肿瘤靶点(如难成药靶点RAS、MYC)结合的可能性。
2. 微环境调节视角:证据表明,植物来源药物(如某些萜类化合物)在抗炎、抗纤维化及改善肿瘤微环境方面具有独特优势,这为晚期肝癌、慢性肝炎等复杂疾病的辅助治疗提供了新思路。
3. 网络药理学地图:这一学科将植物药的评价从“盲盒”转变为“精准地图”,阐明了其“多组分-多通路”的系统作用机制,使治疗方案更具预见性。
四、临床价值:减毒增效与全程管理
在肿瘤的全程管理中,植物来源药物展现出了不可替代的临床价值。
· 化疗增敏:研究证实,某些植物单体(如萜类、木脂素类)能逆转肿瘤细胞的耐药表型(如抑制P-gp外排泵),显著提高经典化疗药物的杀伤效率。
· 脏器保护与耐受提升:肝毒性、肾毒性是抗肿瘤治疗中断的主要原因。来源于水飞蓟、甜瓜蒂、五味子等植物的标准化活性成分,在临床上展现出确切的保肝抗炎作用,为患者耐受高强度化疗提供了重要保障。
· 生存质量(QoL)的优化:天然产物往往具有较低的系统性毒性,在控制疾病进展的同时,能更好地维持患者的体能状态。
五、结语:拥抱自然演化的科学智慧
随着医学向表观遗传学以及肿瘤免疫代谢等方向延伸,植物来源的高纯度单体化合物正展现出抗炎与抗肿瘤双重活性。这并非缺乏科学依据的“经验之谈”,而是经过严谨分离鉴定、具备明确分子靶点、并经受大规模循证医学检验的现代科学产物。
当我们拆解植物药的研发历程、质量标准及分子机制时可以发现,植物来源药物不仅是科学的,而且往往代表了药物化学中最具前瞻性的部分。作为当代临床医生,理解并接纳植物来源药物的科学内涵,不仅是对药学发展史的尊重,更是拓宽临床思路、为患者寻求更优生存获益的必然选择。
[1] Newman DJ, Cragg GM. Natural Products as Sources of New Drugs over the Nearly Four Decades from 01/1981 to 09/2019. J Nat Prod. 2020;83(3):770-803.
[2] 北京协和医院.《肿瘤内科诊疗常规》. 人民卫生出版社.
[3] 孙燕, 石远凯.《临床肿瘤内科手册》(第6版). 人民卫生出版社.
[4] ACS. Discovery of Camptothecin and Taxol - National Historic Chemical Landmark. https://www.acs.org/education/whatischemistry/landmarks/camptothecintaxol.html.
[5] Chaachouay N, Zidane L. Plant-Derived Natural Products: A Source for Drug Discovery and Development. Drugs Drug Candidates. 2024;3(1):184-207.
[6] Cragg GM, Pezzuto JM. Natural Products as a Vital Source for the Discovery of Cancer Chemotherapeutic and Chemopreventive Agents. Med Princ Pract. 2016;25(Suppl 2):41-59.
[7] Muthuraj R, Chandrasekaran J. Nature meets machine: the AI renaissance in natural product drug discovery. Nat Prod Bioprospect. 2026;16(1):37.
[8] Frontiers. Advanced Technologies for the Quality Control and Standardization of Plant Based Medicines. Frontiers Research Topic.
[9] FDA. What is a Botanical Drug? 2025. https://www.fda.gov/about-fda/cder-offices-and-divisions/what-botanical-drug.
[10] FDA. Botanical Drug Development: Guidance for Industry. 2016. https://www.fda.gov/regulatory-information/search-fda-guidance-documents/botanical-drug-development-guidance-industry.
[11] Sun Y, Qian J. Botanical drug clinical trial: Common issues and future options. Acta Pharm Sin B. 2021;11(1):300-303.
[12] Aggarwal BB, et al. Targeting inflammatory pathways for prevention and therapy of cancer: short-term friend, long-term foe. Clin Cancer Res. 2006;12(14):4283-4286.
[13] Dehelean CA, Marcovici I, et al. Plant-Derived Anticancer Compounds as New Perspectives in Drug Discovery and Alternative Therapy. Molecules. 2021;26(4):1109.
排版编辑:肿瘤资讯-ZJN











 苏公网安备32059002004080号
苏公网安备32059002004080号


