日本国立癌症研究中心东医院消化道肿瘤科Kohei Shitara教授以“Beyond PD-1/PD-L1: Novel immunotherapy approaches”为题,系统阐述了消化道肿瘤领域免疫治疗的最新进展与未来方向。在PD-1/PD-L1抑制剂已成为多种消化道肿瘤标准治疗的当下,如何克服原发性和获得性耐药仍是临床亟待解决的核心问题。Shitara教授从增强效应细胞功能、重塑肿瘤微环境、扩展抗肿瘤免疫、重定向细胞毒性及过继性细胞治疗五大维度,全面梳理了新兴免疫治疗策略的机制原理与临床转化进展,为消化道肿瘤免疫治疗的精准化和个体化发展提供了重要参考。
扩展抗肿瘤免疫:疫苗、先天免疫激动剂与微生物组调控
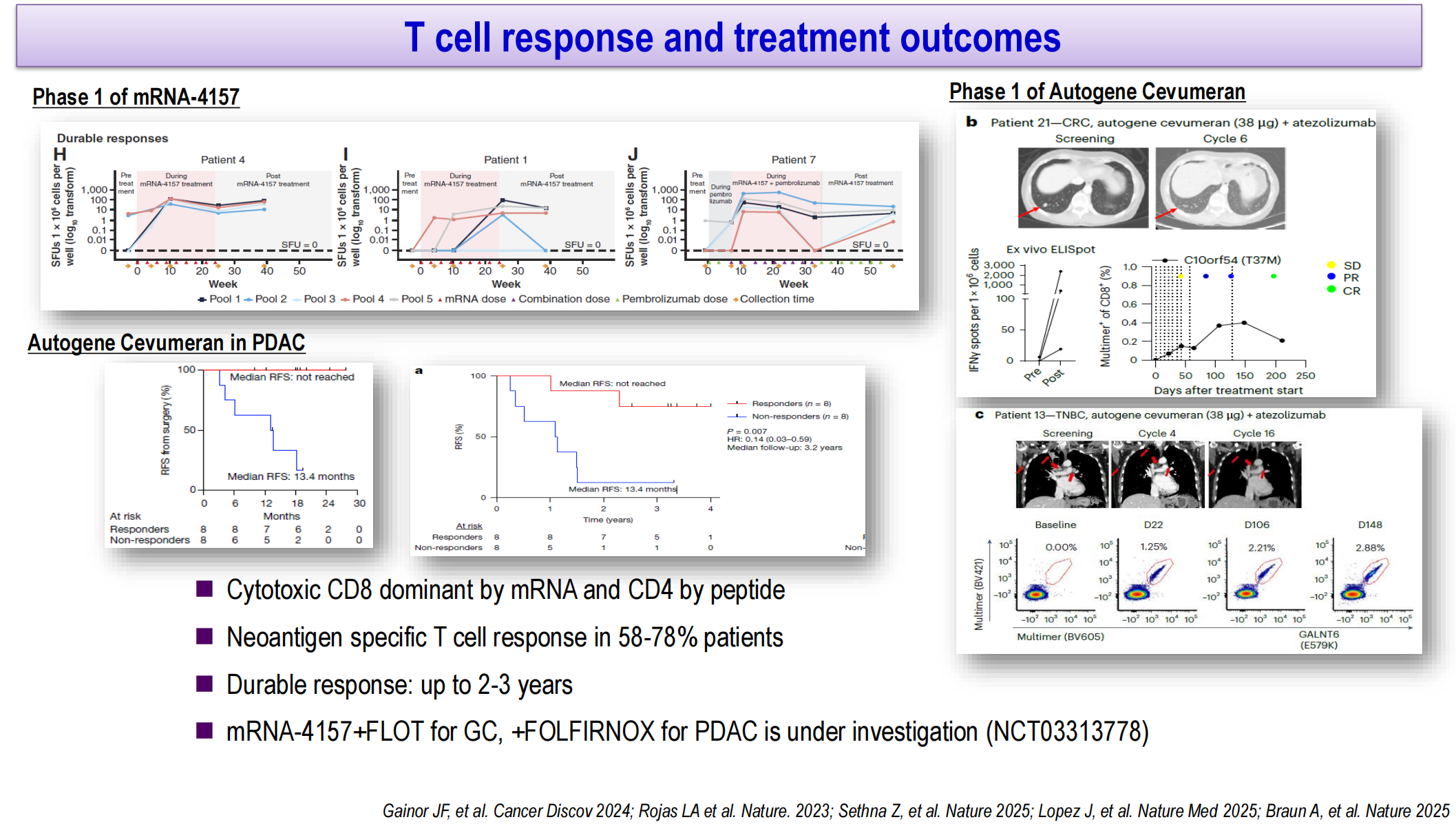
个体化新抗原疫苗是扩展抗肿瘤免疫的前沿方向。mRNA-4157(Moderna)和Autogene Cevumeran(BioNTech)均为基于全外显子组和RNA测序、通过AI模型预测和筛选新抗原的个体化mRNA疫苗,前者经脂质纳米颗粒(LNP)包裹后肌肉注射,后者经RNA-LPX包裹后静脉注射,制备周期分别为4~6周和4周。个体化肽疫苗则通过IFN-γ ELISpot验证筛选排名靠前的15条肽段,经皮下注射给药,制备周期为8~12周。
mRNA疫苗主要诱导细胞毒性CD8+ T细胞反应,而肽疫苗主要诱导CD4+ T细胞反应。早期临床研究显示,58%~78%的患者可检测到新抗原特异性T细胞反应,且反应可持续2~3年。Autogene Cevumeran联合方案在胰腺癌术后辅助治疗中,免疫应答者与无应答者的中位无复发生存期(mRFS)存在显著差异(HR 0.14)。mRNA-4157联合FLOT方案用于胃癌、联合FOLFIRINOX方案用于胰腺癌的研究正在进行中。
一项回顾性研究发现,新冠mRNA疫苗接种与抗PD-1治疗获益改善相关。在非小细胞肺癌和黑色素瘤患者中,接种新冠mRNA疫苗者较未接种者的OS显著延长,而这一趋势在单纯化疗患者或接种流感/肺炎疫苗者中未观察到。机制研究显示,mRNA疫苗可诱导I型干扰素激增、激活APC和扩增肿瘤特异性CD8+ T细胞,并上调肿瘤PD-L1表达。
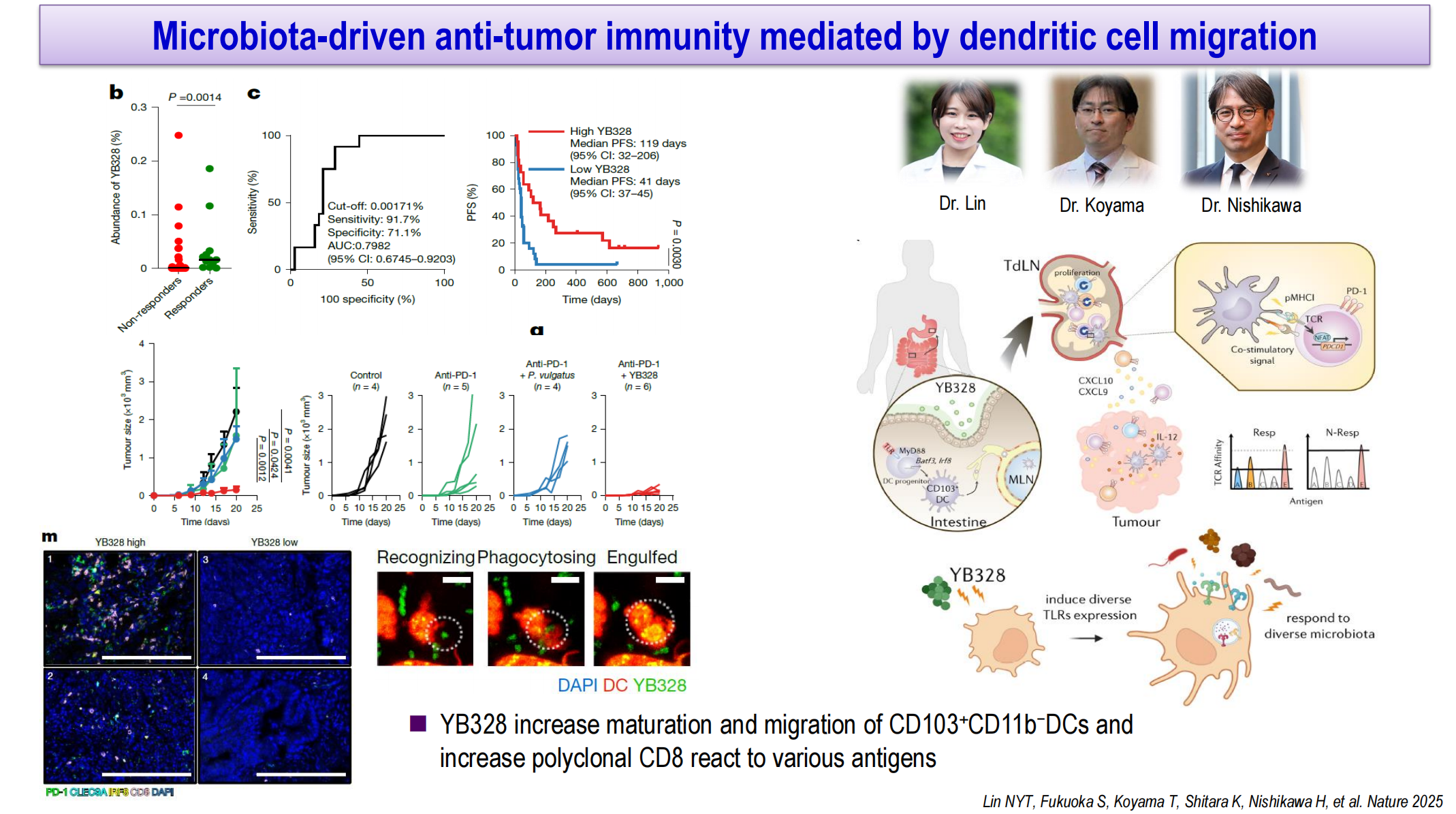
微生物组调控是扩展抗肿瘤免疫的另一个新兴领域。研究发现,肠道菌群中YB328的丰度与抗PD-1治疗反应相关(应答者显著高于无应答者)。YB328高丰度患者的中位PFS为119天,而YB328低丰度患者仅为41天。机制研究表明,YB328可促进CD103+ CD11b-树突状细胞的成熟和迁移,增加对多种抗原产生反应的多克隆CD8+ T细胞。
重定向细胞毒性:T细胞衔接器(BiTE)与双特异性抗体
双特异性T细胞衔接器(BiTE)可同时结合肿瘤相关抗原和T细胞表面的CD3,将T细胞重定向至肿瘤细胞发挥杀伤作用,无需预先的抗原致敏和MHC限制。与CAR-T细胞治疗相比,BiTE具有无需淋巴细胞清除、无需住院(仅早期周期需要)、可重复给药和现成可用等优势。目前FDA已批准8种T细胞衔接器用于血液肿瘤和实体瘤治疗,包括获批用于实体瘤的tebentafusp(用于葡萄膜黑色素瘤)和tarlatamab(靶向DLL3,用于小细胞肺癌)。Tebentafusp的研究显示OS和PFS显著改善,CRS主要表现为皮疹(83%)、发热(76%)和瘙痒(69%)。Tarlatamab的II期研究ORR达40%,CRS发生率为51%,已获FDA加速批准,III期研究证实OS改善。
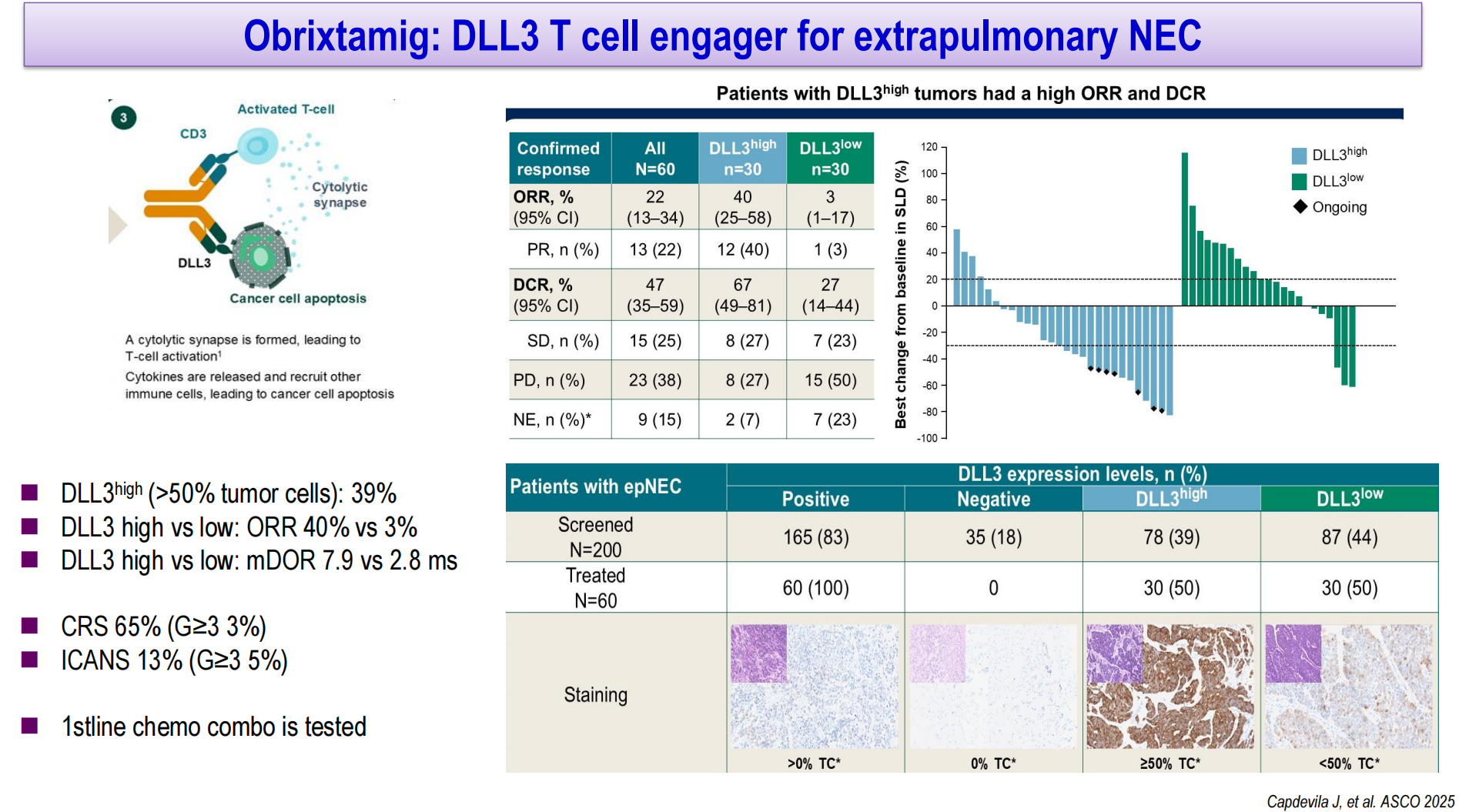
Obrixtamig是一种靶向DLL3的T细胞衔接器,用于肺外神经内分泌癌。研究显示,DLL3高表达(>50%肿瘤细胞)患者占39%,DLL3高表达 vs 低表达患者的ORR分别为40%和3%,中位缓解持续时间(mDoR)分别为7.9个月和2.8个月。CRS发生率为65%(≥3级3%),免疫效应细胞相关神经毒性综合征(ICANS)发生率为13%(≥3级5%)。其联合化疗的一线治疗研究正在进行中。
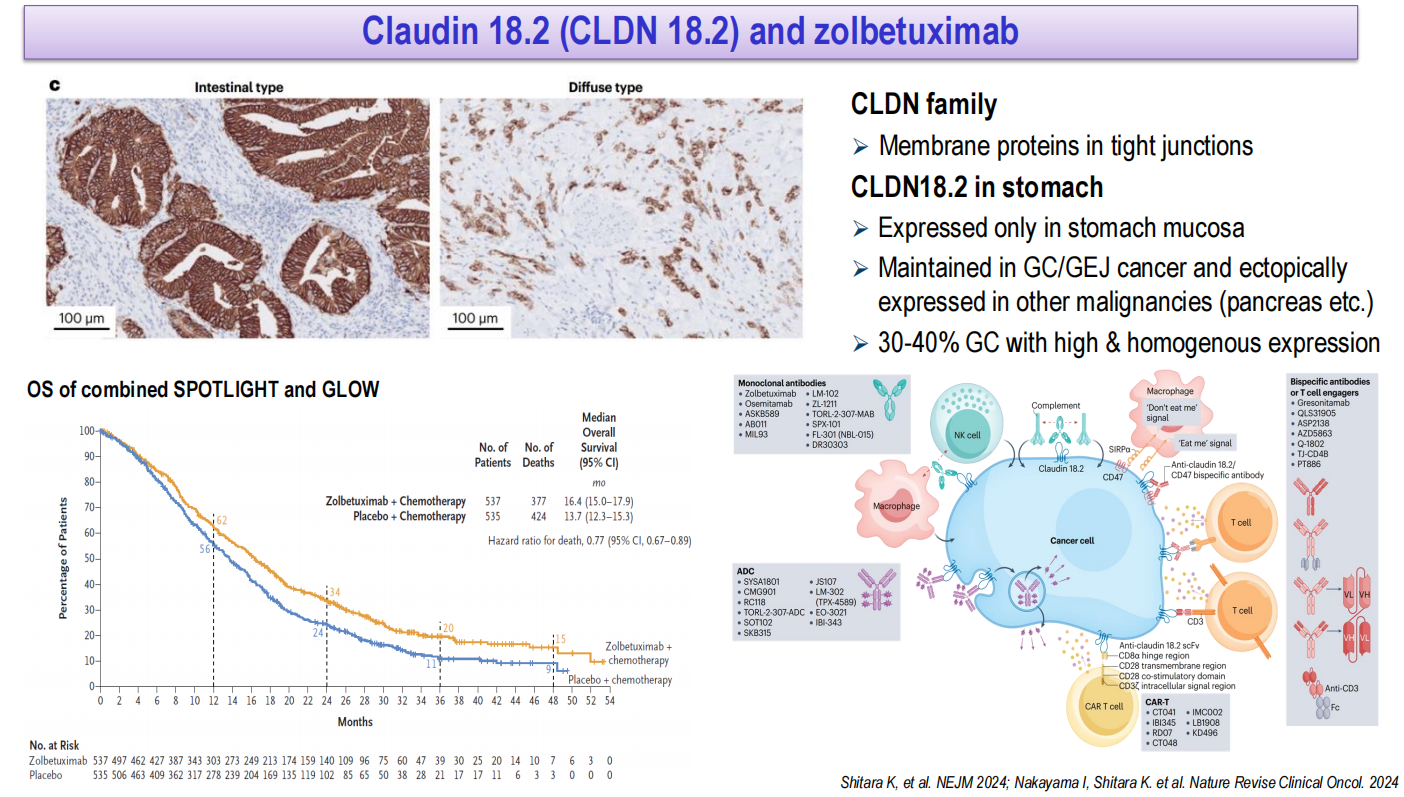
Claudin 18.2(CLDN18.2)是一种紧密连接蛋白,在胃癌和其他恶性肿瘤(如胰腺癌)中表达。30%~40%的胃癌患者呈CLDN18.2高表达。佐妥昔单抗是一种靶向CLDN18.2的单克隆抗体,SPOTLIGHT和GLOW两项III期研究的汇总分析显示,佐妥昔单抗联合化疗较化疗显著改善OS(16.4个月 vs 13.7个月,HR 0.77),降低死亡风险23%。
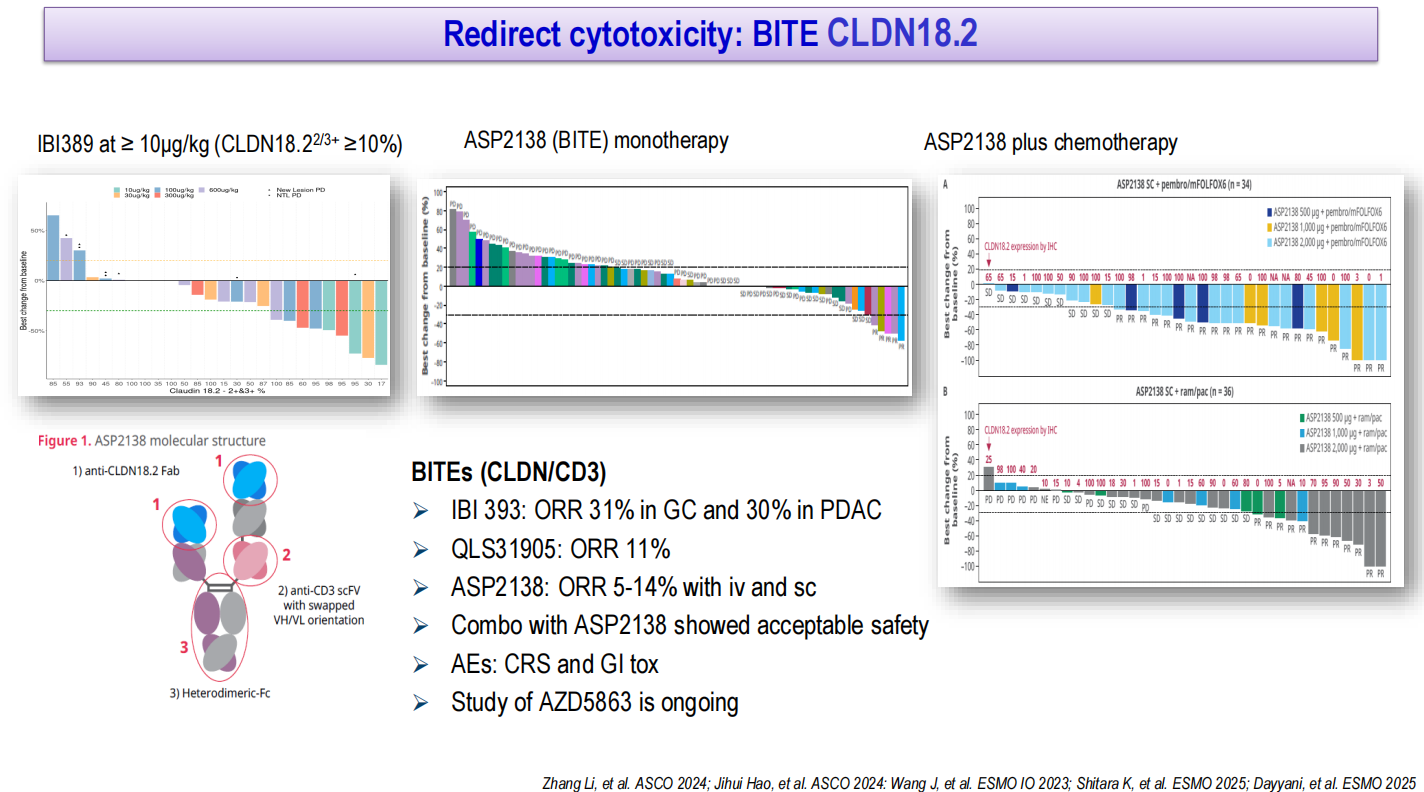
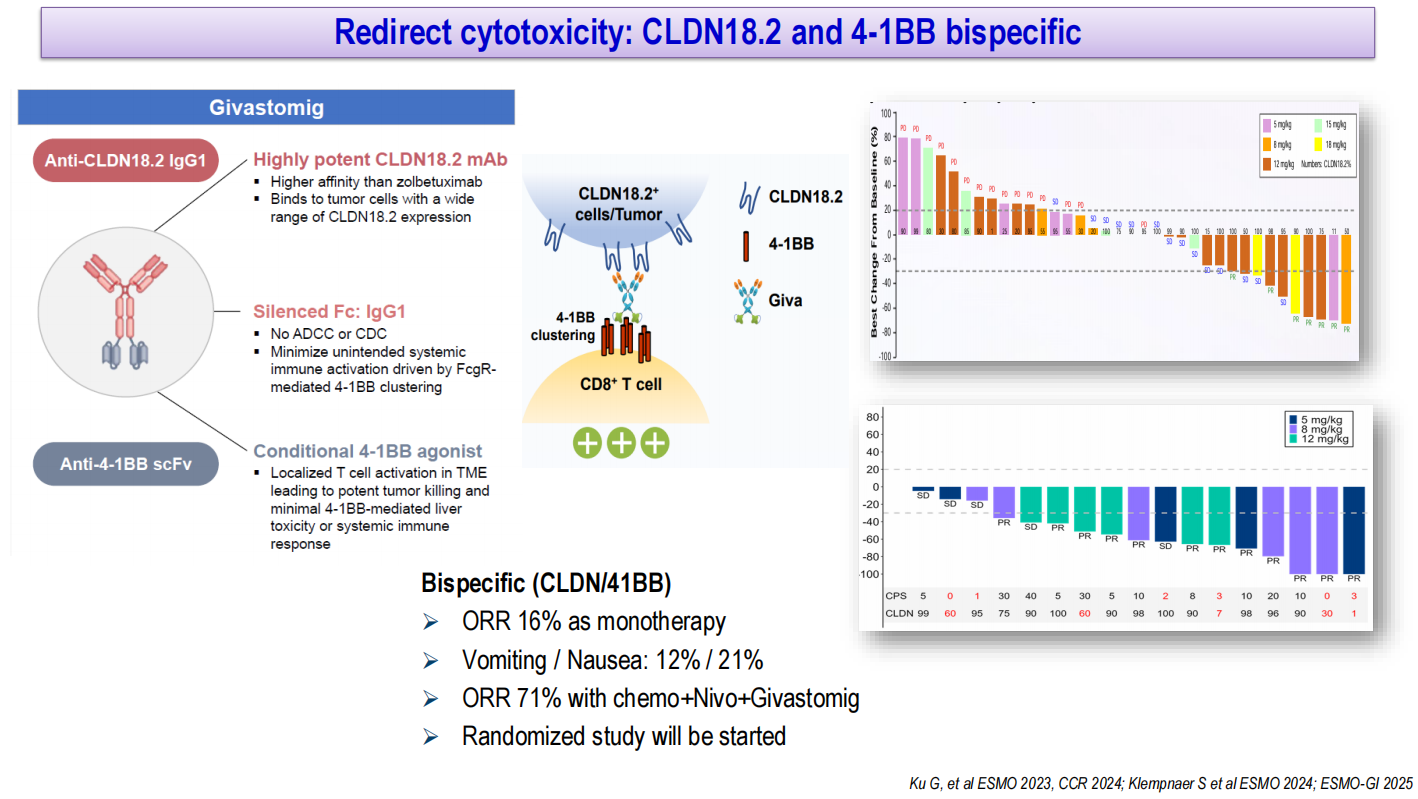
基于CLDN18.2靶点的T细胞衔接器和双特异性抗体正在积极研发中。IBI389是一种CLDN18.2/CD3 T细胞衔接器,在CLDN18.2阳性(2/3+≥10%)胃癌患者中的ORR达31%,胰腺癌中为30%。ASP2138是另一种CLDN18.2/CD3 T细胞衔接器,单药ORR为5%~14%,联合化疗显示可接受的安全性。主要不良事件为CRS和胃肠道毒性。Givastomig是一种CLDN18.2/4-1BB双特异性抗体,可在肿瘤微环境中局部激活4-1BB,而不引起全身性免疫激活。I期研究显示单药ORR为16%,联合化疗和纳武利尤单抗的ORR高达71%,随机对照研究即将启动。
过继性细胞治疗:CAR-T和TCR-T在消化道肿瘤中的探索
过继性细胞治疗包括CAR-T、TCR-T和TIL治疗三种主要模式。CAR-T细胞识别细胞表面抗原,不受MHC限制;TCR-T细胞识别MHC呈递的细胞内肽段,具有HLA限制性;TIL治疗则利用从肿瘤组织中分离扩增的淋巴细胞,具有天然的抗原识别能力和较高的肿瘤浸润能力。
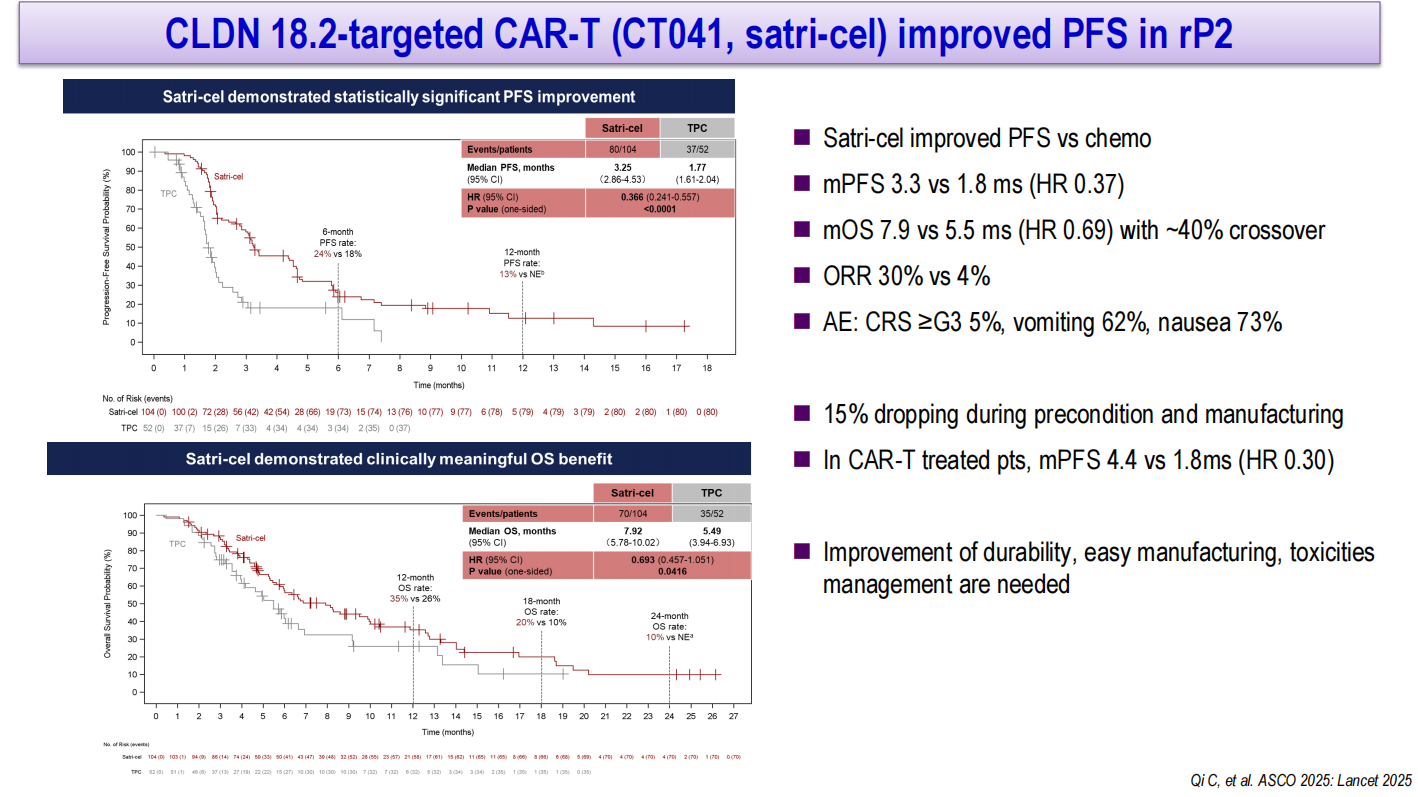
CT041(satri-cel)是一种靶向CLDN18.2的CAR-T细胞疗法。在多项早期研究中,CT041在胃癌和其他消化道肿瘤中显示出鼓舞人心的疗效(ORR 39%~43%),优于既往CAR-T疗法在消化道肿瘤中的表现。随机II期研究评估satri-cel对比医生选择的化疗方案用于经治CLDN18.2阳性胃癌,结果显示satri-cel显著改善PFS(3.25个月 vs 1.77个月,HR 0.37)和OS(7.92个月 vs 5.49个月,HR 0.69,约40%患者交叉),ORR分别为30%和4%。主要不良事件包括恶心(73%)、呕吐(62%)和CRS(≥3级5%)。需要指出的是,CAR-T治疗的复杂流程仍是临床应用的挑战。
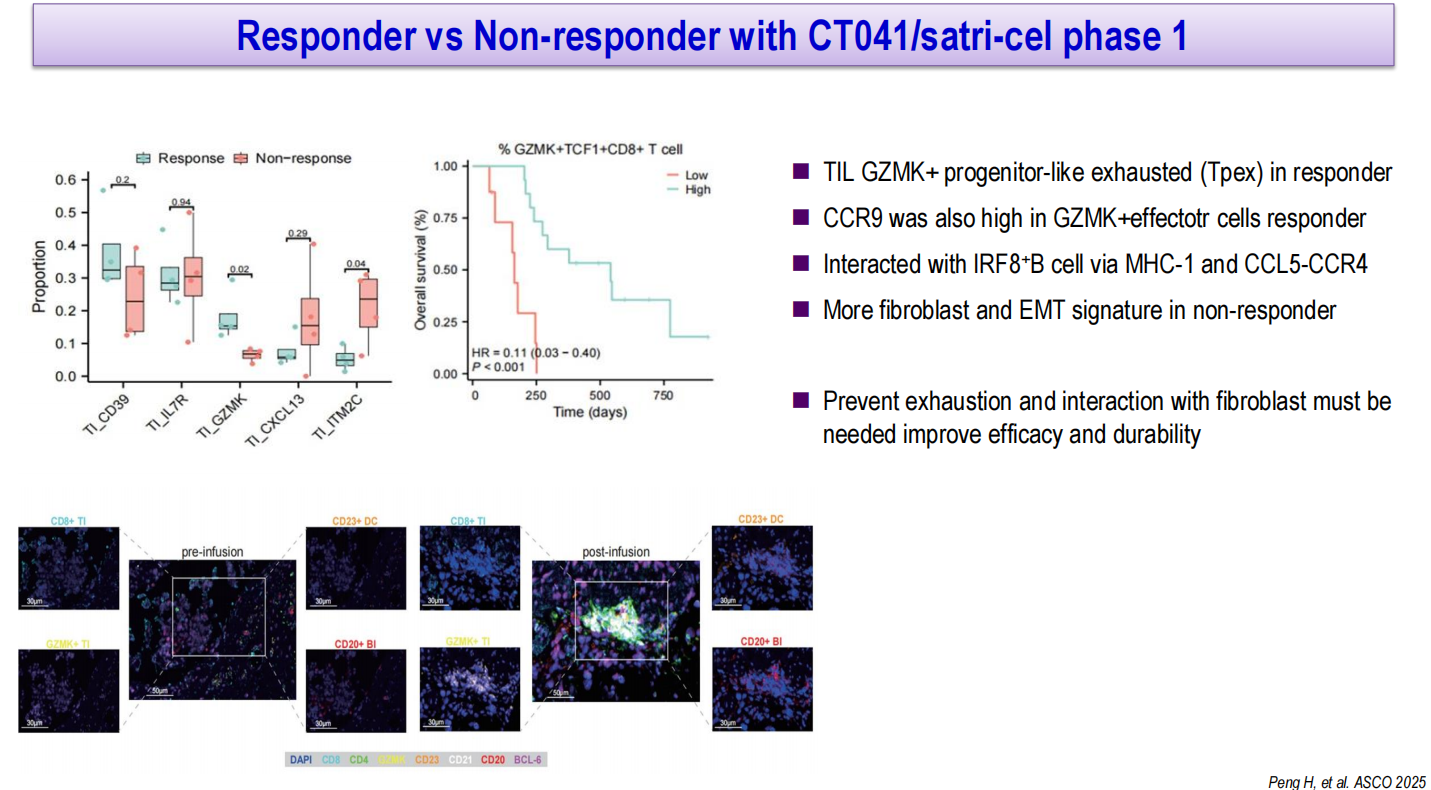
针对CT041(satri-cel)CAR-T治疗的生物标志物探索显示,TIL中GZMK+前体耗竭型(Tpex)CD8+ T细胞比例较高的患者对CT041治疗反应较好,CCR9在GZMK+效应细胞中的高表达也与疗效相关,而无应答者中纤维母细胞和上皮间质转化基因特征更为富集。这提示预防T细胞耗竭和阻断与纤维母细胞的相互作用可能是提高CAR-T疗效和持久性的关键方向。
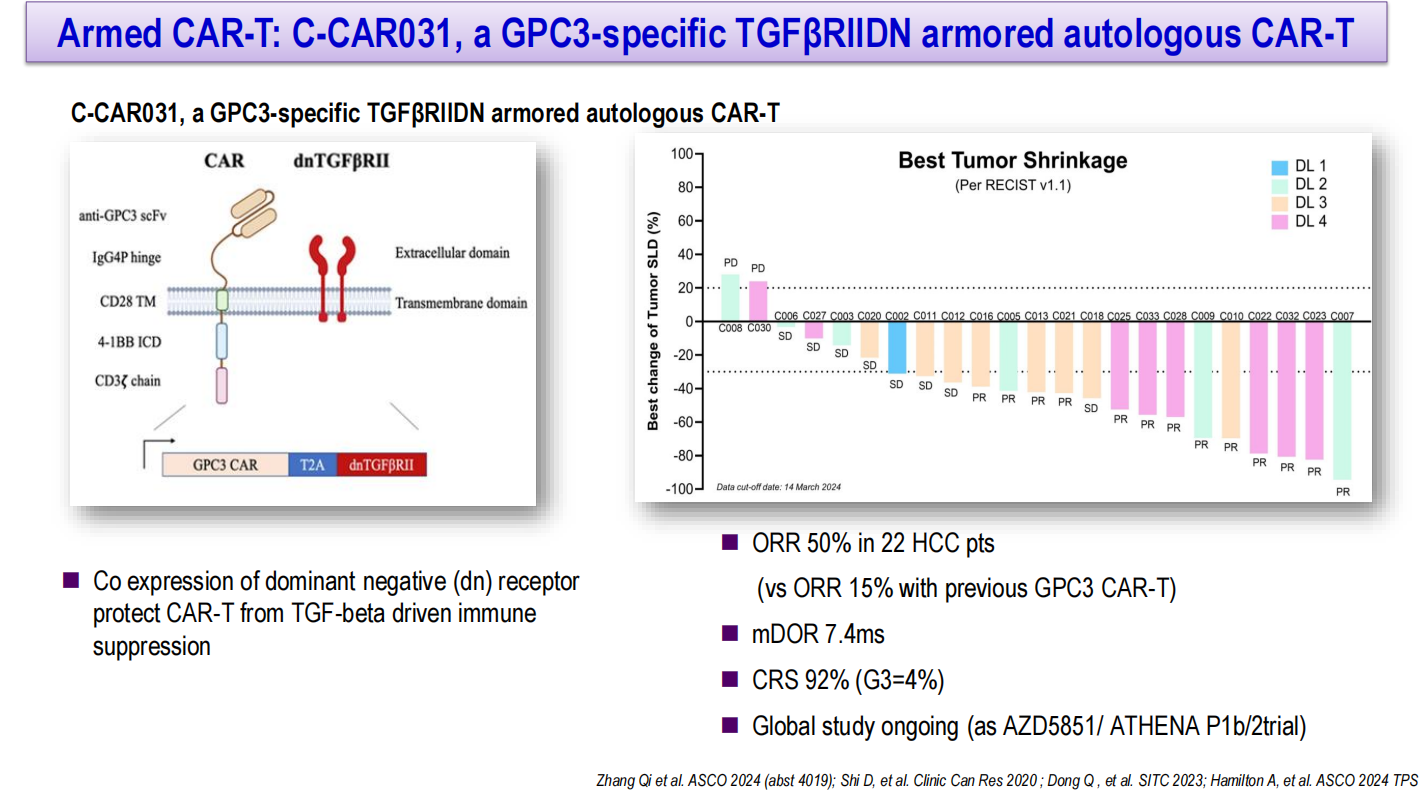
为克服实体瘤CAR-T治疗的局限性,多种改进策略正在探索中,包括新靶点发现、双靶点CAR设计、ScFv亲和力调节、SynNotch受体开关构建、阻断肿瘤微环境抑制信号(如TGF-β)、细胞因子“武装”CAR-T、免疫检查点阻断以预防耗竭、以及联合RNA疫苗等。C-CAR031是一种共表达TGF-βRIIDN的GPC3靶向CAR-T疗法,可保护CAR-T细胞免受TGF-β介导的免疫抑制。研究显示,该疗法在肝细胞癌中的ORR达50%(既往GPC3 CAR-T为15%),中位缓解持续时间为7.4个月,CRS发生率为92%(3级4%),全球I/II期ATHENA研究正在进行中。TAK-102(Prime CAR-T)是一种共表达IL-7和CCL19的GPC3靶向CAR-T疗法,早期研究显示可诱导多种细胞因子升高和肿瘤微环境改善。IL-15“武装”GPC3 CAR-T细胞则表现出更高的细胞毒性功能相关基因表达(如GZMA、GZMM、PRF1),ORR达33%,优于传统CAR-T。
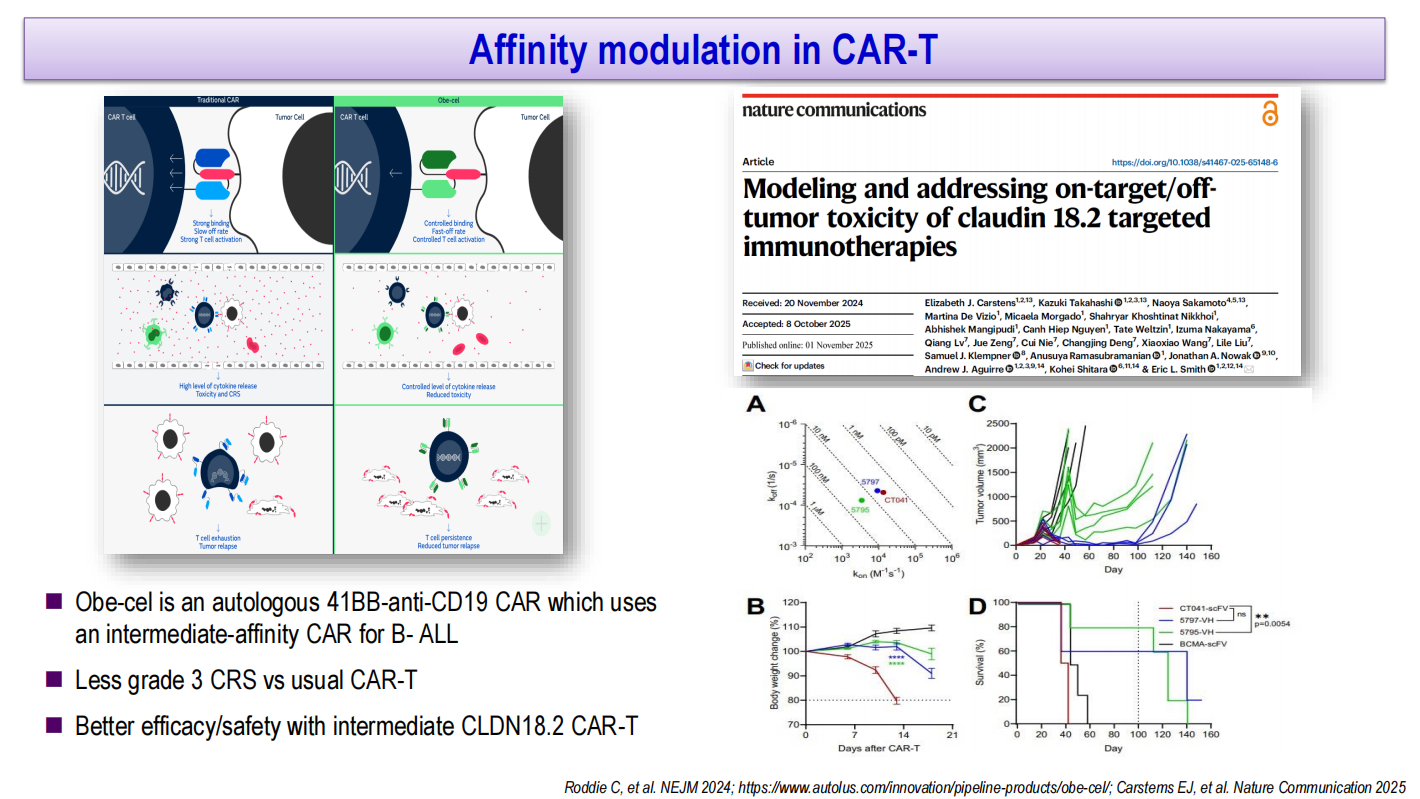
针对CAR-T治疗的毒性管理,除常规的糖皮质激素、IL-6/IL-1R/IL-10BP抑制剂、JAK-1抑制剂、Src抑制剂、PI3K抑制剂等措施外,还可采用局部注射(以克服递送和归巢问题),以及设计“关闭开关”(如单抗介导ADCC清除、抗病毒治疗、mRNA转染策略等)以在毒性发生时清除CAR-T细胞。亲和力调节也是降低毒性的策略之一,obe-cel(一种中等亲和力抗CD19 CAR-T疗法)相比传统CAR-T疗法显示更低的3级CRS发生率;基于计算机模型的研究提示中等亲和力CLDN18.2 CAR-T可能具有更优的疗效/安全性比。
体内CAR-T细胞生成是简化CAR-T治疗流程的前沿方向,通过工程化纳米载体或病毒载体直接注入CAR基因,在体内原位生成CAR-T细胞,可显著降低成本、提高可及性,但高效递送、表达控制和安全性仍是挑战。临床试验已在进行中,据报道已有1例弥漫大B细胞淋巴瘤患者对体内CAR-T治疗产生应答,4例骨髓瘤患者接受了体内CAR-T治疗。
TCR-T细胞治疗可识别细胞内抗原经MHC呈递的肽段,具有更高的亲和力,但受HLA限制。Afami-cel是一种靶向HLA-A*02限制性MAGE-A4的TCR-T疗法,用于滑膜肉瘤或黏液样圆细胞脂肪肉瘤,ORR为37%,mPFS为3.7个月,主要不良事件为骨髓抑制和CRS,已于2024年8月获FDA加速批准。
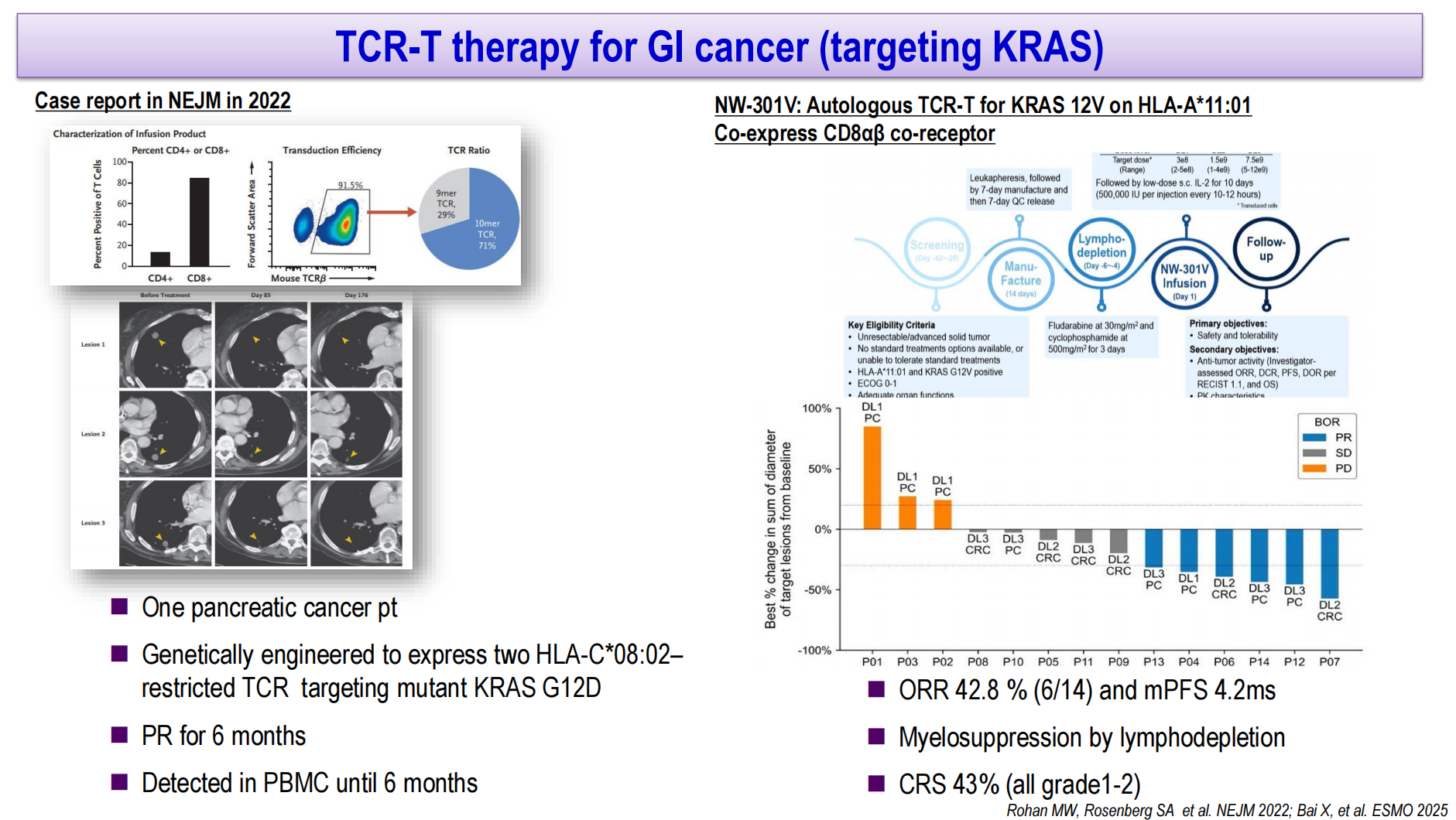
在消化道肿瘤领域,靶向KRAS突变的TCR-T治疗取得了令人瞩目的进展。2022年发表的病例报告显示,1例胰腺癌患者接受靶向HLA-C08:02限制性KRAS G12D的TCR-T治疗后获得持续6个月的部分缓解,外周血中可检测到TCR-T细胞持续6个月。NW-301V是一种靶向HLA-A11:01限制性KRAS G12V并共表达CD8αβ共受体的自体TCR-T疗法,I期研究显示ORR达42.8%(6/14),mPFS为4.2个月,主要不良事件为淋巴细胞清除相关的骨髓抑制,CRS发生率为43%(均为1-2级)。此外,针对个体化新抗原的TCR-T治疗也在探索中,II期研究中期分析显示,7例结直肠癌患者中大多数实现了肿瘤缩小。
面向未来:生物标志物驱动的个体化治疗策略
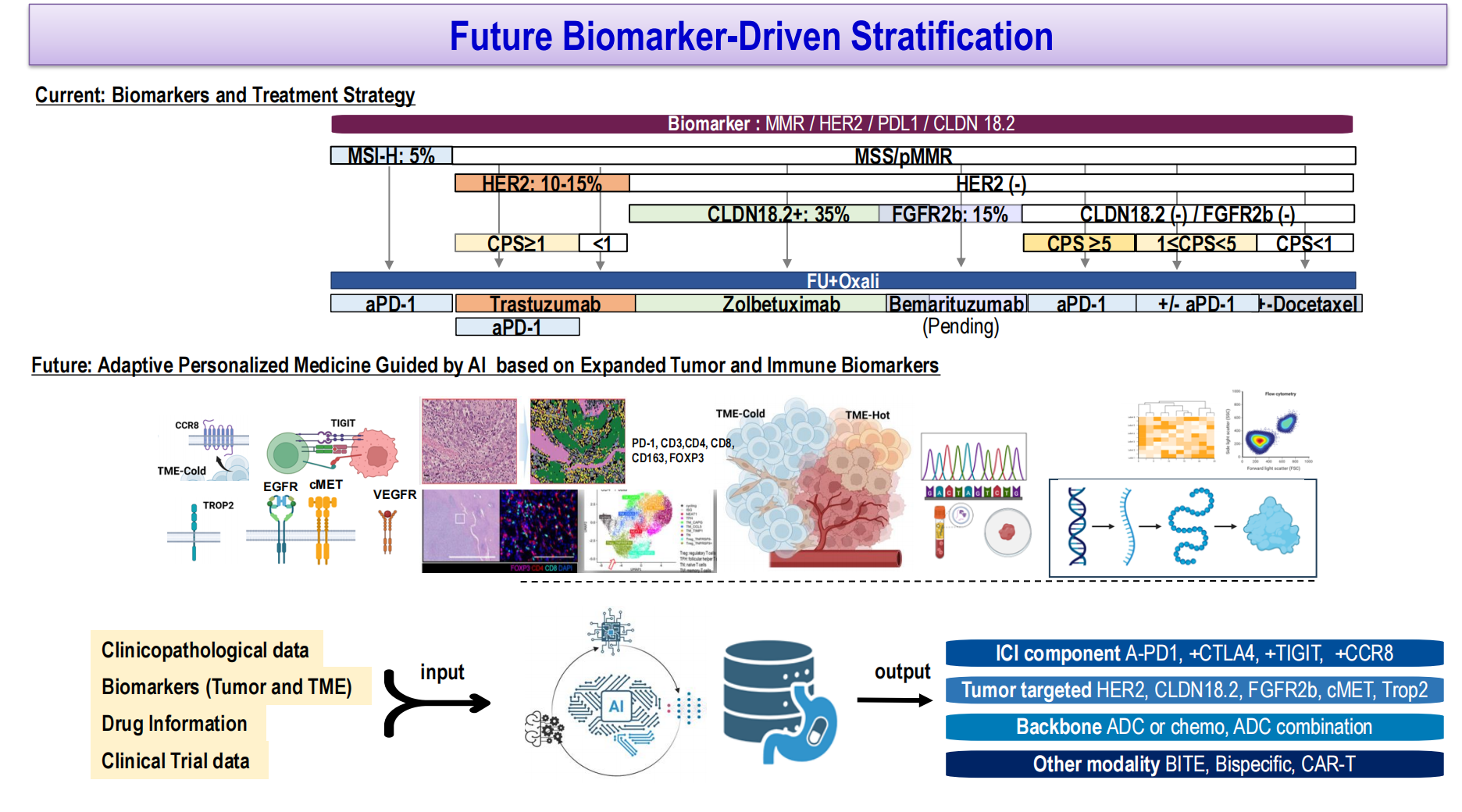
当前消化道肿瘤的治疗决策主要基于MMR状态、HER2、PD-L1 CPS和CLDN18.2表达等少数生物标志物,治疗选择相对有限。未来的方向是整合更广泛的肿瘤和肿瘤微环境生物标志物,包括多种靶向受体(如EGFR、cMET、TROP2、VEGFR等)、免疫细胞表型(如PD-1、CD3、CD4、CD8、CD163、FOXP3等)、空间转录组学、单细胞测序和流式细胞术数据等,结合临床病理学数据、药物信息和临床试验数据,通过人工智能模型输出个体化治疗推荐,包括免疫检查点抑制剂(抗PD-1联合抗CTLA-4、抗TIGIT或抗CCR8等)、靶向药物(HER2、CLDN18.2、FGFR2b、cMET、TROP2等)、治疗骨架(ADC或化疗、ADC联合等)以及其他治疗模式(BiTE、双特异性抗体、CAR-T等)。
超越PD-1/PD-L1(上):消化道肿瘤免疫治疗的新型策略与前沿进展
排版编辑:肿瘤资讯-Marie












 苏公网安备32059002004080号
苏公网安备32059002004080号


