全球每年新发癌症患者约2,000万,其中近半数肿瘤患者携带TP53基因突变。作为人类癌症中最常见的基因变异类型,TP53突变长期被认为是导致肿瘤耐药、复发、高侵袭性及患者预后不良的核心驱动因素。然而,受p53蛋白特殊结构特征的限制,该靶点在过去数十年间始终被肿瘤学界归为“不可成药”靶点。
近日,《新英格兰医学杂志》(NEJM)刊发了PYNNACLE I期临床研究成果。该研究评估了首款口服、高选择性小分子p53再激活剂rezatapopt,在携带TP53 Y220C特异性突变的晚期实体瘤患者中的疗效与安全性。这一研究不仅在临床层面证实了直接激活突变型p53蛋白的可行性,更为经多线治疗失败的晚期癌症患者提供了泛癌种靶向治疗的新策略。

研究背景:跨越近半个世纪的“成药”挑战
要理解本研究的重大突破,需先厘清p53独特的生物学特性,以及既往针对该靶点的药物研发困境。
1. p53:从“肿瘤相关蛋白”到“基因组守护者”
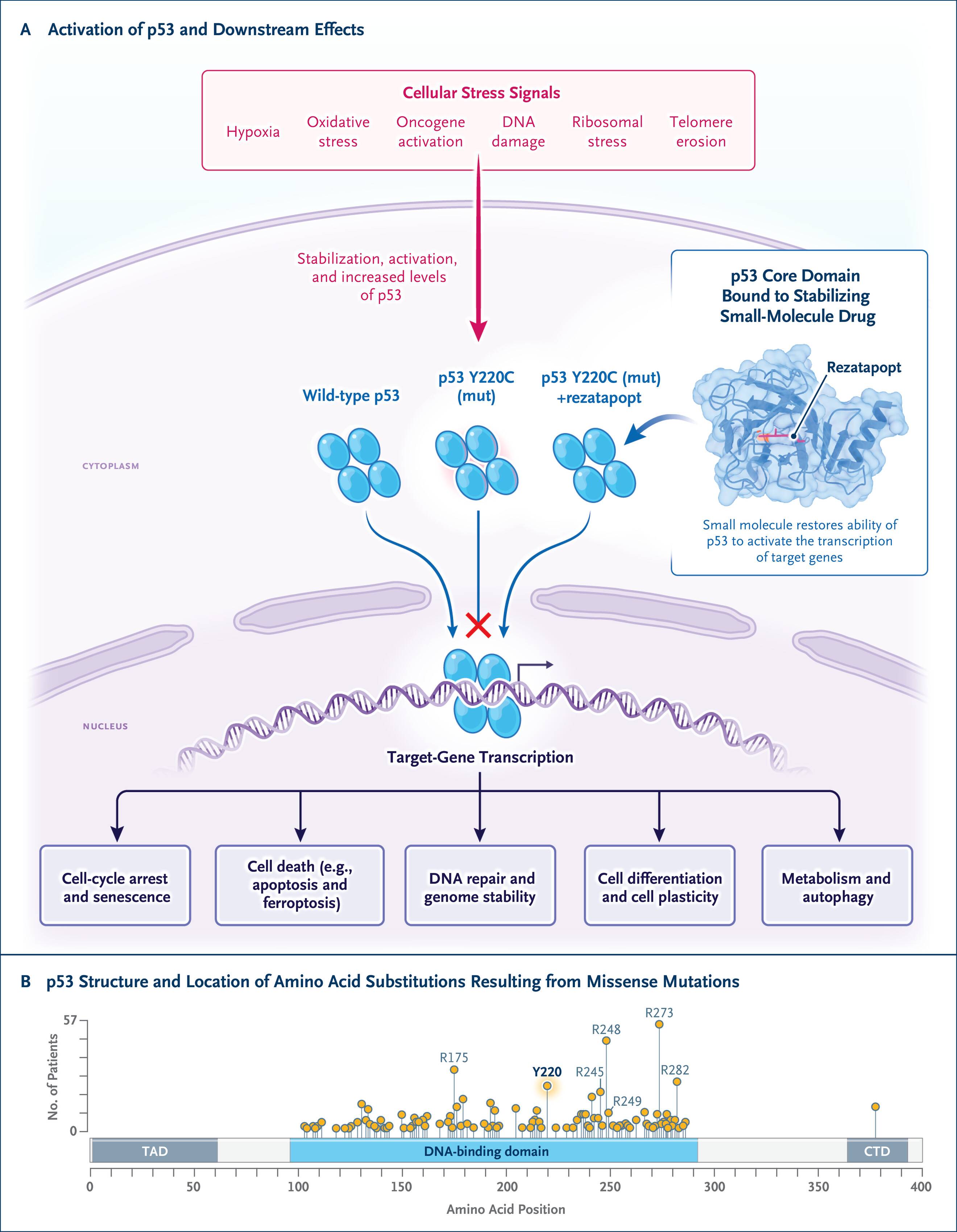
1979年,科学家首次鉴定出分子量为53kDa的肿瘤相关蛋白p53;直至1989年,学界才明确TP53是人类癌症中最常见的突变抑癌基因。野生型p53作为一种转录因子,可通过调控数百个靶基因的表达,诱导细胞周期阻滞、触发细胞凋亡、维持基因组完整性及代谢稳态。一旦p53发生突变,细胞将丧失这一关键防御机制,导致肿瘤不受控增殖,并对传统放化疗产生极强的耐药性。
2. 错义突变与“不可成药”的研发困境
与其他抑癌基因多发生“无义突变”(直接导致蛋白表达缺失)不同,超过73%的TP53突变为“错义突变”——即氨基酸替换导致p53蛋白折叠错误、功能缺陷,且这类突变主要集中在维持蛋白结构稳定的DNA结合结构域。此前,研发人员曾尝试开发非特异性p53再激活剂(如PRIMA-1、APR-246、三氧化二砷等),但此类广谱药物普遍存在脱靶毒性,且单药临床疗效极差。
3. 破局契机:Y220C突变与特异性结构“口袋
TP53 Y220C突变约占所有实体瘤突变的1%(全球每年约有10万名此类癌症患者)。该突变使p53蛋白220位点的酪氨酸被半胱氨酸替代,导致蛋白热力学稳定性急剧下降,最终丧失抑癌功能。而从分子结构来看,该突变会在p53蛋白表面形成一个独特的微小口袋。Rezatapopt正是基于这一结构特征设计的特异性小分子药物——其对该突变位点的结合亲和力高达2.5 nM,可通过非共价氢键紧密嵌合于该口袋内,从热力学层面稳定蛋白结构,选择性地将突变型p53蛋白的三维构象重新锁定为具有正常抑癌功能的野生型构象。
研究方法
PYNNACLE研究是一项I/II期、单臂、多中心临床试验,本次发表的是其I期剂量递增与剂量优化阶段的研究结果。研究纳入携带TP53 Y220C突变的局部晚期或转移性实体瘤患者。所有患者均接受过既往全身治疗,中位线数为3线(范围:1~9线)。研究采用21天为一个治疗周期的连续口服给药方式,其中剂量递增阶段共探索8个剂量组,涵盖rezatapopt 150 mg QD(每日一次)至2500 mg QD,以及1500 mg BID(每日两次)等剂量方案。此外,在确定最大耐受剂量(MTD)后,研究进一步开展多队列的剂量拆分研究,并深入评估了食物对rezatapopt代谢的影响。
研究结果
截至2023年12月,研究共计77例患者入组并接受rezatapopt治疗,常见癌种包括卵巢癌(30%)、胰腺癌(18%)、乳腺癌(13%)及结肠癌(12%)。
1. 安全性与药代动力学(PK):随餐服用显著提升耐受性
安全性:最常见的治疗相关不良事件(TRAEs)以胃肠道反应为主,包括恶心(58%)、呕吐(44%)、血肌酐升高(39%)及疲劳(39%);3级及以上不良事件中,贫血最为常见(16%)。整体而言,药物耐受性良好,因TRAEs导致停药的患者比例仅为3%。
PK特征与食物效应:PK数据显示,与食物同服可借助进食后释放的胆汁盐增强药物溶解度,从而显著提高药物吸收效率——稳态下最大血浆浓度(Cmax)提升约30%,药时曲线下面积(AUC)提升约40%,同时降低了个体内药物暴露量的变异性。更重要的是,随餐服用大幅降低了胃肠道毒性的发生率。基于上述结果,最终确定的II期推荐剂量(RP2D)为2000 mg,每日一次,随餐服用。
2. 初步疗效:展现显著的基因型特异性抗肿瘤活性
总体疗效:在71例具有可测量病灶的患者中,总体客观缓解率(ORR)为20%,中位缓解持续时间(DoR)为7.0个月,中位无进展生存期(PFS)为4.3个月,中位总生存期(OS)达11.4个月。
基于KRAS状态的分层疗效:29%的入组患者同时携带KRAS单核苷酸变异(以胰腺癌、结直肠癌患者为主)。在接受有效剂量治疗且为KRAS野生型的患者中,ORR提升至30%;获得确认缓解的肿瘤类型覆盖卵巢癌、乳腺癌、子宫内膜癌、前列腺癌等多个癌种。值得注意的是,所有获得客观缓解的患者均为KRAS野生型。
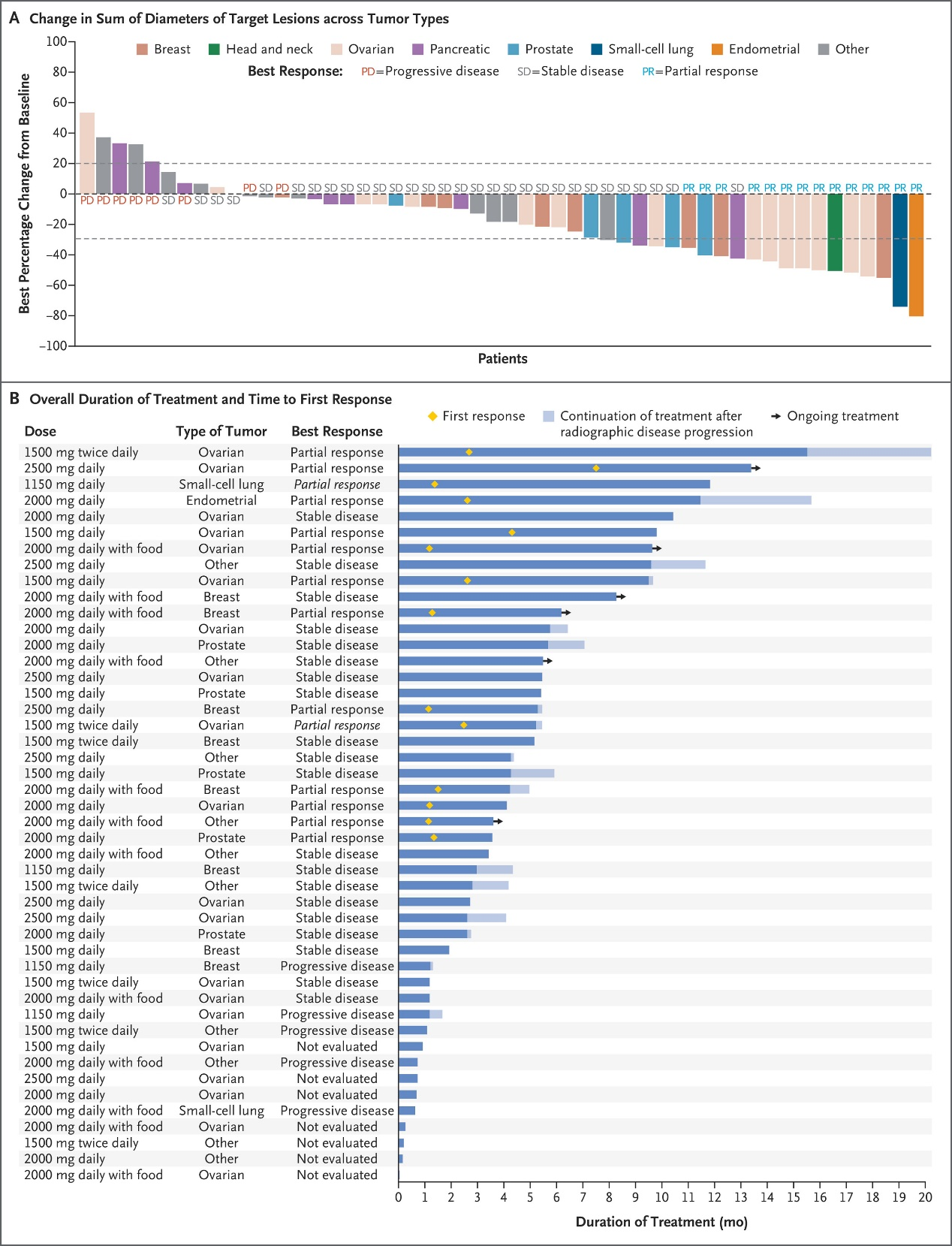
3.分子标志物响应
在具备循环肿瘤DNA(ctDNA)检测数据的患者中,95%(39/41)在治疗早期出现外周血TP53 Y220C突变等位基因频率(VAF)下降;所有达到部分缓解(PR)的患者,其VAF均出现下降(其中71%的患者VAF下降≥50%),这从分子层面证实了药物对靶点的精准结合与生物学活性。
讨论
Rezatapopt的I期临床结果在肿瘤分子靶向治疗领域具有里程碑式的科学价值,其核心意义与启示主要体现在以下维度:
1. 证实“等位基因特异性”直接重激活p53的临床可行性
该研究验证了通过高亲和力小分子纠正特定p53突变体构象、恢复其转录活性这一策略。与既往因缺乏特异性而疗效不佳的广谱p53调节剂不同,rezatapopt的高特异性使其即便在经多线治疗的晚期患者中,仍能展现出单药抗肿瘤响应。这一结果不仅确立了rezatapopt的first-in-class药物地位,也为针对其他高频TP53突变(如R175H、R248Q等)的药物研发提供了可借鉴的成功范式。
2. 揭示致癌网络中“共突变”对疗效的显著制约作用
该研究一项重要发现是:TP53靶向治疗的疗效受共突变基因组特征的显著影响。在携带KRAS共突变的患者中,尽管近60%的患者达到疾病稳定,但无1例实现肿瘤缩小。从分子机制来看,KRAS作为致癌基因,可持续激活细胞增殖信号通路(如RAS-RAF-MAPK、PI3K/AKT/mTOR信号通路)。当TP53 Y220C与KRAS突变共存时,即便rezatapopt成功恢复p53的抑癌功能,这种单方面的修复也难以对抗KRAS驱动的促增殖效应。
这一临床发现不仅解释了不同癌种间的疗效差异(如KRAS突变较少的卵巢癌疗效优异),更明确提示:未来该药物的临床应用需基于严格的生物标志物筛选(排除KRAS突变患者),同时也为“p53再激活剂+KRAS抑制剂/化疗”联合治疗策略的开发提供了明确的循证依据。
3. 剂量优化与药代动力学的精准结合
该研究响应了FDA提出的Project Optimus倡议,彻底摒弃了传统肿瘤药物研发中一味追求MTD的模式。通过精细化的食物效应研究,证实“随餐服用”可借助理化机制(胆盐增溶)同时提升生物利用度、降低消化道毒性。这种基于精准药代动力学分析确定RP2D的严谨思路,大幅提升了患者后续治疗的用药依从性与安全性。
4. 研究的局限性与未来挑战
尽管本研究具有突破性意义,但客观来看仍存在局限性:
适用人群狭窄:TP53 Y220C突变仅占所有实体瘤TP53 突变的1%,rezatapopt的成功无法解决绝大多数TP53突变患者无药可用的问题,距离全面攻克p53靶点仍有很大距离。
单臂设计的局限性:作为I期临床试验,本研究采用单臂设计且样本量较小(77例),纳入的患者涵盖多种异质性较强的癌种;其无进展生存期(PFS)与总生存期(OS)的确切获益,仍需在更大样本量、设有对照组的随机对照试验中验证。
获得性耐药机制的出现:靶向药物往往会出现获得性耐药。研究披露,在 1 例疾病进展后接受穿刺活检的患者中,检测到2个新发TP53突变(G245S、G244D);这提示肿瘤可在药物压力下通过新发突变逃避p53结构锁定,未来需进一步阐明此类耐药克隆的演变规律,并探索应对策略。
小结
Rezatapopt(PC14586)的PYNNACLE I期研究成功打破了p53靶点长达45年的“不可成药”僵局。对于携带TP53 Y220C突变、经多线治疗失败的晚期实体瘤患者,该药物展现出泛癌种的单药抗肿瘤活性,且安全性可控。该研究不仅在微观层面实现了蛋白质结构修复的精准医疗突破,更通过揭示KRAS共突变的耐药现象,深化了对肿瘤复杂信号网络的认知。目前,rezatapopt针对KRAS野生型实体瘤的II期临床试验正在推进,针对血液系统恶性肿瘤的联合治疗研究也已启动。尽管全面攻克各类TP53突变仍任重道远,但rezatapopt的问世,无疑为p53的靶向治疗开辟了切实可行的路径。
Dumbrava EE, Shapiro GI, Parikh AR, et al. Phase 1 Study of Rezatapopt, a p53 Reactivator, in TP53 Y220C-Mutated Tumors. N Engl J Med. 2026;394(9):872-883. Lu X. Restoring Function to a Variant of p53 in Solid Tumors. N Engl J Med. 2026;394(9):922-925.
排版编辑:肿瘤资讯-slb











 苏公网安备32059002004080号
苏公网安备32059002004080号


