乳腺癌是全球女性最常见的恶性肿瘤,2022年中国乳腺癌新发病例数约为35.7万例,死亡病例数约为7.5万例[1],严重危害女性健康。在每年新发病例中,约5%~10%的患者在确诊时即有远处转移[2]。早期患者中,约20%~30%最终发展为晚期乳腺癌[3]。其中,激素受体阳性、人表皮生长因子受体2阴性(HR+/HER2-)乳腺癌是临床最常见的分子亚型。随着新型药物的涌现,晚期乳腺癌治疗格局也在不断演变及更新[4]。瑞波西利是国内首个且目前唯一一个*适应证覆盖绝经前/围绝经期、绝经后乳腺癌患者早期及晚期一线治疗,且晚期一线治疗同时斩获无进展生存期(PFS)、总生存期(OS)双重获益的CDK4/6抑制剂,为不同生理阶段的HR+晚期患者群体均提供优良治疗选择。
本期由新疆医科大学附属肿瘤医院张莘儿医生分享一例46岁HR+/HER2-乳腺癌术后复发患者的诊疗经过,该患者在术后辅助内分泌治疗过程中出现肝转移,接受瑞波西利联合内分泌治疗方案后实现PR。为深入探讨HR+/HER2-晚期转移性乳腺癌的治疗策略,给临床诊疗带来更多参考,特邀新疆医科大学附属肿瘤医赵兵教授对该病例的诊疗进行专业点评。
病例简介
基本信息:患者,女性,46岁。
主诉:右乳癌术后2年余,肝转移1年。
现病史:
患者2022年8月自检时发现右侧乳腺肿块,约蚕豆大小,患者未予重视及诊治。因右乳肿块进行性增大,患者于2023年1月16日就诊外院,乳腺钼靶检查提示:右侧乳腺肿块:BI-RADS 5类,右侧腋下多发肿大淋巴结。
除外相关禁忌,患者2023年1月20日于外院行“右侧单侧根治性乳房切除术(改良根治术)”。
术后病理:(右乳癌改良根治标本)乳腺乳晕区及乳腺上方浸润性小叶癌,组织学分级Ⅱ级,7分,伴多形性小叶原位癌(10%),肿瘤大小4.7cm×4cm×2cm,见脉管内瘤栓及神经侵犯,乳头paget病,皮肤、基底、最近切缘及其余乳腺未见癌累及,腋窝淋巴结见癌转移(16/28)。乳腺肿块:ER(中,90%+),PR(弱,15%+),Her2(2+),Ki-67(40%+),AR(强,90%+),P53(野生型,散在+),P63(-),E-cadherin(-),P120(浆+)。淋巴结转移灶:ER(强,90%+),PR(弱,10%+),Her-2(2+),Ki-67(30%+)。HER-2基因未观测到扩增。术后诊断:右侧乳腺恶性肿瘤(pT2N3M0 Ⅲc期Luminal B型)。
2023年2月8日至2023年7月20日行8周期AC-T方案辅助化疗,后于2023年8月7日至2023年9月12日行左侧胸壁+左侧锁骨上调强放疗Dt5000cGy/25次,放疗期间行戈舍瑞林联合他莫西芬内分泌治疗至2024年10月。期间定时复查未见明显复发及转移征象。
2024年10月23日复查CT示:1.乳癌术后改变;右肺散在实性小结节,同前相仿,建议随诊;右肺下叶钙化灶,同前相仿;2.双肺少许索条,考虑慢性炎症,同前相仿;3.肝内多发结节,较前(2023-9-5)新发,考虑转移瘤(大者位于S6,约1.7x1.5cm),建议随诊;4.重度脂肪肝,同前相仿;5.胆囊、胰腺、脾脏、双肾、双侧肾上腺未见异常;6.纵隔、肺门、腹腔及腹膜后未见确切肿大淋巴结。
月经史:14 岁初潮,平素月经规律,末次月经时间:2023 年 5 月 22 日。
婚育史:22 岁结婚,孕2产2,育有2子。
既往史、个人史、家族史无特殊。
体格检查:右乳缺如,呈术后状态改变,可见长约15cm的手术瘢痕,愈合良好未见胸壁结节,皮肤未见色素沉着,未见毛囊扩张,未见皮肤糜烂,未触及皮肤及皮下组织纤维化,无患侧上肢水肿,对侧乳腺发育良好,未见乳头凹陷,未见乳头乳晕区皮肤糜烂,未触及肿块,双侧颈部、锁骨区未触及淋巴结肿大。
影像学检查:肝脏MRI:肝内多发异常信号,考虑多发转移瘤(大者位于S6,约1.6cmx1.4cm)。 重度脂肪肝,胆汁淤积。

穿刺病理:2024年11月5日行CT引导下肝肿物穿刺活检,(肝脏穿刺标本)肝组织中可见低分化癌浸润,结合病史,考虑转移性癌可能性大;周围肝细胞脂肪变性。免疫组化:ER(强,90%+),PR(-),Her-2(1+),Ki-67(40%+),AR(强,90%+),AE1/AE3(+),GATA3(+),E-cadherin(-),P120(浆+)。
临床诊断:右侧乳腺恶性肿瘤(IV期 luminal B型,HER2阴性);肝继发恶性肿瘤。
治疗方案:
患者于2024年11月25日开始行CDK4/6 抑制剂联合内分泌治疗至今。
具体方案:2024年11月25日至2025年6月9日:瑞波西利 600mg po D1-21,来曲唑 2.5mg po qd,戈舍瑞林 3.6mg 皮下注射 q4w。
辅助检查:


疗效评价:腹部 CT 显示,肝转移病灶明显缩小,评价疗效PR。
实验室检查:


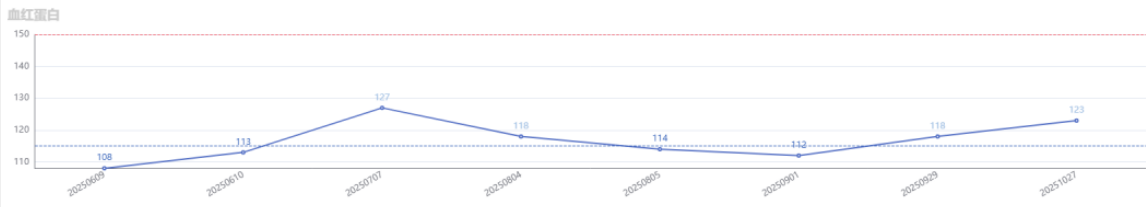
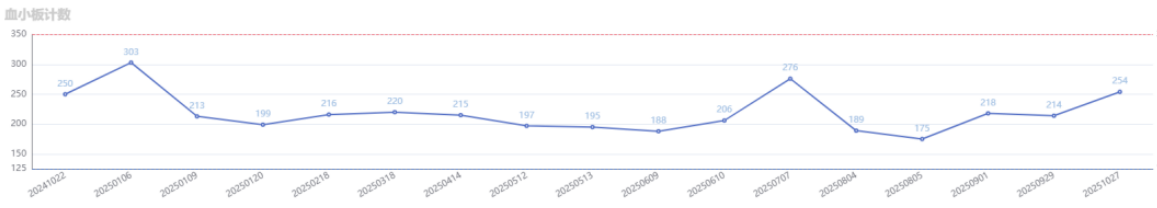

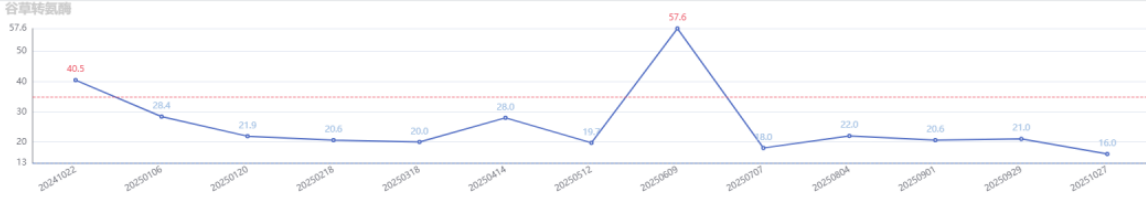
安全性:治疗期间,患者曾出现白细胞、中性粒细胞下降,肝功能异常,通过对症治疗及剂量调整好转,整体安全性可控。
专家点评
我国乳腺癌发病年龄多为40~55岁,绝经前以及围绝经期的女性患者更多,并且年轻乳腺癌和妊娠期乳腺癌发生率也在逐年升高[5]。绝经前女性受于雌激素水平影响,临床中HR阳性的乳腺癌更为多见。本例中患者为46岁围绝经期女性,患者初诊时即为高危的Ⅲc期(pT2N3M0)Luminal B型乳腺癌,在完成AC-T方案标准辅助化疗、放疗及他莫昔芬联合卵巢功能抑制(OFS)的内分泌治疗后,无病生存期(DFS)约21个月即出现肝转移。这种在辅助内分泌治疗期间出现的早期复发转移,通常提示肿瘤生物学行为较为侵袭,且可能存在原发内分泌耐药,是临床治疗中需要重点关注和强化治疗的情况。
患者此时明确乳腺癌肝转移,且肿瘤增殖活性较高{ Ki-67(40%+)},亟需快速、强效控制疾病进展的系统治疗方案。为此,治疗团队自2024年11月25日起为患者制定了瑞波西利+来曲唑联合OFS的晚期一线抗肿瘤治疗方案。经过1年的治疗,患者最大的肝转移灶从1.7cmx1.5cm显著缩小至0.6cm x 0.5cm,疗效评价达到部分缓解(PR),患者目前仍在治疗。在安全性方面,患者在治疗第7周期治疗后出现Ⅲ度骨髓抑制,以及轻度肝功能异常,通过药物减量及对症治疗,后续患者血象稳定,证实了通过对症治疗和剂量调整可以有效管理此类不良反应,从而保障治疗的长期持续。这也提醒我们,在临床应用中,密切的血液学监测和积极主动的剂量管理,是确保患者安全、实现长期治疗获益的基石。
细胞周期蛋白依赖性激酶(CDK)4/6抑制剂联合内分泌治疗是目前包括CSCO BC与NCCN指南等在内的国内外主流权威指南一致推荐的HR+/HER2-晚期乳腺癌标准一线治疗策略。在现有CDK4/6抑制剂中,瑞波西利在HR+/HER2-晚期乳腺癌(包括绝经前及绝经后人群)的一线治疗中,显示出无进展生存期(PFS)与总生存期(OS)的双重获益。其中MONALEESA-7是一项专门针对绝经前/围绝经期HR+/HER2-晚期乳腺癌患者的大型III期临床研究,该研究不仅提示,与单独内分泌治疗相比,瑞波西利联合内分泌治疗使中位OS延长10.7个月(58.7个月 vs. 48.0个月)[6]。此外,瑞波西利联合内分泌治疗组的PFS同样表现亮眼,中位PFS延长约10个月,且具有统计学意义[7]。此外,MONALEESA-7研究的事后分析显示,瑞波西利联合AI可有效抑制绝经前HR+/HER2-晚期乳腺癌的雌二醇水平,降低卵巢逃逸概率,进而改善生存预后。
RIGHT Choice研究[8]则是在HR+/HER2-晚期乳腺癌中,首个比较CDK4/6抑制剂联合内分泌治疗与联合化疗疗效与安全性的头对头研究,该研究共纳入222例绝经前/围绝经期、HR+/HER2-晚期乳腺癌患者,其中亚裔占53.1%,研究数据对中国患者具有重要借鉴意义。研究结果显示,瑞波西利联合内分泌组的中位mPFS显著优于双药化疗组(21.8个月vs.12.8个月),降低39%的疾病进展或死亡风险(HR=0.61)。该研究中内脏转移患者占67.6%,结果显示瑞波西利联合治疗组中位PFS较双药化疗组延长近1年(24.0个月 vs. 12.3个月),降低46%疾病进展或死亡风险(HR=0.54)。
随着治疗理念的更新,如今晚期乳腺癌的治疗决策的制定需综合考量“疗效-毒性-生活质量”间的三维平衡。ESMO临床获益量表(MCBS)要求:对非治愈性疾病,需同时量化生存延长、症状控制及安全性。值得注意的是,并非所有CDK4/6抑制剂都能转化为总生存期(OS)获益,而瑞波西利凭借MONALEESA系列研究所展示的PFS与OS双重显著获益,以及总体生活质量评分较基线持续改善,成为目前唯一*获得ESMO-MCBS评分中相较同类中最高评分的CDK4/6抑制剂,体现了“高效-低毒-高生活质量”的全面治疗优势。
该例患者术后辅助治疗阶段仅接受他莫昔芬联合卵巢功能抑制治疗,未使用CDK4/6抑制剂辅助强化治疗,21个月后出现了肝内多发转移,进入晚期一线治疗阶段。随后患者在接受瑞波西利联合内分泌治疗后达到PR,且不良反应可控、生活质量良好,与MONALEESA系列研究及RIGHT Choice研究结果高度一致。
本病例不仅验证了临床试验成果的可重复性,也再次提示对于围绝经期、快速内脏转移的HR+/HER2-晚期乳腺癌,瑞波西利可作为行之有效的一线治疗方案,为临床实践提供了直观而有力的证据。期待该患者在后续治疗中持续获益,也期待瑞波西利在真实世界的应用中造福更多HR+/HER2-晚期乳腺癌患者。
*声明:瑞波西利的注册研究结果未涉及侵袭性疾病患者的有效性和安全性数据
*NCCN指南唯一:联合AI
新疆医科大学附属肿瘤医院 党委委员,副院长
新疆医科大学校级“教学名师”
中国临床肿瘤学会(CSCO)乳腺癌专家委员会委员
中国抗癌协会乳腺癌专业委员会委员
中国临床肿瘤学会(CSCO)患者教育专家委员会常务委员
中国健康促进基金会乳腺疾病专家委员会常务委员
北京癌症防治学会乳腺癌精准靶向诊疗专业委员会委员
新疆抗癌协会副理事长
《JCO》中文版 乳腺专刊 青年编委
新疆抗癌协会乳腺癌专业委员会常务委员
新疆医科大学附属肿瘤医院 乳腺内科 住院医师
新疆医科大学 肿瘤学硕士
专业领域:乳腺癌的诊断与治疗
参考文献
[1] Bray F, Laversanne M, Sung H, Ferlay J, Siegel RL, Soerjomataram I, Jemal A. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2024 Apr 4.
[2] Benitez Fuentes JD, Morgan E, de Luna Aguilar A, et al.Global stage distribution of breast cancer at diagnosis: a systematic review and meta-analysis[J]. JAMA Oncol, 2024, 10(1):71-78.
[3] Coles CE, Earl H, Anderson BO, et al. The Lancet breast cancer commission[J]. Lancet, 2024, 403(10439):1895-1950.
[4] 国家肿瘤质控中心乳腺癌专家委员会, 中国抗癌协会乳腺癌专业委员会, & 中国抗癌协会肿瘤药物临床研究专业委员会. (2024). 中国晚期乳腺癌规范诊疗指南(2024版). 中华肿瘤杂志, 46(12), 1079-1106.
[5] Global burden and trends in premenopausal and postmenopausal breast cancer: a population-based study. Lancet Glob Health. 2020 Aug;8(8):e1027-e1037.
[6] Lu YS, et al. Clin Cancer Res. 2022;28(5):851-859.
[7] Debu Tripathy, et al. Lancet Oncol. 2018 Jul;19(7):904-915.
[8] Lu YS, Mahidin EIBM, Azim H, et al. Final Results of RIGHT Choice: Ribociclib Plus Endocrine Therapy Versus Combination Chemotherapy in Premenopausal Women With Clinically Aggressive Hormone Receptor-Positive/Human Epidermal Growth Factor Receptor 2-Negative Advanced Breast Cancer. J Clin Oncol. 2024 Aug 10;42(23):2812-2821.
[9] US Food and Drug Administration. Clinical trial endpoints for the approval of cancer drugs and biologics. Available at:
https://www.fda.gov/media/71195/download. Accessed December.
[10] atthew P,MasakazuT,Jens H, et al.2023 SABCS.GS01-12.
[11] Hortobagyi GN, et al. N EngI J Med. 2022;386(10):942-950.
[12] Richard S. Finn, et al.N Engl J Med 2016;375:1925-1936.[18]Yen-Shen Lu, et al.2022 Mar 1;28(5):851-859.
[13] Bishal Gyawali, et al. Nat Rev Clin Oncol. 2022 Oct;19(10):613-614.
[14] Bishal Gyawali, et al. Nat Rev Clin Oncol.2022 Oct;19(10):613-614.
[15] Oosting SF, et al. Ann Oncol. 2023 Apr;34(4):431-439.
[16] https://www.esmo.org/guidelines/esmo-mcbs/esmo-mcbs- for-solid-tumours/esmo-mcbs-scorecards?scorecard=9.[MONALEESA-2]
[17] https://www.esmo.org/guidelines/esmo-mcbs/esmo-mcbs- for-solid-tumours/esmo-mcbs-scorecards?scorecard=159.[monarch 3]
[18] https://www.esmo.org/guidelines/esmo-mcbs/esmo-mcbs- for-solid-tumours/esmo-mcbs-scorecards?scorecard=7.[PALOMA-2]
[19] https:// www.esmo.org/guidelines/ esmo-mcbs/ esmo-mcbs- for-solid-tumours/ esmo -mcbs-scorecards/scorecard-338-1.[NATALEE]
[20] NCCN Guidelines 2025.v4 Invasive Breast Cancer. Available at: https: // www. nccn. Org / professionals/physician_gls/pdf/breast.pdf
审批码KI20057335-118369,有效期为2025-11-24至2026-11-24,资料过期,视同作废
排版编辑:肿瘤资讯-C Y X












 苏公网安备32059002004080号
苏公网安备32059002004080号


