多发性骨髓瘤(MM)是以浆细胞异常增殖为特征的恶性血液系统肿瘤,其临床表现多样。其中,骨骼系统的受累尤为突出,是导致MM患者生活质量下降和预后不良的关键因素。MM细胞与骨髓微环境的复杂相互作用,打破了骨重塑的稳态,导致溶骨性病变、病理性骨折和剧烈骨痛等一系列骨骼相关事件(SREs)。因此,有效的骨保护治疗不仅是缓解症状、预防并发症的重要手段,更是MM全程管理中不可或缺的一环,对于维持患者的骨骼健康、改善其功能状态和延长生存期具有至关重要的价值。为进一步改善患者的临床结局,【肿瘤资讯】特别邀请南京市第一医院张学忠教授围绕MM骨保护治疗实践要点及未来探索方向进行分享。
南京市第一医院
江苏省社会办医疗机构协会血液学专委会副主任委员
江苏省医学会血液学分会委员、感染学组副组长
南京市医学会血液学分会副主任委员
江苏省预防医学会血液病预防与控制专委会常委
江苏省抗癌协会血液专业委员会常委
江苏省老年医学会血液学分会委员
江苏省医师协会血液学分会委员
江苏省研究型医院学会白血病和MDS专业委员会委员
江苏省科普演讲专家
抽丝剥茧:揭秘MBD的发病机制及其对MM患者预后的深远影响
MM相关骨病(MBD)的发生机制复杂且对患者的预后及生活质量构成严重威胁。MM细胞在骨髓微环境中通过分泌多种细胞因子,扰乱了骨重塑的生理平衡。具体而言,MM细胞通过上调核因子κB受体活化因子配体(RANKL)的表达,同时下调其天然拮抗剂骨保护素(OPG)的水平,从而过度激活破骨细胞,导致骨吸收作用显著增强[1]。此外,MM细胞还通过分泌Dickkopf-1(DKK1)和硬骨素(Sclerostin)等抑制剂,有效阻断Wnt信号通路,从而抑制成骨细胞的分化与功能,最终导致骨形成受损[2]。
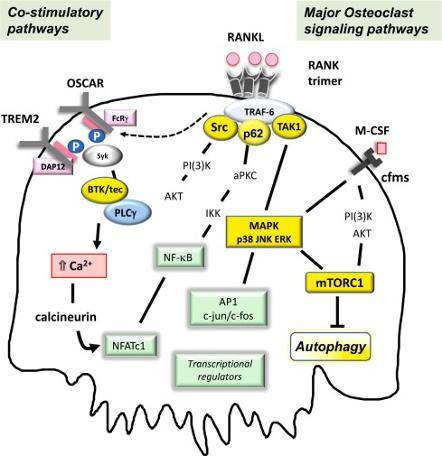
这种“促破骨、抑成骨”的双重失衡,是MM患者发生骨质破坏、溶骨性病变乃至病理性骨折的根本原因。临床上,溶骨性病变在MM患者中极为常见。据统计,约有80%的患者在初诊时即表现出溶骨性病变,在疾病复发或进展期,这一比例更是高达90%[3]。这类患者发生SREs如病理性骨折、脊髓压迫以及高钙血症等的风险较高,而SREs是MM患者致残甚至致死的重要原因[4]。
另外,病理性骨折,特别是椎体压缩性骨折,常导致难以忍受的慢性疼痛、身高变矮和脊柱畸形。更为严重的是,当椎体骨折或肿瘤组织直接侵犯MM患者的椎管时,可引发急性脊髓压迫,或可导致MM患者出现截瘫、大小便失禁等问题,需要紧急放疗或外科手术减压。此外,持续的疼痛和功能障碍严重限制了MM患者的日常活动能力,导致其生活质量急剧下降,并常常因此需要反复住院治疗,极大地增加了医疗资源的消耗。因此,深入理解MBD的发生机制,并对SREs进行有效的预防和管理,对于改善MM患者预后、维持其功能状态和生活质量具有至关重要的临床意义。
全程护航:MM骨保护治疗选择分析及临床实践要点
既往研究发现,有效的骨保护治疗不仅能预防或延迟SREs的发生,更是MM综合管理中不可或缺的一环。当前的骨保护策略主要遵循两大路径,即抑制破骨细胞活性和促进成骨细胞功能。
在临床实践中,抑制破骨细胞活性是应用较为广泛的骨保护策略。两大类药物——双膦酸盐和RANKL抑制剂,构成了该类治疗的基石。
双膦酸盐主要通过诱导破骨细胞凋亡,有效抑制骨吸收[5]。大量的临床试验证据和长期的随访数据证实了双膦酸盐类药物在降低SREs风险方面的疗效。然而,双膦酸盐治疗MBD同样存在局限性,包括需要通过静脉输注给药,以及潜在的肾毒性风险[6]。
以地舒单抗为代表的RANKL抑制剂,是MM骨保护治疗的重要选择。地舒单抗是一种全人源化单克隆抗体,可特异性地结合并中和RANKL,从而阻断其与破骨细胞前体表面的RANK受体结合,抑制破骨细胞的形成、功能和存活[7]。一项关键的国际多中心、随机、双盲Ⅲ期临床试验,比较了地舒单抗与双膦酸盐类药物在预防新诊断MM患者SREs方面的疗效与安全性。结果显示,地舒单抗在延迟首次SREs发生时间方面不劣于双膦酸盐类药物,且在探索性的无进展生存期(PFS)分析中,观察到地舒单抗组有延长PFS的趋势[8]。此外,地舒单抗通过皮下给药,并经内皮系统代谢的特点,为其带来了独特的临床优势。
结合现有证据和药物特点,MM骨保护治疗的临床路径日益清晰。在治疗开启时机方面,权威指南推荐,所有需要治疗的活动性MM患者,特别是初诊时即伴有溶骨性病变的患者,应尽早启动骨保护治疗[9-10]。在选择药物时,若MM患者优先考虑门诊治疗的便捷性、存在静脉通路困难或静脉输注资源受限,地舒单抗是理想的选择。
在治疗持续时间方面,现有指南亦普遍推荐MM骨保护治疗应持续至少2年[9-10]。而对于后续是否停药或调整频率,应根据MM患者的疾病状态(是否达到完全缓解)、SREs风险以及个体耐受性综合判断。对于疾病持续活动的MM患者,通常建议继续治疗。
最后,在整个治疗过程中,临床医生必须对MM患者进行系统的监测,包括定期的牙科评估以预防颌骨坏死(ONJ)、监测血清钙、磷和维生素D水平以管理低钙血症风险以及定期评估肾功能。
不断超越:MM骨保护治疗的未来图景
在未来研究层面,应优先开展地舒单抗与新型抗肿瘤药物(包括靶向药物、免疫治疗等)的系统性联合与序贯治疗策略研究,以明确这些组合对骨髓微环境与抗MM治疗疗效的相互影响。既有前瞻性与综述性研究提示,RANKL 抑制剂地舒单抗与免疫治疗之间可能存在生物学协同或互补效应,但在包含细胞免疫疗法的情形下,需对MM患者骨代谢的动态变化、免疫相关不良反应及感染风险进行评估。因此,相关临床试验应同时纳入骨代谢学终点(如骨转换标志物、影像学骨结构变化)与血液学/免疫学终点(如MRD状态与免疫细胞谱系学改变),以便解析治疗顺序对患者疗效和安全性的影响[11]。
关于以“修复”为导向的骨保护策略,成骨促进剂在MBD中的应用正处于探索阶段,应以严谨设计的早期临床试验评估其安全性与修复效能。已有针对促骨生成药物在伴发骨质疏松或 MM相关骨流失患者中的初步研究,显示患者短期内的骨密度和骨强度指标可能改善且未见明确促瘤信号,但研究的样本量有限且随访时间短。因此,未来研究需重点评估成骨药物与抗吸收药物联用或序贯给药时对MM患者的骨破坏修复、局灶性骨病学改变及肿瘤生物学行为的长期影响[12]。
在骨保护治疗停药管理和优化序贯方案方面,研究者未来应系统筛选并验证可预测停药后反弹及骨折风险的生物标志物,以实现个体化停药决策。
综上所述,未来MM骨保护领域的研究应从单一抗骨吸收治疗迈向系统性、精准化的综合管理模式。一方面,应通过高质量的临床研究探索地舒单抗与新型抗MM药物的联合与序贯策略,以阐明其在骨髓微环境重塑与抗瘤效应增强中的潜在协同作用;另一方面,以“修复”为导向的骨保护理念亟需进一步验证成骨促进剂在骨重建及疾病长期控制中的价值。此外,建立基于生物标志物的停药风险预测体系,将有助于优化骨保护治疗的时长与策略,推动MM全程管理从“延缓破坏”走向“重建平衡”,最终实现高质量、长期生存的治疗目标。
[1] Terpos, E., Ntanasis-Stathopoulos, I., Gavriatopoulou, M., & Dimopoulos, M. A. (2018). Pathogenesis of bone disease in multiple myeloma: from bench to bedside. Blood Cancer Journal, 8(1), 1-12.
[2] Giuliani, N., Rizzoli, V., & Roodman, G. D. (2016). The role of the Wnt signaling pathway in the pathogenesis of multiple myeloma bone disease. Journal of Bone and Mineral Research, 21(S2), 162-167.
[3] Kyle, R. A., Gertz, M. A., Witzig, T. E., Lust, J. A., Lacy, M. Q., Dispenzieri, A., ... & Greipp, P. R. (2003). Review of 1027 patients with newly diagnosed multiple myeloma. Mayo Clinic Proceedings, 78(1), 21-33.
[4] Zervas, K., Mihou, D., Katodritou, E., & Kouraklis-Symeonidis, A. (2006). Clinical, oncological, and skeletal-related events in patients with bone metastases. Journal of BUON, 11(4), 437-445.
[5]Rogers, M. J., Crockett, J. C., Coxon, F. P., & Mönkkönen, J. (2011). Biochemical and molecular mechanisms of action of bisphosphonates. Bone, 49(1), 34-41.
[6] Lacy, M. Q., Dispenzieri, A., Gertz, M. A., Greipp, P. R., Goll, V., Srkalovic, G., ... & Rajkumar, S. V. (2006). Mayo Clinic consensus statement for the use of bisphosphonates in multiple myeloma. Mayo Clinic Proceedings, 81(8), 1047-1053.
[7] Lacey, D. L., Boyle, W. J., Simonet, W. S., Kostenuik, P. J., Dougall, W. C., Sullivan, J. K., ... & Sarosi, I. (2012). Bench to bedside: elucidation of the OPG-RANK-RANKL pathway and the development of denosumab. Nature Reviews Drug Discovery, 11(5), 401-419.
[8] Raje, N., Terpos, E., Willenbacher, W., Shimizu, K., García-Sanz, R., Durie, B., ... & San-Miguel, J. (2018). Denosumab versus zoledronic acid in bone disease treatment of newly diagnosed multiple myeloma: an international, double-blind, double-dummy, randomised, controlled, phase 3 study. The Lancet Oncology, 19(3), 370-381.
[9]NCCN Clinical Practice Guidelines in Oncology™ Multiple Myeloma. V2. 2020
[10]中华医学会血液学分会, 中国抗癌协会血液肿瘤专业委员会. 中国多发性骨髓瘤骨病诊治指南(2022年版). 中华内科杂志 , 2022, 61(11): 1235-1241.
[11]Mabrut E, Mainbourg S, Peron J, Maillet D, Dalle S, Fontaine Delaruelle C, Grolleau E, Clezardin P, Bonnelye E, Confavreux CB, Massy E. Synergistic effect between denosumab and immune checkpoint inhibitors (ICI)? A retrospective study of 268 patients with ICI and bone metastases. J Bone Oncol. 2024 Sep 21;48:100634. doi: 10.1016/j.jbo.2024.100634. PMID: 39381634; PMCID: PMC11460504.
[12]Mariana Diz Lopes, Francesco Pollastri, Francesca Mastropaolo, Rosanna Somma, Mattia Tugnolli, Emma Pasetto, Camilla Benini, Valeria Messina, Davide Gatti, Ombretta Viapiana, Maurizio Rossini, Elena Marchetti, Martina Tinelli, Giovanni Adami, Romosozumab in postmenopausal women with smoldering multiple myeloma: a prospective 12-mo study, JBMR Plus, Volume 9, Issue 10, October 2025, ziaf144, https://doi.org/10.1093/jbmrpl/ziaf144
排版编辑:肿瘤资讯-LBJ











 苏公网安备32059002004080号
苏公网安备32059002004080号


