骨转移是晚期恶性肿瘤患者常见的并发症,不仅会引发病理性骨折和脊髓压迫等一系列骨相关事件(SREs),严重影响患者的生活质量,也往往预示着疾病的进展和不良预后。如何有效地评估与处理骨转移,延缓疾病进程,是肿瘤治疗领域面临的重要挑战。为深入探讨这一议题,在近期举办的三方研讨会上,我们邀请到复旦大学附属肿瘤医院骨软组织外科孙正望教授,为我们系统性地讲解骨转移癌的诊疗机制、危害评估与干预决策。
复旦大学附属肿瘤医院骨软组织外科
中国医药教育协会骨与软组织肿瘤专业青年委员
中国医药教育协会肢体肿瘤分会委员
中国老年学和老年医学学会老年骨科分会委员
全国卫生产业企业管理协会骨科分会委员
全国卫生产业企业管理协会脊椎健康分会常务委员
上海市抗癌协会肉瘤专委会委员
上海市抗癌协会黑色素瘤专委会青年委员
上海市康复医学会脊柱脊髓专业委员会脊柱肿瘤学组组员
作为课题负责人主持上海市卫健委基金,参与多项,第一作者或通讯作者发表SCI论文20余篇,最高影响因子18分,实用新型专利第一发明人4项
长期从事脊柱、骨肿瘤、软组织肉瘤、恶性黑色素瘤的临床工作和基础研究。擅长脊柱肿瘤、骨原发肿瘤与转移性肿瘤、软组织肉瘤及恶性黑色素瘤的疑难病诊断和治疗。专业特色:脊柱转移瘤的微创治疗,脊柱肿瘤的En-bloc切除,软组织肉瘤屏障切除、恶性黑色素根治性切除、挽救性手术和综合治疗
点击观看完整视频
骨转移的流行病学与危害
肿瘤骨转移是困扰人类数千年的难题。在现代临床中,不同癌种发生骨转移的概率有显著差异。前列腺癌的骨转移发生率最高,可达80%;乳腺癌次之为75%;肺癌和肾癌的发生率分别为40%和30%,肝细胞癌则约为20%。孙正望教授结合临床经验提到,有时患者的首发症状仅为骨痛,经过反向追查,最终才发现原发病灶为肺癌。
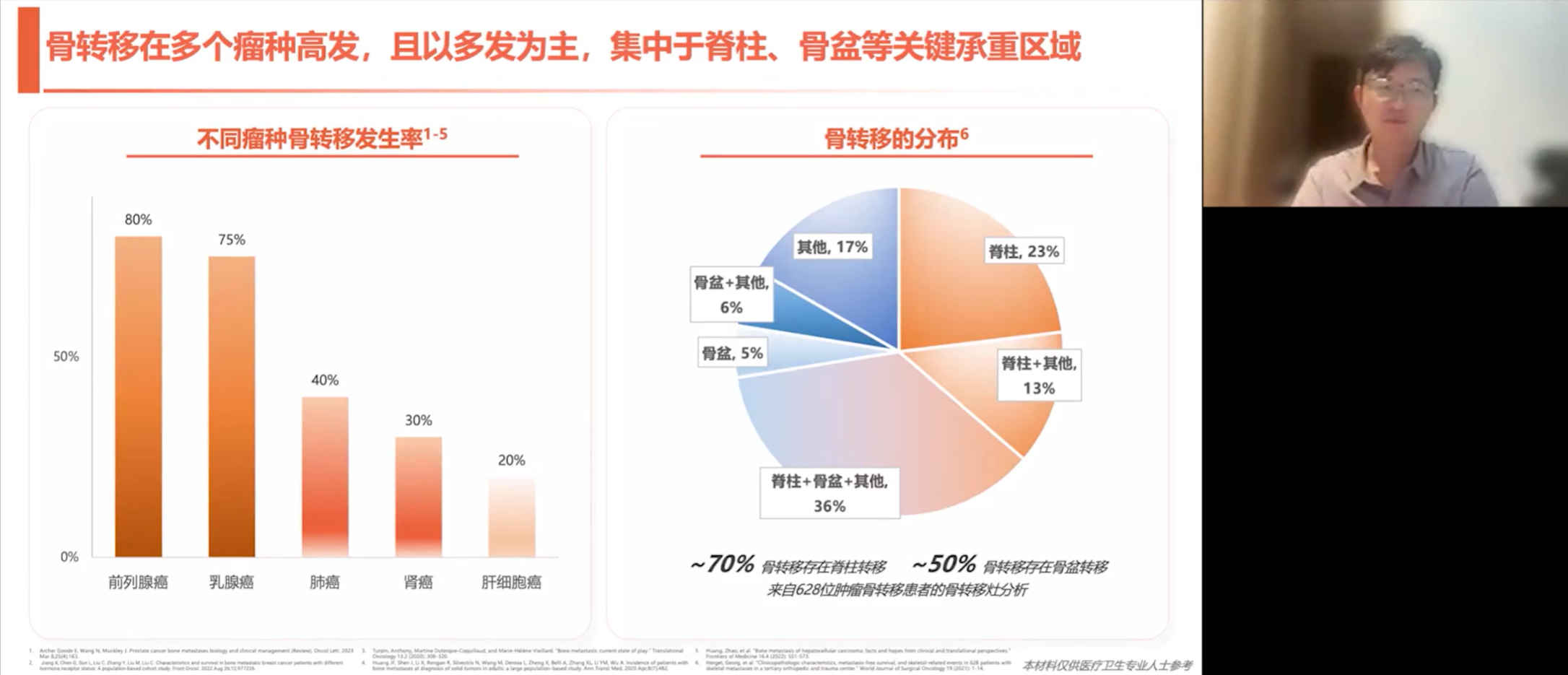
从骨转移的解剖分布来看,中轴骨是其最常侵犯的区域,尤其是脊柱和骨盆。统计数据显示,约23%的骨转移单独发生在脊柱,36%同时累及脊柱与骨盆,而单纯发生在骨盆的占5%。相较之下,四肢骨骼的转移则相对少见。
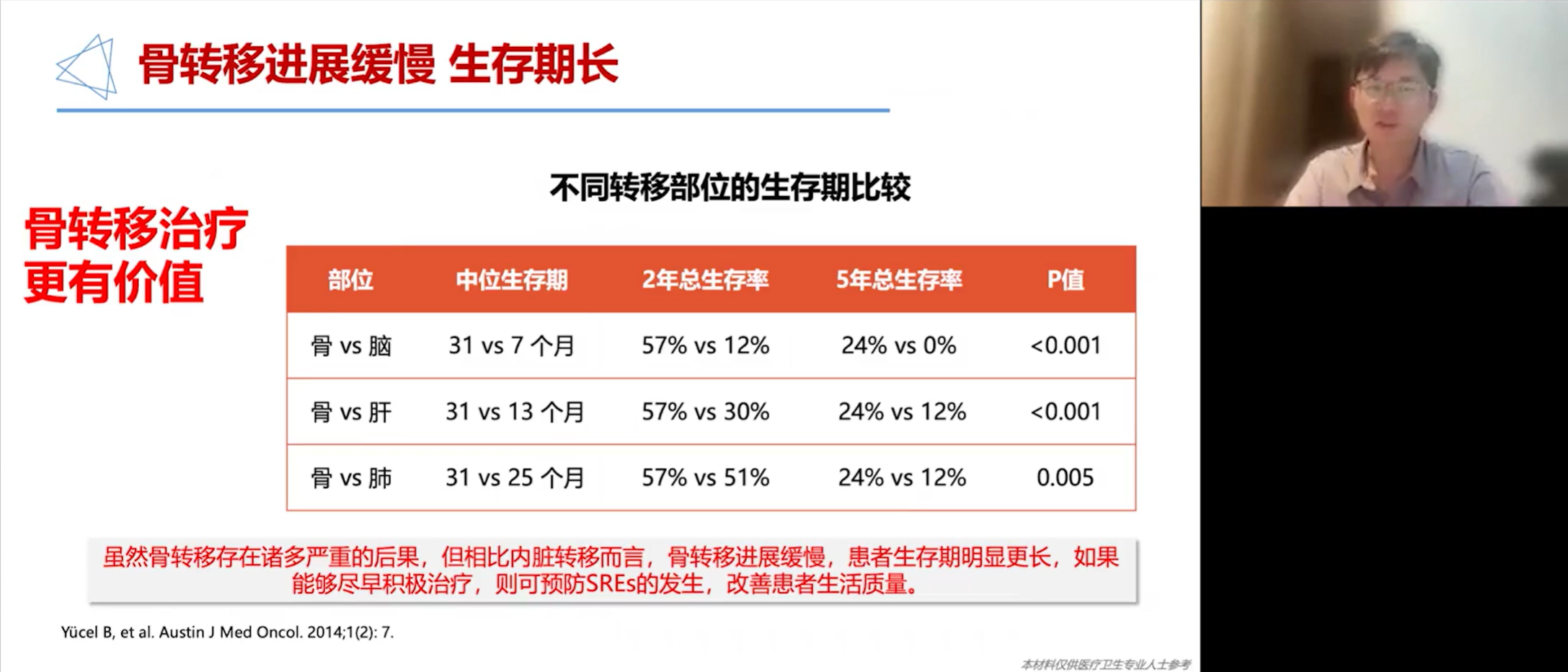
一旦患者出现骨转移,积极治疗仍具有重大价值。通过对比不同转移部位患者的生存数据可以发现,骨转移患者的中位生存期(31个月)明显长于脑转移(7个月)、肝转移(13个月)和肺转移(25个月)的患者。这表明,虽然骨转移会带来严重的后果,但其病程进展相对内脏转移更为缓慢。因此,对骨转移患者进行尽早、积极的治疗,可以有效预防骨相关事件(SREs)的发生,从而显著改善患者的生活质量。
SREs包括病理性骨折、骨放疗、因病理性骨折进行的骨外科手术以及脊髓压迫。这些并发症不仅会延长患者的住院时间、增加死亡风险,还可能导致剧烈疼痛、瘫痪、甚至昏迷和死亡。在所有SREs中,病理性骨折和脊髓压迫是两种最为经典的并发症,也是骨科医生面临的主要挑战。

病理性骨折:由于肿瘤对骨质的侵蚀,患者骨骼变得异常脆弱,即使在轻微外力下也可能发生骨折,严重影响生活质量并带来巨大痛苦。
脊髓压迫:当椎体转移灶压迫脊髓时,可导致不可逆的神经损伤。恶性肿瘤脊髓压迫属于急症,一旦确诊,患者的中位生存期仅3至4个月。孙正望教授提醒,若患者发展为全瘫,即使紧急手术,神经功能恢复的概率也仅有34%。
针对肿瘤转移导致的脊柱压迫,临床上采用ESCC(Epidural Spinal Cord Compression)评分系统进行评估。该系统根据肿瘤对椎管内结构的压迫程度进行分级。例如,当肿瘤突破椎体后壁(EA级),进入椎管(EB级),并接触到脊髓(EC级)时,分级随之提升。ESCC二级意味着脊髓已受压变形,但周围的脑脊液循环仍然通畅。而到了三级,脑脊液循环被完全阻断,形成非常严重的压迫。对于达到二级甚至三级的患者,建议进行手术治疗,以尽快解除压迫,恢复脊髓功能。

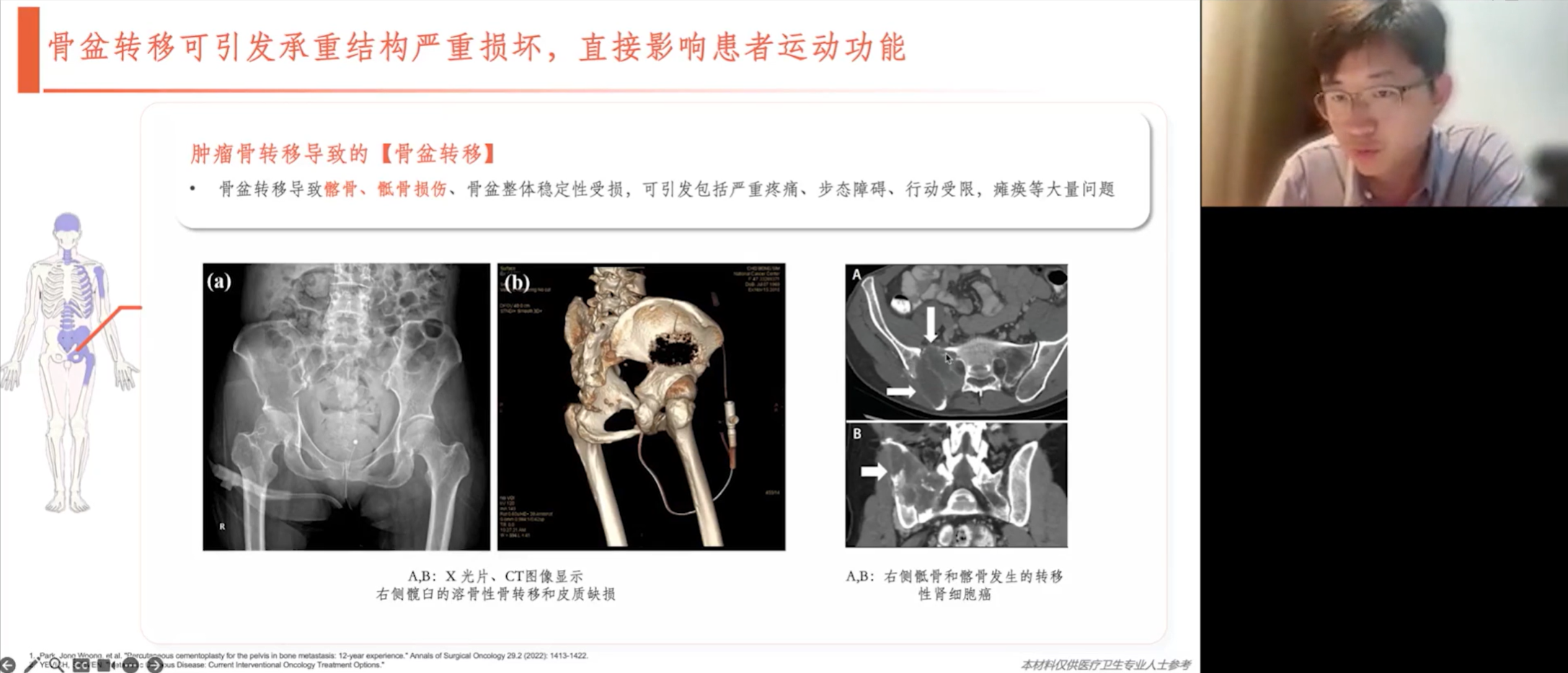
骨盆转移也较为常见。骨盆可划分为四个区域:一区为髂骨,此处的病灶通常不会引起骨折或失稳;二区为髋臼,此处的病灶会影响行走功能,需要处理;三区为耻骨联合;四区与骶骨翼相交。例如,当骶髂关节(一个主要的承重关节)同时受到骶骨翼和髂骨病灶的破坏时,会导致结构不稳,患者将难以行动或站立。
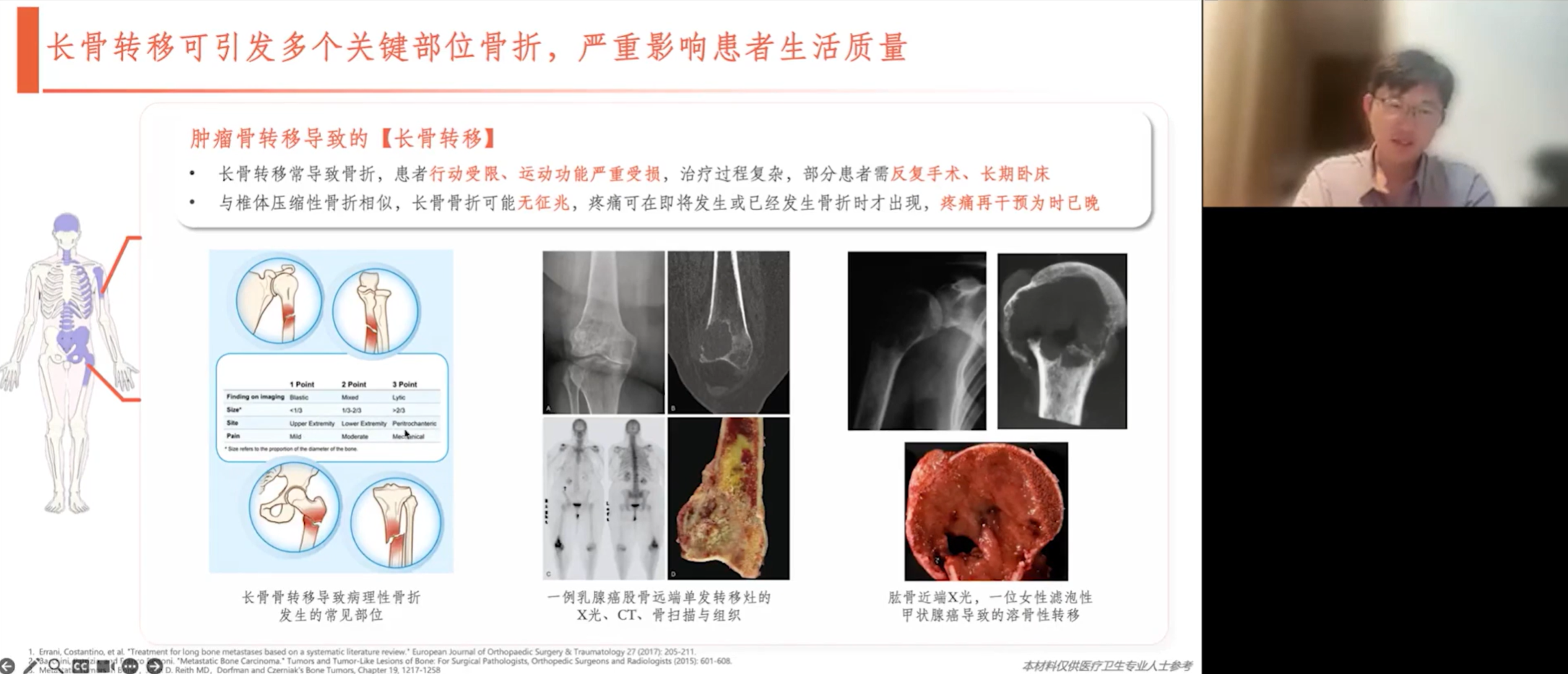
对于长骨转移,临床上采用专门的Mirels评分系统来评估其不稳定性及病理性骨折风险。该评分系统从多个维度进行评估:
病灶类型:成骨性病变计1分,混合性病变计2分,溶骨性病变计3分。
病灶大小:肿瘤侵犯骨骼横截面积小于1/3计1分,1/3至2/3计2分,大于2/3计3分。
部位:上肢病灶因受力较小计1分,下肢计2分,转子间区域因受力巨大计3分。
疼痛程度:根据疼痛情况计1至3分。
通过这些维度的综合评分,可以判断长骨转移的稳定性。
骨转移与骨破坏的机制及治疗
研究证实,发生骨折的肿瘤患者其死亡风险会显著增加。与非肿瘤患者相比,肿瘤患者的骨折风险更高、更普遍。除了前臂骨折外,几乎所有部位的病理性骨折都与肿瘤患者死亡风险的增加相关。肿瘤患者在发生骨折后的第一年内,死亡风险增加最为显著。即使在确诊肿瘤十年后,发生骨折仍会增加患者的死亡风险。
随着内科、放疗科及多学科治疗的进步,肿瘤患者的生存时间越来越长,这也意味着将有更多患者在生存期内面临濒临骨折的风险,需要骨科医生进行专业鉴别和探讨,以决定是否需要外科处理。

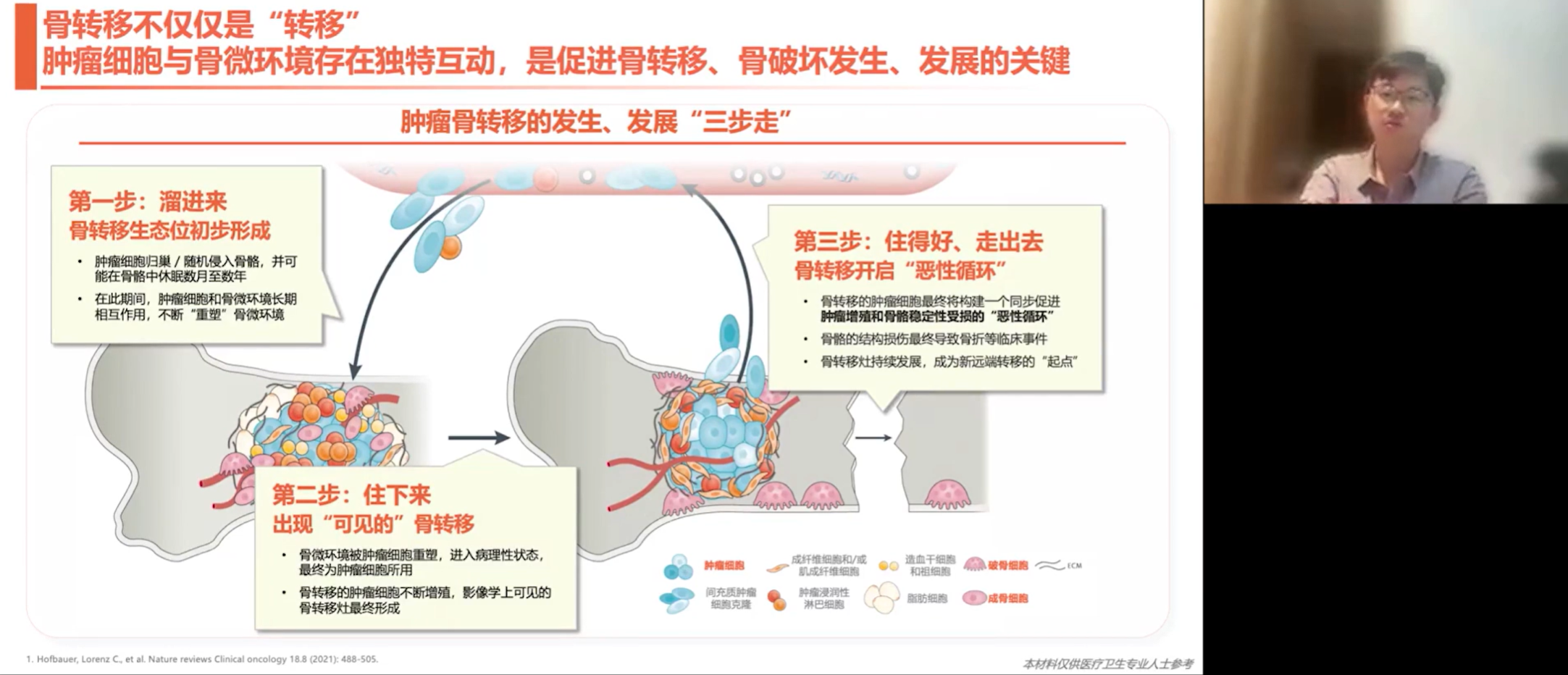
肿瘤的骨转移与破坏机制是一个包含“发生”与“发展”的三步过程:
肿瘤细胞的转移与休眠:肿瘤细胞转移并进入骨骼,可能在骨骼中处于休眠状态。在此过程中,肿瘤细胞与骨微环境相互作用,不断重塑骨微环境。
新病灶的形成与增殖:肿瘤细胞“定居”下来形成新的病灶。骨微环境被肿瘤细胞重塑后进入病理状态,肿瘤细胞在此不断增殖。
恶性循环与再转移:肿瘤增殖和骨稳定性受损形成恶性循环。结构性损伤导致骨折等临床事件。骨转移病灶的持续发展成为新的远端转移起点,进一步扩散。
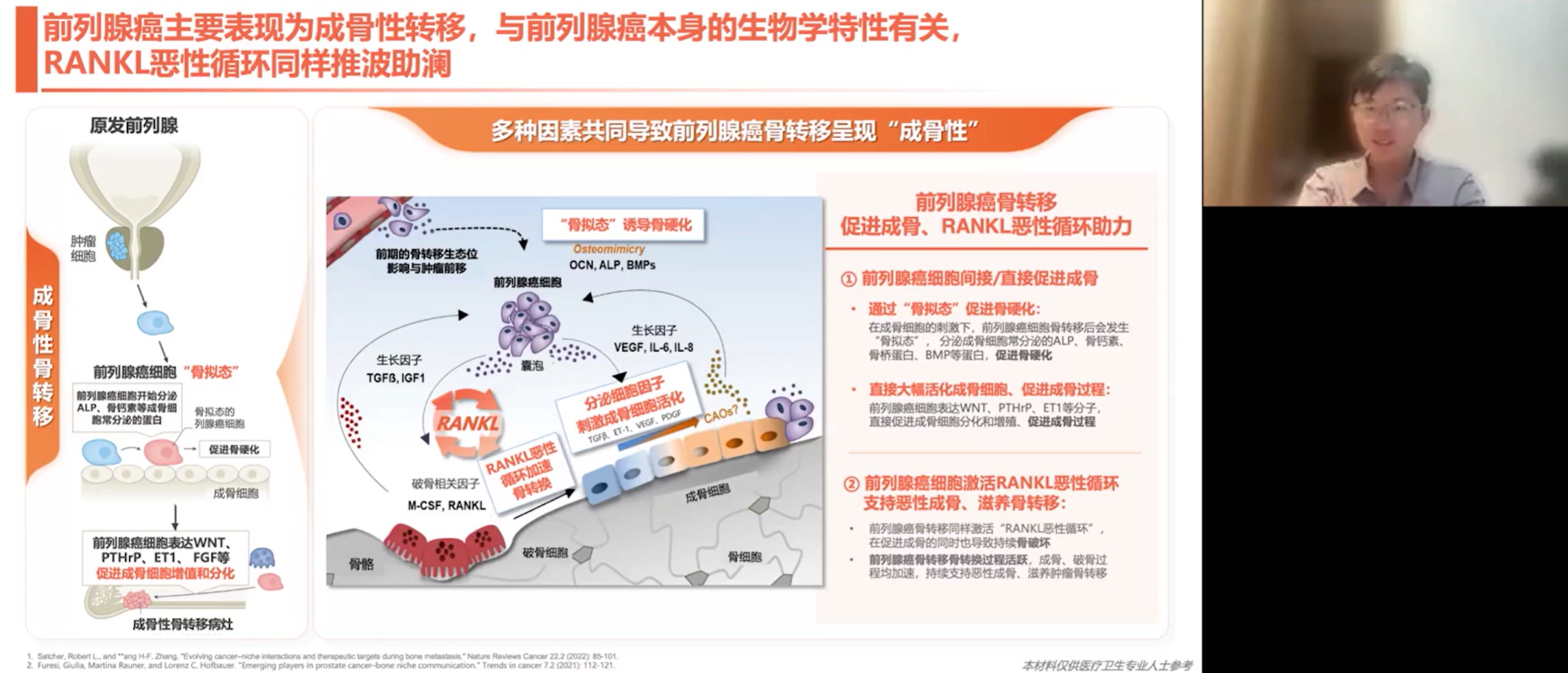
溶骨性病变主要见于乳腺癌和肺癌,而成骨性病变则主要与前列腺癌相关,但乳腺癌和肺癌也可出现成骨性改变。在溶骨性骨转移中,原发灶肿瘤细胞激活一系列溶骨因子,形成恶性循环。这些因子促使成骨细胞分泌RANKL,RANKL与破骨细胞前体表面的RANK受体结合,诱导其分化为成熟的破骨细胞,进而增强其功能和增殖,导致骨质破坏。
成骨性病变主要由前列腺癌细胞通过直接和间接途径促进。一方面,通过“骨拟态”促进骨硬化;另一方面,大幅活化成骨细胞以促进成骨。此外,前列腺癌细胞也能激活恶性循环,支持恶性成骨和肿瘤滋养。这种病理性成骨并非健康的骨骼,而是结构异常的、不健康的骨组织。这种结构异常是导致骨骼机械功能受损的主要原因。
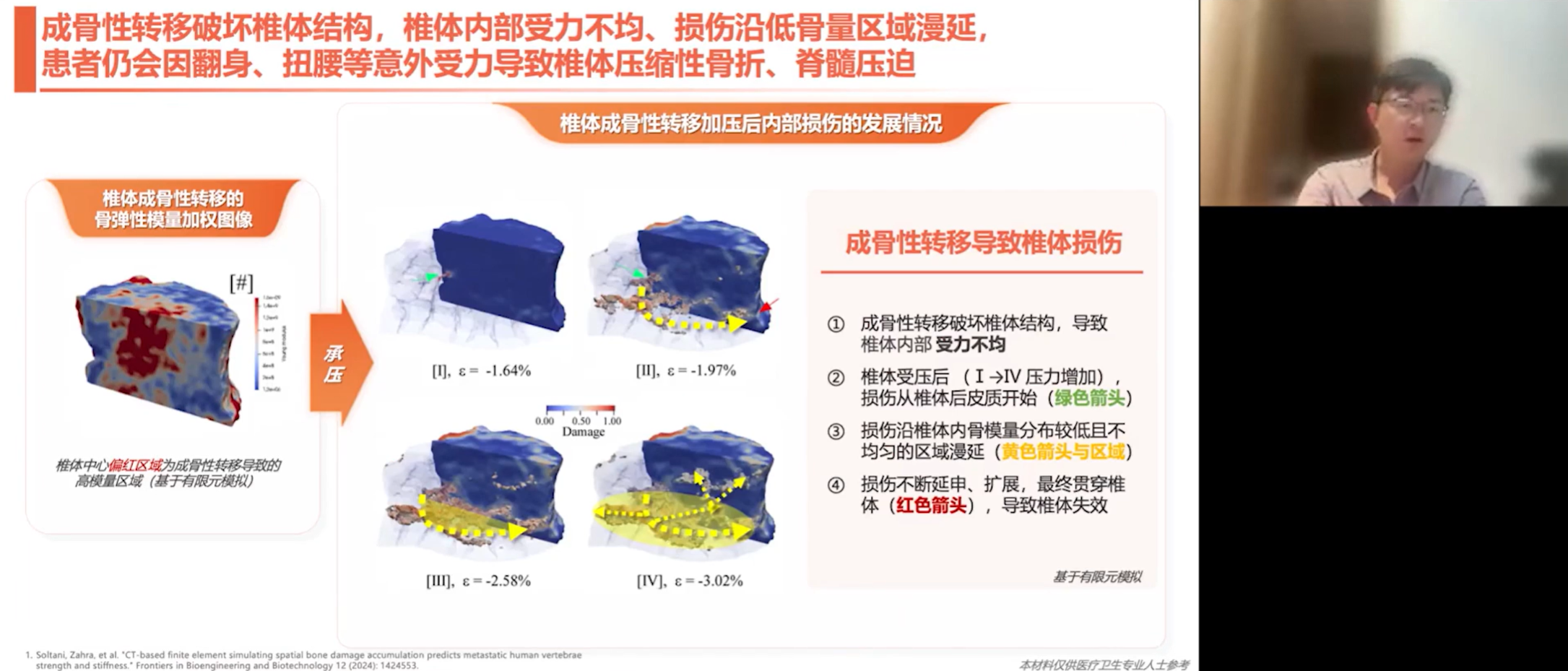
成骨性转移会导致病理性骨折,例如在股骨小转子区域的成骨性病变最终可导致骨的破坏和断裂。在椎体中,成骨性转移会导致椎体中心区域出现弹性模量增高的区域,引起椎体受力不均。当椎体受压时,损伤首先从后皮质开始,随后沿着骨量分布较低的区域蔓延,最终贯穿整个椎体,导致其承重结构失效。对于股骨而言,成骨性转移会影响骨矿化,尽管整体骨密度看似增加,但关键的内侧转子间区域的皮质密度却显著下降,而该区域是股骨承重能力最强的部位,因此增加了骨折风险。
外科干预决策
骨转移的治疗方案包括内科治疗(如地舒单抗)、放射治疗以及外科手术干预。对于脊柱和四肢的骨转移,外科手术可通过切除重建的方式进行治疗。

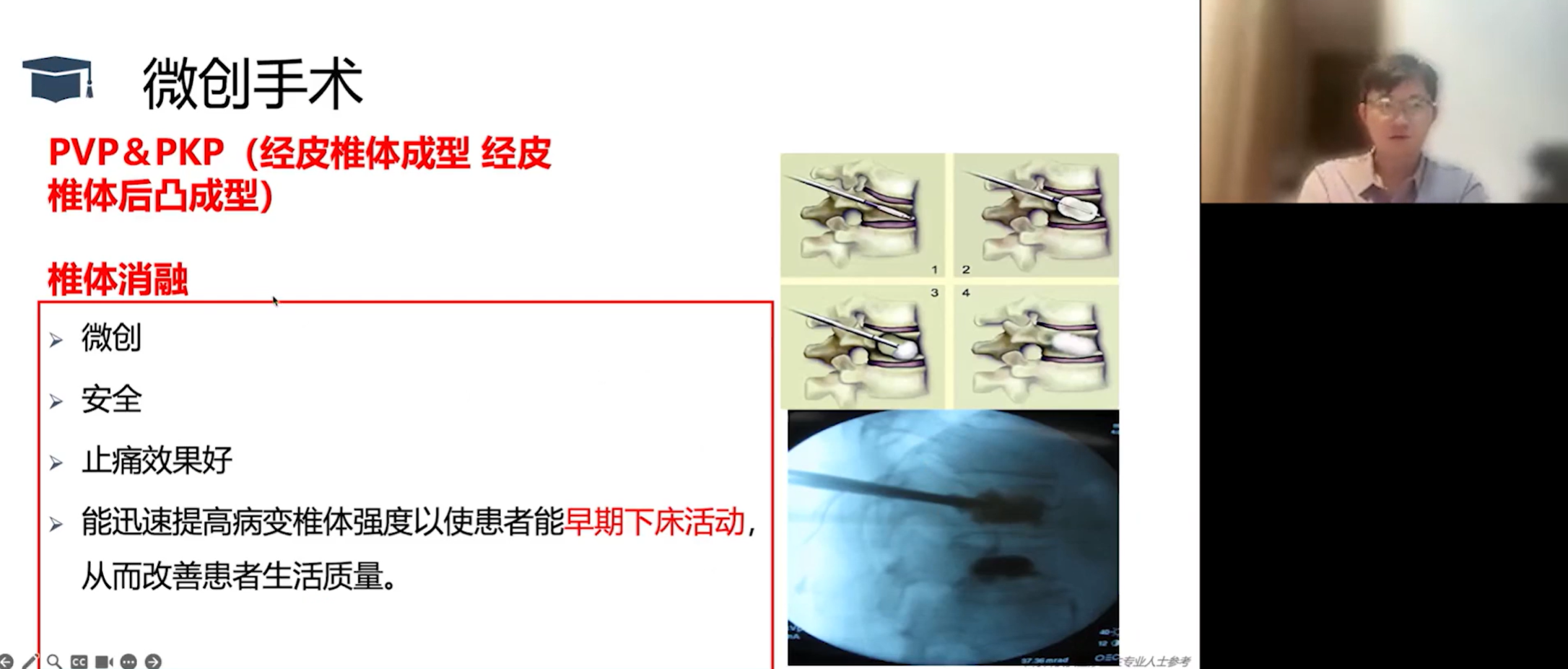
脊柱外科手术技术包括微创的椎体成形术,其中会联合射频微波,冷冻和消融技术;以及开放的分块切除或全脊椎切除术(TES),目前临床上更多采用的是“分离手术(Separation Surgery)”。
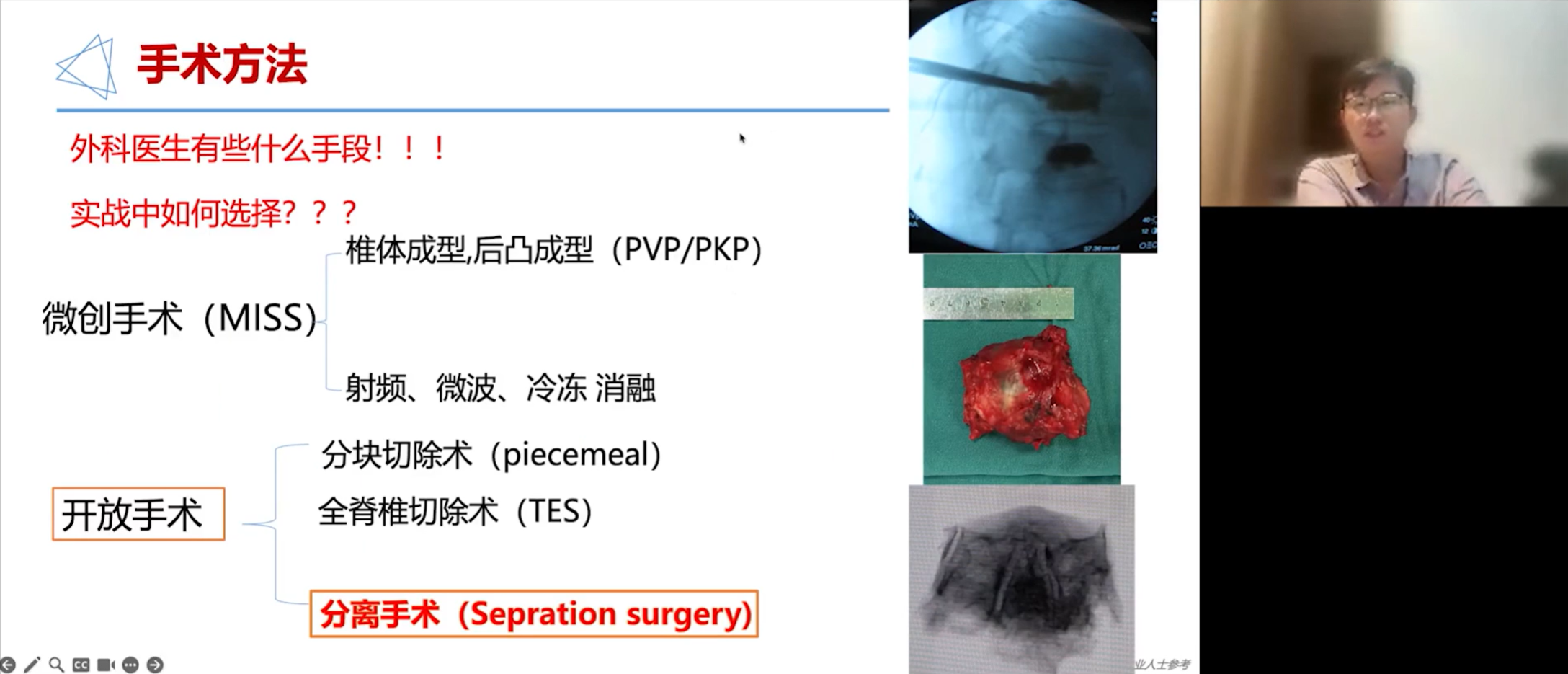
微创手术,如经皮穿刺椎体成形术,通过侧方入路将操作针精准置入椎体中央,注入骨水泥进行填充。该手术切口极小,创伤轻微,患者术后第二天即可下地活动,同时还能获取病理组织。此外,还可联合射频消融等技术,在杀灭肿瘤的同时注入骨水泥,以期达到更好的局部控制效果。
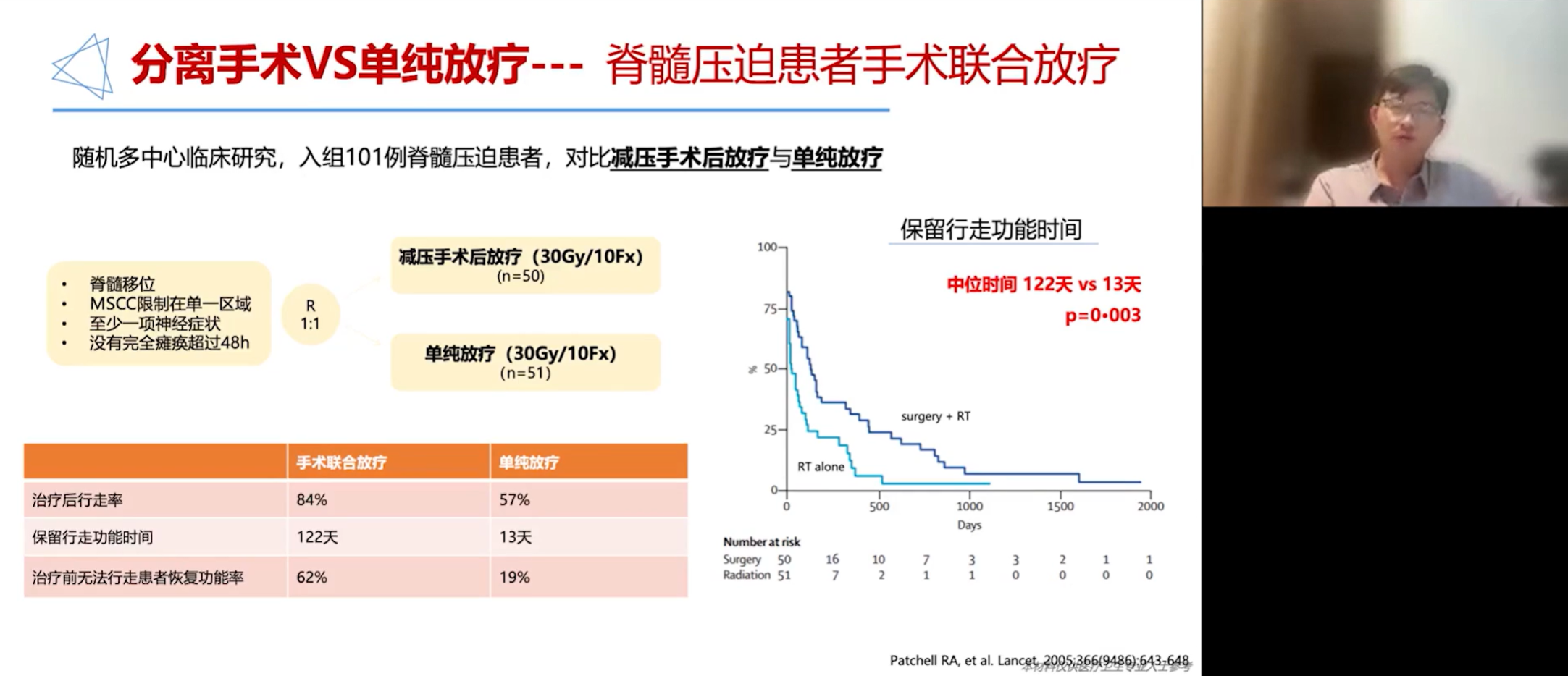
“分离手术”由纪念斯隆-凯特琳癌症中心(MSKCC)于2010年提出,是目前脊柱转移癌治疗中最常用的术式之一。其核心要求是将肿瘤与脊髓彻底分离,术后衔接立体定向放射治疗(SBRT),以实现外科与放疗科“1+1>2”的协同效应。手术要求的分离距离最初为2毫米,但临床实践中通常会达到5至8毫米甚至1厘米以上,为后续大剂量放疗提供足够的安全边界,从而彻底杀灭肿瘤。

与传统的整块切除相比,这种方法创伤更小,患者恢复更快。一项多中心随机临床研究对比了“减压手术+放疗”与“单纯放疗”治疗脊髓压迫患者的效果,结果显示,手术联合治疗组的中位行走功能维持时间为122天,而单纯放疗组仅为13天,差异极其显著。
外科干预的局限性与多学科诊疗案例
尽管分离手术效果显著,但在国内临床应用中仍存在一些局限性:
患者依从性问题:部分患者术后未能及时进行SBRT,导致局部肿瘤复发。
手术技术熟练度:技术不熟练可能导致脑脊液漏等并发症,延长恢复时间,影响后续SBRT的实施。
SBRT普及度:国内SBRT技术普及不足,可能导致局部肿瘤控制效果不理想。
案例一:一位肺癌术后三年的患者,在胸3、胸11和腰3椎体出现高摄取病灶,表现为双下肢活动障碍和不全瘫。影像学显示其胸椎病灶已达到ESCC三级,完全压迫脊髓,脑脊液循环中断。综合评估显示其脊柱处于不稳定状态。最终的治疗方案为“手术+放疗+地舒单抗”的综合治疗。手术采用了混合技术(Hybrid),对相对稳定的上胸椎进行短节段固定和单纯减压,对不稳定的胸腰段则进行了人工椎体置换和四对钉的坚强固定,并在最下方的椎体进行了微创手术。这种结合了三种不同术式的方法,取得了良好的治疗效果。

案例二:一位肺癌术后四个月的患者,在外院接受了胸椎椎体成形术(PVP)后出现病理性骨折和神经压迫。孙正望教授团队为其进行了充分的神经减压、前方椎体挖除及骨水泥填充术。该患者在三年后复发,再次接受了局部肿瘤切除。目前患者状况良好,仍在随访中。

案例三:一位肾癌患者,左上臂疼痛两周,核磁共振检查发现肱骨孤立性转移灶,已发生病理性骨折,疼痛剧烈。为其进行了微创的髓内钉固定,并对病灶进行了开放刮除植骨。术后建议进行局部放疗,但患者未能坚持。在持续使用地舒单抗一年后,影像学显示骨骼出现了恢复性生长。然而,一年后局部肿瘤再次复发。近期,由于费用问题,为该患者设计了肱骨截骨、并利用髓内钉和多个铆钉重建肱骨头外形及肩袖肌腱附着点的方案。术后患者外形与功能恢复良好,仍在随访中。
目前,孙正望教授所在的团队在骨与软组织肿瘤领域的手术技术已十分全面,覆盖了从四肢到躯干的各类肿瘤切除与功能重建,并积极开展导航、3D打印等辅助下的微创与精准手术。针对不同情况的手术方案都已相当成熟,展现了多学科综合治疗在处理复杂骨转移病例中的重要价值。
在骨转移的“恶性循环”中,RANKL信号通路扮演着核心角色。因此,靶向该通路的治疗,如使用地舒单抗等药物,已成为骨转移管理的重要基石。有效阻断RANKL循环,不仅能够显著减少SRE的发生,从而维持患者的骨骼健康和生活质量,更重要的是,越来越多的证据表明,改善骨微环境、抑制破骨细胞的过度活化,还可能与全身性抗肿瘤治疗产生协同增效的作用,进而提升整体治疗的疗效,为患者带来更长的生存获益。
讨论
脊柱转移癌的治疗策略
1. 椎体压缩性骨折的处理:对于近期发生、伴有明显疼痛或导致椎体压缩的病理性骨折,可考虑使用骨水泥(椎体成形术)进行微创治疗。病理性骨折的骨水泥渗漏率很高,可达50%。为降低风险,可采用先进技术,如球囊扩张(后凸成形术)和椎体内支架。
2. 严重脊髓压迫的处理:对于已出现明显脊髓压迫症状(如肢体麻木、无力,甚至瘫痪)的患者,只要尚存感觉功能且身体能耐受,应优先考虑紧急外科手术。核心目标是尽快解除对脊髓的压迫。这不仅能挽救神经功能,还能为后续有效的放疗创造安全距离。
骨转移患者的外科干预指征评估
1. 系统性评估方法:
脊柱稳定性评估(依据SINS评分原则):生理曲度交界处(如颈胸段、胸腰段)的病灶比稳定节段(如中段胸椎)的风险更高,更需要处理。后方附件(关节突)的破坏比单纯椎体破坏更影响稳定;双侧附件破坏比单侧风险更高。溶骨性病变比成骨性更不稳定;椎体压缩超过1/3则需要处理。
四肢长骨骨折风险评估(依据Mirels评分原则):肿瘤侵犯骨骼横断面周径超过1/3至2/3时,通常需要进行预防性内固定。下肢承重骨的干预需求高于上肢。
骨盆稳定性评估:髋臼(二区)病灶影响承重,但大型手术创伤大。可采用打骨水泥等微创方式处理。骶髂关节(四区)是关键的承重结构,一旦破坏极不稳定。放疗难以重建其稳定性,手术干预的效果通常更优。
2. 疼痛点的评估:对于多发骨转移且痛点不固定的患者,需通过仔细的物理查体来确定最主要的疼痛部位,结合影像学表现,针对性地进行局部微创治疗。
骨保护药物相关并发症的管理:颌骨坏死(ONJ)的预防
地舒单抗和双膦酸盐类药物均有导致颌骨坏死的风险(发生率约1%-12%)。
口腔卫生是关键:临床研究表明,口腔卫生状况与颌骨坏死的发生密切相关。必须嘱咐患者保持良好的口腔卫生。
牙科操作的管理:如需进行拔牙等有创牙科操作,建议遵循“前三后三”原则,即操作前停药三周,操作完成后再停药三周,以最大限度降低风险。
治疗理念的演进:
针对骨转移的外科治疗已从过去出血量大、恢复慢的大型开放手术,发展到更多地采用微创技术。现代手术的目标是“手术越小越好”,旨在通过微创方式快速解决如疼痛、濒临骨折、神经压迫等关键问题,使患者能够迅速康复,并及时回归到相应科室接受后续的全身系统性治疗。骨转移的治疗,关键在于“早诊早治”。应尽早、规范地使用地舒单抗等骨保护药物进行干预,这不仅能从机制上有效抑制骨破坏、推迟并降低病理性骨折、脊髓压迫等SRE的发生率,对于延长患者生存期、显著改善其生活质量也至关重要。
排版编辑:肿瘤资讯-IRIS











 苏公网安备32059002004080号
苏公网安备32059002004080号


