随着社会老龄化进程的加速以及医疗技术的日新月异,我国恶性肿瘤的发病率持续居高不下。值得注意的是,在靶向治疗、免疫治疗等先进手段广泛应用下,原发肿瘤得到了前所未有的有效控制,患者的生存期被显著延长。随之而来的是肿瘤骨转移的发生风险攀升,其带来的疾病负担亦日益沉重。
近期,在由基金会举办的三方研讨会上,温州医科大学附属第一医院陈雷教授对恶性肿瘤骨转移的预防和治疗进行了深入浅出的解析。他回溯临床实践演变时指出,既往临床医生面对骨转移患者常感束手无策,甚至无奈地劝慰病人“该吃吃该喝喝,回家吧”。但时至今日,我们已经进入了“与瘤共存”的新时代,骨转移已不再是终末期的代名词,而是成为一个需要长期管理、积极干预的临床挑战。
点击观看完整视频
骨转移的生物学根基:“种子与土壤”的现代诠释
恶性肿瘤的骨转移并非一个随机过程,其背后蕴含着深刻的生物学逻辑。早在1889年,Stephen Paget教授便在《柳叶刀》发文提出了经典的“种子与土壤”假说,他将肿瘤细胞比作“种子”,而将特定器官的微环境视为其赖以生长的“土壤”。这一理论至今仍是解释器官选择性转移的核心。
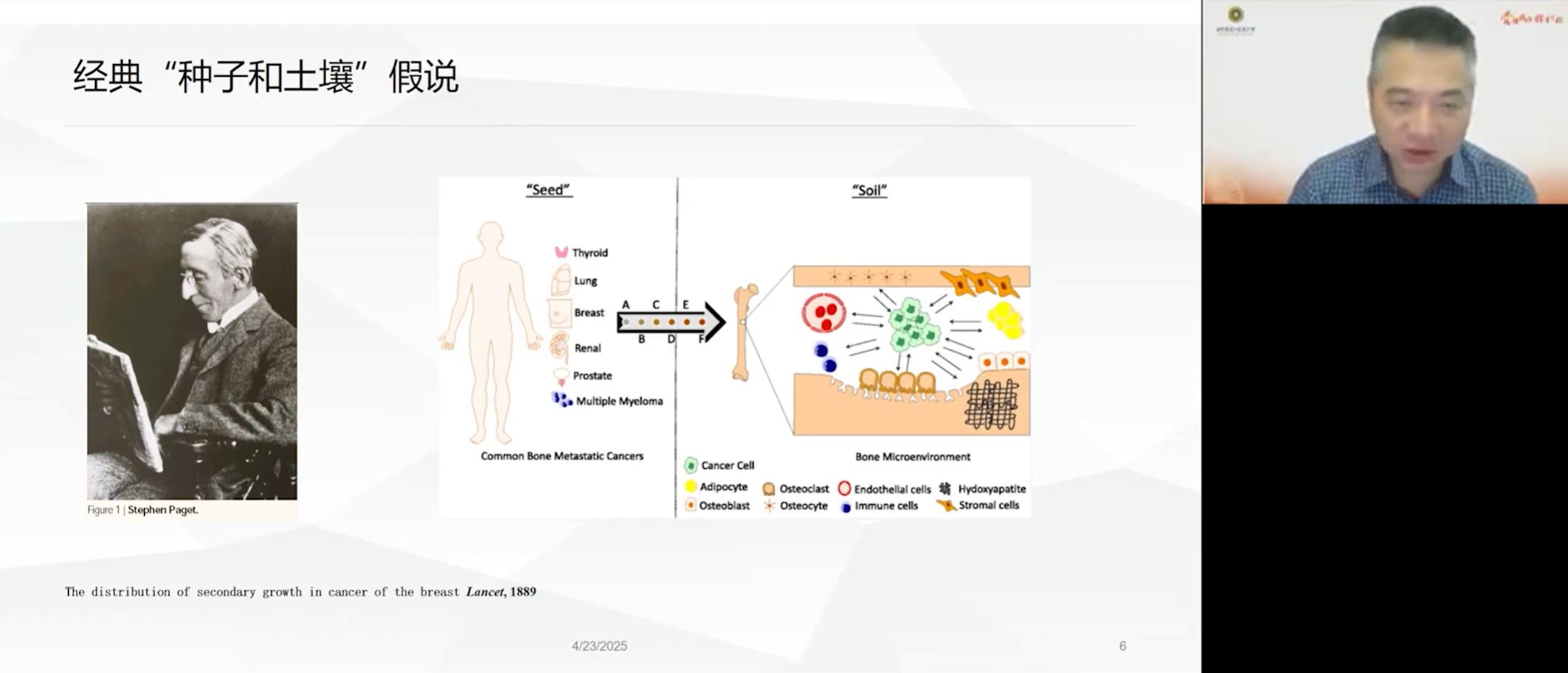
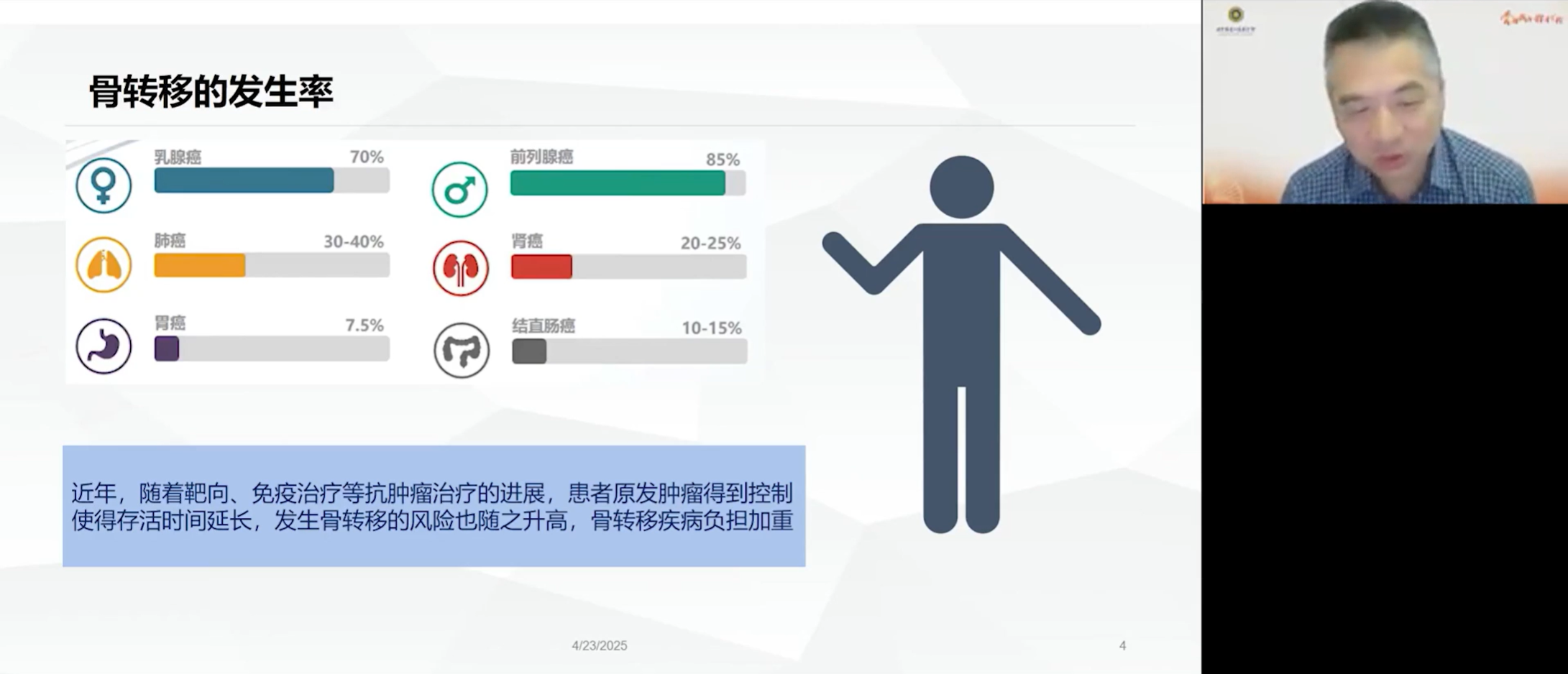
乳腺癌(70%)、前列腺癌(85%)、肺癌(30-40%)等特定癌种的“种子”,似乎对骨骼这片“土壤”情有独钟。而关于骨转移的好发部位,中轴骨是其主要“目的地”,其中脊柱(87%)、肋骨(77%)和骨盆(63%)尤为常见,其次是股骨与肱骨的近心端(53%)。相比之下,肘、膝关节以下的远端骨骼则极为罕见。
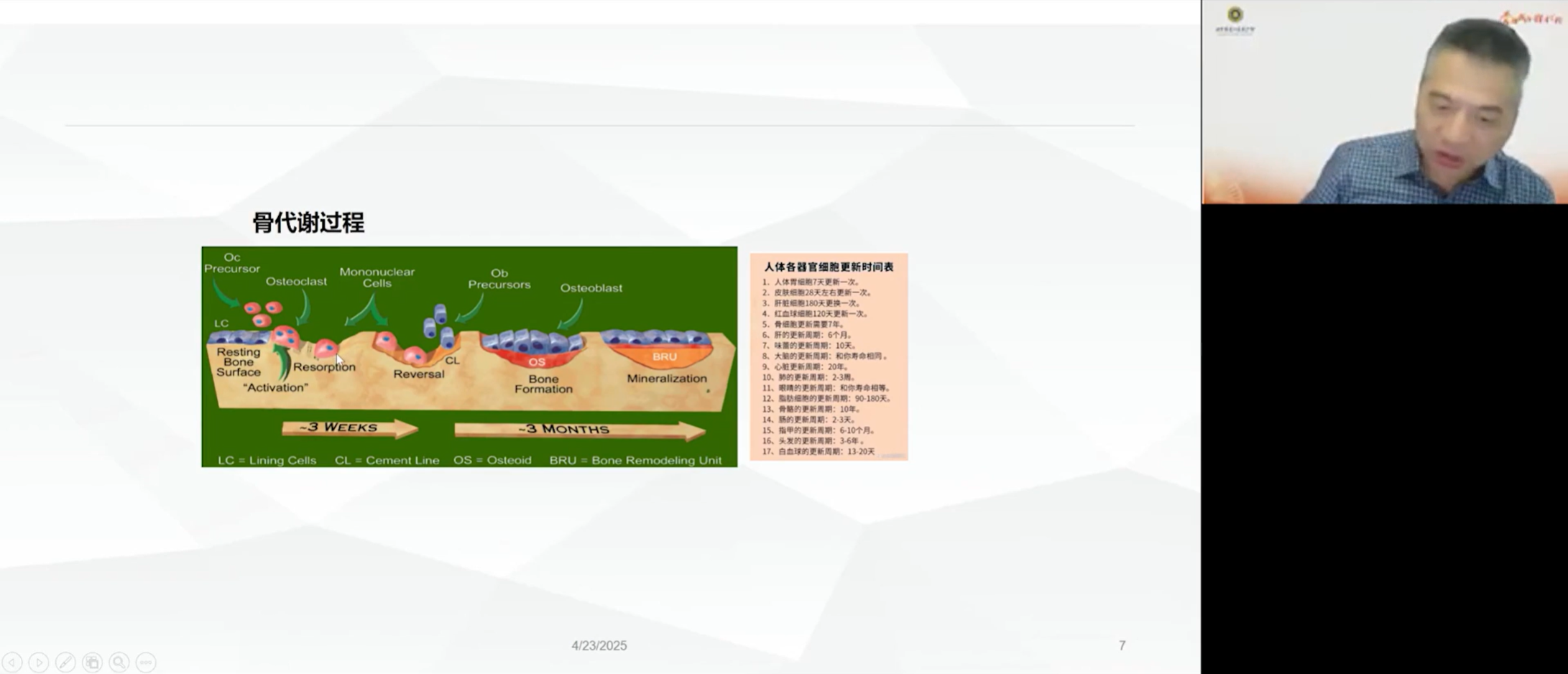
要阐明肿瘤细胞在骨骼定植的机制,需深入解析骨骼的动态平衡系统。骨骼并非静止的器官,它以大约十年的周期完成一次彻底的自我更新,这一过程被称为“骨重建”。骨重建依赖于两种核心细胞的协同作用:破骨细胞(Osteoclasts)与成骨细胞(Osteoblasts)。破骨细胞源自造血干细胞,负责吸收、分解陈旧的骨质,过程约需三周;而成骨细胞则源自间充质干细胞,负责形成新的骨质,周期长达三个月。可见,这是一个“破骨快,成骨慢”的过程。
这一平衡的维系,关键在于一个名为“RANKL/RANK/OPG”的信号轴。成骨细胞分泌的RANKL(核因子κB受体活化因子配体),与前破骨细胞表面的RANK受体结合,驱动其分化成熟。与此同时,骨保护素(OPG)作为可溶性诱饵受体,通过竞争性结合RANKL阻断该通路。在生理状态下,雌激素、降钙素等会促进OPG的分泌,抑制骨破坏;而在病理微环境(如炎症或肿瘤浸润)中,炎性因子风暴则显著上调RANKL分泌,导致破骨活性失控性增强,加速骨质破坏进程。
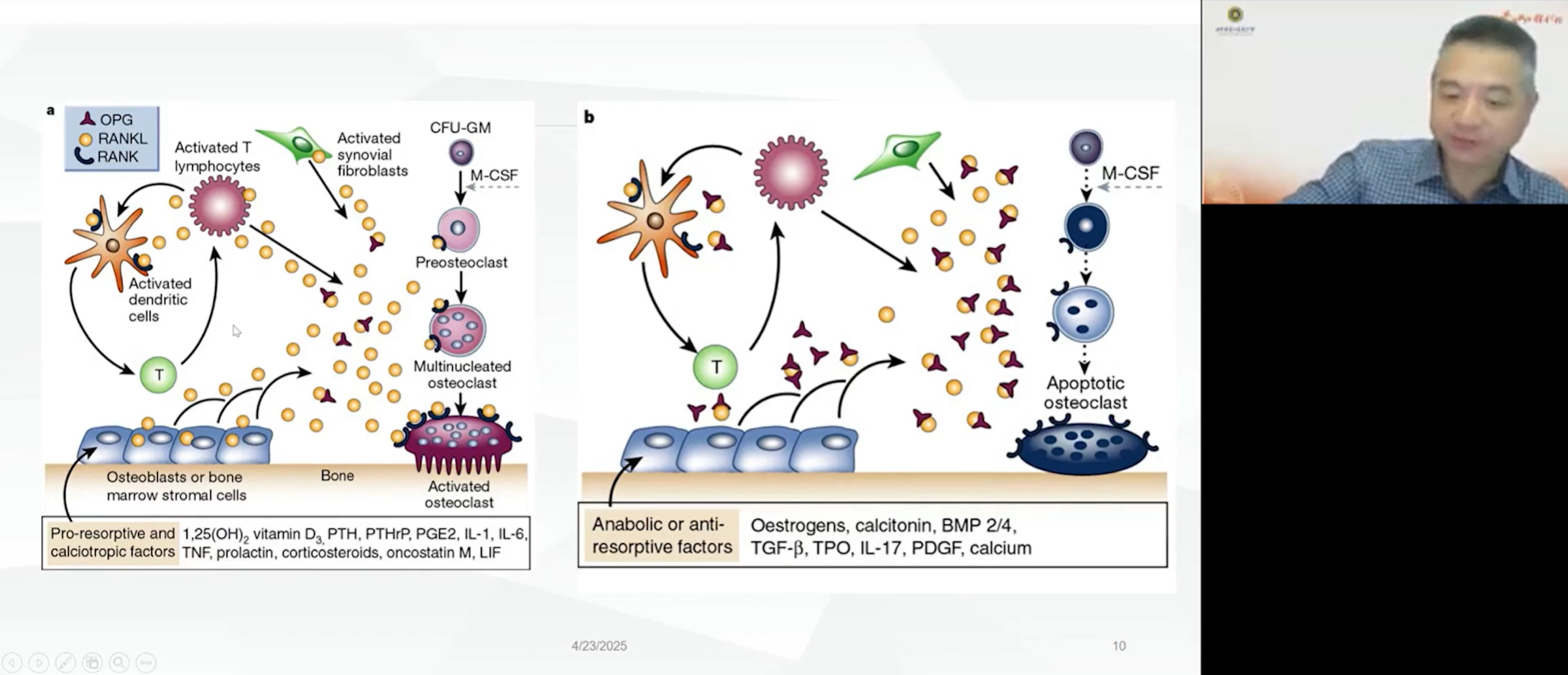
当肿瘤这颗“种子”落入骨骼这片“土壤”时,上述生理平衡便被彻底打破。肿瘤细胞自身会分泌甲状旁腺激素相关蛋白(PTHrP)、多种白介素及肿瘤坏死因子-α等细胞因子。这些因子一方面直接刺激成骨细胞表达RANKL,另一方面募集肿瘤相关巨噬细胞及T细胞协同扩增RANKL分泌。RANKL的急剧增加导致破骨细胞被过度激活,溶解骨质。破骨细胞通过分泌蛋白水解酶来消化骨基质中的胶原纤维,同时营造酸性环境来溶解骨盐。这一过程不仅破坏了骨骼结构,更重要的是,它会从被溶解的骨基质中释放出储存的生长因子。这些生长因子反过来又成为滋养肿瘤细胞的“养料”,刺激其进一步增殖。

由此,一个自我强化的恶性循环便形成了,导致骨破坏愈演愈烈。这便是溶骨性转移的核心机制。而在成骨性转移中(典型如前列腺癌),肿瘤细胞通过分泌内皮素-1等因子,过度刺激成骨细胞,导致其产生大量结构脆弱的新骨,同样形成了恶性循环。少数情况下肺癌会刺激成骨,形成混合性转移。

骨相关事件(SREs):骨转移的临床危害与疾病负担
肿瘤对骨骼的侵蚀性破坏,最终会演变为一系列严重的临床后果,我们将其统称为骨相关事件(Skeletal-Related Events, SREs)。
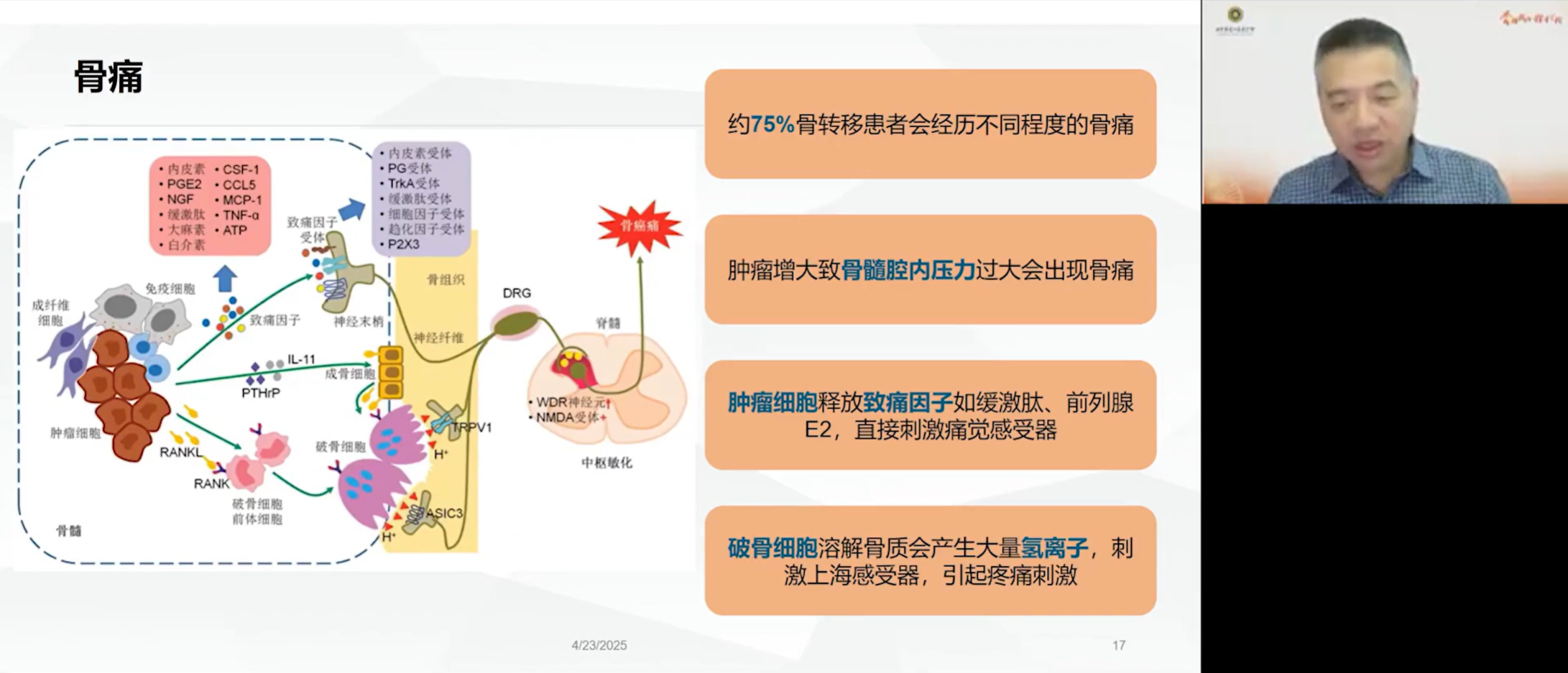
骨痛的发生涉及多重病理生理机制协同作用。首先,破骨细胞在溶骨时产生的酸性微环境,其释放的大量氢离子本身就是强烈的致痛物质。其次,肿瘤细胞和周围的免疫细胞会分泌前列腺素E2、缓激肽等致痛介质,这些物质不仅直接刺激神经末梢,更能“敏化”疼痛感受器,使其反应阈值降低,从而放大疼痛信号。此外,肿瘤在骨髓腔内的生长会增加内部压力,形成机械性压迫,同样引发剧痛。
高钙血症往往见于广泛溶骨性转移。当大量破骨细胞同时活跃时,骨骼中储存的钙离子被迅速释放入血,超出机体的代偿能力,便会引发高钙血症。值得警惕的是,对于已存在高钙血症的患者,在使用地舒单抗等强效骨保护药物时,由于药物迅速抑制了破骨细胞活性,可能导致血钙水平急剧下降,甚至引发症状性低钙血症,临床上需要密切监测。

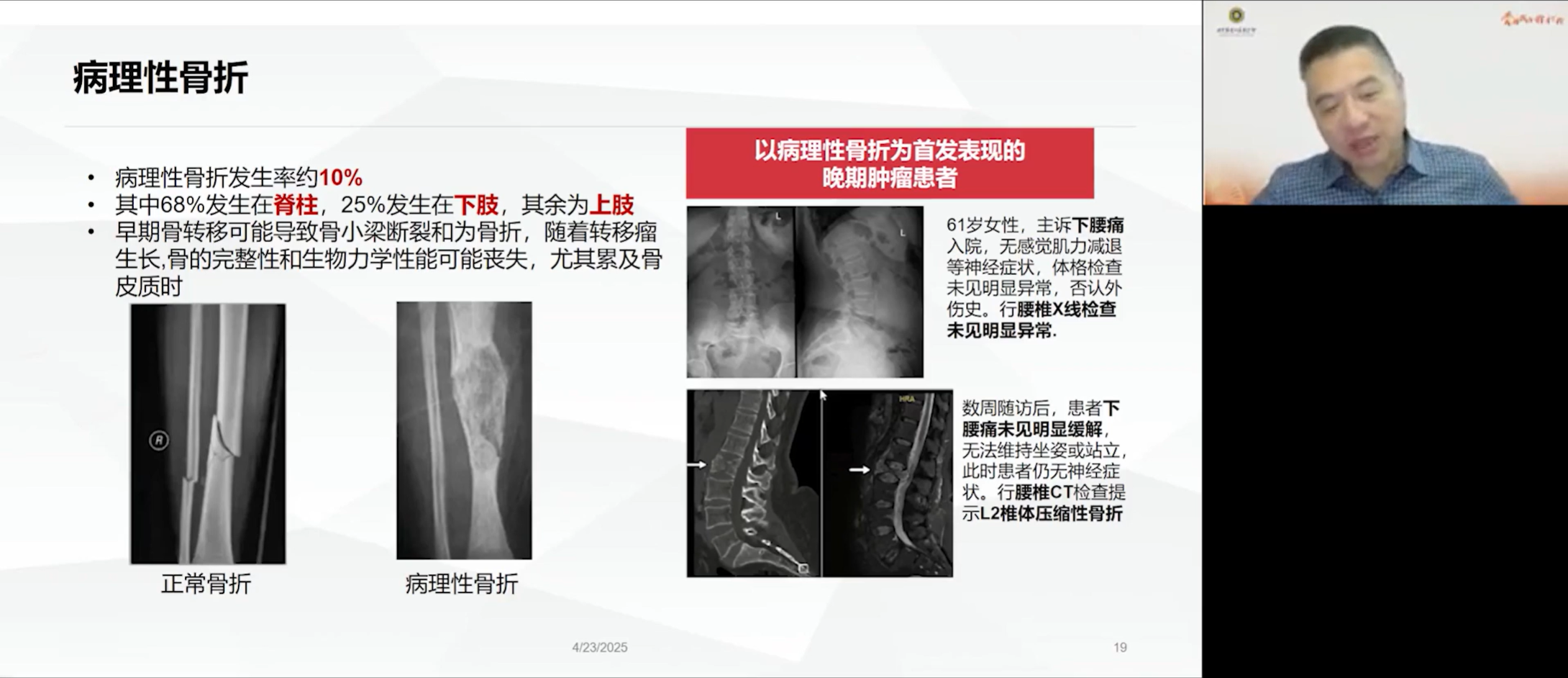
当局部骨质被严重破坏后,骨骼的结构完整性下降,即使是轻微外伤或正常的生理活动也可能导致骨折,我们称之为病理性骨折。病理性骨折总体发生率约为10%,其中近七成发生在脊柱,25%-30%发生在下肢承重骨。与创伤性骨折清晰的骨折线不同,病理性骨折的影像学表现为骨质结构的紊乱与破坏。
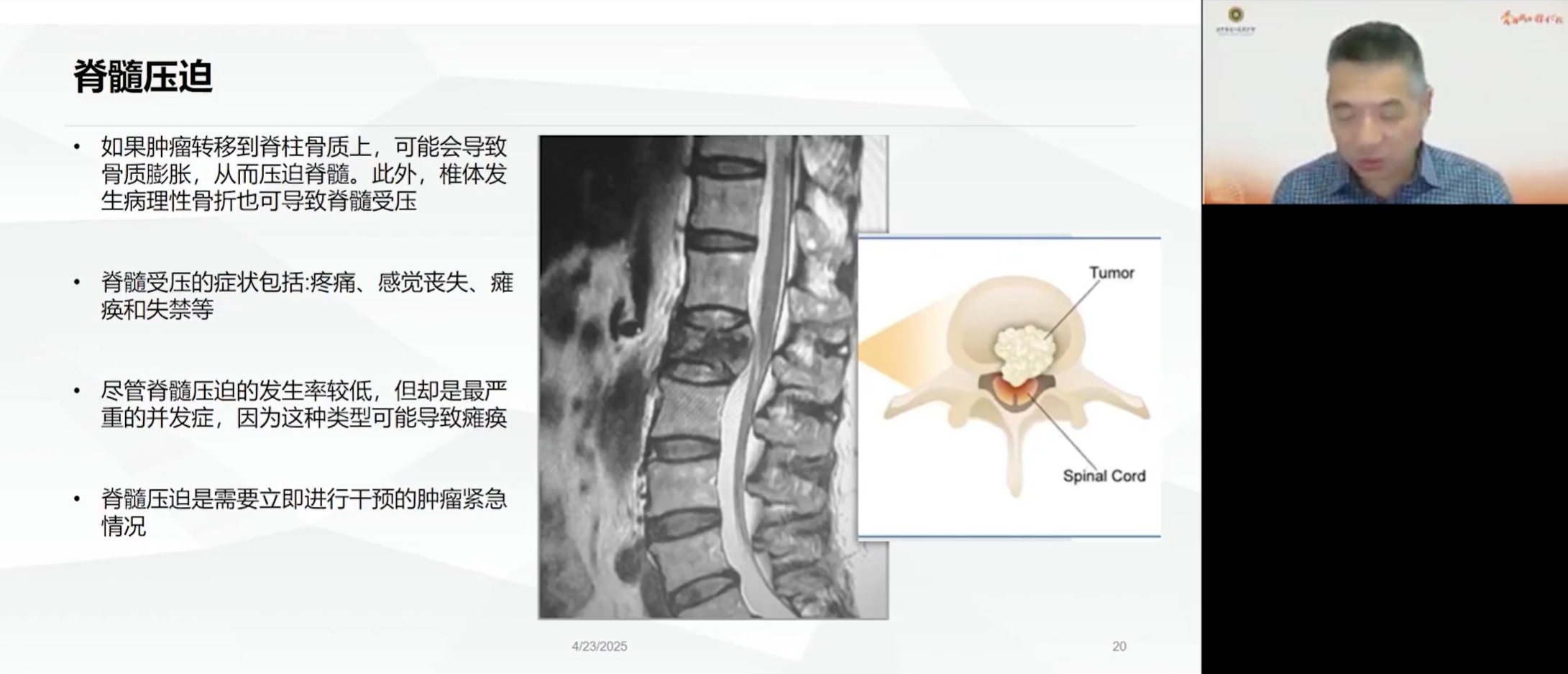
脊柱是最常见的转移部位,约占所有骨转移的60%以上。肿瘤通过侵蚀椎体后缘皮质直接侵入椎管,或病理性骨折致椎体塌陷形成后移的骨折碎片,均可导致脊髓压迫。高位脊髓(如颈椎、胸椎)受压引起的症状更为严重,因为这些节段的脊髓耐受性差,一旦受损可能导致截瘫。相比之下,腰1椎体以下的椎管内是马尾神经束,其耐受性相对较强,但受压同样会引起严重的神经功能障碍。
在骨相关事件(SREs)的四类主要临床表现中,病理性骨折、脊髓压迫及高钙血症具有客观诊断标准,故被确立为骨靶向药物临床试验的主要疗效终点。而骨痛由于其主观性较强,通常需要结合客观的干预措施(如放疗)来进行评估。这些事件的发生不仅是疾病进展的独立预测因子,更是影响患者生存质量的核心指标。

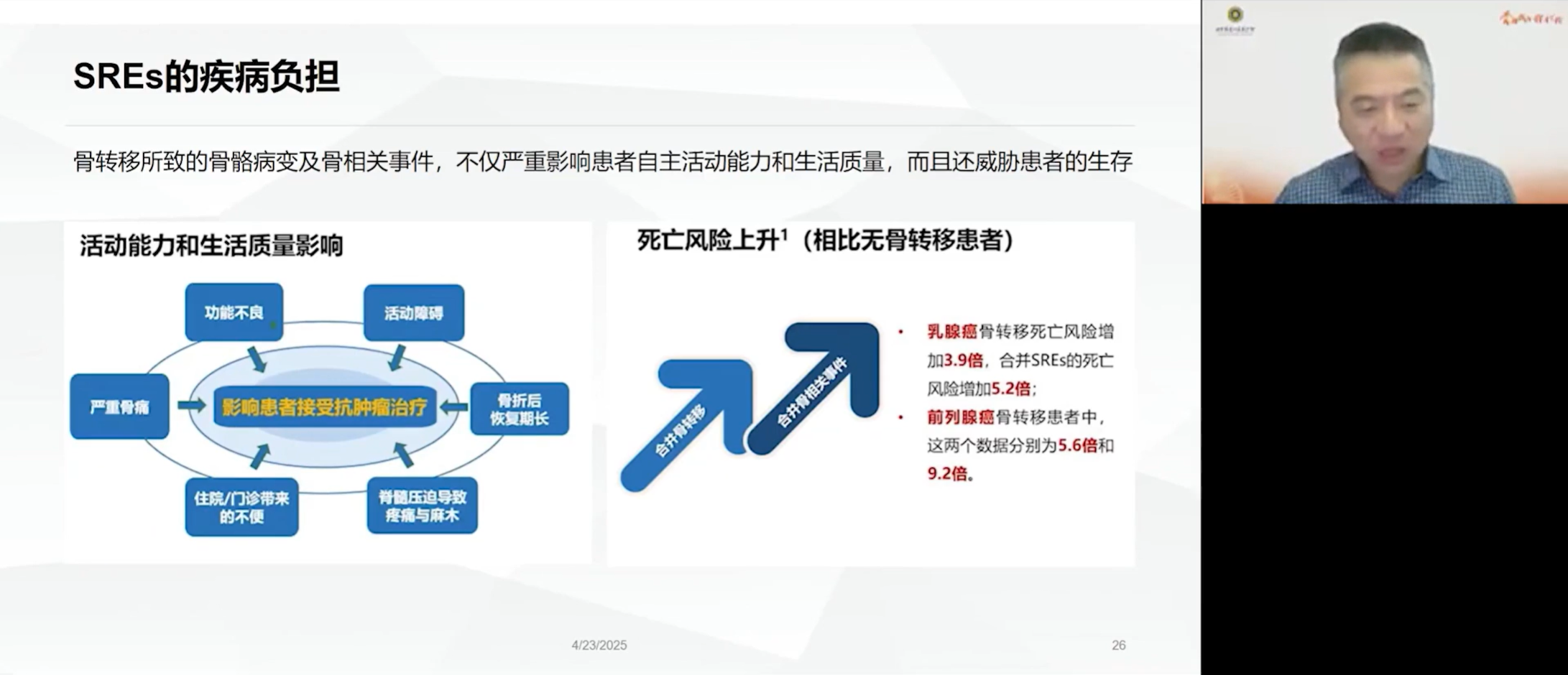
SREs的发生,为患者带来了沉重的疾病负担。它不仅严重影响患者的生活质量,更会动摇其治疗信心,甚至可能因行动不便而中断或延迟关键的全身性抗肿瘤治疗。SREs作为患者死亡风险的独立预测因子,与无骨转移的乳腺癌患者相比,发生骨转移者的死亡风险增加3.9倍,若发生SRE则升至5.2倍;前列腺癌中相应风险达5.6倍与9.2倍。这并非因为骨转移本身直接致命,而是SREs严重削弱了患者接受有效治疗的能力与依从性,从而间接缩短了其生存时间,故预防SREs具有生存获益与生活质量改善的双重临床价值。
骨转移的综合诊疗策略:多学科协作下的个体化管理
骨转移的综合诊疗目标包含三层级:首要阻断肿瘤驱动的骨破坏恶性循环(如抑制RANKL介导的破骨活化),其次预防并处置骨相关事件(SREs)以修复骨质结构,终极目标在于提升患者生存质量并保障后续抗肿瘤治疗的实施。这需依托多学科团队(MDT)构建动态治疗路径。
诊断是治疗的基石。过去作为初筛手段的全身骨扫描(ECT),因其假阳性率高,现已不再作为确诊依据。目前,X线/CT能清晰显示骨质破坏,是评估骨折风险的利器;PET-CT兼具功能与解剖成像优势,特异度和敏感度俱佳;而MRI则凭借其卓越的软组织分辨率,成为评估脊髓受压和脊柱稳定性的“金标准”。此外,骨活检作为诊断的“金标准”,其价值已远超确诊本身。通过获取转移灶组织进行基因检测等分子病理分析,我们可以判断肿瘤是否发生耐药或出现了新的治疗靶点,从而为后续的个体化治疗提供精准导航。

治疗手段上,抗肿瘤治疗是根本,而骨保护药物则是阻断骨破坏恶性循环的核心武器。目前主流的骨保护药物分为两大类。一类是以地舒单抗为代表的RANKL抑制剂。地舒单抗是一种全人源单克隆抗体,它能精准地结合并中和RANKL,从源头上阻断破骨细胞的活化,其作用机制如同为骨骼系统补充了天然的“骨保护素”。另一类是含氮双膦酸盐,它们能特异性地吸附于骨表面,被破骨细胞摄取后,通过抑制其关键代谢通路,诱导其凋亡。荟萃分析显示,在预防SREs方面,地舒单抗相较于安慰剂可降低51%的风险,其疗效优于唑来膦酸等双膦酸盐类药物。
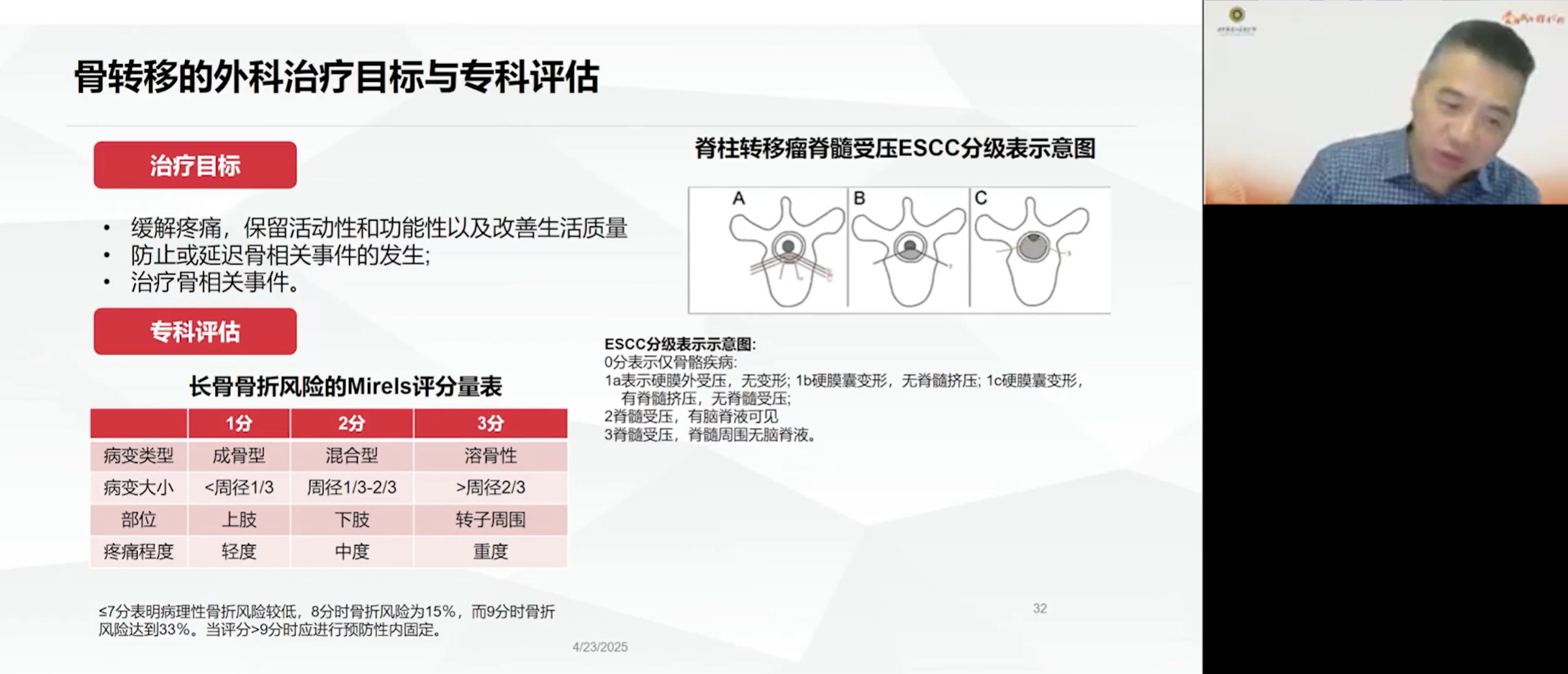
外科治疗的目标在于处理或预防迫在眉睫的SREs。对于长骨,我们可以使用Mirels评分系统来量化病理性骨折的风险,当评分>9分时,骨折风险高达33%,应果断进行预防性内固定。临床上曾有一例股骨存在巨大溶骨性病灶的患者,本应在穿刺活检时同步进行内固定,却错失良机,最终在活检后不久便发生骨折,付出了更大的代价。对于脊柱,ESCC分级系统则用于评估脊髓受压程度,一旦出现2级以上的压迫,即应积极考虑手术减压。外科干预的原则是,在患者预期生存期允许的前提下,通过坚强的内固定重建骨骼稳定性,使其在生存期内无需再次翻修,且手术重建需要涵盖被破坏骨质全长。
放射治疗同样是局部控制的重要手段。根据患者的预期生存期和病灶情况,可选择根治性高剂量放疗或姑息性低剂量放疗。但需注意的是,对承重骨进行放疗可能在短期内增加骨折风险,需要审慎评估。

总结
恶性肿瘤骨转移的诊疗策略已实现从被动应对到主动干预的范式转变,其核心在于深刻理解肿瘤与骨骼微环境相互作用所形成的“恶性循环”,并以其为靶点进行干预。通过多学科团队的协作,灵活运用影像学诊断、骨保护药物、手术、放疗等多种手段,为每一位患者制定个体化的治疗方案,我们不仅能够有效缓解患者的痛苦,更能维持其功能、改善其生活质量,最终为其赢得更长的生存时间与更优的生命尊严。
讨论环节要点精析
成骨性骨转移的治疗:
成骨性转移的启动过程仍需破骨细胞参与,且肿瘤细胞会分泌促成骨因子,形成恶性循环。因此,对于确诊的成骨性骨转移,仍需使用骨保护药物(如地舒单抗或双膦酸盐)。
许多成骨性转移随时间推移可能转变为溶骨性转移。
核素治疗对成骨性转移效果较好,是一种有前景的治疗方式。
特殊部位骨转移的处理:
对于胸三椎体等风险较高的部位,椎体成形术(注射骨水泥)是可行的,但风险较高,可借助机器人辅助等技术提高精准度。
射频消融是另一种有效的治疗方法,通过椎弓根插入电极进行治疗。
骨转移的手术时机:
对于“寡转移”(少数转移灶),可考虑根治性手术。
若为广泛转移,则以姑息性治疗为主。
骨保护药物的使用:
确诊骨转移后尽早启用骨保护药物,可有效延缓SRE发生,对于改善患者生存质量与预后有着重要价值。
用药前需检测血钙,常规补充钙剂和维生素D。已有高钙血症的患者,在使用骨保护药物后发生低钙血症的风险更高。
目前对于骨保护药物的疗效评估和停药尚无统一标准。
推荐疗程为两年。若计划停用地舒单抗,建议序贯使用双膦酸盐以避免骨密度“断崖式”下降的反弹效应。病情稳定后可考虑延长给药间隔。
排版编辑:肿瘤资讯-IRIS











 苏公网安备32059002004080号
苏公网安备32059002004080号


