2024年12月23日,中国国家药品监督管理局(NMPA)正式批准莫妥珠单抗(mosunetuzumab)单药用于治疗既往接受过至少两线系统性治疗的复发或难治性滤泡性淋巴瘤(R/R FL)成人患者。据悉,莫妥珠单抗是全球首款获批用于FL治疗的双特异性抗体,是创新的人源化1:1 CD20/CD3双特异性抗体,其“即诊即用”的便捷性和固定周期的治疗模式,为R/R FL患者带来了新的曙光。
为进一步提升广大医疗工作者对双抗药物的了解,提升双抗药物临床应用的规范化水平,【肿瘤资讯】特别推出“全景双抗”医生教育专栏,旨在赋能医患,助力解锁治愈密码。本期特邀复旦大学附属肿瘤医院陶荣教授,结合其专业见解及相关研究,深度解读莫妥珠单抗的结构特点、机制优势及其临床价值,以期提升临床医生对这一创新疗法的认知与应用水平,为R/R FL患者带来更优治疗选择。

结构精粹,匠心独运:莫妥珠单抗的分子设计与临床意义
FL是最常见的惰性B细胞淋巴瘤,其病程反复。R/R FL患者生存期随复发次数增多而缩短,第3次复发后中位PFS仅7.1个月[1]。再者,约20%的患者发生早期进展(POD24),5年OS率仅50%[2],且该类患者尚无统一的标准治疗。机制探索提示R/R FL的发生并非取决于单一因素,与肿瘤免疫微环境改变相关,如肿瘤抗原丢失[3]、T细胞数目减少及功能受损[4]等。这构成了R/R FL治疗的巨大挑战。
面对R/R FL的治疗困境,现有治疗如CD20单抗、小分子靶向药及CAR-T疗法均取得一定成效,但仍存在局限。莫妥珠单抗作为一种人源化1:1 CD20/CD3双特异性抗体,其分子结构的精巧设计是其临床优势的核心。它能同时靶向B细胞的CD20和T细胞的CD3,精准重定向T细胞杀伤肿瘤[5]。陶荣教授指出,莫妥珠单抗的结构设计体现了高度的工程化智慧。首先,它保留了经过“沉默处理”的Fc段,这赋予了其更优的结构稳定性和显著延长的半衰期,支持了临床间歇给药,方便管理;其次,通过关键的N297G氨基酸位点置换,有效消除了Fc段介导的ADCC效应,避免了对免疫系统的非特异性过度激活,提升了药物的整体安全性。这种设计使得莫妥珠单抗即便在FL患者CD20表达降低或效靶比较低时,仍能保持强大的肿瘤杀伤能力(图1)[5, 6]。”
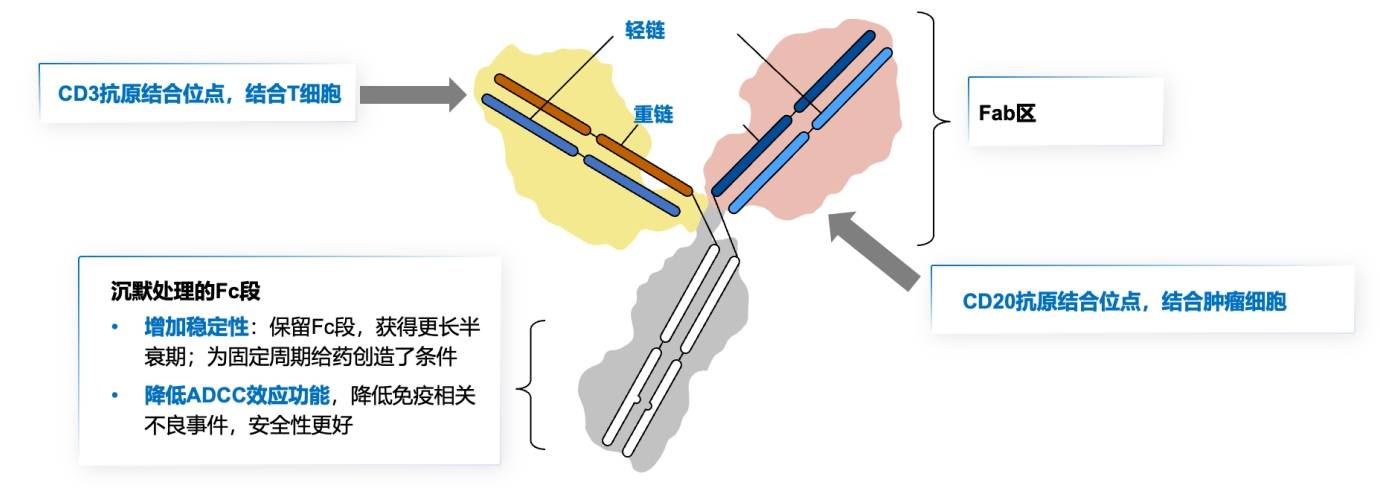
这些结构特点共同赋予了莫妥珠单抗优异的临床潜能。陶荣教授总结道:“莫妥珠单抗这种兼顾了结构稳定性、作用持久性与高安全性的分子设计,为其临床上展现卓越疗效和良好耐受性奠定了坚实的分子基础,为R/R FL患者提供了极具价值的全新治疗选择。”
机制卓越,效能彰显:莫妥珠单抗克服治疗挑战的独特优势
莫妥珠单抗凭借其独特的结构设计与精准的T细胞重定向杀瘤机制,在克服肿瘤免疫逃逸,尤其是在CD20表达降低或T细胞功能障碍等复杂临床情境下,展现出较传统CD20单抗的显著优越性。
传统CD20单抗疗效易受患者免疫细胞功能及肿瘤CD20表达量的影响。莫妥珠单抗则通过更为直接和主动的方式发挥作用。陶荣教授深入剖析道:“莫妥珠单抗的核心机制在于其‘分子桥梁’作用,将患者自身T细胞‘强制’招募至表达CD20的肿瘤B细胞周围,形成高效免疫突触。这种连接直接触发T细胞活化、增殖,并促进其释放穿孔素和颗粒酶等细胞毒性分子,对恶性B细胞进行直接、高效的清除。这实现了对肿瘤的‘精准打击’(图2)[5, 6]。”
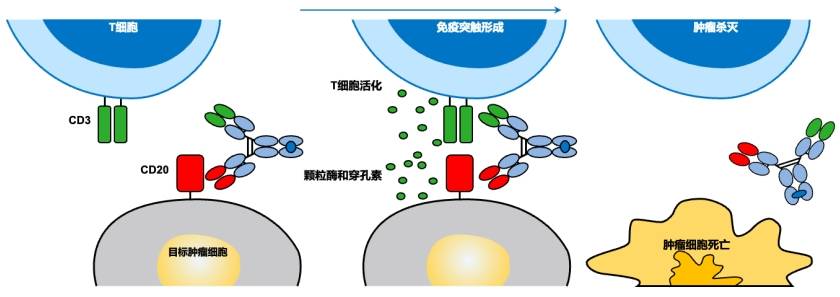
莫妥珠单抗在应对T细胞功能不足方面具有独到之处。临床中晚期或多线治疗后的R/R FL患者常出现T细胞数量减少或功能衰竭[7]。莫妥珠单抗即使在效靶比极低至1:18的条件下,仍能有效激活并扩增T细胞,重新赋予其杀伤肿瘤的活力[5]。这在很大程度上克服了传统抗CD20抗体因T细胞功能障碍或数量不足而疗效受限的瓶颈(图3)。
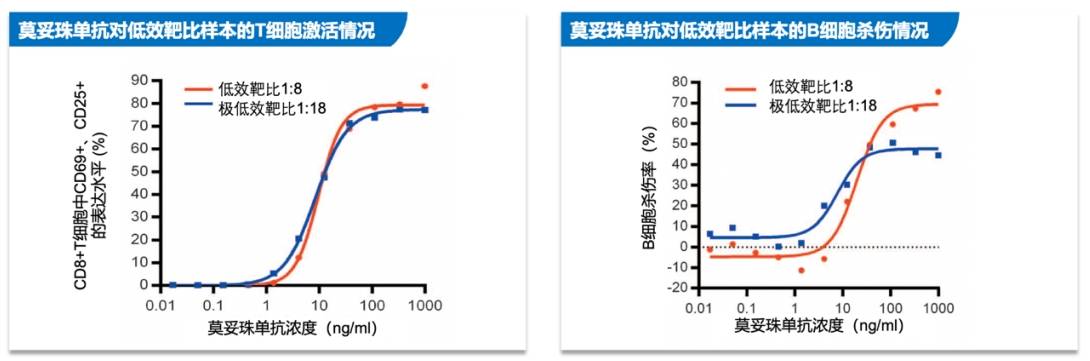
对于因CD20表达下调而导致的肿瘤耐药,莫妥珠单抗也展现出其应对能力。体外实验表明,莫妥珠单抗对CD20低表达肿瘤细胞系EC50 <10 ng/ml,证明其仍有较强的杀灭作用[5]。陶荣教授补充说:“即使在CD20表达水平相对较低的FL亚型中,莫妥珠单抗依然能够介导显著的抗肿瘤活性。甚至在体外及小鼠体内试验中观察到,即便预先存在低浓度的利妥昔单抗,莫妥珠单抗的抗肿瘤作用也几乎不受影响 ,这对于先前接受过CD20单抗治疗的患者具有重要临床意义[5, 8]。”
临床巧思,价值彰显:剂量递增策略的疗效与安全双重获益
莫妥珠单抗采用的剂量递增给药策略,是其兼顾疗效与安全性的关键。陶荣教授对此评价道:“莫妥珠单抗的剂量递增方案(首周期C1D1给1mg,C1D8给2mg,C1D15或C2D1给负荷剂量如60mg,后续维持剂量如30mg),是一种巧妙的‘免疫脱敏’式给药。其核心在于通过初始低剂量暴露,让免疫系统逐步适应,避免T细胞骤然大规模激活,从而显著降低CRS发生的频率及严重程度[9]。”
临床研究显示,采用剂量递增后,多数CRS为1-2级[10],主要发生在首次足量给药后,通过标准处理均可控,≥3级CRS发生率极低 (2%)[10]。这使莫妥珠单抗治疗总体耐受性良好。
关于剂量递增是否影响疗效,陶荣教授解释道:“合理的剂量递增旨在通过逐步达到并维持有效药物暴露,持续有效激活抗肿瘤免疫反应。临床及PK/PD模型分析数据表明,这种方式不仅未削弱疗效,反而可能通过优化药物在体内的浓度和作用时间,促进了更理想的治疗结果[9]。如高剂量暴露组(1/2/60/30mg方案)的患者组,中位PFS可达24个月,显著优于较低暴露水平的患者组(1/2/30mg与1/2/13.5mg方案)。这提示剂量递增不仅降低CRS风险,也通过实现理想PK特性,促进更持久的抗肿瘤应答,实现了疗效与安全的双赢(图4)[9]。”
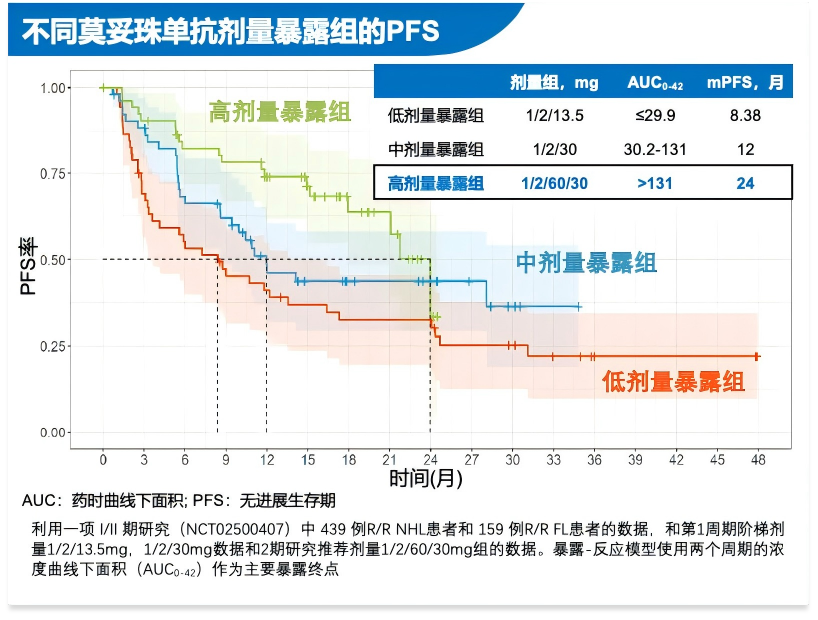
实践指引,智慧领航:莫妥珠单抗临床应用的关键考量
将莫妥珠单抗的理论优势和临床研究成果成功转化为患者的实际获益,离不开临床医生的规范操作和精细管理。
结合临床经验,给出了具体的建议:“在实际临床应用中,为最大化发挥莫妥珠单抗的治疗优势,需重点关注:首先,不良反应的预防和管理。特别是CRS,虽已通过剂量递增显著降低风险,仍需对初始周期保持高度警觉,密切监测。多数1-2级CRS通过对症处理即可缓解,≥3级CRS发生率极低。其次,必须严格遵循批准的剂量递增方案,这不仅控制毒性,也是确保药物充分暴露、优化长期缓解的关键。再者,其与其他药物的联合应用是研究热点,需更多数据积累,但原则是权衡疗效与安全性。最后,通过规范化管理流程,加强医患沟通,提升患者依从性,对确保疗效最大化及安全性可控至关重要。”
陶荣教授最后总结道:“莫妥珠单抗以其独特的结构和机制优势,为R/R FL的治疗带来了深刻变革。科学合理的给药、积极有效的毒性管理及严谨的临床操作,是充分释放其治疗价值、造福更多患者的根本保障。我们期待随着经验积累和研究深入,能进一步优化其应用策略,使其在FL乃至其他B细胞恶性肿瘤治疗中发挥更大作用。”
专家简历
复旦大学教授,博士研究生导师
复旦大学附属肿瘤医院淋巴瘤科 主任
复旦大学附属肿瘤医院淋巴瘤多学科 首席专家
上海市抗癌协会淋巴瘤专委会副主任委员
中国抗癌协会淋巴瘤专委会委员
中国医药教育协会转化医学专委会常务委员
擅长淋巴瘤的诊治,对NK/T细胞淋巴瘤,外周T细胞淋巴瘤,高危弥漫大B细胞淋巴瘤的诊治有较为深入的研究。

[1] LIU J, HU Y, ZHAO L, et al. Management and clinical outcomes of follicular lymphoma across continuous lines of treatments: a retrospective analysis in China [J]. Front Oncol, 2023, 13: 1264723.
[2] CASULO C, BYRTEK M, DAWSON K L, et al. Early Relapse of Follicular Lymphoma After Rituximab Plus Cyclophosphamide, Doxorubicin, Vincristine, and Prednisone Defines Patients at High Risk for Death: An Analysis From the National LymphoCare Study [J]. J Clin Oncol, 2015, 33(23): 2516-22.
[3] 陈缘, 高福, 谭曙光. 以T细胞受体为基础的免疫疗法研究进展 [J]. 生物工程学报, 2023, 39(10): 4004-28.
[4] LIU J, FU M, WANG M, et al. Cancer vaccines as promising immuno-therapeutics: platforms and current progress [J]. J Hematol Oncol, 2022, 15(1): 28.
[5] SUN L L, ELLERMAN D, MATHIEU M, et al. Anti-CD20/CD3 T cell-dependent bispecific antibody for the treatment of B cell malignancies [J]. Sci Transl Med, 2015, 7(287): 287ra70.
[6] BUDDE L E, SEHN L H, ASSOULINE S, et al. Mosunetuzumab, a Full-Length Bispecific CD20/CD3 Antibody, Displays Clinical Activity in Relapsed/Refractory B-Cell Non-Hodgkin Lymphoma (NHL): Interim Safety and Efficacy Results from a Phase 1 Study [J]. Blood, 2018, 132(Supplement 1): 399-.
[7] LIU L, YU X, LI Z, et al. Revealing the evolution of the tumor immune microenvironment in follicular lymphoma patients progressing within 24 months using single-cell imaging mass cytometry [J]. J Hematol Oncol, 2022, 15(1): 115.
[8] BENDER B, LI C C, MARCHAND M, et al. Population pharmacokinetics and CD20 binding dynamics for mosunetuzumab in relapsed/refractory B-cell non-Hodgkin lymphoma [J]. Clin Transl Sci, 2024, 17(6): e13825.
[9] LI C-C, BENDER B, WILKINS J, et al. A Novel Step-Up Dosage Regimen for Enhancing the Benefit-to-Risk Ratio of Mosunetuzumab in Relapsed or Refractory Follicular Lymphoma [J]. Clinical Pharmacology & Therapeutics, 2025, 117(2): 465-74.
[10] BARTLETT N L, ASSOULINE S, GIRI P, et al. Mosunetuzumab monotherapy is active and tolerable in patients with relapsed/refractory diffuse large B-cell lymphoma [J]. Blood Adv, 2023, 7(17): 4926-35.

排版编辑:肿瘤资讯-tong











 苏公网安备32059002004080号
苏公网安备32059002004080号


