由北京科创医学发展基金会主办的【肿瘤规范化诊疗项目——2025“颈彩纷呈”头颈肿瘤专家学术沙龙】第二期MDT中心交流会,于5月18日成功在线上举办。本次会议汇聚了国内三大知名医院的MDT中心团队:山东省肿瘤医院、重庆医科大学附属第一医院以及浙江省肿瘤医院。各团队展示了其MDT团队的构成和取得的成果,并分享了头颈肿瘤MDT治疗中的复杂病例。与会专家就MDT模式在临床实践中的应用经验及创新思路进行了深入的探讨和交流。
会议伊始,大会主席胡漫教授、张涛教授、方美玉教授进行开场致辞。头颈肿瘤的复杂性,要求外科、放疗科和内科等多学科共同面对和解读临床细节,MDT团队在其中扮演着重要的作用。此次交流活动旨在促进不同中心MDT的互相学习和共同提高,以帮助医生在延长患者生命的同时提升患者生活质量。各中心的成熟运行经验、临床研究及数据,将为临床诊疗提供宝贵参考。希望通过本次会议,能够吸取各团队的经验和特色,使临床实践更加完善。感谢所有参与本次会议的专家、同仁,预祝本次会议取得圆满成功。
山东省肿瘤医院MDT团队

病例分享:一例喉癌质子二次放疗联合靶向治疗 贺科文教授
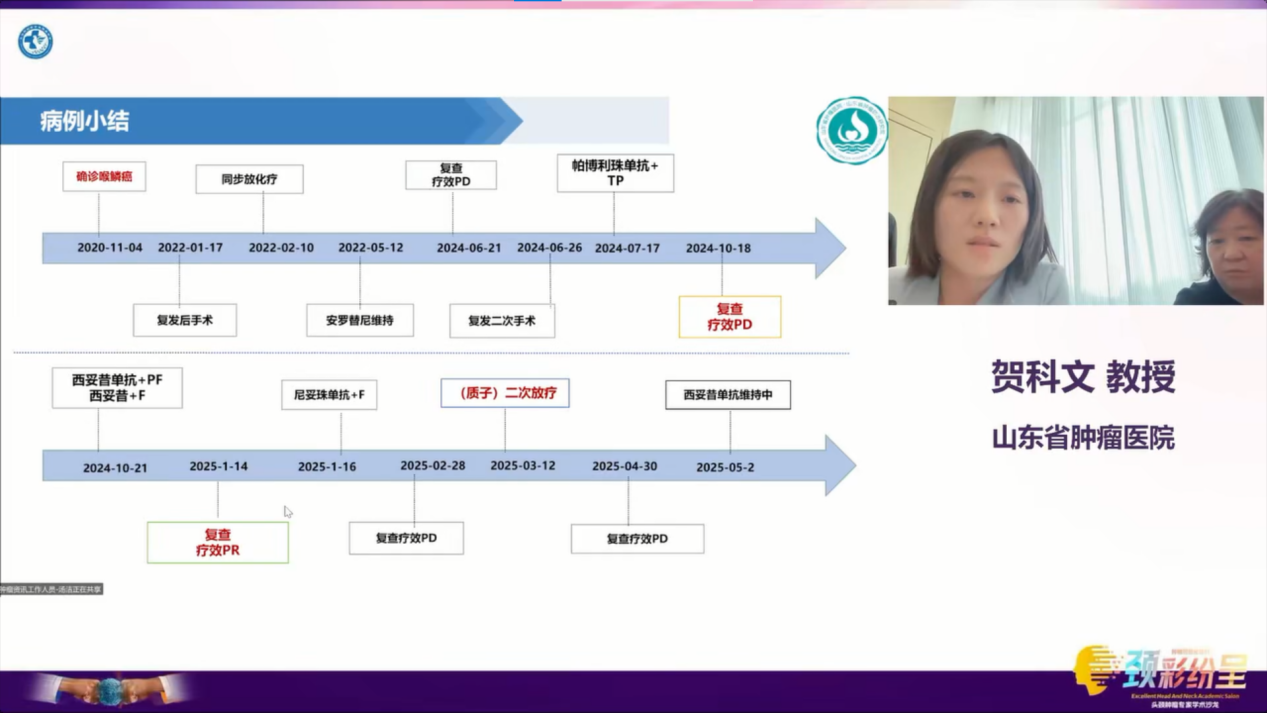
患者,男,67岁,喉癌(声门鳞癌二次术后复发,rT4N0M1),因“喉癌术后放化疗后3年余,复发术后综合治疗后3周余”收入院。2020-11患者因“声音嘶哑2月”外院行喉镜检查:右侧声带全长可见菜花样肿物。2020-11-4于外院行“支撑喉镜下CO2激光喉垂直部分切除术+喉病损激光烧灼术”,术后病理:右侧声带鳞状细胞癌,中分化。2022-1 CT:甲状腺左叶上份近峡部颈前结节。2022-1-17在外院行“颈深部探查+颈部肿物切除术”,术中快速病理示:鳞状细胞癌。与家属充分沟通,家属决定暂不扩大切除。术后病理示:喉前肿物,鳞状细胞癌,中分化,侵及甲状腺组织。
2022-2-7 PET-CT:声门癌术后,颈前软组织外侵再次术后,前联合及颈前软组织影增厚伴高代谢,考虑受侵;下咽后部高代谢。2022-2-7喉镜诊断:声带术后改变。2022-2-10起给予放疗DT70GY/35F同步顺铂50mg,qw(2周期后因骨髓抑制未能完成)。患者拒绝化疗,2022-5起给予安罗替尼靶向维持。期间多次复查提示,术区、前联合及颈前受侵无著变。
2024-2因“咽部出血”停药安罗替尼。2024-3咽部出现颈部疼痛,呈持续性,吞咽时加重,患者自行服用氨酚双氢可待因控制。2024-2-19(放疗后23个月)及2024-5-22CT提示:声门癌二次术后改变,术区、前联合及颈前受侵,较前片范围增大。
2024-6外院PET-CT示:喉部肿瘤复发不除外;肺转移。2024-6-21 CT示:喉部肿瘤术后改变,右侧喉旁间隙、甲状软骨周围软组织肿块,甲状软骨破坏,符合肿瘤复发CT表现,向上累及口咽,向下累及甲状腺右侧叶;双肺多发结节灶。2024-6-26行“喉部分切除术+右肺肺叶切除+双侧颈淋巴结清扫+甲状腺部分切除术”,术后病理示:(喉肿物1)纤维组织慢性炎,(喉肿物2)查见鳞状细胞癌,高分化;(右肺中叶)鳞状细胞癌,中-高分化,切面积1*1.5cm,支气管残端未见癌;(颈部肿物)鳞状细胞癌,高分化,累及甲状腺,切面积1.5*1.2cm;(右侧甲状腺)淋巴细胞性甲状腺炎;(右颌下腺)鳞状细胞癌,高分化,体积2.6*2*1.1cm。PD-L1 CPS=20。
2024-7-17起行帕博利珠单抗联合卡铂+多西他赛(4周期),疗效评价PD。2024-10-18(放疗后31月)CT:声门癌术后,考虑术后及周围复发或转移,舌骨及甲状软骨周围转移较前(2024-8-13)加重;考虑左侧颌下区转移。
2024-10-21起改行西妥昔单抗+PF(顺铂+氟尿嘧啶),2周期后因患者出现重度骨髓抑制,更改方案为:西妥昔单抗+氟尿嘧啶,4周期后疗效评价PR。因患者出现3级皮肤不良反应(痤疮样皮疹)停用西妥昔单抗,2025-1-16起改为:尼妥珠单抗+氟尿嘧啶,2周期后疗效评价PD。
2025-3-10 PET-CT:声门癌术后,术区软组织形态不规则伴高代谢,累及右侧舌根部软组织、右颌下、舌骨右侧份及右侧甲状软骨,考虑肿瘤活性残留。因患者拒绝同步靶向治疗,2025-3-12起行姑息性二次放疗(质子),DT=50Gy/25f,2025-4-30二次放疗结束。
2025-4-30 CT:声门癌术后,术区周围复发或转移,较前(2025-2-27)基本变化不显著;舌骨及甲状软骨周围转移,较前坏死范围增大;考虑左侧颌下区转移较前基本变化不显著;左侧颌面部及右侧颈后部肌间隙内结节灶,较前新发,转移可能大。2025-5-2给予西妥昔单抗治疗1次, 患者拒绝qw方案,要求q3w,2周后PD。

大咖论道-病例讨论:
浙江省肿瘤医院:
患者前期接受激光治疗,但因肿瘤突破环甲膜,治疗后残留导致复发。后续行放疗和安罗替尼维持治疗,效果较好。复发后手术发现肿瘤严重,应考虑全喉切除而非部分切除。二次放疗在头颈部患者中需谨慎。患者再次复发并出现肺结节,难以确定是肺转移癌还是原发性肺癌。若为原发性肺癌,可尝试二次放疗,但需严格控制剂量,且患者局部出现溃疡、坏死,凸显二次放疗风险。内科治疗上,对标准治疗失败患者,各中心有多种临床研究和药物应用,如ADC药物、双抗等,还会联合西妥昔单抗,但需注意用量与耐药问题。目前,安罗替尼维持治疗证据有限,临床应用较少,后续可开展相关临床研究提供指导。
重庆医科大学附属第一医院:
该病例较为复杂,最初在微创手术后出现复发可能已达T4a期,且累及软骨。对于复发性T4a病变,单纯放疗疗效可能不佳,更倾向手术干预。此外,首次放疗剂量为70Gy/35次,喉道肿瘤的单次剂量可能相对偏低。而且在对复发性肿瘤患者进行放疗时,可考虑采用超分割、大分割等不同的分割方式。2024年起,患者病情愈发复杂,需明确肺部病灶到底是转移瘤还是原发肿瘤。若为转移瘤,外科治疗作用有限;若是原发肿瘤,则需评估手术可行性及切除范围,并考虑是否需要皮瓣修复。术后病理检查,如CPS表达水平、p16是否阳性等因素,可能影响后续治疗方案选择。如果CPS高,理论上可考虑联合靶向及免疫治疗方案;对于p16阴性患者,已有Ⅱ期研究证据显示,CDK4/6抑制剂联合西妥昔单抗的疗效尚可。总之,依据患者病理类型、影像学表现、分子特征、身体状况及个人意愿等,制定规范化且个性化的诊疗方案,以达成最佳治疗效果。
重庆医科大学附属第一医院MDT团队

病例分享:局部晚期颊黏膜癌化靶免联合治疗 张祥教授

患者,男,80岁,因“左侧面颊包块1月余”于2024-6就诊于重庆医科大学附属第一医院。患者1月余发现左侧面颊包块,并进行性增大,张口受限伴疼痛,当地医院穿刺活检:(左颊包块)高分化鳞状细胞癌;PD-L1表达TPS=10%,CPS=12。2024-6-6颌面部及颈部增强磁共振:1.左面峡部不规则片状异常信号,考虑恶性肿瘤性病变。2.双侧颈部多发淋巴结显示,较大者位于左侧颈II区。3.扫及双侧筛窦、上颌窦炎。查体:左颊黏膜见包块伴有糜烂,前界到口角,后界达翼领韧带区,上下界均达前庭沟,基底硬,边界不清。吸烟50年,抽叶子烟,每月半斤,未戒烟;偶有饮酒;余无特殊。诊断:左颊部高分化鳞状细胞癌(cT4aN1M0,IVA期)。
2024-6-5、2024-7-10、2024-8-6、2024-9-19予以白蛋白紫杉醇(300mg,d1,q3w)+替雷利珠单抗(200mg,d1,q3w)+西妥昔单抗(600mg d1,400mg qw)治疗。
2024-8-29、2024-10-13颌面部及颈部增强MRI均显示,1.左面颊黏膜区软组织影稍增厚,对比2024-6-6 MRI,病灶缩小。2.双侧颈部多发淋巴结较前相仿。
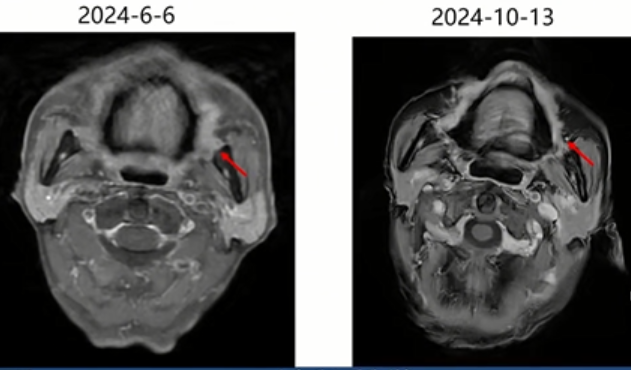
随后给予根治性放疗(GTV DT69.96Gy/33F,CTV 60.06Gy/33F,PTV60.06Gy/33F)同步西妥昔单抗(400mg,qw,6次)。
2024-12-30颌面部增强MRI:1.左面颊黏膜稍增厚,对比2024-10-13MRI稍缩小,左侧口咽旁结构紊乱。2.右侧颌下小淋巴结,较前缩小。3.扫及双侧筛窦、上颌窦炎,较前稍增多。
2025-2-24颌面部增强MRI:右侧颊黏膜稍增厚,对比2024-12-30MRI变化不大,左侧口咽旁结构紊乱。


大咖论道-病例讨论:
山东省肿瘤医院:
鉴于患者高龄,全麻耐受性较差,故未选择手术治疗,而是先给予新辅助治疗。治疗方案采用免疫治疗联合西妥昔单抗以及化疗。经过4个周期的治疗后,影像学检查显示局部病灶缩小,随后对患者进行了根治性放疗,并在放疗期间继续联合靶向治疗。在治疗全过程中,密切监测患者的骨髓抑制、皮疹等不良反应情况。完成放疗后,选择观察患者的病情变化,期盼能够延长患者的长期生存时间。此病例显示,在免疫治疗时代,靶向联合免疫和化疗对局晚期头颈部肿瘤患者效果良好。治疗方案考虑患者肾功能、心肺功能等状况,全身治疗有效后巩固并联合局部放疗,能有效控制肿瘤,提高生存率,且患者耐受性较好,为高龄患者治疗提供了有益经验。
浙江省肿瘤医院:
此患者新辅助阶段“化靶免”方案强度足够,且有医学证据支持,使肿瘤明显退缩,之后放疗联合靶向治疗也取得较好效果。但淋巴结只是缩小未完全消退,需后期随访。由于放疗后可能存在黏膜下浸润复发,而磁共振难以早期发现,建议做PET-CT查看原发灶和淋巴结情况。整体治疗策略合理,对于高龄患者未用标准铂类方案而采用替代方案,可降低毒性、提高耐受性。放疗同期选西妥昔单抗是标准选择,若考虑用PD-1抑制剂替代靶向药,可能降低毒性,可进一步开展研究来深入探讨。放疗结束后是否靶向或维持治疗,目前证据不足,需个体化决策,若淋巴结有残留,要考虑穿刺或挽救手术等诊疗措施。
重庆医科大学附属第一医院:
该患者初始肿瘤较大,直接手术创伤大且需皮瓣修复,但新辅助治疗后肿瘤显著缩小,利于手术开展。鉴于患者年龄和意愿,倾向于微创手术,放疗也是可选项。不过,新辅助治疗后,在头颈部肿瘤放疗剂量和手术切除范围上存在争议:降低剂量或缩小范围可减少创伤,但可能增加复发风险;按原计划则可能削弱新辅助治疗的效果。目前缺乏明确数据指导,需结合患者意愿及耐受能力决策。老年患者更注重功能保留和生活质量,根据患者具体情况制定个性化治疗方案,体现了MDT的价值。当前相关探索性研究的循证级别较低,未来需加强合作以获取更多证据指导临床。
浙江省肿瘤医院MDT团队

病例分享:多原发肿瘤患者的治疗 曹君教授

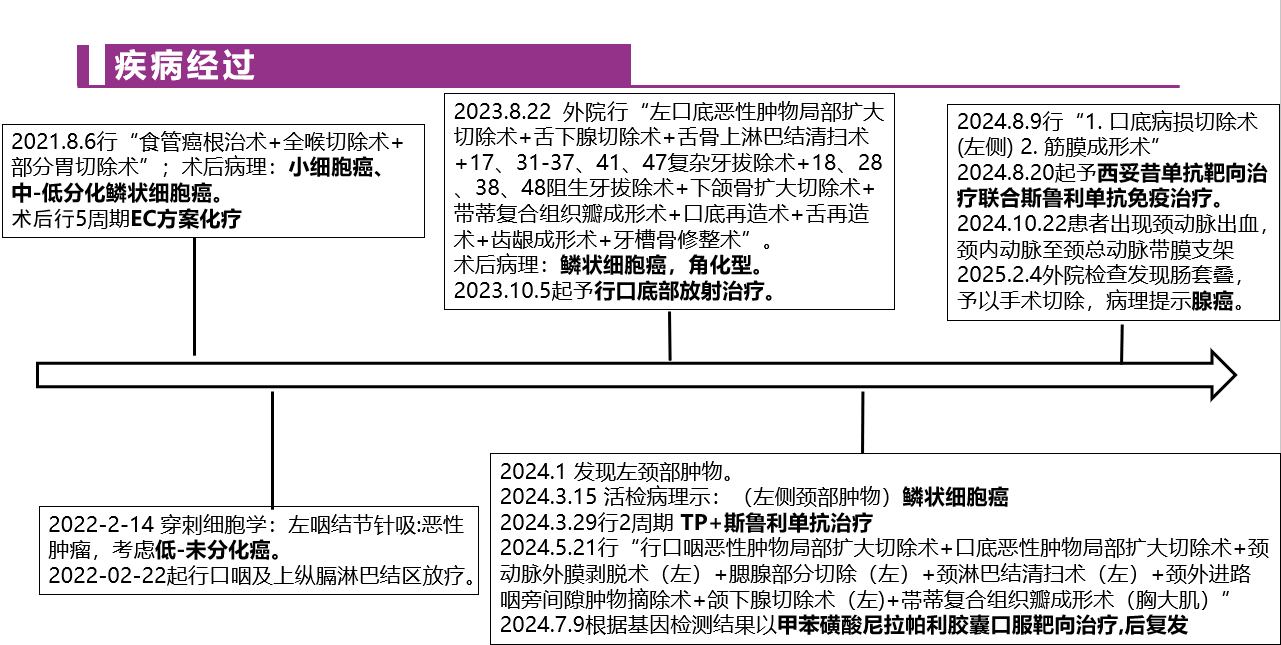
患者,男,63岁。2021-8-2患者因“吞咽困难2月”至外院就诊,颈胸部增强CT示:食管上段腔内占位;口咽前壁、左侧壁局部软组织增厚。2021-8-3患者突发呕血,考虑肿瘤出血,转至ICU气管切开。2021-8-6行“食管癌根治术+全喉切除术+部分胃切除术”。
术后病理:1.食管上段近咽喉处隆起肿块大小6*6cm,侵犯全层;另一游离6*3.5cm,均为小细胞癌,累及横纹肌组织。2.食管下段见溃疡,1*0.8cm,中-低分化鳞状细胞癌,局限于黏膜层;见另一游离肿瘤组织,大小5.5*3cm,镜示为小细胞癌。3.冰冻送检肿瘤组织一块,2*2*1cm;镜示为小细胞癌,局部低分化鳞状细胞癌,累及横纹肌组织;切缘均为阴性。送检淋巴结0/20。免疫组化:xs202114284c片:Syn&CD56 (小细胞癌成分+), P40&CK-pan(鳞癌成分+) ; xs2021-14285z6片:CgA(弱) 、Syn (+)、LCA (-), CD56 (+)、SSTR2 (+)、Ki-67 (70%~80%+)、CK-pan (局灶核旁点状+)、P63(-)、P40(-)。
诊断:食管恶性肿瘤(上段小细胞癌pT3N0M0,下段鳞癌pT1N0M0 G2-3)。
2021-9-7、2021-9-28、2021-10-9、2021-11-9、2021-11-30予以第1-5周期EC方案(依托泊苷150mg,d1-3;卡铂AUC 4-5,d1)化疗。
2021-12-2予以放疗科会诊,会诊意见:患者食管双原发肿瘤术后化疗后,根据疾病分期需要行术后放疗,但是BMI低(167cm, 55kg,病来体重下降15kg),营养情况差,手术范围较大,且食管小细胞癌需要尽早化疗,建议先完成术后化疗,待一般情况好转,营养情况变佳后进行术后放疗。
患者目前化疗后气管右旁散在小淋巴结,较前明显缩小、减少,与放射科联系,倾向转移,但无法明确术前还是术后出现淋巴结转移。考虑患者化疗后一般情况欠佳,化疗后反复发热,故暂缓第6周期化疗。2021-12-30 PET-CT:1.食管恶性肿瘤术后,现术区未见明确肿瘤复发征象;2.上纵隔气管右旁多发小淋巴结伴代谢轻度增高,较本院2021-9-14 CT,明显缩小,考虑治疗后改变;3.左侧口咽部软组织增厚伴FDG代谢增高。MRI提示,口咽左侧型肿块(21*29mm)。2022-2-14穿刺细胞学检查(左结节针吸):恶性肿瘤,考虑低-未分化癌。经头颈MDT讨论,考虑行口咽部及食管旁淋巴结放疗治疗。
2022-2-22起行口咽及上纵隔淋巴结区放疗,采用VMAT技术,口部病灶66Gy/30F,上纵淋巴结60Gy/30F,淋巴结引流区60Gy/30F。放疗期间患者各项营养指标及血象低下,放射性黏膜炎明显,予以营养支持等对症处理后好转。
2023-6-2 MRI:1.口咽左侧壁恶性肿瘤治疗后,目前口咽部未见明显占位。2.双侧副鼻窦及左侧乳突少许炎症,较前(2023-2-27MR)相仿。3.鼻咽部未见明显占位。
2023-8患者口腔内肿胀明显,可见新生物。2023-8-22外院行“左口底恶性肿物局部扩大切除术+舌下腺切除术+舌骨上淋巴结清扫术+17、31-37、41、47复杂牙拔除术+18、28、38、48阻生牙拔除术+下颌骨扩大切除术+带蒂复合组织瓣成形术+口底再造术+舌再造术+齿龈成形术+牙槽骨修整术”。
术后病理:肿瘤大小2.5×1.3×1.1cm,鳞状细胞癌,角化型,肿瘤浸润横纹肌及脂肪组织,累及涎腺组织,浸润深度约9mm,切缘阴性。淋巴管-血管侵犯:阴性。神经侵犯:阳性。淋巴结0/14阳性。pTNM分期:pT2N0Mx。
经头颈MDT讨论,建议行口底部放射治疗。2023-10-5起予行口底部放射治疗。放疗期间患者各项营养指标及血象低下,且放射性黏膜炎明显,予以营养支持等对症处理后好转。
2024-1发现左颈部肿物,约红豆大小,逐渐增大,表面发红,当时未予以重视。2024-3-15 外院活检病理示:(左侧颈部肿物)鳞状细胞癌。
2024-3-19外院PET-CT示:1.左侧口底斑片状等低密度灶伴糖代谢升高,左侧颌下腺区域软组织FDG增高灶,不除外恶性可能;2.食管癌术后改变,术区FDG增高,考虑炎性或生理性摄取。上侧上颌窦炎,两肺肺气肿3。升结肠壁结节状FDG升高,考虑为炎性病变或腺瘤。颈部CTA:左侧椎动脉起始处重度狭窄。
经头颈MDT讨论,建议先行新辅助免疫+化疗,根据病灶退缩情况确定后续治疗。2024-3-29、2024-4-19行2周期TP+免疫(白蛋白结合型紫杉醇400mg D1、卡铂 AUC4-5 d1、PD1单抗 0.3g D1)治疗。
化疗达2疗程,复查颈部CT提示口咽肿物及颈部较前缩小。2024-5-21行“口咽恶性肿物局部扩大切除术+口底恶性肿物局部扩大切除术+颈动脉外膜剥脱术(左)+腮腺部分切除(左)+颈淋巴结清扫术(左)+颈外进路咽旁间隙肿物摘除术+颌下腺切除术(左)+带蒂复合组织瓣成形术(胸大肌)”,病程中并发咽瘘,2024-5-31急诊行“咽瘘切开引流术”,术后予抗感染、补液治疗后好转。
术后病理:左颈部肿物,皮肤真皮及皮下组织内见高-中分化鳞状细胞癌,局灶累及横纹肌组织,可见神经侵犯,另见8枚淋巴结未见明显癌转移。PD-L1 CPS=20,基因检测显示BRCA1突变。
2024-7-9起予以甲苯磺酸尼拉帕利胶囊口服靶向治疗(拒绝静脉治疗)。半月后再次出现左侧面部肿物,质地韧,活动度差,考虑肿瘤复发。2024-8-9行“1.口底病损切除术(左侧);2.筋膜成形术”。术后病理:(左侧下颌肿物)皮肤真皮至皮下纤维、横纹组织内见高-中分化鳞状细胞癌,局灶累及神经束。
经头颈MDT讨论,建议术后西妥昔单抗靶向+免疫维持治疗。2024-8-20起予以西妥昔单抗联合PD-1单抗治疗。
2024-10-22患者出现颈动脉出血,急诊就诊外院,自诉医生告知颈外动脉假性动脉瘤破裂,颈内动脉至颈总动脉带膜支架;无明显肿瘤。
2025-2-4患者因右侧腹痛不适,外院检查发现肠套叠,予以手术切除,局部有肿块压迫。病理:1.(右半结肠)高-中分化腺癌,部分粘液腺癌,浸润至深肌层,未见脉管及神经侵犯。2.阑尾黏膜慢性炎。3.淋巴结均未见癌转移。
经多原发MDT团队讨论,结肠癌为早期,可随访观察。继续予以靶免治疗。
2025-3-14 MRI:对比2024-7-25MR,1.下咽部及左颈部术后改变,术区软组织增厚,较前明显。2.右颈多发淋巴结,部分较前稍大。双侧上颌窦及右侧乳突炎症。
2025-4-30予第1周期靶向治疗,具体:芦康沙妥珠单抗 200mg, d1。2025-5-13予第2周期靶向治疗,具体:西妥昔单抗400mg,d1+芦康沙妥珠单抗200mg,d1。

大咖论道-病例讨论:
重庆医科大学附属第一医院:
该病例病程较为复杂,涉及多个部位不同类型的病灶,需外科、病理科、内科等多学科综合考虑。对于食管合并口咽等部位肿瘤,若时间允许,可先处理食管肿瘤,再处理口咽部肿瘤。此例因情况紧急,直接选择手术。同时,需注意可能涉及的同源性问题,关注病理类型,包括是否可能存在神经内分泌瘤的情况等。建议进行特殊检测以明确病理类型,为后续治疗提供依据。总体而言,从手术时机、病理检测、治疗策略等方面进行了深入分析,强调了多学科协作及病理诊断对后续治疗的重要性,以期为患者制定更精准的治疗方案。
山东省肿瘤医院:
该病例肿瘤原发部位涉及食管、口咽、口底等多处,病理类型多样,包括食管的小细胞癌和中-低分化鳞癌,以及口底的高-中分化鳞癌,还存在纵隔淋巴结复发转移。后期出现左颈部和口底肿瘤;经多次手术、放化疗等治疗后又发现肠癌。食管上段小细胞癌和肠腺癌控制较好,主要治疗集中在口咽和口底。通过多学科协作、基因检测和靶向药物调整,肿瘤得到部分控制,生存期延长。近期的ADC药物在头颈部肿瘤的效评估尚不明确,需更长时间随访。此病例在检查和放疗方面较细致,为临床诊疗提供了宝贵的经验。总体而言,此病例强调了综合治疗手段的应用及疗效,突出了治疗难点和经验总结,体现了多学科团队协作的重要性,为后续复杂病例治疗提供了重要参考。
大会总结

会议尾声,胡漫教授、张涛教授、方美玉教授对本次交流会进行总结陈词。头颈部肿瘤MDT模式可整合各学科优势,为患者提供全面、规范的治疗方案,推广该模式能优化患者治疗效果。未来应提前介入头颈肿瘤治疗全程管理,兼顾患者生存时间和生理功能保全。本次会议中,三家单位MDT团队深入交流,成功剖析病例,成效显著。期待未来举办更多类似研讨会,以促进共同学习进步,推动头颈部肿瘤治疗发展。
排版编辑:肿瘤资讯-TJ











 苏公网安备32059002004080号
苏公网安备32059002004080号


