子宫平滑肌肉瘤是子宫肉瘤最常见的类型,其恶性程度高,易发生复发和(或)转移。其治疗原则以手术为主,对于全身多处转移不适合手术的患者,考虑全身系统性治疗(化疗±靶向/免疫治疗)和(或)姑息性放疗[1]。然而,患者抗肿瘤治疗期间常伴有肿瘤治疗所致血小板减少症(cancer treatment-induced thrombocytopenia,CTIT),不仅会增加患者出血风险,而且可导致治疗剂量降低、治疗时间推迟,甚至治疗停止,影响抗肿瘤疗效,最终影响患者生存寿命及生存质量[2],因此临床实践中应及时、有效地处理CTIT。
本期重庆大学附属肿瘤医院雷翠蓉医师分享了一例子宫平滑肌肉瘤患者化疗联合靶向治疗期间CTIT的管理,李蓉教授进行了精彩点评,医脉通特别整理,期待为子宫平滑肌肉瘤治疗期间CTIT的防治与管理提供参考。
病例资料
1、基本信息
一般资料:患者女,40岁。
主诉:诊断“子宫平滑肌肉瘤”6年余,多次复发治疗后进展10月余。
现病史:患者于6年余前诊断为子宫平滑肌肉瘤,经多次手术及抗肿瘤治疗后出现反复复发,本次入院因第4次复发,为行抗肿瘤治疗于2023年05月11日收住我科。
2、辅助检查
血常规:白细胞 9.31x109/L;红细胞 3.31x1012/L;血红蛋白 94g/L;血小板 150x109/L。
CT:1.子宫未见显示,阴道残端未见增厚。2. 腹盆腔多发结节、肿块,考虑肿瘤复发或转移可能,较前增多增大;腹盆腔积液,伴渗出性病变可能,较前增多。3. 腹盆腔腹膜增厚,转移待排,较前新增。4. 直肠肠壁稍增厚。5.双肺上叶及右肺下叶小结节,部分较前增大,转移可能。6.双侧心膈角区、左侧锁骨上及纵隔内多发淋巴结显示,部分较前增大。
3、初步临床诊断
子宫平滑肌肉瘤术后复发
4、治疗经过
1、2016年2月12日 手术
患者因“下腹胀痛伴阴道大出血”在外院急诊行开腹子宫峡部包块剔除术,术后病检考虑平滑肌肉瘤。2016年2月29日在外院行经腹全子宫双附件大网膜切除+部分盆腔淋巴结清扫术,术后切缘干净。
2、2016年7月4日
第一次复发后行手术+化疗
于我院复查肿瘤标志物及核磁提示肿瘤复发。给予多西他赛+吉西他滨治疗,2个疗程后疗效评估提示疾病进展(PD)。更换为VADC方案(长春地辛+吡柔比星+环磷酰胺+氮烯咪胺)治疗2个疗程。于2016年11月23日行剖腹探查术+肠粘连松解术+妇科恶性肿瘤减瘤术等,术后病检明确复发。术后给予VADC方案2个疗程。于2016年12月28日至2017年2月16日行固定野调强放疗,顺利完成,疗效评估为完全缓解(CR),治疗结束后定期随访。
3、2020年4月14日
第二次复发后抗肿瘤治疗
(化疗、靶向治疗)
就诊于我院复查CT见盆腔肿块(大小>3cm)考虑复发,建议入院,患者要求随访。2020年07月26日于外院查B超提示盆腔肿块(大小>10cm),之后于我院查PET-CT提示平滑肌肉瘤复发并转移。
2020年08月04日给予洛铂胸腔灌注化疗,之后给予VADC方案2个疗程后,疗效评估为PD。
2020年09月30日至2021年5月18日给予多西他赛+吉西他滨3个疗程,贝伐珠单抗+多西他赛+吉西他滨5个疗程。疗效评价为部分缓解(PR)。期间出现3-4级骨髓抑制(血小板减少、中性粒细胞减少为主),其中因血小板减少延误了贝伐珠单抗+多西他赛+吉西他滨方案第1疗程d8的吉西他滨治疗,给予对症处理后好转。之后因化疗耐受性差,更换为安罗替尼口服治疗,末次口服该药时间为2021年7月19日。
4、2021年7月21日
第三次复发后行靶向联合化疗
复查B超提示盆腔肿块(约7cm),评估疗效为PD。
于2021年9月14日给予贝伐珠单抗+脂质体阿霉素+卡铂共8个疗程。期间出现骨髓抑制(血小板减少为主),给予升板处理后好转。
5、2023年5月11日
第四次复发后行靶向联合化疗
复查CT后请多学科会诊建议:1.入组临床研究;2.继续脂质体阿霉素、贝伐珠单抗、卡铂治疗。患者及家属选择继续同前抗肿瘤治疗,于2023年5月17日给予脂质体阿霉素+贝伐珠单抗+卡铂3个疗程,期间给予预防性升血小板治疗,过程顺利。
5、CTIT 治疗经过
1、2020年8月6日 贝伐珠单抗+多西他赛
+吉西他滨治疗导致CTIT的治疗
复查血小板计数为70×109/L,给予重组人白细胞介素‑11(rhIL‑11)和重组人血小板生成素(rhTPO)治疗,19天后逐渐恢复至正常水平。于2021年4月17日复查血小板计数为95×109/L,给予rhIL‑11治疗,期间血小板计数最低降至23×109/L ,治疗19天后恢复至正常水平。
2、2022年6月5日 脂质体阿霉素+贝伐珠
单抗+卡铂治疗导致CTIT的治疗
复查血小板计数为10×109/L,给予输注血小板及应用rhTPO和rhIL‑11治疗后,12天后逐渐恢复至101×109/L。于7月23日复查血小板计数为82×109/L,给予rhTPO和rhIL‑11治疗,血小板计数最低降至13×109/L,治疗46天后逐渐恢复至84×109/L。
3、2023年5月17日 脂质体阿霉素+贝伐珠
单抗+卡铂治疗期间CTIT二级预防
鉴于患者既往抗肿瘤过程中出现过≥3级血小板减少,并出现过抗肿瘤治疗的延误,故在2023年5月17日、6月28日行脂质体阿霉素+贝伐珠单抗+卡铂治疗2个疗程期间,口服海曲泊帕进行CTIT二级预防,期间血小板计数均超过90×109/L,顺利保证了患者抗肿瘤治疗的正常进行。

诊疗思考
子宫平滑肌肉瘤是子宫肉瘤最常见的类型,约占子宫肉瘤的40%~50%,呈高度恶性,其治疗以手术为核心,辅以术后放疗、化疗等。对于晚期复发患者,在常规治疗失败的情况下,可尝试个体化靶向治疗[1]。故在患者进行多次手术后,选择使用化疗联合靶向药物治疗(如贝伐珠单抗+多西他赛+吉西他滨方案、脂质体阿霉素+贝伐珠单抗+卡铂等)。而上述方案治疗肿瘤患者过程中容易发生CTIT,例如一项贝伐珠单抗+多西他赛+吉西他滨方案治疗子宫肉瘤的研究显示,3级CTIT发生率高达25%,4级则为11%[3]。另一项脂质体阿霉素+贝伐珠单抗+卡铂治疗复发性卵巢癌的研究指出,所有级别CTIT发生率为19%[4]。上述数据表明,虽然多种治疗手段为患者燃起了生存希望,然而在这一丝希望的前方,CTIT的阴云仍笼罩着。因此,在患者的治疗过程中需密切监测血小板的变化情况,以迅速地识别及有效地处理CTIT。
该例患者在第二、三次复发后的抗肿瘤治疗期间发生了4级CTIT,为避免患者因为CTIT而影响后续抗肿瘤治疗正常进行,并降低严重出血风险,给予输注血小板,应用rhIL‑11和rhTPO对症治疗后好转。在之后的治疗中,考虑到反复出现CTIT的患者使用传统升板药物时,将由于免疫原性等原因导致疗效不佳,此时需要使用无免疫原性,且兼具有效性和安全性的升板药物进行治疗。因此,在患者第四次肿瘤复发后抗肿瘤治疗期间,为避免患者再发生重度CTIT,使用海曲泊帕进行二级预防。采用海曲泊帕进行CTIT预防后,抗肿瘤治疗2个疗程期间血小板计数基本维持正常(>90×109/L)。
该患者使用海曲泊帕获得了两方面的获益。首先,海曲泊帕为本例患者带来了良好的升板疗效,使用海曲泊帕后患者血小板计数的最低值均>90×109/L,后续亦未发生重度CTIT,未影响后续的抗肿瘤治疗。其次,海曲泊帕便捷的口服给药形式,为这种多数时间需院外居家治疗的患者提供了更多便利。因此,海曲泊帕为本例子宫肉瘤患者接受化疗联合靶向药物治疗的CTIT管理提供了很大的帮助。
子宫肉瘤患者在抗肿瘤治疗过程中,CTIT的发生率如何?发生CTIT可造成哪些不良后果?
李蓉教授:目前对于不适合手术的子宫肉瘤患者,常使用全身系统性治疗(化疗或联合靶向治疗/免疫治疗)和(或)姑息性放疗,而抗肿瘤治疗过程中常出现CTIT。不同抗肿瘤治疗方案导致CTIT的发生率和严重程度不同。吉西他滨联合多西他赛方案的3-4级CTIT发生率为30.0%[5],吉西他滨联合多西他赛及贝伐珠单抗为36.5%[3],而多柔比星联合顺铂及异环磷酰胺的所有级别CTIT发生率高达89%[6]。
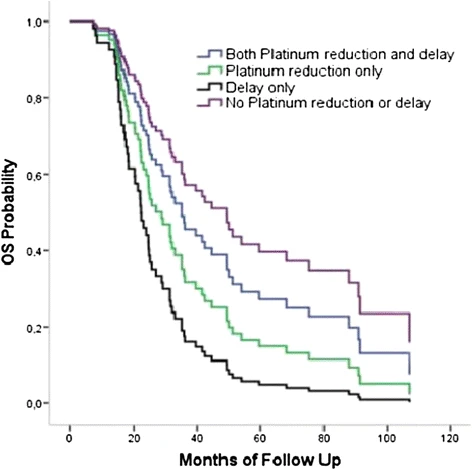
CTIT的发生对患者和医护人员均有不良影响。患者方面,CTIT的发生影响患者接受按时、足量的抗肿瘤治疗,导致治疗效果不佳,严重时还可能引发危及生命的出血并发症。医护人员方面,CTIT将增加医护人员对患者进行疾病全程管理的难度[2,7]。一项对立陶宛大学治疗的82例卵巢癌患者进行分析的研究结果显示,与未经历任何化疗方案调整的患者相比,仅经历化疗延迟的患者的死亡风险高出3.3倍,p=0.016[8](图2)。因此,临床中及时有效地处理CTIT,不但可以保障抗肿瘤治疗顺利进行,降低患者的出血风险,而且有助于医护人员更有效地实施患者的全程管理。
在您看来,本例患者为什么要进行CTIT的二级预防?您是如何选择CTIT二级预防药物的?
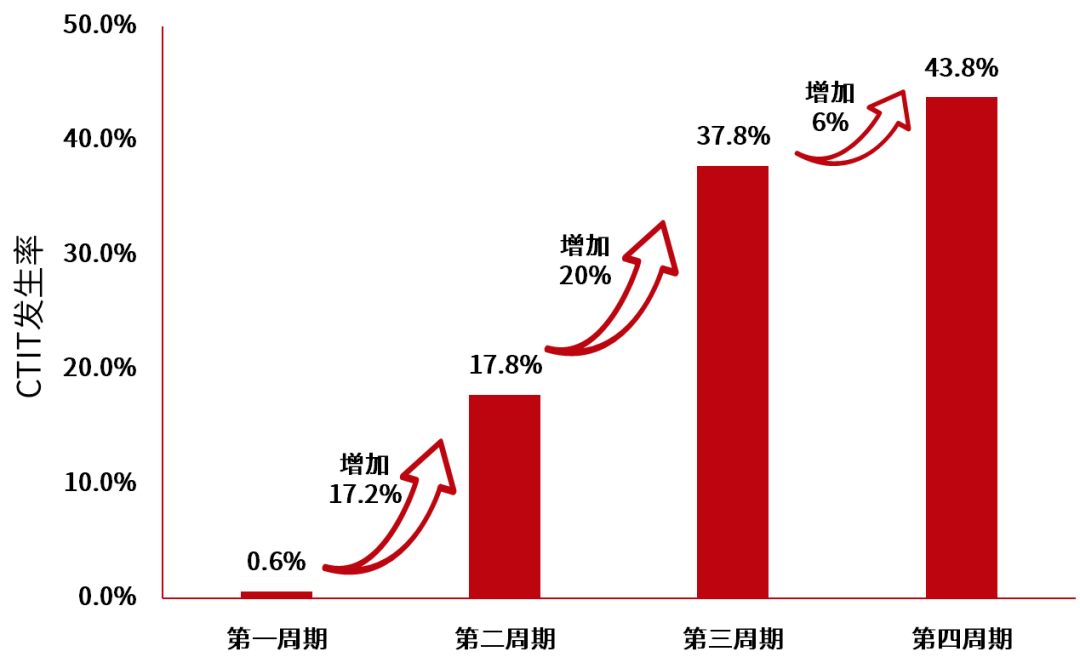
李蓉教授:患者在抗肿瘤治疗过程中,若前一周期出现CTIT,后续治疗中可能再次出现更严重的CTIT。研究表明,随着治疗周期的累积,血小板减少的发病率会显著增加:第一周期为0.6%,第二周期为17.8%,第三周期为37.8%,第四周期为43.8%[9](图3)。预防性治疗可以降低血小板减少的发生率和严重程度。对于出血风险较高的患者,采取二级预防措施可以有效保证下一个治疗周期的按时、足量进行。因此,子宫肉瘤患者化疗联合靶向治疗期间,有必要参照指南推荐进行CTIT二级预防。
2023年中国临床肿瘤学会(CSCO)《肿瘤治疗所致血小板减少症诊疗指南》[10]明确指出,对于上一周期血小板计数<50×109/L的患者,以及<75×109/L且有出血高风险因素(如既往接受含铂类药物治疗)的患者,可使用升板药物,如口服药物海曲泊帕(II级推荐,2A类证据)进行二级预防。
本例患者采用海曲泊帕进行CTIT二级预防后,近4个月血小板计数基本维持正常(>90×109/L),提示海曲泊帕可有效预防重度CTIT的发生,并可保障后续抗肿瘤治疗按时、足疗程进行,也提示其在CTIT二级预防领域具有广阔的研究价值和使用前景。
请您结合本病例谈谈海曲泊帕在CTIT的治疗和预防中的应用前景?
李蓉教授:在该子宫肉瘤患者抗肿瘤治疗期间,海曲泊帕有效预防了靶向联合化疗后重度CTIT的发生,将治疗期间血小板的最低值提升至90×109/L以上。使用海曲泊帕期间未发生严重的不良反应,充分证明了其良好的有效性和安全性。海曲泊帕成功预防该例脂质体阿霉素+贝伐珠单抗+卡铂治疗期间CTIT的案例,为该类患者的预防CTIT提供了新的思路。
海曲泊帕是我国自主研发的新一代口服小分子非肽类TPO-RA,而作为唯一一个获得2023版CSCO《肿瘤治疗所致血小板减少症诊疗指南》[10]Ⅱ级推荐用于CTIT的治疗和二级预防的TPO-RA类药物,在CTIT的治疗和预防方面均具有良好的应用前景:
治疗方面:一项探索海曲泊帕治疗同步/序贯放化疗所致CTIT的有效性和安全性研究的最新研究成果,登上2023年欧洲临床肿瘤学会年会(ESMO)(摘要号:2100P)。结果表明,2级CTIT患者治疗14天内血小板计数≥75×109/L的比例达100%,3级CTIT患者治疗14天内血小板计数≥75×109/L的比例达80%,未见3-4级不良反应[11]。此结果印证了海曲泊帕治疗CTIT良好的疗效和安全性,为同步/序贯放化疗所致CTIT管理提供了重要的参考依据。
预防方面:一项海曲泊帕II期临床研究[12]显示,在因血小板减少导致化疗延迟≥7天且血小板计数<75×109/L的实体瘤患者中,连续口服海曲泊帕7.5mg/天可使72%的患者完成2个周期化疗,同时未发生因血小板减少导致的化疗方案调整[12]。一项前瞻性真实世界研究纳入计划接受含铂化疗且评估为CTIT高风险的肺癌患者,在化疗结束后预防性口服海曲泊帕7.5mg/天,所有患者的血小板计数在第10天均维持正常水平(≥100×109/L)且整体安全性可控[13]。
海曲泊帕在临床试验和真实世界研究中展现出良好的疗效和安全性,为其在CTIT治疗及预防领域的广泛应用打下坚实基础。而海曲泊帕口服给药的便捷性更有利于CTIT患者的院外居家管理。期待未来有更多海曲泊帕相关前瞻性和真实世界研究开展,让更多CTIT患者获益。
[1]中国抗癌协会妇科肿瘤专业委员会. 子宫肉瘤诊断与治疗指南(2021年版)[J]. 中国癌症杂志,2021,31(6):513-519.
[2]中国抗癌协会肿瘤临床化疗专业委员会,中国抗癌协会肿瘤支持治疗专业委员会. 中国肿瘤药物相关血小板减少诊疗专家共识(2023版)[J]. 中华医学杂志,2023,103(33):2579-2590.
[3]Hensley ML, Miller A, O'Malley DM, et al. Randomized phase III trial of gemcitabine plus docetaxel plus bevacizumab or placebo as first-line treatment for metastatic uterine leiomyosarcoma: an NRG Oncology/Gynecologic Oncology Group study. J Clin Oncol. 2015;33(10):1180-1185.
[4]Pfisterer J, Shannon CM, Baumann K, et al. Bevacizumab and platinum-based combinations for recurrent ovarian cancer: a randomised, open-label, phase 3 trial [published correction appears in Lancet Oncol. 2022 Jun;23(6):e248]. Lancet Oncol. 2020;21(5):699-709. Supplementary Table S1.
[5]Takano T, Niikura H, Ito K, et al. Feasibility study of gemcitabine plus docetaxel in advanced or recurrent uterine leiomyosarcoma and undifferentiated endometrial sarcoma in Japan. Int J Clin Oncol. 2014;19(5):897-905.
[6]Hadoux J, Rey A, Duvillard P, et al. Multimodal treatment with doxorubicin, cisplatin, and ifosfamide for the treatment of advanced or metastatic uterine leiomyosarcoma: a unicentric experience. Int J Gynecol Cancer. 2015;25(2):296-302.
[7]唐伟林. 化疗药物致血小板减少患者的临床护理[J]. 中国实用护理杂志,2008,24(z2):176-177.
[8]Liutkauskiene S, Janciauskiene R, Jureniene K, Grizas S, Malonyte R, Juozaityte E. Retrospective analysis of the impact of platinum dose reduction and chemotherapy delays on the outcomes of stage III ovarian cancer patients. BMC Cancer. 2015;15:105. Published 2015 Mar 7.
[9]Zhang X, Chuai Y, Nie W, Wang A, Dai G. Thrombopoietin receptor agonists for prevention and treatment of chemotherapy-induced thrombocytopenia in patients with solid tumours. Cochrane Database Syst Rev. 2017;11(11):CD012035. Published 2017 Nov 27.
[10]中国临床肿瘤学会指南工作委员会.中国临床肿瘤协会(CSCO)非小细胞肺癌诊疗指南2023[M]. 北京:人民卫生出版社,2023.
[11]J. Wang,et al.2023 ESMO Abstract 2100P
[12]Jun Ma, et al. A multicenter, randomized phase II trial on the efficacy and safety of hetrombopag for the treatment of chemotherapy-induced thrombocytopenia in patients with advanced solid tumors. 2023 European Congress of Internal Medicine, Abstract 2360.
[13]Qin H, Zeng Z, Wang S, Gao F, Liu X. 351P Real-world study of herombopag in primary prevention and treatment of chemotherapy-induced thrombocytopenia (CIT) in advanced lung cancer. Annals of Oncology. 2022;33:S1579-S1579.
排版编辑:肿瘤资讯-展思懿
版权声明











 苏公网安备32059002004080号
苏公网安备32059002004080号


