根据2020年中国最新数据,胃癌发病率和死亡率在各种恶性肿瘤中均位居第三。且我国早期胃癌占比很低,大多数发现时已是进展期,总体5年生存率不足50%[1]。基于该情况,胃癌治疗的策略是以外科为主的综合治疗。而处于进展期的胃癌大多需要通过化疗、靶向、免疫等手段的联合用药进行综合治疗。
多种治疗手段的联合使用也导致患者更易出现骨髓抑制,包括血小板减少等治疗相关不良反应,严重影响着患者的治疗进程和疾病预后。因此,积极控制肿瘤治疗所致血小板减少症(CTIT)是提高进展期胃癌患者的治疗效果,改善患者生活质量的关键
本期内容带来了同济大学附属东方医院海亚楠医师分享1例初始体能状态相对较差的晚期胃癌患者经过多线治疗应用血小板生成素受体激动剂(TPO-RA)的二级预防过程,并邀请同济大学附属东方医院高勇教授对该病例诊疗过程进行精彩点评。
同济大学附属东方医院肿瘤科主治医师
上海交通大学医学院肿瘤学博士
上海市浦东新区肿瘤专业委员会秘书
上海市中西医结合学会第二届胰腺疾病专委会青委上海健康生活促进会肿瘤科普与综合诊疗专委会委员上海市社会医疗机构协会肿瘤学分会患教专委会委员
一般资料
基本情况
患者女,64岁,2022-02-02主因“气促1月,确诊晚期胃癌1周”就诊我院。
现病史
患者于2022-01因“胸闷气促”就诊于某医院,行胸部CT(2022-01-26)示:两肺间质性改变,癌性淋巴结炎可能;纵隔及肺门淋巴结肿大,心包积液。
PET-CT(2022-02-07)示:1.左肺上叶舌段实变影,MT待排;双肺癌性淋巴管炎待排;2.双侧锁骨区淋巴结、双肺门、纵膈淋巴结、肝胃间隙淋巴结、腹膜后淋巴结增大伴糖代谢增高;3.双侧胸腔、心包、盆腔少量积液;4.胃小弯侧糖代谢增高。
胃镜显示(2022-02):胃体MT。
既往史、个人史、家族史无特殊
查体
患者身高150 cm,体重42 kg,体表面积(BSA)1.37m2。ECOG-PS评分2分。
心率108次/分,律齐,未闻及明显病理性杂音;全身浅表淋巴结未触及;双肺呼吸音低,散在干啰音;腹平软,肝脾肋下未及;移动性浊音阴性。
辅助检查
影像学检查
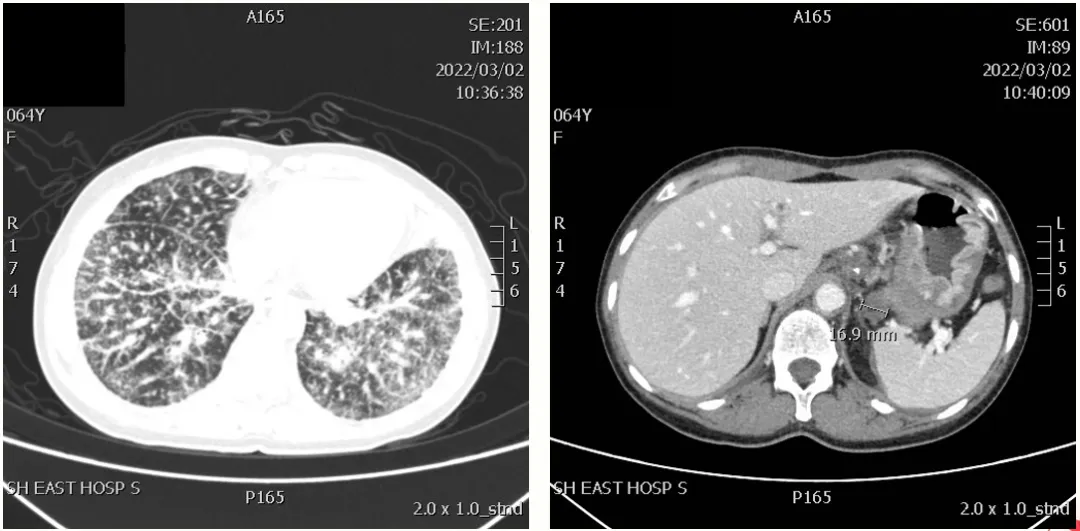
2022-03-03提示(如下图):双肺癌性淋巴管炎,转移性淋巴结。
胃镜及病理:镜下胃体部,见一巨大溃疡浸润灶侵及大部分胃壁,病灶底部覆黄苔及污秽苔,边缘隆起;其他未见异常。病理结果示,较多渗出、坏死组织,小灶异型腺体及黏液,符合腺癌;免疫组化,HER-2(0) PD-L1(-)。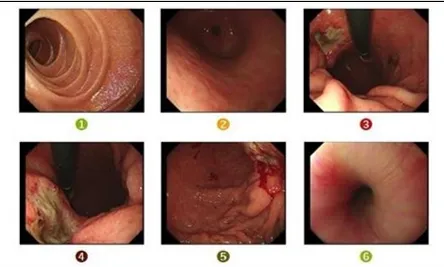
诊断
胃恶性肿瘤(胃体腺癌,Her-2 IHC阴性,MSS,PD-L1阴性,bTMB 13.42Muts/Mb)cTxN+M1b(M:非区域淋巴结、双肺)IV期,ECOG-PS 2分;
双肺癌性淋巴管炎;
双侧胸腔、心包、盆腔少量积液;
营养风险。
治疗经过
1、患者抗肿瘤治疗过程
01 2022-03-02至2022-07-29
【一线治疗】:行SOX方案(奥沙利铂175 mg ivgtt d1+替吉奥50 mg bid po d1-14,q3w)。
PFS 4个月,最佳疗效疾病稳定(SD),主要不良反应(AE):4级CTIT。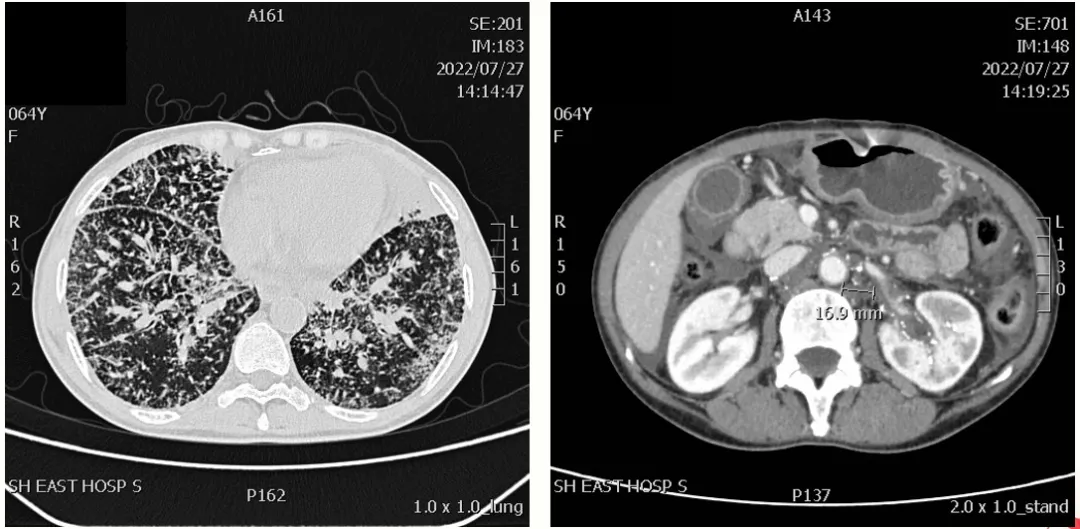
02 2022-09-01至2022-12-23
【二线治疗】:因患者疾病进展(PD)及严重AE,更换治疗方案为PD-1+Nab-p(卡瑞利珠单抗200 mg ivgtt d1+白蛋白紫杉醇200 mg ivgtt d1,q3w)。因考虑患者既往CTIT程度重且恢复时间长,此次给予Nab-p以约50%标准剂量起始,拟根据血象逐步加量。
PFS 4个月,最佳疗效SD,主要AE 3级CTIT。
03 2023-01-29及02-01
行腹腔热灌注化疗CDDP 80 mg/次×3;2023-02-02行脾栓。最佳疗效SD,无严重AE。疾病进展(PD)。
04 2023.02.17-至今
【三线治疗】:PD-1+IRI+呋喹替尼(节律化疗,卡瑞利珠单抗200 mg 静滴 d1+伊立替康100 ml 静滴 d1+呋喹替尼5 mg/d po d1-10,q2w)。
PFS 5个月以上,最佳疗效SD,主要AE 4级CTIT。应用TPO-RA二级预防+按期治疗。
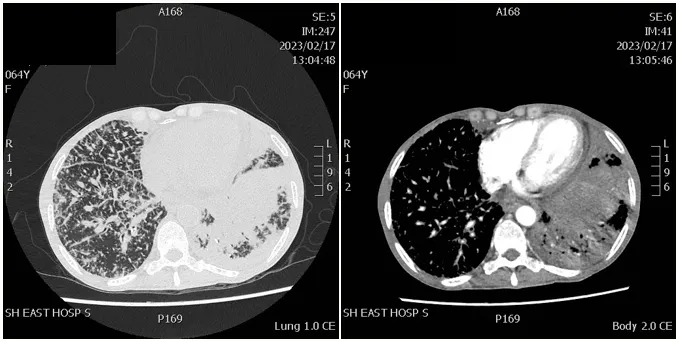
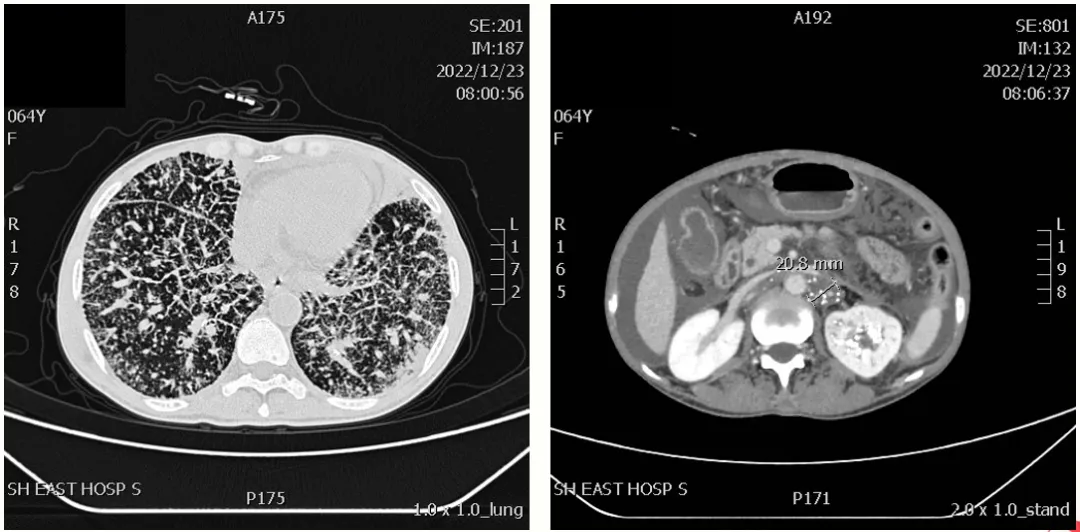
图 CT检查示:双肺癌性淋巴管炎,左肺下叶实变
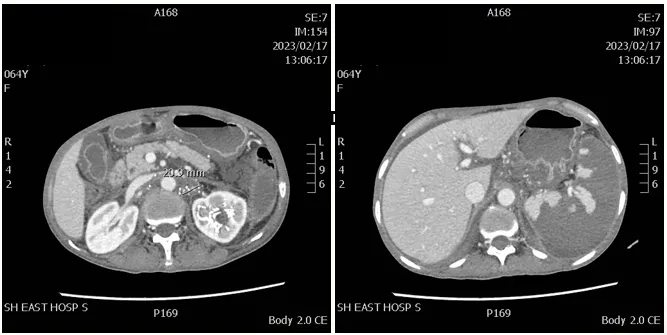
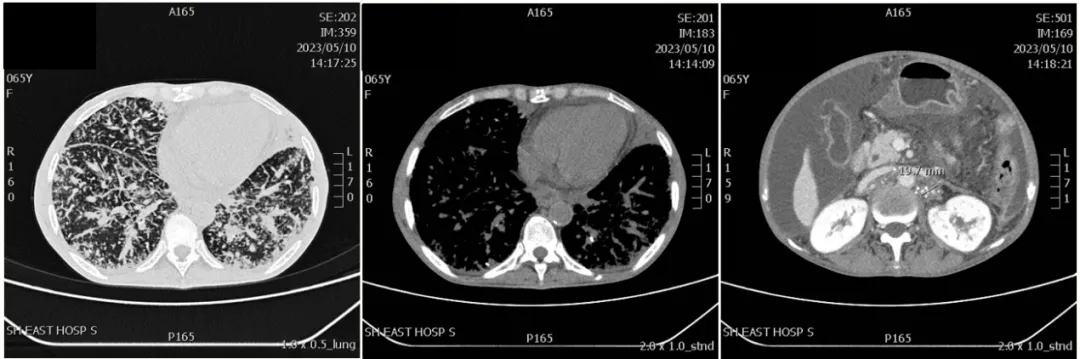
图 CT检查示,转移性淋巴结:SD+;脾脏栓塞后表现
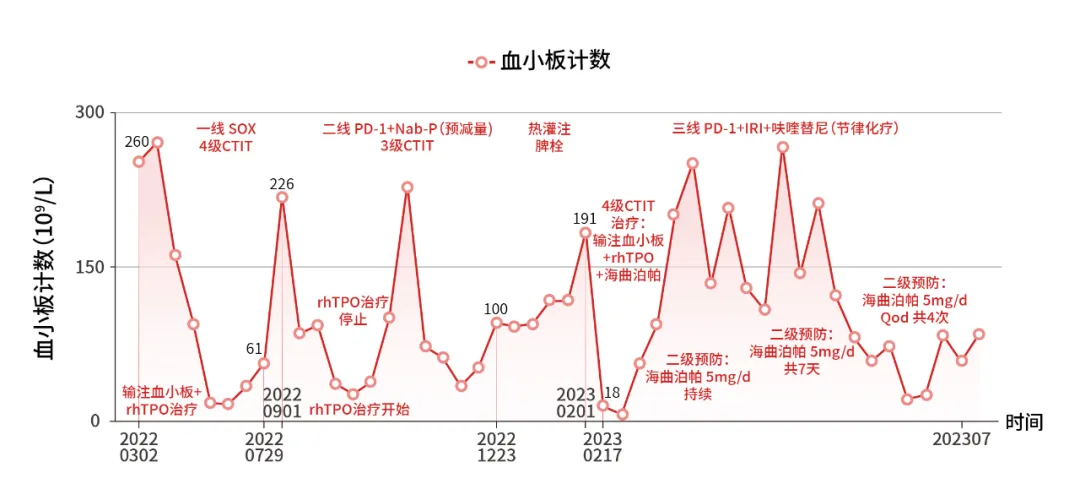
2、患者严重CTIT治疗过程
01 2022-03
【一线治疗】:患者在SOX方案化疗期间出现4级CTIT,临床表现为血涕、痰中带血,血小板(PLT)计数下降至20×109/L,予以重组人血小板生成素(rhTPO)15000U 皮下注射(ih)12天以及输注血小板,经治疗PLT计数上升至61×109/L停用。
02 2022-09
【二线治疗】:治疗期间,患者出现3级CTIT,临床表现为痔疮出血。期间最低PLT计数30×109/L。给予rhTPO15000U ih 9天,PLT计数上升至105×109/L后停用。
03 2023-02
【三线治疗】:患者经治疗再次出现4级CTIT,PLT最低降至10×109/L,临床表现为痔疮出血,予以输注血小板;rhTPO 15000U ih联合海曲泊帕5 mg/d空腹治疗治疗13天,PLT计数60×109/L后停用。
04
【预防性治疗经过】:此后应用海曲泊帕进行CTIT二级预防治疗,患者院外治疗,故采用口服方式。方案1:治疗结束后24h开始5 mg/d持续使用至下次用药前,未发生CTIT;方案2:治疗结束后24h开始5 mg/d共7d,未发生CTIT;方案3:治疗结束后24h开始5 mg/d qod 共4次,4级CTIT。
病例总结
本例患者就诊时ECOG-PS评分及BSA均较低,是发生CTIT发生的独立危险因素。不出意料,患者在一线接受化疗时,就已发生较严重的CTIT。据《肿瘤化疗所致血小板减少症诊疗中国专家共识(2021版)》[2](以下简称“《诊疗共识》”)推荐,给予血小板+rhTPO输注得以改善。在后续的二线、三线治疗中,患者仍出现了3-4级CTIT。
对于预防严重CTIT的发生,降低药物剂量、改变治疗方案、脾脏栓塞,都是可以考虑的方案。但通过有效的一、二级预防维持良好的骨髓功能,进而保证抗肿瘤治疗方案不因CTIT因素而改变方为上策。根据最新版《CSCO肿瘤治疗所致血小板减少症诊疗指南》[3](以下简称“《CTIT诊疗指南》”)推荐,在三线治疗再次出现4级CTIT后,计划进行二级预防的给药。
在CTIT二级预防的药物选择上,rhTPO及促血小板生长因子包括重组人白细胞介素11(rhIL-11)因剂型原因限制了其院外的便捷使用。TPO-RA已被初步证实其在CTIT预防性使用的有效性和安全性。因而予该患者TPO-RA——海曲泊帕预防性治疗,此后患者血小板水平维持稳定,通过二级预防保证了大多数治疗周期按期、按量进行。在该患者用药过程中,对于TPO-RA预防使用的给药剂量、开始时间、给药频次、持续时间、血小板监测频率、安全性监测方式等细节,也进行了一定探索,之后期待更多研究结果的公布,更好造福患者。
总之,虽然本例治疗最佳疗效仅SD,但已实现晚期胃癌18个月长生存并仍继续保持。更灵活的给药方式在高危CTIT肿瘤患者的二级预防中是提高肿瘤患者生活质量、保证抗肿瘤治疗顺利完成的重要“武器”。
专家点评
能否谈谈在晚期胃癌治疗中,血小板减少症的发生情况如何?
CTIT是肿瘤治疗中最常见的血液学毒性,可以导致化疗的剂量、强度降低,治疗时间延迟,甚至治疗终止,从而影响抗肿瘤治疗的效果。靶向治疗和免疫治疗常常与化疗联合,虽然提高了治疗的疗效,但同时也增加了CTIT发生的风险以及管理的难度。
有研究显示,靶向药物在胃癌的治疗中血小板减少症的发生率可达11%[4],如贝伐珠单抗、尼拉帕利等药物3-4级CTIT发生率大于15%;化疗含吉西他滨、铂类的方案3-4级CTIT发生率大于10%;免疫治疗全等级CTIT发生率高于9%[5,6]。且有研究显示,免疫治疗所致CTIT无法纠正时可导致死亡[7],治疗后需密切关注血小板数值。此外,多周期抗肿瘤治疗还会增加骨髓抑制的发生风险和严重程度,需引起重视。
该患者初始即判定存在CTIT的高危因素,对于这类CTIT患者应如何进行管理?
“CTIT诊疗指南和共识”中均明确指出,应根据肿瘤患者导致CTIT的危险因素进行分层,从而对患者发生CTIT的概率及严重程度做好预期和全程管理。如果患者在基础情况、原发病和合并症3类中符合的危险因素数量≥2条,则后续抗肿瘤治疗期间发生CTIT的风险较高。
本例患者初始即ECOG-PS评分及BSA均较低,均为CTIT发生的独立危险因素。在治疗期间,无论是一线化疗还是后续免疫联合治疗,患者均发生了严重的CTIT。给予患者TPO-RA——海曲泊帕预防性治疗之后,患者血小板水平维持在相对稳定的水平,保证了大多数治疗周期按期、按量进行。
“CTIT诊疗指南和共识”中均提到,应根据危险因素及原因评估采用不同的防治策略,治疗的主要目的是避免因血小板计数降低引起化疗延迟和(或)剂量降低,并防止出血事件发生。回顾这例患者的治疗经过,引发我们更多思考的是,对于评估后CTIT较高危的患者,是否应更早选择更为有效的药物来预防CTIT,以尽可能地提升治疗效果。
从本例患者出发,评价新一代TPO-RA海曲泊帕在高危CTIT人群的治疗中有何优势?
海曲泊帕是我国自主研发的新一代口服TPO-RA,受到《CTIT诊疗指南》Ⅱ级推荐用于CTIT的治疗和二级预防。在CTIT的治疗和预防上具有良好的应用前景。
已经公布的海曲泊帕Ⅱ期临床研究结果显示[8],海曲泊帕预防性连续给药可有效保证下一化疗周期的正常进行,有效率达72%,显著高于安慰剂组29%[8]。真实世界研究也显示,海曲泊帕可以有效预防高龄高风险肿瘤患者发生CTIT,应答率达100%[9]。
相较于安慰剂,海曲泊帕连续给药可显著提高患者的治疗有效率(60.7% vs. 12.9%,OR=10.4,P=0.0001)。联合rhTPO治疗的研究也表明海曲泊帕联合组可使CTIT患者的PLT计数快速恢复,中位治疗时间较rhTPO单药组缩短3天,效果优于rhTPO单药。
本例患者应用海曲泊帕预防治疗后疗效显著,PLT计数相对稳定,有效防止了由于CTIT可能导致ADC类药物减量或停药,影响肿瘤治疗疗效。而且海曲泊帕口服治疗便捷,在患者多周期ADC治疗过程中有助于提升患者的用药依从性,更好地实现了相关CTIT患者的院外管理,保障了患者治疗的完整性和疗效。总而言之,海曲泊帕升血小板有效、安全、使用便捷,对于合并高危因素CTIT患者的治疗和预防中具有明显的应用优势。
[1]《胃癌诊疗指南(2022版)》[2] TUMOR, 2021, 41 (12): 812-827[3] 中国临床肿瘤学会指南工作委员会. 中国临床肿瘤学会(CSCO)肿瘤治疗所致血小板减少症指南2023[M].北京:人民卫生出版社,2023.[4] Thuss-Patience PC, et al. Lancet Oncol. 2017 May;18(5):640-653.[5]Ying Wu et al. Clinical Therapeutics, 2009, 31: 2416-2432
[6]肿瘤治疗相关血小板减少症的临床管理专家共识(2021)[5] LEE J L, et al. Br J Cancer, 2008, 99(4):584-590.[7] 王理伟.肿瘤,2021,41(12):828-831.[8] Jun Ma, et al. 2023 European Congress of Internal Medicine, Abstract 2360.[9] Haifeng Qin.Annals of Oncology (2022) 33 (suppl_9): S1560-S1597.
排版编辑:肿瘤资讯-邓文普











 苏公网安备32059002004080号
苏公网安备32059002004080号


