在当今医学领域,肿瘤治疗所致血小板减少症(cancer treatment‑induced thrombocytopenia,CTIT)仍然是一个复杂且难以攻克的难题,它显著地影响了患者的治疗效果和生活质量1。然而,随着科学研究的不断探索和深化,新型的治疗策略和药物正逐步崭露头角,为攻克这一难题提供了更为有力的武器。本文将深入剖析CTIT治疗的现存困境和革新之路,旨在为临床医生提供更为系统、深入、前沿的CTIT管理策略,以期能够为患者带来更为显著的治疗效果和生活质量的提升。
CTIT治疗困局:传统策略亟需突破
当前,针对CTIT的传统治疗手段主要集中在两个方面:输注血小板和应用促血小板生长因子。就促血小板生长因子而言,主要包括传统升板药物如重组人白介素-11(recombinant human interleukin 11,rhIL-11)和重组人血小板生成素(recombinant human thrombopoietin,rhTPO)等生物制剂,以及新型升板药物血小板生成素受体激动剂(thrombopoietin receptor agonist,TPO-RA)等2。
中国临床肿瘤学会(CSCO)《肿瘤治疗所致血小板减少症诊疗指南2023》明确指出,输注血小板是严重血小板减少症患者的最快最有效的治疗方法之一,当血小板计数≤10×109/L时,需预防输注血小板2。然而,血小板输注并非万全之策,它存在着显著的局限性。具体而言,由于异体血小板在体内的存活时间较短,通常只能维持3~5天,因此CTIT患者往往需要接受多次输注;与此同时,血小板的捐献难度较大,且符合条件的捐献者较少,血小板血源紧张的情况较为普遍,这给CTIT患者的救治工作带来了一定的影响;此外,输注血制品还潜藏着传播血液感染性疾病的风险,如艾滋病、乙型及丙型肝炎等;更为严重的是,部分患者可能因产生血小板抗体而导致输注无效,甚至引发输注后的免疫反应2。
传统的升板药物,如rhIL-11和rhTPO,在提升化疗前血小板计数及降低输血需求方面已展现出一定的疗效,且这两种药物在相关指南中也有所推荐1,2。CSCO指南指出,对于不符合血小板输注指征的CTIT患者,当血小板计数低于(25~75)×109/L时,可考虑使用rhIL-11;当血小板计数<100x109/L时,可考虑使用rhTPO,对上一个化疗周期发生过2级以上CTIT的患者或出血风险较大的患者,也可给予rhTPO进行二级预防治疗2。
然而,rhIL-11和rhTPO也存在一定的局限性。在给药方式方面,rhIL-11和rhTPO均为皮下注射,这给患者带来了用药的不便2。在安全性方面,rhIL-11的不良反应较为明显,首次给药或多次给药后可能会发生过敏或超敏反应,且具有一定的心脏毒性,有增加中老年患者心房颤动发生率的可能2,3;rhTPO的不良反应相对较少而轻微,但过量使用可能引起血小板计数过度增加并诱发血栓形成1。这些安全性问题也在一定程度上限制了两种传统升板药物在CTIT患者中的广泛应用。
鉴于这些传统治疗手段的局限性,CTIT的治疗仍面临诸多挑战,这也凸显了该领域对于创新和改进的迫切需求。其中,TPO-RA正是在CTIT的这种困局下脱颖而出的一种新兴治疗手段。那么,TPO-RA能否更为有效、便利且安全地提升CTIT患者的血小板计数呢?
TPO-RA破局之路:CTIT治疗的新探索与新发现
随着医学研究的持续深入,TPO-RA已被证明是一种安全高效的治疗手段,可为CTIT患者提供了新的治疗选择和希望。在我国,目前已经获批上市的TPO-RA类药物包括海曲泊帕、艾曲泊帕、阿伐曲泊帕以及罗普司亭等2。
TPO-RA发挥促血小板生成的主要作用机制为,通过与巨核细胞表面的TPO受体c-Mpl蛋白结合,促进造血前体细胞向巨核细胞系分化,抑制其凋亡,增加巨核细胞的多倍体数,进而促进巨核细胞的集落形成,增加血小板的生成4;其中,口服小分子非肽类TPO-RA不与内源性TPO分子竞争结合位点,与内源性TPO具有累加效应5。
目前,TPO-RA在CTIT治疗领域已展开多项研究。一项关于艾曲泊帕的I期临床研究表明,在接受吉西他滨治疗的实体肿瘤患者中,艾曲泊帕能够显著减少化疗延迟和剂量减少的情况6;我国一项多中心、单臂研究显示,阿伐曲泊帕可使CTIT患者的血小板计数较基线显著增加,加速实体瘤患者化疗后血小板减少的 恢复 ,且安全性和耐受性良好7。这些临床研究初步揭示了TPO-RA在治疗CTIT中的潜在疗效。然而,艾曲泊帕的一项后续II期随机对照临床研究8以及阿伐曲泊帕的关键III期注册临床研究9均未能达到预期效果,这强调了我们需要进一步探索更多疗效确切且安全性良好的TPO-RA类药物。
与艾曲泊帕和阿伐曲泊帕不同的是,海曲泊帕在CTIT治疗中的表现却令人瞩目。一项随机双盲多中心的II期临床研究结果显示,与安慰剂相比,海曲泊帕能够使CTIT患者的血小板计数快速且稳定地恢复至正常水平,从而显著缩短恢复时间,让更多患者确保后续的化疗周期能够按计划顺利进行9。这使得海曲泊帕有望成为CTIT患者的一种更高效、更便捷的治疗选择。
CTIT治疗破局新星:海曲泊帕
海曲泊帕,作为我国自主研发的创新型口服、小分子、非肽类TPO-RA药物10,因其在提升血小板方面的独特优势以及较高的可及性,已成为CTIT治疗的革新选择,在CTIT治疗领域具有广阔应用前景12,13。
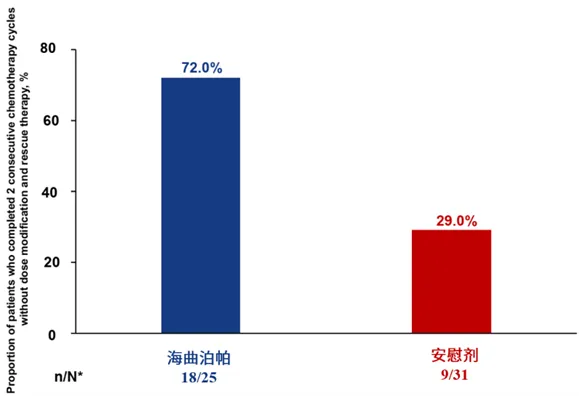
2023年欧洲内科医学大会(ECIM)公布的一项随机双盲多中心II期临床研究结果显示,海曲泊帕可快速恢复血小板水平,血小板水平恢复至≥100X109的中位时间仅需7.5天,较安慰剂组13天显著缩短5.5天。此外,在恢复了第一个计划的化疗周期的患者中,海曲泊帕组有72.0%的患者完成了两个连续的化疗周期,而无需进行剂量修改或补救治疗(图1),安慰剂组仅为29.0%。这些数据表明,海曲泊帕不仅升板速度快,可显著缩短CTIT患者治疗时间,同时连续使用能保证下一周期化疗的正常进行,避免患者因血小板减少而调整治疗方案10。
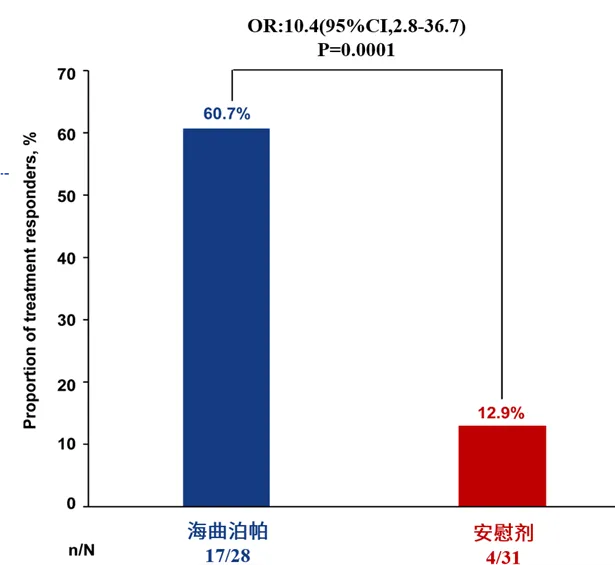
海曲泊帕的治疗有效率(患者在14天内恢复化疗,并连续完成两个计划化疗方案,期间没有因血小板减少调整化疗方案,且未使用升血小板援救治疗)达到了60.7%,显著超越了安慰剂组的12.9%(OR:10.4[95%CI, 2.8-36.7], P=0.0001)(图2)。这一显著差异表明海曲泊帕能够有效提升患者血小板计数,减少因血小板减少导致的化疗剂量调整或延迟,从而改善CTIT患者预后10。
海曲泊帕的安全性和耐受性数据也呈现出积极的结果,整个治疗周期内,未报告任何与海曲泊帕直接相关的严重不良事件,这充分证实了其良好的安全性特征。对于化疗患者而言,升板治疗的安全性尤为重要,因为这类患者通常处于多种并发症风险之中,急需一种既高效又可避免额外健康风险的治疗手段来应对CTIT 10。海曲泊帕的出现,为这类患者提供了一个值得信赖的治疗选择。
除此之外,海曲泊帕联合治疗也取得了积极结果。2022年美国血液学会年会(ASH)公布的一项临床研究显示,海曲泊帕联合rhTPO治疗血小板水平<50×109/L的CTIT患者的中位治疗时间为6.5天,较rhTPO单药组缩短3天,且海曲泊帕联合rhTPO组的7天应答率达75%,显著高于rhTPO单药组30%14。
在2023年欧洲临床肿瘤学会年会(ESMO)上公布的最新研究数据进一步佐证了海曲泊帕的卓越疗效。在同步或序贯放化疗的患者群体中,海曲泊帕展现出高达93%的治疗有效率,且在整个治疗过程中未报告任何3-4级不良事件,这再次凸显了其出色的安全性和有效性15。
值得一提的是,海曲泊帕具备快速提升血小板计数的特点,这一优势能够大幅缩短患者的治疗时间,且有助于降低CTIT患者的住院成本,进而减轻其经济负担;同时,作为一款口服小分子TPO-RA药物,海曲泊帕相较于需要注射的同类药物,在使用的便捷性和患者的治疗依从性方面也具备显著优势11。这些特点共同使得海曲泊帕成为CTIT治疗领域中的“破局”新星。
海曲泊帕在CSCO指南中的推荐地位,充分彰显了其在CTIT治疗领域的重要性。该指南明确推荐,对于有或无出血症状的CTIT患者,可优先考虑使用海曲泊帕单药治疗(2A类证据支持);同时,也可考虑将其与rhTPO联合使用(2B类证据支持)2。这一推荐建议不仅建立在海曲泊帕在多项临床研究中展现出的积极成果之上,更体现了医学专家对其疗效的一致认可与信赖。此外,海曲泊帕还在2024年的医保续约过程中成功实现了7.5%的价格下调,其最新的医保价格已降低至每片116.5元。这一重要举措无疑极大地提高了海曲泊帕的药物可及性,使更多需要接受CTIT治疗的患者能够负担得起这一创新药物,并从中获益16。
总结
CTIT治疗领域长期以来面临着传统治疗手段的局限性,包括血小板输注的潜在风险和不便,以及传统升血小板药物的注射给药方式和安全性等问题。这些挑战凸显了对创新治疗策略的迫切需求。在这一背景下, TPO-RA作为新型治疗选择,展现出显著的优势和潜力。特别是海曲泊帕,作为我国自主研发的创新型TPO-RA药物,在多项国际临床研究中表现出色,显著提升了CTIT患者的血小板计数,确保了化疗方案的连续性,并展现出良好的安全性和耐受性。其口服给药方式和快速提升血小板的特点,为患者带来了极大的便利性和依从性。海曲泊帕在CSCO指南中的推荐地位以及医保续约中的价格下调,进一步提升了其可及性,使更多患者能够受益于这一创新治疗。海曲泊帕的成功应用不仅为CTIT治疗领域带来了新的突破,也为临床医生提供了更为高效、安全的治疗选择,有力地推动了该领域的进步与发展。
[1]中国抗癌协会肿瘤临床化疗专业委员会,中国抗癌协会肿瘤支持治疗专业委员会. 中国肿瘤药物相关血小板减少诊疗专家共识(2023版)[J].中华医学杂志,2023,103(33):2579-2590.
[2]中国临床肿瘤学会(CSCO)肿瘤治疗所致血小板减少症诊疗指南2023
[3]Xu J, Ren JF, Mugelli A, Belardinelli L, Keith Jr JC Jr, Pelleg A. Age-dependent atrial remodeling induced by recombinant human interleukin-11: implications for atrial flutter/fibrillation. J Cardiovasc Pharmacol. 2002;39(3):435-440.
[4]李洋,杨仁池.血小板生成素受体激动剂的临床应用及研究进展.国际输血及血液学杂志,2014,37(6):584-588.
[5]中华医学会血液学分会血栓与止血学组. 促血小板生成药物临床应用管理中国专家共识(2023年版) [J] . 中华血液学杂志, 2023, 44(7) : 535-542.
[6]Winer ES, Safran H, Karaszewska B, et al. Eltrombopag with gemcitabine-based chemotherapy in patients with advanced solid tumors: a randomized phase I study. Cancer Med. 2015;4(1):16-26.
[7]Gao Y, Liu Q, Shen Y, et al. Effect of avatrombopag in the management of severe and refractory chemotherapy-induced thrombocytopenia (CIT) in patients with solid tumors. Platelets. 2022;33(7):1024-1030.
[8]Winer ES, Safran H, Karaszewska B, et al. Eltrombopag for thrombocytopenia in patients with advanced solid tumors receiving gemcitabine-based chemotherapy: a randomized, placebo-controlled phase 2 study. Int J Hematol. 2017;106(6):765-776.
[9]Al-Samkari H, Kolb-Sielecki J, et al. Avatrombopag for chemotherapy-induced thrombocytopenia in patients with non-haematological malignancies: an international, randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Haematol. 2022 Mar;9(3):e179-e189.
[10]Jun Ma, et al. 2023 European Congress of Internal Medicine, Abstract 2360.
[11]中国临床肿瘤学会(CSCO)抗肿瘤药物治疗安全管理专家委员会. 海曲泊帕临床应用指导原则[J].白血病·淋巴瘤,2022,31(10):577-582.
[12]Kellum A, Jagiello-Gruszfeld A, Bondarenko IN, Patwardhan R, Messam C, Mostafa Kamel Y. A randomized, double-blind, placebo-controlled, dose ranging study to assess the efficacy and safety of eltrombopag in patients receiving carboplatin/paclitaxel for advanced solid tumors. Curr Med Res Opin. 2010;26(10):2339-2346.
[13]Winer ES, Safran H, Karaszewska B, et al. Eltrombopag for thrombocytopenia in patients with advanced solid tumors receiving gemcitabine-based chemotherapy: a randomized, placebo-controlled phase 2 study. Int J Hematol. 2017;106(6):765-776.
[14]https://ash.confex.com/ash/2022/webprogram/Paper164490.html
[15]Jun Wang, et al. An exploratory study of the efficacy and safety of hetrombopag in the treatment of thrombocytopenia induced by concurrent or sequential chemoradiotherapy. P2100 , ESMO 2023 0ct.
[16]国家基本医疗保险、工伤保险和生育保险药品目录(2023年)
排版编辑:肿瘤资讯-邓文普











 苏公网安备32059002004080号
苏公网安备32059002004080号


