阳春三月,春意渐浓,万物复苏,血液学领域的研究也如春日繁花般绚烂多彩。从滤泡性淋巴瘤(FL)的预后标志物优化,到慢性淋巴细胞白血病(CLL)以MRD为指导的创新治疗策略,再到骨髓纤维化的靶向治疗革新,众多国际顶级期刊,如Blood、JAMA Oncology、British Journal of Haematology杂志相继发表多项有望改变临床实践的研究成果,为临床治疗和研究方向提供了新的思路和依据。【肿瘤资讯】特整理此文,与您分享前沿突破,共同见证血液学研究的春天!
British Journal of Haematology
高肿瘤负荷FL的POD24预测标志物:淋巴细胞/单核细胞比值
原文标题:A low lymphocyte-to-monocyte ratio is independently associatedwith early relapse (POD24) in high tumour burden follicularlymphoma: A RELEVANCE subanalysis
主要内容:
FL是一种通常预后较好的非霍奇金淋巴瘤,但部分患者表现出更具侵袭性的行为。肿瘤微环境(TME)在FL的发病机制、进展和治疗反应中起着关键作用,其中肿瘤相关巨噬细胞(TAM)是TME中的关键细胞。研究表明,单核细胞的增加可能反映更高的M2型TAM活性,与更有利于肿瘤生长的TME相关,此外,淋巴细胞绝对值(ALC)可能反映机体的免疫状态,较低的循环淋巴细胞可能意味着较差的抗肿瘤免疫反应。基于此,多项研究已证实外周血淋巴细胞-单核细胞比值(LMR)可以预测FL的预后。
近日,British Journal of Haematology杂志发表了一项在大型RELEVANCE研究中的验证结果,显示LMR是一个易于获取的指标,能够独立预测高肿瘤负荷FL患者的早期复发风险,尤其是在低危FLIPI患者中更为显著。
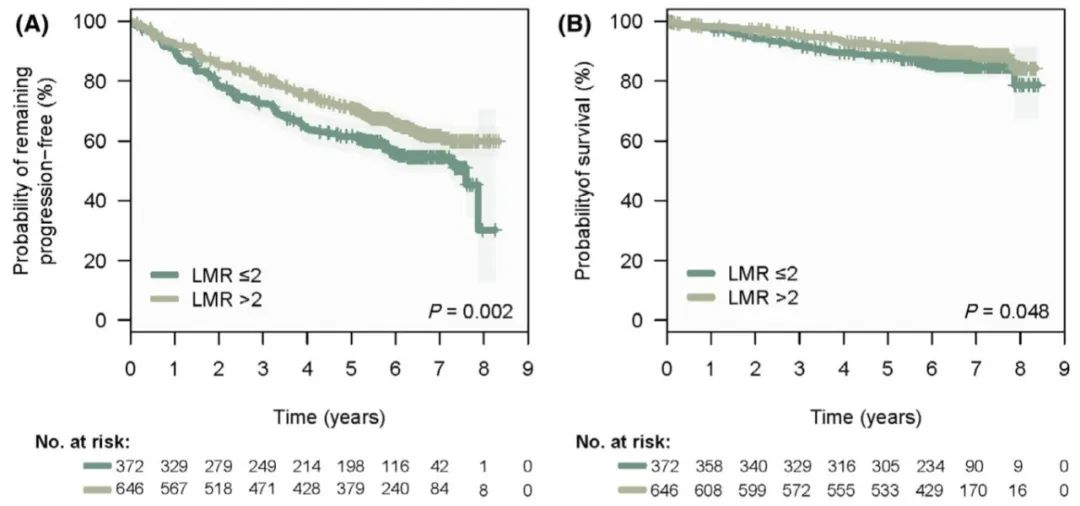
研究纳入1018例未经治疗的高肿瘤负荷FL患者,通过计算淋巴细胞绝对值与单核细胞绝对值的比值确定LMR。结果显示,中位LMR为2.5,最佳cut-off值为2。LMR<2与较短的无进展生存期(PFS)和总生存期(OS)相关,且在R-化疗组中,LMR与PFS的相关性更为显著。此外,LMR在低危FLIPI组中具有重要的预后价值,能进一步细化风险分层,可独立预测高肿瘤负荷FL患者的早期复发风险。
Nature Medicine
Pelabresib+芦可替尼治疗初治骨髓纤维化的Ⅲ期研究结果
原文标题:Pelabresib plus ruxolitinib for JAK inhibitor-naive myelofibrosis: a randomized phase 3 trial.
主要内容:
骨髓纤维化(MF)是一种以JAK-STAT信号通路异常激活为特征的骨髓增殖性肿瘤,常由JAK2、CALR或MPL基因突变驱动。BET蛋白BRD4在调节NF-KB介导的炎症中起关键作用,而NF-KB信号网络在MF中促进炎症因子的产生,因此,同时抑制BET和JAK可能是一种有效的治疗策略。
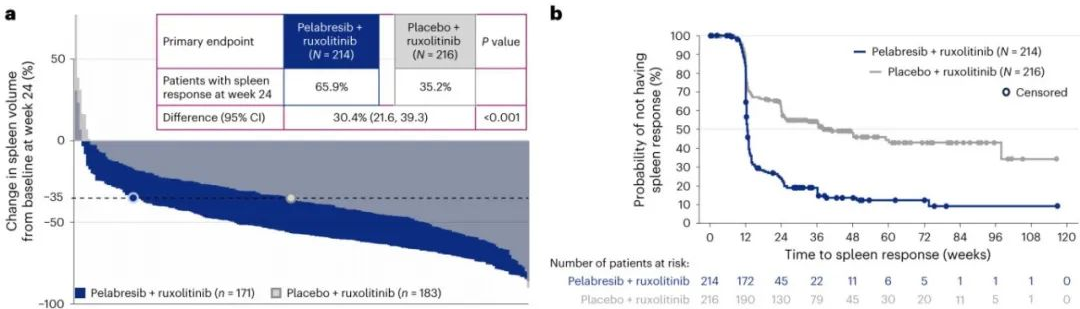
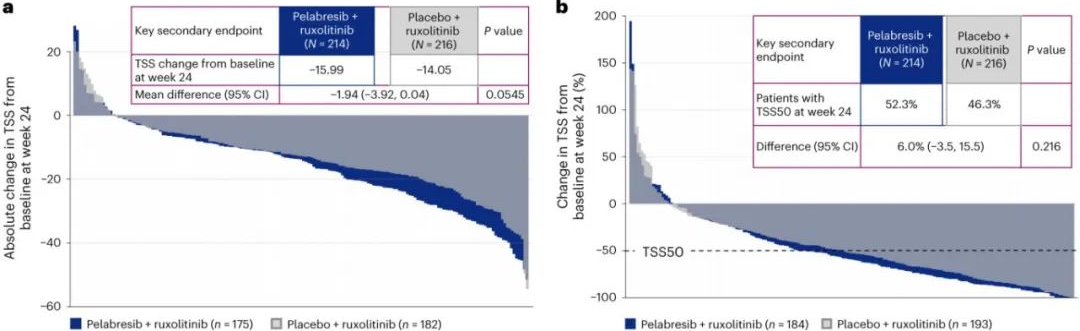
近日,Nature Medicine杂志发表了一项全球Ⅲ期研究,比较了Pelabresib联合芦可替尼与安慰剂联合芦可替尼在初治MF患者中的疗效和安全性。研究
结果显示,Pelabresib联合芦可替尼组在第24周脾脏体积减少≥35%的患者比例显著高于安慰剂联合芦可替尼组,症状改善方面也更优,且在降低炎症因子水平、改善MF上效果更好。两组不良事件发生率相当,联合治疗组的> 3级不良事件发生率低于单药治疗组。总之,这一联合治疗策略为初治MF患者提供了新的选择。
Blood
以MRD为指导的治疗在复发难治CLL中表现出显著的临床获益
原文标题:MRD-guided zanubrutinib, venetoclax, and obinutuzumab in relapsed CLL: primary end point analysis from the CLL2-BZAG trial
主要内容:
近年来,CLL的治疗格局随着BTK抑制剂和BCL22抑制剂的引入发生了显著变化,患者预后得到显著改善。然而,在复发/难治性(R/R)CLL患者中,尤其是那些已经接受过BTK抑制剂和/或BCL-2抑制剂治疗的患者,治疗选择仍然有限。
CLL2-BZAG试验是一项Ⅱ期、研究者发起的研究,共纳入42例R/R CLL患者。患者接受泽布替尼、维奈克拉和奥妥珠单抗的三药联合诱导治疗和维持治疗。主要终点是诱导治疗6个周期后外周血中MRD阴性的患者比例。
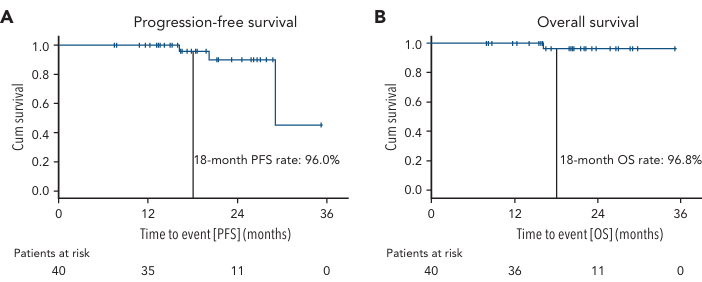
中位随访21.5个月,所有患者均获得缓解,其中52.5%的患者在诱导治疗结束后达到MRD阴性。随着时间推移,缓解程度加深,最佳MRD阴性率达到85%。18个月PFS率为96%,OS率为96.8%。最常见的不良事件为COVID-19(61.9%)、腹泻(35.7%)和输注相关反应(35.7%)。未观察到意料之外的毒性反应。
该研究结果表明,基于MRD指导的泽布替尼、维奈克拉和奥妥珠单抗三药联合治疗在R/R CLL患者中具有良好的疗效和耐受性,尤其是在那些既往接受过BTK抑制剂和/或BCL-2抑制剂治疗的高危患者中。
JAMA Oncology
FDG-PET反应指导的挽救治疗策略在儿童复发/难治性霍奇金淋巴瘤中的应用
原文标题:Transplant and nontransplant salvage therapy in pediatric relapsed or refractory Hodgkin lymphoma: The EuroNet-PHL-R1 phase 3 nonrandomized clinical trial
主要内容:
复发/难治性经典型霍奇金淋巴瘤(cHL)的当前标准挽救治疗包括高剂量化疗(HDCT)联合自体干细胞移植(ASCT)。然而,这种治疗方案的毒性较大,且并非所有患者都能从中获益。因此,研究者们希望通过风险分层和氟脱氧葡萄糖-18(FDG)正电子发射断层扫描(PET)对再诱导化疗的反应评估,来识别那些可能仅通过化疗和放疗就能治愈的低危患者,从而避免HDCT/ASCT的毒性,同时保留HDCT/ASCT用于高危患者。
EuroNet-PHL-R1是一项非随机临床试验,共纳入了来自13个欧洲国家的68个中心的118例18岁以下的首次R/R cHL患者。根据FDG-PET反应,患者被分为低危组(晚期复发且对再诱导化疗有良好反应)和高危组(原发进展或对再诱导化疗反应不佳)。低危组患者接受第二周期TEP/ABVD化疗和放疗,而高危组患者接受第二周期TEP/ABVD化疗后进行HDCT/ASCT,部分患者还接受放疗。主要终点是5年无事件生存(EFS)率。
中位随访时间为67.5个月,整体5年PFS率为71.3%,OS率为82.7%。低危组(n=59)中,41例接受非移植挽救治疗的患者5年PFS率为89.7%,OS率为97.4%;18例接受HDCT/ASCT的患者5年PFS率为88.9%,OS率为100%。高危组(n=59)中,所有患者均接受HDCT/ASCT,5年PFS率为53.3%,OS率为66.5%。
总体而言,FDG-PET反应指导的挽救治疗策略可以识别出那些通过非移植治疗就能获得良好预后的患者,同时将HDCT/ASCT保留给高危患者。
[1]A low lymphocyte-to-monocyte ratio is independently associated with early relapse (POD24) in high tumour burden follicular lymphoma: A RELEVANCE subanalysis. Br J Haematol. 2025 Mar 3. doi: 10.1111/bjh.20038.
[2]Rampal, R.K., Grosicki, S., Chraniuk, D. et al. Pelabresib plus ruxolitinib for JAK inhibitor-naive myelofibrosis: a randomized phase 3 trial. Nat Med (2025). https://doi.org/10.1038/s41591-025-03572-3
[3]Fürstenau M, Robrecht S, Schneider C, et al. MRD-guided zanubrutinib, venetoclax, and obinutuzumab in relapsed CLL: primary end point analysis from the CLL2-BZAG trial[J]. Blood, 2025, 145(12): 1282-1292.
[4]Daw S, Claviez A, Kurch L, et al. Transplant and nontransplant salvage therapy in pediatric relapsed or refractory Hodgkin lymphoma: The EuroNet-PHL-R1 phase 3 nonrandomized clinical trial[J]. JAMA oncology, 2025.
排版编辑:mathilda











 苏公网安备32059002004080号
苏公网安备32059002004080号


