圣安东尼奥乳腺癌研讨会(SABCS)作为全球乳腺癌研究的年度盛会,持续吸引全球专家关注。近期,2025 SABCS精粹中国行·上海站于1月12日圆满落下帷幕。OlympiA研究6.1年数据闪耀SABCS,亦是基于III期OlympiA研究的试验结果,奥拉帕利在中国获批用于BRCA突变HER2阴性高危早期乳腺癌的辅助治疗。此次,OlympiA中国牵头研究者邵志敏教授主持上海站活动。在此背景下,【肿瘤资讯】针对复旦大学附属肿瘤医院范蕾教授所深度解读的OlympiA研究长期随访结果,进行了精心编纂与整理,旨在使读者深刻洞察该领域的重要学术进展。

BRCA1/2突变HER2阴性高复发预后差
OlympiA 研究掀起“iDFS、DDFS、OS”
早期显著获益浪潮
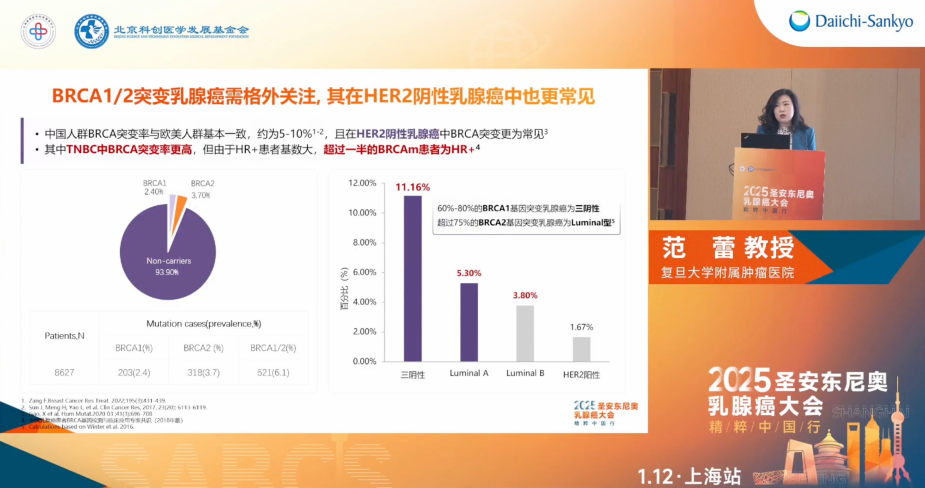
早期诊治是乳腺癌实现治愈的关键时机,一旦疾病进展至晚期阶段时,不仅整体医疗资源消耗显著增加,患者的预后状况亦急剧恶化。因此,对于早期乳腺癌患者,应尽早采用有效、系统的治疗方案,为患者提供治愈机会。对携带BRCA1/2突变的乳腺癌病例需给予特别重视,此类突变在HER2阴性乳腺癌中亦尤为普遍。具体来看,三阴性乳腺癌(TNBC)中的BRCA突变率高达11.16%,而在Luminal A型乳腺癌中这一比例为5.3%,在Luminal B型中则为3.8%。尽管从绝对数值上看,突变率有所差异,但鉴于HR+患者群体基数庞大,超过半数的BRCA突变患者实际上属于HR+亚群。不过,总体来说,BRCA基因突变在HER2阴性乳腺癌中的重要性不容忽视,其对于该疾病类型的临床管理与治疗策略制定具有深远意义[1-3]。
既往研究表明,相较于非BRCA突变患者,携带BRCA突变的乳腺癌患者面临更高的同侧及对侧乳腺癌复发风险。此类患者的无病生存期(DFS)显著缩短,同时远处转移风险也相应增加。荟萃分析显示,BRCA突变乳腺癌患者的死亡风险较非突变患者高出近30%[4,5]。鉴于此,国内外权威指南均一致推荐对高危乳腺癌患者进行BRCA基因检测。然而,值得注意的是,尽管各指南均强调BRCA检测的重要性,但在具体推荐细节上仍存在一定的差异。ASCO乳腺癌胚系基因检测指南2024指出,所有新诊断出患有I-III 期或新发 IV 期/转移性疾病、诊断时年龄在 65 岁或以下的乳腺癌患者都应接受gBRCA1/2 检测。NCCN 乳腺癌临床实践指南2024 V5推荐,确诊时乳腺癌患者年龄≤50岁,有高风险家族史、TNBC患者以及晚期乳腺癌和早期高危HER2阴性乳腺癌评估PARPi用药适应症的患者进行BRCA基因检测。基于中国人群的BRCA胚系突变筛查专家共识(2024年版)推荐BRCA胚系突变相关肿瘤的遗传高风险人群建议进行基因检测,暂未确定为高风险人群的个体建议在自愿原则下完成基因检测。当前,随着基因突变检测技术的普及与成本逐步降低,推荐对所有患者进行此类检测,尽早获取其基因突变信息,以便在疾病治疗早期及晚期阶段,能够针对性地采取相应靶向治疗措施进行干预[6-8]。
现如今,PARP 抑制剂(PARPi)在包括乳腺癌在内的多种实体瘤,尤其是晚期肿瘤中,展现了重要的临床价值。其作用机制在于通过合成致死机制,阻止DNA损伤修复,诱导BRCA突变肿瘤细胞凋亡。当BRCA1/2突变而引起同源重组缺陷(HRD)时,PARP能代偿BRCA的修复作用。然而,当两种DNA损伤修复途径均出现障碍,则促进肿瘤细胞的凋亡。
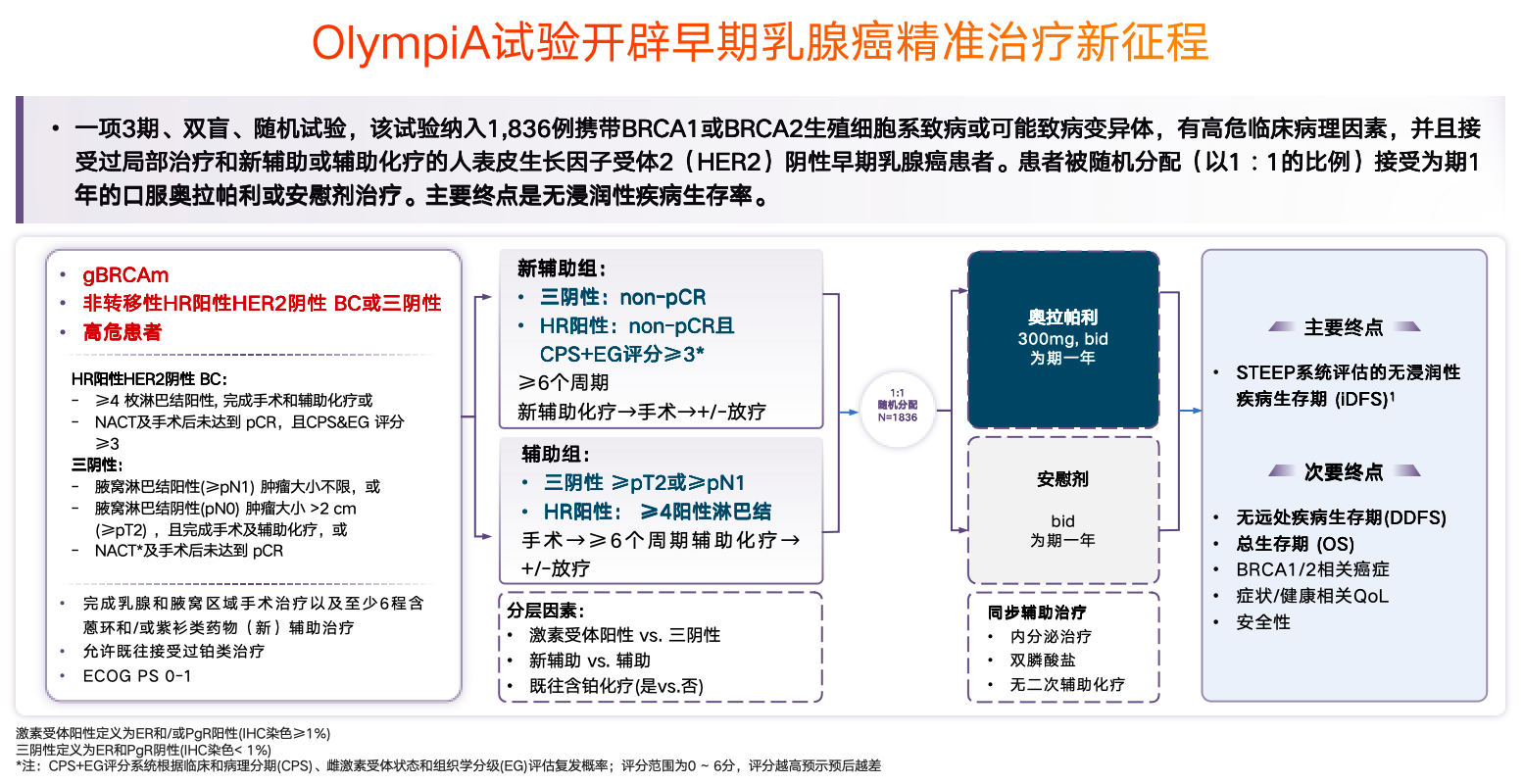
针对乳腺癌的治疗目标,是使患者在早期阶段获得治愈,从而最大限度地减少复发与转移的风险。OlympiA研究为早期乳腺癌的精准治疗开辟了新的道路,引领了治疗策略的发展方向。该研究为一项3期、双盲、随机试验,该试验纳入1836例携带BRCA1或BRCA2生殖细胞系致病或可能致病变异体,有高危临床病理因素,并且接受过局部治疗和新辅助或辅助化疗的HER2阴性早期乳腺癌患者。患者被随机分配(以1∶1的比例)接受为期1年的口服PARPi奥拉帕利或安慰剂治疗。主要终点是无浸润性疾病生存期 (iDFS)[9]。
在此研究中奥拉帕利组81.5%为TNBC,18.2%为HR+/HER2-。差异原因在于在相对于奥拉帕利联合内分泌治疗的复发风险方面(对于HR+按照机构治疗指南给予辅助内分泌治疗),监管机构认可了安全性依据,之后试验方案于2015年做出修订,纳入高危HR+乳腺癌患者,并将样本量增加至目前的1800例患者。总体上,OlympiA研究入组患者组间保持平衡,方案修订后纳入了HR+患者[9]。
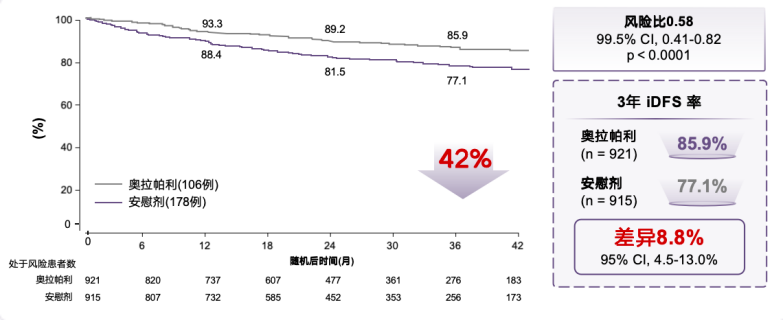
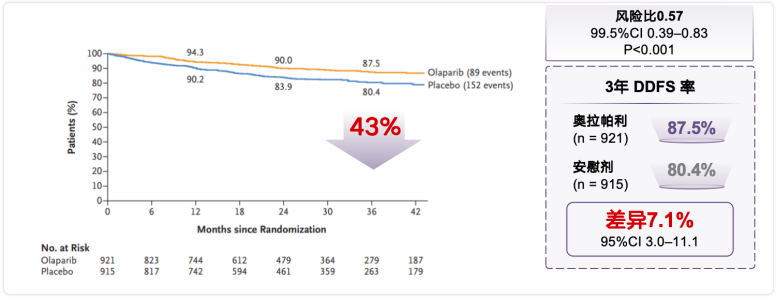
OlympiA 研究首次分析结果显示,奥拉帕利组较对照组显著提高3年iDFS率8.8%。同时,奥拉帕利组较对照组显著降低远处疾病复发风险43%,两组3年无远处疾病生存期(DDFS)率差异7.1%(87.5% VS 80.4%)[9]。
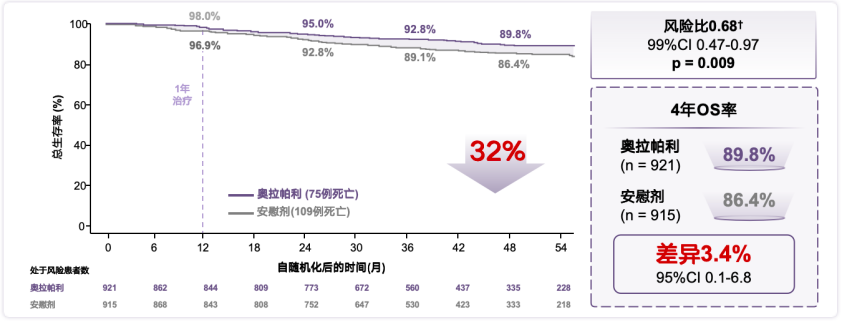
二次分析结果显示,奥拉帕利组4年总生存期(OS)率高达89.8%,较对照组显著降低死亡风险32%,两组4年OS率差异3.4%(89.8% VS 86.4%)。后续将继续进行两次OS随访,而最终OS随访结果预计将于2029年公布。OlympiA成为首个且唯一针对gBRCA1/2突变、HER2阴性高危早期具有OS获益的研究,期待通过未来随访能够进一步揭示治疗方案的长期益处,为患者带来更大的获益[10-12]。
OlympiA 研究6.1年亮眼随访再更新
指引gBRCA突变高危早期乳腺癌辅助治疗优选策略
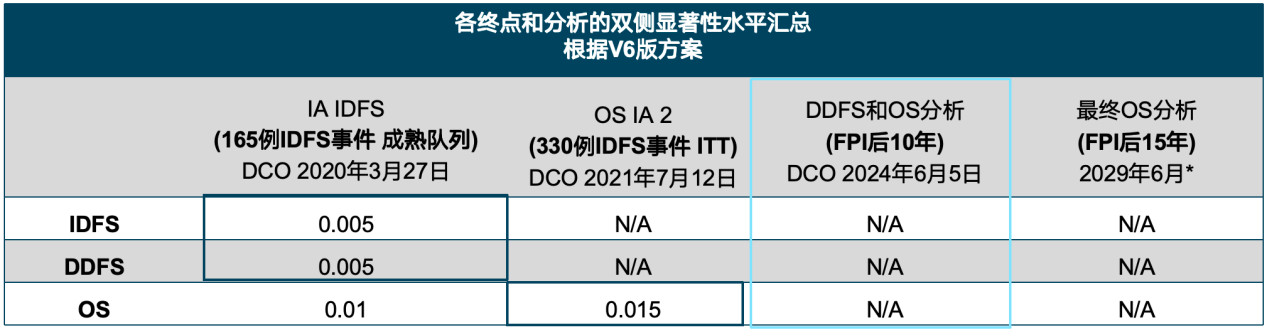
鉴于在首次期中分析(IA)时,奥拉帕利IDFS和DDFS均达到了显著性界限,而在OS的第二次中期分析(OS IA2)中亦达到了显著性界限。因此,未进行进一步的显著性检验。2024 SABCS公布了OlympiA研究中位随访时间6.1年分析结果。此次更新分析报告了自首例患者入组后10年的第三次预设分析的结果,中位随访时间为6.1年(最长9.6年),自上次分析以来继续随访了2.6年[13]。
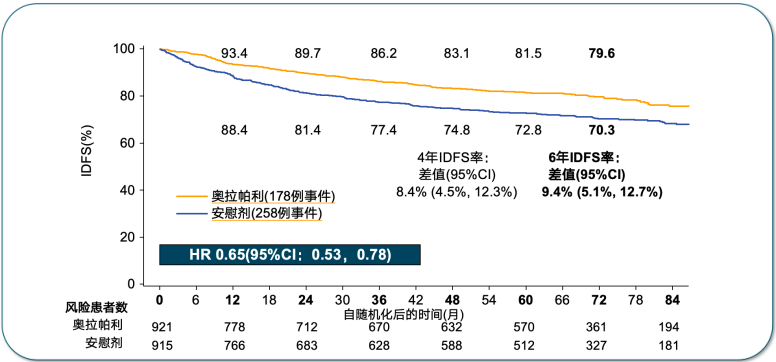
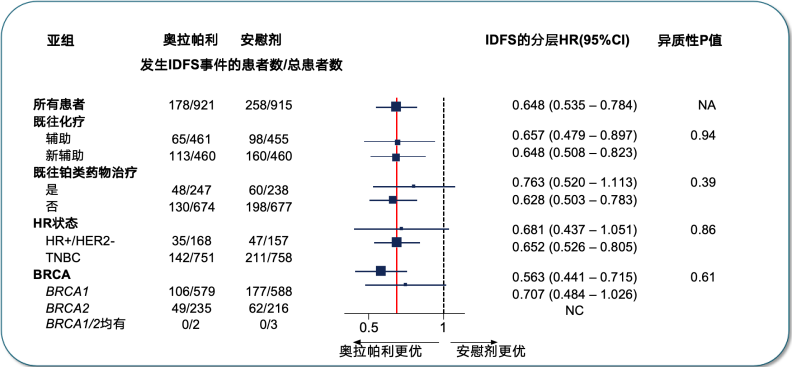
OlympiA研究首次iDFS事件的类型以远处复发为主,而长期随访数据显示,奥拉帕利组较对照组提高4年iDFS率8.4%,提高6年iDFS率9.4%,凸显了持续的临床获益。iDFS的亚组分析,同样显示出奥拉帕利组获益更优。特别是,HR+/HER2-人群,IDFS的分层HR(95%CI)为0.681,与TNBC的0.652非常接近。按HR状态分析IDFS获益一致,均可降低近30%疾病复发、新发、死亡风险[13]。
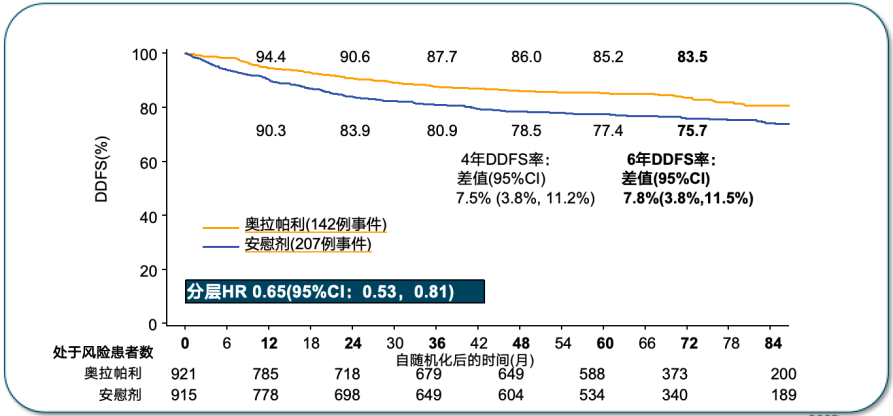
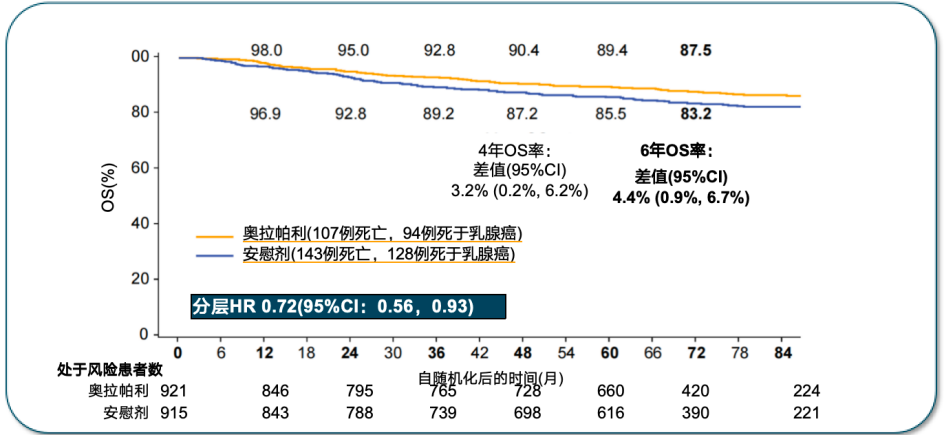
次要终点中,奥拉帕利组6年DDFS率为83.5%,较对照组降低远处疾病复发风险35%,绝对获益为7.8%。DDFS的亚组分析同样倾向于奥拉帕利获益更优。死亡事件分析显示,最主要死因为乳腺癌复发。总生存方面,奥拉帕利组的6年OS率为87.5%,安慰剂组则为83.2%,绝对获益为4.4%[13]。
安全性方面,主要不良事件为血液学毒性及消化道反应,未观察到新的安全性信号。针对随访期间新发乳腺癌和卵巢癌分析发现,奥拉帕利组新发原发性恶性肿瘤更少。其中,新发原发性卵巢癌或输卵管癌患者中,奥拉帕利组仅5例,而安慰剂组14例。研究期间妊娠结局探索性分析发现,奥拉帕利不影响患者妊娠[13]。然而,针对这部分特定人群,强烈建议进行生育咨询,以便实施突变基因检测筛选,旨在辅助患者未来在子代中规避BRCA突变的遗传风险。
综上,在中位随访6.1年(最长9.6年)时,(新)辅助化疗后接受12个月的奥拉帕利治疗后,在gBRCA1/2突变、HER2阴性高危早期乳腺癌患者中,持续显示了具有临床意义的生存获益(IDFS Δ 9.4%、DDFS Δ 7.8%和OS Δ 4.4%) ,奥拉帕利在所有关键亚组中的获益一致,包括ER和/或PgR+高危患者。这些数据继续支持奥拉帕利辅助治疗作为gBRCA1/2突变、HER2阴性高危早期乳腺癌患者的标准治疗,从而强调了gBRCA检测对治疗方案的重要性。
奥拉帕利早期乳腺癌辅助获批
更多探索及获益未来可期
2018年8月,奥拉帕利首次在中国获批上市,针对上皮性卵巢癌、输卵管癌或原发性腹膜癌,以及前列腺癌,已累计获得4个适应症的批准。随着研究的不断深入,基于III期OlympiA研究的积极试验结果,2024年12月25日,奥拉帕利迎来了乳腺癌适应症的获批,为患者提供了更多的治疗选择和希望。此次获批的适应症具体为奥拉帕利适用于接受过新辅助或辅助化疗的携带有害或疑似有害gBRCA突变、HER2阴性高危早期乳腺癌成人患者的辅助治疗 。

然而,新药引入的同时,也引发了一系列对既往标准治疗方案的挑战。例如,针对BRCA突变的TNBC,需要深入探讨新药如何与化疗联合应用,以及如何与免疫治疗药物(例如帕博利珠单抗)进行联合。同样,在HR+乳腺癌中,新药如何与CDK4/6抑制剂(CDK4/6i)联合使用也是一个亟待解决的问题。这些都是新药上市后面临的重要议题。
特别是,在HR+乳腺癌的治疗中,CDK4/6i已经展现出了显著的临床优势。那么,BRCA突变 HR+高危人群可否考虑奥拉帕利联合CDK4/6i?然而,当前诊疗推荐指出,对于符合OlympiA试验入组标准的HR+人群,奥拉帕利(联合内分泌)应是辅助治疗的优选方案,考虑加入CDK4/6i时可以在奥拉帕利治疗满1年后序贯应用。其原因在于该治疗方案调整的时机是同时符合OlympiA/monarchE/NATALEE三大临床试验随机分组方案。OlympiA研究患者入组情况为理想情况下,在最后一次治疗(手术、化疗或放疗)12周内随机;monarchE研究患者入组情况为必须在确定性乳腺癌手术后的16个月内被随机分配;而NATALEE研究患者入组情况则为在随机前12个月内接受任何标准(新)辅助性内分泌治疗。总体来看,这些研究的入组时间窗口相对较为宽泛。
另外,值得注意的是,及时确定BRCA突变状态对制定有效治疗策略至关重要,但相比欧美,我国在检测方面仍有不足,早期乳腺癌患者的gBRCA检测率偏低,亟需加强科普教育。

因此,提高早期乳腺癌的普遍检测率成为未来策略的重点,同时期望奥拉帕利能为早期患者提供更多治愈的可能性。未来,为了更准确地指导奥拉帕利等新药的临床应用,需要进一步制定和完善相关的指南或共识,以明确其最佳的用药时机和联合治疗方案。这将有助于临床更好地利用这些新药,提高乳腺癌患者的治疗效果和生存质量。
专家介绍
复旦大学附属肿瘤医院 乳腺外科
复旦大学肿瘤学博士,硕士生导师
中国抗癌协会乳腺癌专业委员会青委委员
中华医学会肿瘤学分会乳腺学组青委委员
上海女医师协会乳腺专业委员会副主委
上海市医学会肿瘤靶分子分会青委副主委
中国抗癌协会国际医疗交流分会委员
上海市抗癌协会乳腺癌专委会委员
上海市医学会心身医学专委会委员
上海女医师协会科普委员会委员
哈佛大学医学院麻省总医院肿瘤中心Fellow
主持及参与国家级及上海市级基金多项
SCI收录论文30余篇,第一及通讯作者文章20余篇,收录于《柳叶刀肿瘤》《JAMA Oncol》等
[1] Gao, X et al. Hum Mutat.2020 03 ;41(3):696-708.
[2] 中国乳腺癌患者BRCA基因检测与临床应用专家共识(2018年版).
[3] Calculations based on Winter et al. 2016.
[4] Pierce LJ, Levin AM, Rebbeck TR, et al. J Clin Oncol. 2006;24(16):2437-2443.
[5] Ye F, et al. Cancer Med. 2020 Jan 7.
[6] Isabelle Bedrosian, et al. J Clin Oncol . 2024 Feb 10;42(5)-584-604.
[7] 2024 NCCN BC V5.
[8] 基于中国人群的BRCA胚系突变筛查专家共识(2024年版).
[9] Andrew N J Tutt, et al. N Engl J Med . 2021 Jun 24;384(25):2394-2405.
[10] Tutt A, et al. Presented at ESMO Virtual Plenary; March 16th–17th, 2022; Virtual; abstract VP1-2022;
[11] Gianni L, et al. Lancet Oncol 2011;12:236–244;
[12] Masuda N, et al. N Engl J Med 2017;376:2147–2159.
[13] Garber J, et al. OlympiA: A phase 3, multicenter, randomized, placebo-controlled trial of adjuvant olaparib after (neo)adjuvant chemotherapy in patients w/ germline BRCA1 & BRCA2 pathogenic variants & highrisk HER2-negative primary breast cancer: longerterm follow. 2024 SABCS. GS1-09.
排版编辑:肿瘤资讯-邓文普











 苏公网安备32059002004080号
苏公网安备32059002004080号


