PIK3CA突变可导致PI3K/AKT/mTOR信号通路(PAM信号通路)的异常激活,刺激肿瘤增殖、转移和侵袭,并与乳腺癌治疗耐药密切相关。最新III期INAVO 120研究证实,新型PI3Kα抑制剂Inavolisib联合哌柏西利和氟维司群一线治疗可为PIK3CA突变的HR+/HER2-晚期乳腺癌带来显著的无进展生存期(PFS)获益,而在2024 SABCS大会上公布的MORPHEUS-pan BC研究则进一步探索了Inavolisib和氟维司群联合不同CDK4/6抑制剂(CDK4/6i)用于HR+/HER2-晚期乳腺癌的安全性和疗效,展现了以Inavolisib为基础的治疗的可行性。值此机会,【肿瘤资讯】特邀四川省肿瘤医院王浩教授从MORPHEUS-pan BC研究出发,畅谈PI3K抑制剂的发展和最新研究成果。
PAM通路与乳腺癌多种治疗方案耐药有关,而PI3K是其中的关键节点
王浩教授:PAM通路参与了细胞增殖、存活、代谢调节以及细胞周期的控制。该通路通过PI3K及其下游的AKT和mTOR信号传导,调节着细胞生长和代谢等多个方面。在乳腺癌细胞中,PAM通路的异常激活往往会导致癌细胞的持续增殖、逃避凋亡、增强侵袭性和耐药性,从而促进肿瘤的发生发展[1]。
在HR+/HER2-乳腺癌患者中,超过40%的患者存在PIK3CA基因突变,而PIK3CA突变会增强PI3K蛋白的催化活性,这种异常激活是肿瘤细胞对常规治疗,特别是内分泌治疗产生耐药性的主要原因之一[2]。因此,PIK3CA突变导致的PAM通路激活与HR+/HER2-乳腺癌的恶性进展和预后差密切相关。
既然通路的异常活化同内分泌耐药相关,那么针对异常活化的PIK3CA靶点进行阻断,就是延缓甚至逆转内分泌耐药的重要手段。BYLieve研究[3]显示,PI3Kα抑制剂Alpelisib在HR+/HER2-乳腺癌中已经展示了一定的疗效,但遗憾的是,Alpelisib的不良反应较重,患者耐受性差,因此,开发更具疗效优势和低毒特征的PI3Kα抑制剂成为目前HR+/HER2-乳腺癌药物研发的一个热点。值得庆幸的是,III期INAVO 120研究[4]显示新一代高选择性的PI3Kα抑制剂伊那利塞在一线治疗中大幅提高患者PFS的同时,具有更低的不良反应,尤其是3/4级不良反应发生率,从而使PAM通路抑制具有更高的实用性。
PI3Kα抑制剂研发历经波折,安全性和肿瘤异质性是两大拦路虎
王浩教授:鉴于PAM通路在肿瘤生物学中的关键作用,PI3Kα抑制剂作为一种靶向治疗策略,已经在多种癌症治疗中展现了潜力。然而,其研发过程并非一帆风顺。PI3K抑制剂的研发主要面临两个问题:安全性和肿瘤异质性。
安全性方面,PI3K抑制剂研发的发展经历了广谱-PI3K抑制剂(pan-PI3K抑制剂)到亚型特异选择性PI3K抑制剂的阶段。第一代广谱-PI3K抑制剂(pan-PI3K抑制剂,代表有Buparlisib(BKM120)[5]等)和第二代β sparing PI3K抑制剂(Taselisib等)和PI3Kα亚型抑制剂,虽然体现了一定疗效优势,然而由于伴随着严重的肝毒性、高血糖和皮疹等不良反应导致研发停止。随着技术进步和对蛋白的深入了解,α亚型选择性抑制剂可能具有更高的药物疗效和更低的安全性。Alpelisb作为首个获批上市的PI3Kα抑制剂,显著改善患者的PFS。但既往研究[6]显示约1/3的患者会出现≥3级以上的高血糖,这使得其在真实世界中的应用受到限制,尤其在控制代谢问题方面存在挑战,因此需要开发新一代针对突变体具有高选择性的PI3Kα抑制剂。Inavolisib作为一种高选择性PI3Kα抑制剂,其对PI3Kα的选择性和抑制作用是其它I类PI3K亚型的300倍,而且可以特异性地降解p110α突变体,防止PIP3累积,使下游AKT信号传导减弱,从而抑制细胞增殖,且减少因抑制野生型信号传导所致的全身性副作用[7,8,9]。
肿瘤异质性方面,PAM信号通路与ER介导的信号通路存在交互作用,可协同ER下游信号传导通路过度激活,使HR阳性乳腺癌对内分泌治疗产生耐药[6]。除此以外,PAM通路的过度激活也可以使RB蛋白磷酸化,增加Cyclin D1的表达水平,从而导致CDK4/6抑制剂耐药[10]。值得注意的是,PI3K-AKT-mTOR的传导机制并非PAM信号通路唯一的传导机制,其中作为“信号枢纽”的AKT,尽管受到上游PI3K的调控,但也可能因为其他因素而导致异常激活。因此,PI3Kα抑制剂疗效受不同突变类型和肿瘤异质性的影响,提示需要根据患者的突变类型和个体差异制定更精准的治疗方案。
2024 SABCS MORPHEUS-pan BC研究为Inavolisib与不同CDK4/6i联合打下坚实基础
王浩教授:Inavolisib是一款具有高选择性的PI3Kα抑制剂,既往III期INAVO120研究[4]证实Inavolisib联合哌柏西利和氟维司群一线治疗内分泌耐药的HR+/HER2-晚期乳腺癌患者具有优异的PFS获益和良好的安全性。
2024 SABCS大会上公布的Ib/II期MORPHEUS-pan BC研究[11](P4-07-23)旨在探索Inavolisib和氟维司群与不同CDK4/6i(阿贝西利或瑞波西利)联合使用的安全性。研究共纳入了12例患者,分别分配至阿贝西利组(6例)和瑞波西利组(6例)。

截至数据截止日期(2024年9月9日),安全性数据显示,无论是阿贝西利还是瑞波西利联合方案(Inavolisib+氟维司群+瑞波西利/阿贝西利)治疗的持续时间大致相似(5~6周期)。治疗过程中,所有患者均发生了任意等级的不良事件(AE),阿贝西利组3级AE的发生率为83.3%,而瑞波西利组为16.7%,但两组未观察到4/5级AE和导致停止治疗的不良事件(AE),最常见的AE为高血糖、腹泻、恶心和呕吐。在选定的≥3级关键AE中,阿贝西利组分别有1例患者(16.7%)发生了需要胰岛素治疗的高血糖和口腔/黏膜炎,而瑞波西利组仅有1例患者(16.7%)发生了需要胰岛素治疗的高血糖。在导致治疗调整和中断的最常见AE方面,阿贝西利组(6例)和瑞波西利组(2例)均为高血糖和腹泻。
表2. MORPHEUS-pan BC研究中,安全性总结
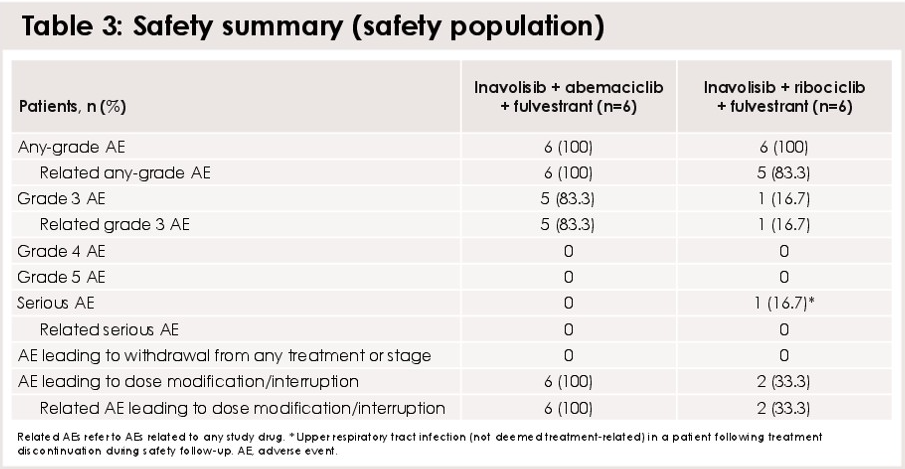
表2. MORPHEUS-pan BC研究中,选定的≥3级的AE
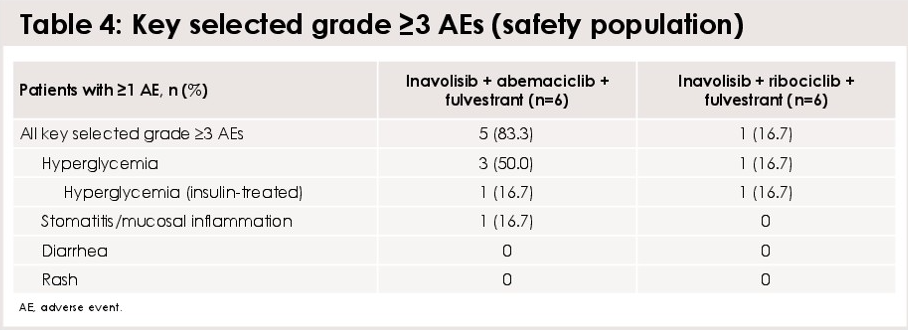
此外,药代动力学数据显示,本研究中Inavolisib、阿贝西利和瑞波西利的浓度与历史数据一致。尽管阿贝西利组中,Inavolisib的平均浓度略高于历史数据,但患者个体的血药浓度均在3期研究中群体药代动力学预测暴露范围内。
表3. MORPHEUS-pan BC研究中药代动力学数据

总之,研究结果提示Inavolisib与瑞波西利或阿贝西利联合使用安全性亦表现良好,无患者因AE停止治疗,这为未来的疗效分析奠定了基础。
聚焦PAM通路抑制剂的不良反应管理,助力患者获益最大化
王浩教授:不良反应的管理对于保证治疗效果及提高患者生活质量至关重要。PAM通路抑制剂总体安全性可控,不良反应谱相似,但发生率上存在差异。最新《PI3K/AKT/mTOR信号通路抑制剂治疗乳腺癌临床应用专家共识(2024版)》强调鉴于不同靶向药的不良反应谱往往不同,因此应全面认识和关注不同PAM通路抑制剂可能面临的不良反应,早期预防,密切监控,并及时采取合理有效的治疗措施。对于重度不良反应,应暂停或终止PAM通路抑制剂给药。
既往 PI3K 抑制剂联合标准治疗的方案由于毒性及副作用较大难以在临床应用中发挥价值。而Inavolisib单药和联合治疗均表现出良好的安全性,INAVO 120研究[4]中因AE导致停药率更低,仅为6.8%。并且Inavolisib的主要AE通常发生在前6个月,而在随后的治疗周期中逐渐减少,长期使用inavolisib未观察到新的安全事件[12]。现有循证证据提示,Inavolisib长期治疗的耐受性良好,安全性特征便于临床管理,可极大消除患者对于使用PI3Kα抑制剂安全性的担忧。
*请上下滑动填写
专家介绍
四川省肿瘤医院, 乳腺科副主任(主持工作)
加拿大麦吉尔大学访问学者
中华医学会肿瘤学分会乳腺肿瘤学组委员
中国抗癌协会乳腺癌整合防筛专业委员会常务委员
中国抗癌协会乳腺癌专委会委员
中国抗癌协会中西整合乳腺癌专委会委员
四川省预防医学会乳腺疾病预防与控制分会副主任委员
四川省抗癌协会乳腺癌专业委员会副主任委员
四川省医学会乳腺病学专业委员会 副主任委员
四川省医师协会第二届乳腺专业分会副会长
四川省肿瘤性疾病质控中心乳腺专业组秘书
成都市抗癌协会临床科研与转化医学专委会主任委员
[1] 中国抗癌协会肿瘤药物临床研究专业委员会,等. PI3K/AKT/mTOR信号通路抑制剂治疗乳腺癌临床应用专家共识[J]. 中华肿瘤杂志, 2022, 44(7):673-692.
[2] Vasan N, Toska E, Scaltriti M. Ann Oncol. 2019 Dec 1;30(Suppl_10):x3-x11.
[3] Rugo HS, Lerebours F, Ciruelos E, et al. Lancet Oncol. 2021 Apr;22(4):489-498.
[4] Jhaveri KL, Im SA, Saura C, et al. Cancer Res (2024) 84 (9_Supplement): GS03-13.
[5] Vanhaesebroeck B, Perry MWD, Brown JR, et al. Nat Rev Drug Discov. 2021 Oct;20(10):741-769.
[6] André F, et al. N Engl J Med. 2019;380(20):1929‐1940.
[7] VANHAESEBROECK B, PERRY M W D, BROWN J R, et al. Nat Rev Drug Discov, 2021, 20(10): 741-769.
[8] HANAN E J, BRAUN M G, HEALD R A, et al. J Med Chem, 2022, 65(24): 16589-16621.
[9]HONG Y R, SALLOUM R G, YADAV S, et al. Value Health, 2020, 23(12): 1592-1598.
[10] Rampioni Vinciguerra G L, Sonego M, Segatto I, et al. Frontiers in Oncology, 2022, 12: 891580.
[11] Einav Nili Gal-Yam, et al. Preliminary safety in the inavolisib + fulvestrant + ribociclib/abemaciclib arms of MORPHEUS-pan breast cancer: A Phase 1b/2 study of efficacy & safety of multiple treatment combinations in patients with metastatic/locally advanced breast cancer. SABCS 2024 P4-07-23.[6] Brufsky A M, Dickler M N. The Oncologist, 2018, 23(5): 528-539.
[12]JURIC D, KALINSKY K, TURNER N C, et al. Journal of Clinical Oncology, 2024, 42(16_suppl): 1003-1003..
排版编辑:肿瘤资讯-Awa











 苏公网安备32059002004080号
苏公网安备32059002004080号


