2024年第47届圣安东尼奥乳腺癌研讨会(SABCS)于当地时间12月10日至13日在美国得克萨斯州圣安东尼奥以线上线下形式同步盛大召开。作为乳腺肿瘤领域极具声威的国际盛会之一,2024 SABCS汇聚了全球乳腺癌的最新研究成果、临床实践经验、治疗进展和技术创新等内容。本次大会上,来自河南省肿瘤医院刘真真教授团队的一项关于三阳性乳腺癌的真实世界研究(P3-11-12)亮相于 Poster专场,在国际舞台上再度展现了中国在早期乳腺癌研究领域的卓越成果[1]。值此之际,【肿瘤资讯】特邀该研究的PI刘真真教授深度综合解读该项研究,并就我国三阳性乳腺癌的真实诊疗现状、治疗模式与发展发表核心观点。现将访谈内容整理如下,与君同鉴。
专家介绍
河南省肿瘤医院乳腺科主任 、主任医师
河南省乳腺癌诊疗中心 主任
国家肿瘤质控中心乳腺癌专业委员会 委员
中华医学会肿瘤学分会乳腺癌学组 委员
中华医学会外科分会乳腺外科学组 委员
中国医师协会外科分会乳腺癌专家工作组 副组长
中国抗癌协会乳腺癌专业委员会 常委
中国临床肿瘤学会乳腺癌专家委员会 常委
河南省肿瘤诊疗质量控制中心乳腺癌专家委员会 主任委员
河南省医师协会乳腺医师分会 会长
河南省临床肿瘤学会乳腺癌专业委会 主任委员
河南省医学会乳腺病学分会 候任主任委员
迄今关于三阳性早期乳腺最大样本的中国真实世界研究,曲帕双靶显示长期预后优势
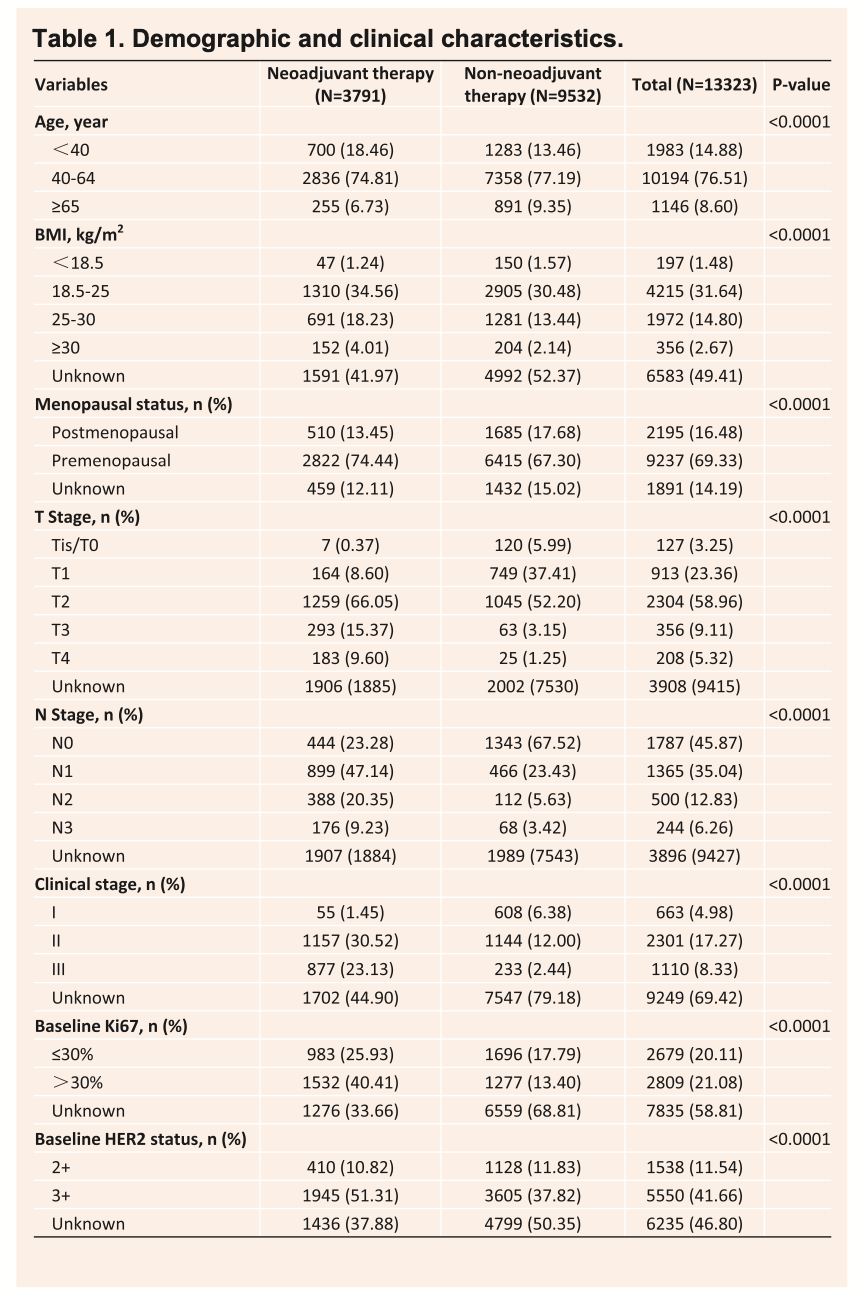
刘真真教授:作为本研究的主要研究者,我很荣幸能在2024年SABCS大会上分享这项关于中国三阳性乳腺癌治疗的最新研究成果。这项研究是迄今为止在中国开展的最大规模HR+/HER2+(三阳性)早期乳腺癌真实世界研究,涵盖了13,323名患者的临床数据,覆盖全国27个省份的51家医院。本研究基于国家癌症信息数据库(NCID),不仅确保了数据的代表性,更重要的是捕捉了2019年帕妥珠单抗在中国获批后治疗模式的重要转变(表1)。
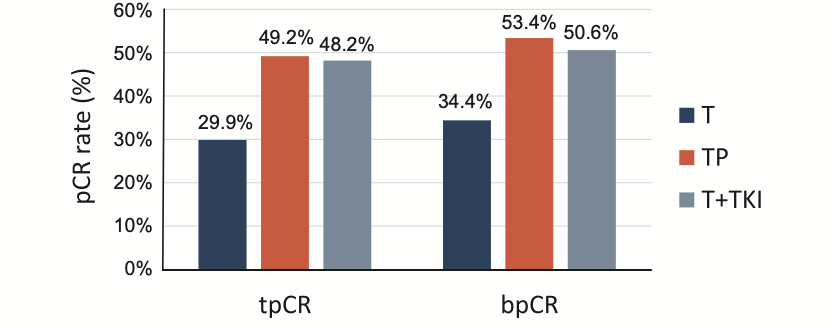
从研究的核心发现来看,我们观察到双靶治疗方案在改善患者短期疗效方面展现出显著优势。具体而言,在新辅助治疗中,采用曲妥珠单抗联合帕妥珠单抗的双靶方案(HP)获得的总病理完全缓解率(tpCR)达到49.2%,相比单靶治疗的29.9%有了质的飞跃(图1)。在乳腺病理完全缓解率(bpCR)方面也呈现类似趋势,双靶治疗组达到53.4%,显著优于单靶治疗组的34.4%。
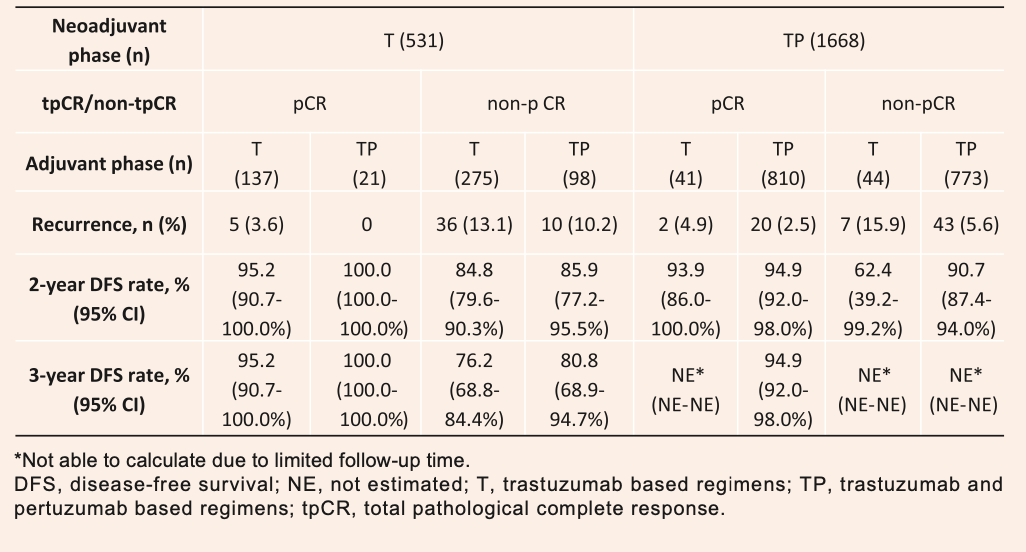
特别值得关注的是,我们发现tpCR与长期预后之间存在紧密关联。研究数据显示,达到tpCR的患者3年复发率仅为2.5%,而未达到tpCR的患者复发率则升至5.6%。从长期生存数据来看,双靶治疗组的3年无病生存率(DFS)达到88.6%,明显优于单靶治疗组的82.0%,在所有接受新辅助治疗的患者中,达到tpCR的患者复发率为2.5%(3年DFS为94.9%),未达到tpCR的患者复发率为5.6%(3年DFS未成熟,NE)。总体来看,达到tpCR的患者复发率低于未达到tpCR的患者(见表2)。这进一步证实了双靶方案在改善患者长期预后方面的优越性。通过多变量回归分析,我们识别出了几个影响治疗效果的关键因素。研究结果表明,双靶治疗(OR=2.18,p<0.001)、绝经后状态(OR=1.47,p<0.001)以及高Ki67表达(Ki67>30%)(OR=1.32,p=0.002)是显著的正向预测因素。与此同时,我们也注意到年龄≥65岁(OR=0.73,p=0.037)和临床分期III期(OR=0.80,p=0.019)可能会降低治疗效果。
作为临床医生,我认为这些研究发现对指导临床实践具有重要意义。考虑到三阳性乳腺癌的独特生物学特性,特别是其受HER2和ER信号通路交互影响的特点,其治疗反应可能与其他亚型存在显著差异。我们的研究不仅为双靶向治疗在三阳性乳腺癌中的应用提供了强有力的真实世界证据,也为进一步优化个体化治疗策略奠定了重要基础。这些发现将有助于临床医生在实践中做出更精准的治疗决策,最终使我们的患者获得更好的治疗效果。
真实世界数据验证病理完全缓解里程碑意义,双靶治疗推动三阳性乳腺癌个体化诊疗进程
刘真真教授:作为一名临床研究者,我认为这项研究在评估病理完全缓解(pCR)作为治疗决策点的价值方面提供了重要的临床洞见。通过分析大规模真实世界数据,我们首次系统地证实了pCR与三阳性乳腺癌患者长期预后之间的密切关联。研究数据清晰地显示,达到tpCR的患者其3年复发率显著降低至2.5%,而未达到tpCR的患者复发率则达到5.6%,这一发现为临床决策提供了重要的参考指标。
从真实世界研究的角度来看,我们的数据具有独特的价值。基于13,323名来自全国27个省份51家医院的患者数据,这项研究真实反映了中国三阳性乳腺癌患者的疾病特征和治疗现状(表1)。我们注意到,中国患者在疾病特征、经济状况和医保覆盖等方面与国际患者存在明显差异,这使得来自中国本土的真实世界数据对指导临床实践显得尤为重要。特别值得关注的是,我们的研究揭示了HP在提高pCR方面的显著优势。这一发现对于解决高雌激素受体表达患者治疗效果欠佳的临床难题提供了新的思路。基于这些数据,我相信HP双靶治疗将在未来的临床实践中发挥更重要的作用。
展望未来,我认为基于真实世界数据的治疗模式优化将继续深入。一方面,双靶联合化疗在提高tpCR和改善DFS方面的优异表现,将推动其在临床实践中的进一步普及。另一方面,考虑到三阳性乳腺癌的独特生物学特性,我们可能需要进一步探索双靶治疗与内分泌治疗的最佳联合策略,以期实现更个体化的治疗方案。这些真实世界研究数据不仅为临床决策提供了重要依据,也为未来的治疗策略优化指明了方向。
创新给药方式赋能三阳性乳腺癌治疗,皮下注射双靶推动临床实践迈向新纪元
刘真真教授:从技术创新的角度来看,皮下制剂将传统静脉输注的治疗时间从数小时缩短至仅需5-8分钟。这一突破性进展极大改善了患者的治疗体验,同时其固定剂量设计简化了给药流程,显著降低了剂量计算错误的风险,为临床实践提供了更高的用药安全性保障。III期FeDeriCa研究证实,皮下制剂在药代动力学、有效性和安全性方面与传统静脉输注方案相当。《CSCO乳腺癌诊疗指南2024版》同样肯定了皮下给药方案的临床价值,而PHranceSCa研究显示,87.5%的医护人员认为皮下给药方案优于传统输注方式[3]。
在当前乳腺癌逐渐走向慢病管理的趋势下,皮下制剂的推出具有深远的临床实践意义。首先,它显著提升了患者的治疗依从性,尤其是对那些需要长期接受抗HER2治疗的患者而言,皮下注射带来的便利性可能会直接影响治疗效果。其次,从医疗资源配置的角度来看,皮下给药方案能够显著提高医疗效率,减轻输液室负担,这对于我国医疗资源紧张的现状具有重要的缓解作用。
更具前瞻性的是,皮下制剂有望推动双靶治疗在基层医疗机构的普及。根据PHaTiMa研究结果,皮下给药方案显著节省了患者和医护人员的时间,这一优势在基层医疗机构可能发挥更大的作用[4]。同时,研究显示皮下给药方案可使非药物成本降低73%-80%,这对于推进医保支付方式改革和医院精细化管理具有重要意义[5]。这一创新也将推动我国乳腺癌治疗模式向着更加人性化、精细化的方向发展。
医保创新助力双靶皮下制剂,推动乳腺癌诊疗步入规范化、便利化和普惠化新时代
刘真真教授:首先,从经济可及性角度来看,双靶治疗的高额成本一直是制约其推广使用的主要障碍。医保覆盖将显著降低患者的自付比例,这对于经济欠发达地区的患者尤其重要。通过减轻患者经济负担,我们有望看到更多患者能够按照标准治疗方案完成全程治疗,而不是因为经济原因被迫中断或改变治疗方案。其次,在治疗模式优化方面,医保覆盖将加速以双靶为核心的标准治疗方案在全国范围内的推广。特别是对于创新皮下给药方案,由于其显著缩短的给药时间和简化的操作流程,结合医保支持后将更容易在基层医疗机构普及。这不仅能提高医疗资源使用效率,更能推动优质医疗资源向基层下沉,有效缓解“看病难”的问题。
从患者预后改善的角度来看,基于我们的研究数据,更广泛的双靶治疗覆盖必将提升tpCR和DFS。当更多患者能够获得标准治疗时,我们预期将看到总体生存率的提升和生活质量的改善。长期来看,这也将帮助降低疾病复发率,减轻远期治疗负担。特别值得关注的是,在乳腺癌逐步迈向慢病化管理的背景下,皮下制剂的医保覆盖将为整个治疗模式带来积极变革。
作为一线临床工作者,我深知医保支付方式改革是提升医疗服务质量的关键。通过将创新药物纳入医保目录,并确保其能够顺利进入医院、最终服务于患者,我们将真正实现从“保基本”到“提质量”的转变。这不仅体现了我国医疗保障制度的进步,更展现了以患者为中心的医疗服务理念。随着这一政策的落地实施,我们将看到HER2+乳腺癌患者获得更规范、更便捷、更可及的治疗,最终实现更好的临床获益。
*请上下滑动填写
1. Liu, Z., P3-11-12: (Neo)adjuvant Therapy Patterns and Outcomes in Patients with HR-Positive/HER2-Positive Early Breast Cancer: a Real-World Study Using National Cancer Information Database in China. 2024.
2. Tan, A.R., et al., Fixed-dose combination of pertuzumab and trastuzumab for subcutaneous injection plus chemotherapy in HER2-positive early breast cancer (FeDeriCa): a randomised, open-label, multicentre, non-inferiority, phase 3 study. The Lancet Oncology, 2021. 22(1): p. 85-97.
3. O'Shaughnessy, J., et al., Preference for the fixed-dose combination of pertuzumab and trastuzumab for subcutaneous injection in patients with HER2-positive early breast cancer (PHranceSCa): A randomised, open-label phase II study. Eur J Cancer, 2021. 152: p. 223-232.
4. González-Santiago, S., et al., 116P Time and motion randomised study of a subcutaneous (SC) pertuzumab and trastuzumab fixed-dose combination (PH FDC) for the treatment of HER2-positive early breast cancer (HER2 EBC): PHaTiMa. ESMO Open, 2023. 8(1).
5. Jackisch, C., et al., White Paper on the Value of Time Savings for Patients and Healthcare Providers of Breast Cancer Therapy: The Fixed-Dose Combination of Pertuzumab and Trastuzumab for Subcutaneous Injection as an Example. Adv Ther, 2022. 39(2): p. 833-844.
排版编辑:肿瘤资讯-Awa











 苏公网安备32059002004080号
苏公网安备32059002004080号


