尽管儿童肿瘤相对罕见,但仍是儿科人群的第二大死亡原因[1]。NTRK基因融合已被证实是多种肿瘤类型的致癌驱动基因之一,且在儿童肿瘤的发生率显著高于成人。根据FoundationCORE 数据库的大样本数据显示,NTRK 基因融合肿瘤在所有儿童肿瘤中发生率约为2.28%,在婴儿型纤维肉瘤(IFS)中可高达 90%[2]。拉罗替尼是全球首个且唯一含新生儿适应证的用于治疗NTRK 基因融合实体瘤患者的药物,也是首个不分癌种、只看突变的广谱抗癌靶向药,既往研究数据显示拉罗替尼在儿童肿瘤患者中的疗效较成人患者更佳,在临床上备受关注。【肿瘤资讯】特别邀请首都医科大学附属北京儿童医院王焕民教授,结合今年的研究进展,分析拉罗替尼治疗NTRK基因融合儿童肿瘤最新的临床数据,展望领域内的未来发展方向。
主任医师 教授 博士生导师
现为国际小儿肿瘤外科学会IPSO会员
亚洲小儿肿瘤协作组APHOG核心组成员
现任国家卫生健康委儿童恶性肿瘤外科专家委员会副主委
国家卫生健康委能力建设和继续教育儿科学专委会血液肿瘤学组组长
中华医学会小儿外科分会委员及肿瘤学组组长
中国抗癌协会小儿肿瘤专业委员会(CCCG)主委
中国研究型医院学会儿童肿瘤专委会(COC)主委
北京抗癌协会小儿肿瘤专委会主委等
并担任《World Journal of Pediatric Surgery》编委、《临床小儿外科杂志》副主编、《中华肝胆外科杂志》编委、《中华小儿外科杂志》编委、《中国小儿血液和肿瘤杂志》编委、《中国研究型医院杂志》编委
承担国家级和省部级课题十余项,发表核心期刊和SCI论文百余篇,主要研究访问为小儿外科和小儿肿瘤
不限癌种,NTRK融合肿瘤儿童患者治疗进展
NTRK融合肿瘤儿童患者整合数据
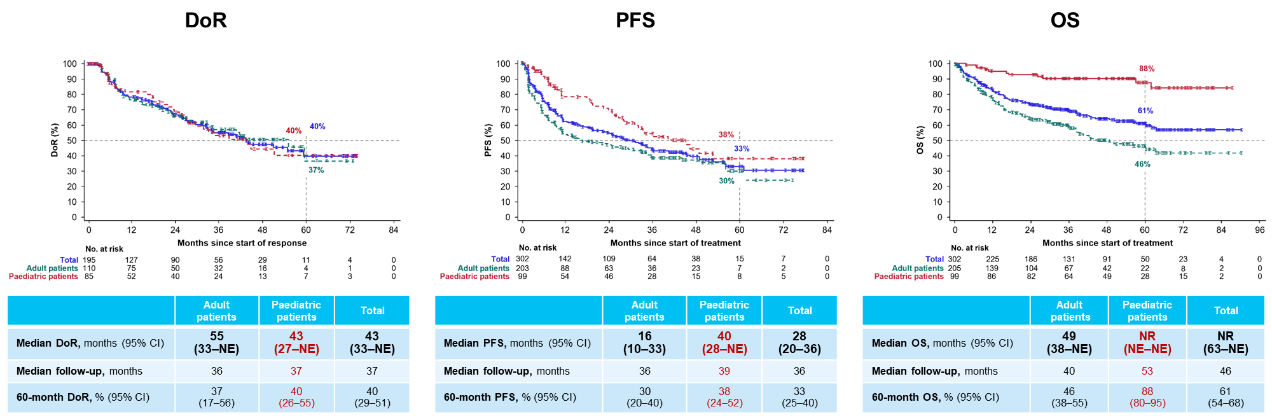
今年ESMO和SIOP大会分别报告了拉罗替尼治疗NTRK基因融合肿瘤儿童患者的长期随访结果,最新分析纳入了 SCOUT(NCT02637687)和NAVIGATE(NCT02576431)研究中99例TRK融合肿瘤儿童患者,结果显示在所有IRC可评估的儿童患者中,客观缓解率(ORR)为86% (95% CI:77-92),其中35%的患者可达到完全缓解,16%的患者可达病理完全缓解,中位至缓解时间为1.8个月 (范围:0.9-7.3),治疗持续时间(包括“观察期”)为1-87+个月。在数据截止时,中位缓解持续时间(DoR)为43个月,5年DoR率为40%;中位无进展生存期(PFS)为40个月,5年PFS率为38%;中位总生存期(OS)仍未达到,5年OS率为88%。在安全性方面,拉罗替尼治疗相关不良事件(TRAEs)多为1/2级,在儿童患者中具有良好的耐受性[3,4]。

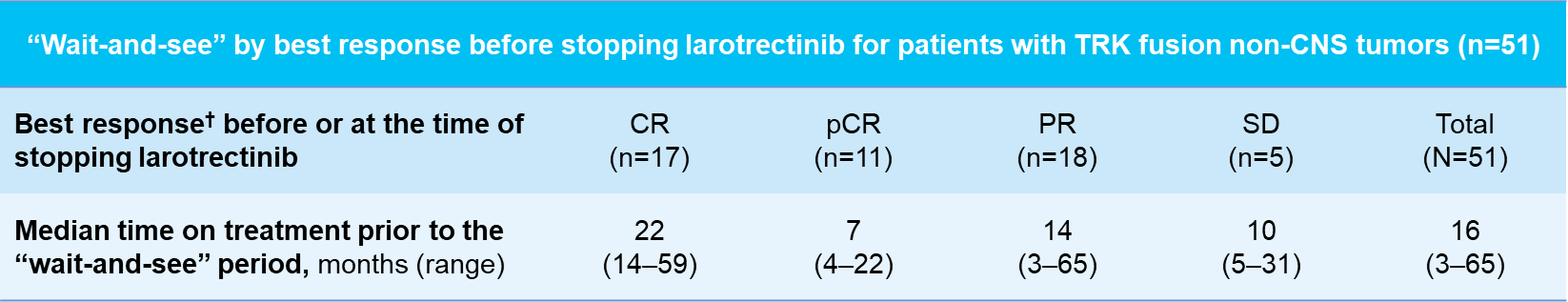
在治疗过程中无疾病进展的情况下,允许SCOUT研究的患者停用拉罗替尼(“观察期”),根据方案积极随访患者的进展情况。在最新分析中,51例TRK融合肿瘤儿童患者被纳入“观察期”分析,首个“观察期”前接受治疗的中位时间为16个月(范围:3-65),首个“观察期”的中位持续时间为22个月(范围:0-72+)。在28例(55%)停止首个“观察期”的患者中,17例出现疾病进展并恢复治疗,结果包括5例完全缓解,6例部分缓解,2例待确认,5例疾病稳定,1例不可评估,另外11例患者退出研究,但在数据截止时均存活[4]。
NTRK融合肿瘤儿童患者一线治疗数据
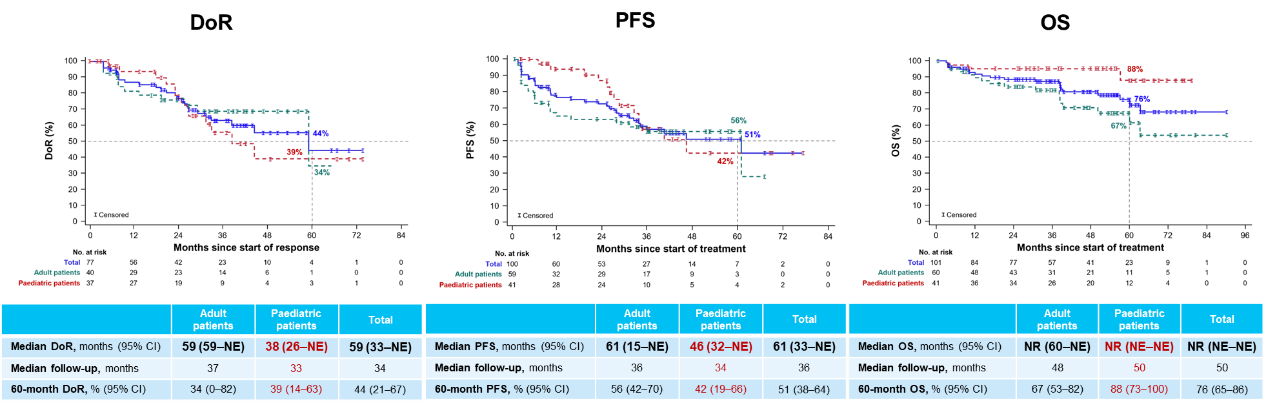
今年ESMO年会还更新了拉罗替尼一线治疗TRK融合肿瘤患者的疗效和安全性的最新数据,共纳入41例未接受系统治疗(不包括手术、放疗和放射性碘) 的局部晚期或转移性TRK融合肿瘤患者,在所有IRC可评估的儿童患者中,拉罗替尼治疗的ORR达90% (95% CI:77-97),其中51%的患者可达到完全缓解,22%的患者可达病理完全缓解。数据截止时,中位DoR为38个月,5年DoR率为39%;中位PFS为46个月,5年PFS率为42%;中位OS尚未达到,5年OS率为88%[5]。拉罗替尼的数据持续更新,再次证实了兼具疗效和安全性的显著优势,是临床上有效的治疗选择之一。

NTRK基因融合婴儿纤维肉瘤患者
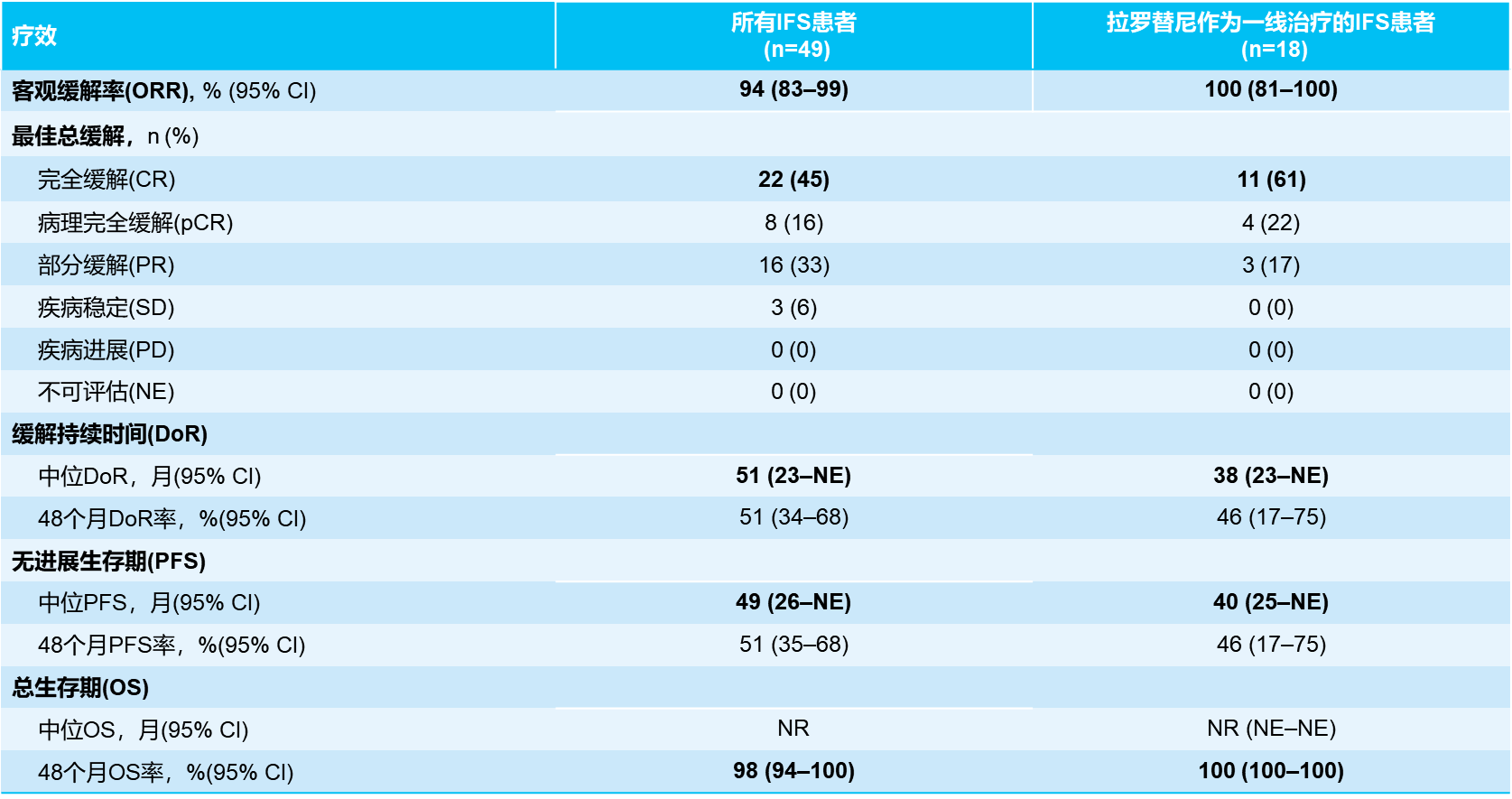
婴儿纤维肉瘤(IFS)是一种罕见且通常在婴儿期出现的恶性肿瘤,其中NTRK基因融合在IFS中的发生率较高。拉罗替尼的问世,为IFS患者带来了新的希望。2024 CTOS大会对拉罗替尼治疗TRK融合肉瘤患者的临床数据进行了更新。在数据截止时,共纳入49例IFS患者,结果显示,在所有IRC可评估的IFS患者中,拉罗替尼治疗的ORR为94%,中位DoR为51个月,中位PFS为49个月,4年OS率为98%[6]。对于既往未接受过系统治疗的IFS患者,最新数据显示拉罗替尼一线治疗的ORR高达100%,其中61%的患者可达到完全缓解,22%的患者可达病理完全缓解,中位缓解持续时间达38个月,4年PFS率为46%,4年OS率达100%[7]。这两项研究进一步证实了拉罗替尼在TRK融合IFS患者中具有快速且持久的抗肿瘤疗效,为临床实践提供更多参考依据。
NTRK基因融合儿童原发性CNS肿瘤患者
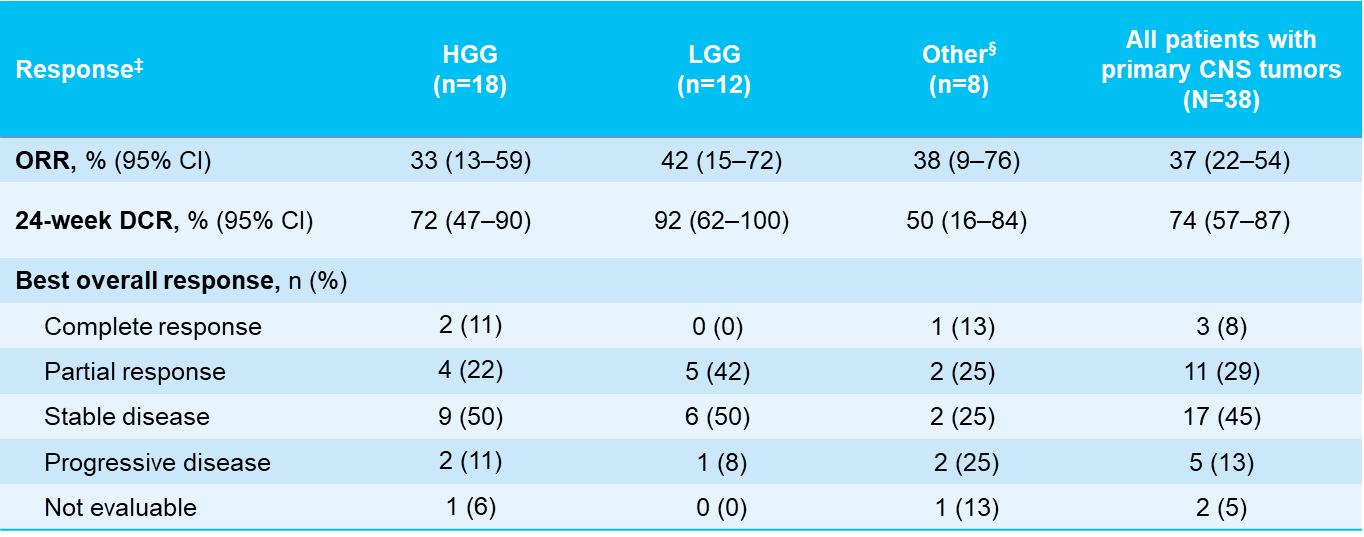
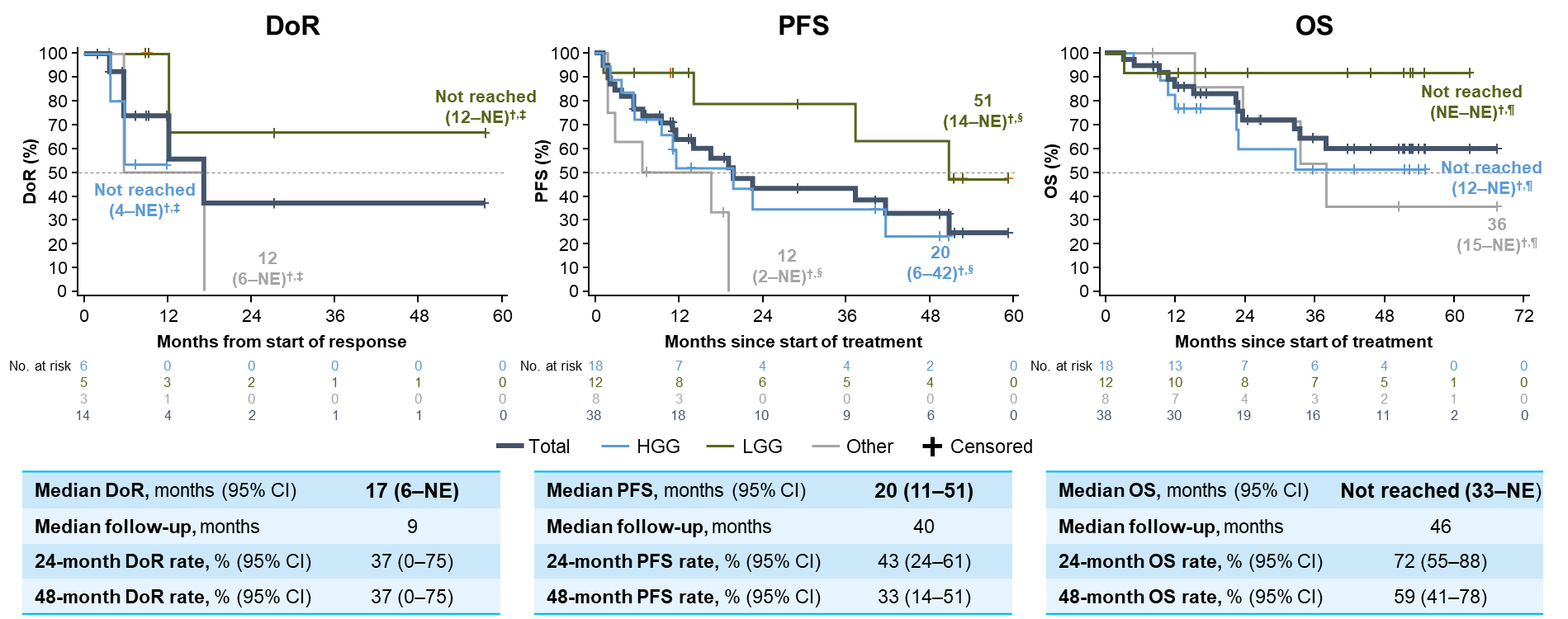
原发性中枢神经系统(CNS)肿瘤是儿童癌症的第二大病因[8],传统的放/化疗等治疗手段仍具有一定的局限性。NTRK基因融合已被证实为原发性CNS肿瘤的致癌驱动基因之一,在儿童高级别胶质瘤(HGG)和低级别胶质瘤(LGG)中的发生率分别达5.3%和2.5%[9]。2024 SIOP大会报告了拉罗替尼治疗原发性CNS TRK融合肿瘤儿童患者的最新数据,结果显示,在入组的38例患者中,拉罗替尼治疗所有原发性CNS肿瘤患者的ORR为37%,其中有可测量病灶患者(n=27)的ORR为52%,初治患者(n=10)的ORR为40%。拉罗替尼在原发性CNS肿瘤患者也显示出持久的缓解,中位DoR为17个月,中位PFS为20个月,48个月OS率为59%[4]。
检测先行,NTRK基因检测赋能精准治疗
随着更多长期生存数据的积累和更多患者的加入,拉罗替尼不断证实了在儿童NTRK基因融合肿瘤患者中的疗效和安全性,强调了进行全面NTRK基因融合检测的必要性。《NCCN 儿童中枢神经系统肿瘤指南(2023年 v1版)》和《加拿大儿童患者 TRK 融合肿瘤的生物标志物检测和治疗共识(2021年)》强调了儿童肿瘤患者 NTRK 基因融合检测的重要性[10,11]。基于研究证据和指南推荐,《拉罗替尼治疗TRK融合儿童肿瘤中国专家共识 》建议对所有的晚期儿童肿瘤患者于治疗前或治疗期间进行NTRK基因融合检测,对NTRK基因融合高发肿瘤类型的局部晚期儿童肿瘤患者在新辅助治疗前进行NTRK基因融合检测。全面及时地精准检测,可筛选出携带NTRK基因融合的患者,进而为其选择有效的治疗方案,实现治疗效果的最大化。
专家点评
王焕民教授:儿童肿瘤是威胁儿童生命健康的主要疾病之一,具有其独特性。NTRK基因融合在儿童肿瘤患者中的整体发生率显著高于成人患者。拉罗替尼不限瘤种、不限年龄,解决了儿童肿瘤治疗迫切的临床需求。随着随访时间的延长,拉罗替尼的优势也在进一步扩大,最新数据显示拉罗替尼治疗的ORR达86%,其中一线治疗的ORR高达90%。对于拉罗替尼治疗TRK融合IFS患者的结果则更值得一提,在所有IFS患者中,ORR为94%,中位DoR为43个月。其中在拉罗替尼作为一线治疗的患者中,ORR高达100%,4年OS率达100%。此外,在恶性程度较高的原发性CNS肿瘤中,拉罗替尼也显示出持久的缓解和良好的安全性,进一步证实拉罗替尼在穿透血脑屏障方面的能力。这些积极的研究结果进一步强调了对于儿童肿瘤患者基因检测显得尤为重要,《中国实体瘤NTRK融合基因临床诊疗专家共识》也建议所有晚期儿童实体瘤患者均进行NTRK融合基因检测,以确保拉罗替尼的精准靶向治疗能更早且更好地发挥作用。随着拉罗替尼纳入2025国家医保目录,这些结果为拉罗替尼治疗儿童NTRK基因融合肿瘤患者带来了实质性的希望,弥补其他治疗手段的不足。本次国家医保目录更新,填补了12岁以下儿童NTRK融合实体瘤患者临床治疗的空白,减轻患者家庭压力及社会负担,为儿童肿瘤患者保驾护航,使更多患者能“吃得起好药”、能“长时间吃药”,为儿童肿瘤患者赋能新的希望和可能。
[1] Trubicka J, et al. Molecular Markers of Pediatric Solid Tumors-Diagnosis, Optimizing Treatments, and Determining Susceptibility: Current State and Future Directions. Cells. 2022 Apr 6;11(7):1238.
[2] 中国抗癌协会小儿肿瘤专业委员会. 拉罗替尼治疗TRK融合儿童肿瘤中国专家共识. 中国肿瘤临床,2023,50(17):865-872.
[3] Alexander Drilon, et al. Long-term efficacy and safety of larotrectinib in non-primary central nervous system TRK fusion cancer. 2024 ESMO. Abstract 627P.
[4] Mascarenhas L, et al. Long-Term Efficacy and Safety of Larotrectinib in Pediatric Patients With Primary CNS and Non-Primary CNS TRK Fusion Tumors. 2024 SIOP.
[5] David S. Hong, et al. Efficacy and safety of larotrectinib as first-line treatment for patients with TRK fusion cancer: an updated analysis. 2024 ESMO. Abstract 628P.
[6] Federman N, et al. Updated Efficacy, Safety, and Treatment Discontinuation Outcomes of Larotrectinib in Pediatric Patients with TRK Fusion Sarcomas. 2024 CTOS.
[7] Albert CM, et al. Efficacy and Safety of Larotrectinib as First-line Treatment in Patients with TRK Fusion Sarcomas. 2024 CTOS.
[8] Steliarova-Foucher E, et al. International incidence of childhood cancer, 2001-10: a population-based registry study. Lancet Oncol. 2017 Jun;18(6):719-731.
[9] Okamura R, et al. Analysis of NTRK Alterations in Pan-Cancer Adult and Pediatric Malignancies: Implications for NTRK-Targeted Therapeutics. JCO Precis Oncol. 2018;2018:PO.18.00183.
[10] Gajjar A, et al. Pediatric central nervous system cancers, version 2.2023, NCCN clinical practice guidelinesin oncology[J]. J Natl Compr Canc Netw, 2022, 20(12):1339-1362.
[11] Perreault S, et al. Canadian consensus for biomarker testing and treatment of TRK fusion cancer in pediatric patients[J].Curr Oncol, 2021, 28(1):346-366.
审核码:MA-LAR-CN-0271-1
排版编辑:肿瘤资讯-jyy











 苏公网安备32059002004080号
苏公网安备32059002004080号


