整理:肿瘤资讯
来源:肿瘤资讯
以下内容仅供中国大陆地区执业的医学药学专业人士阅读参考,如您非前述专业人士,请离开本页面
病例点评:中国医学科学院肿瘤医院 张业繁教授
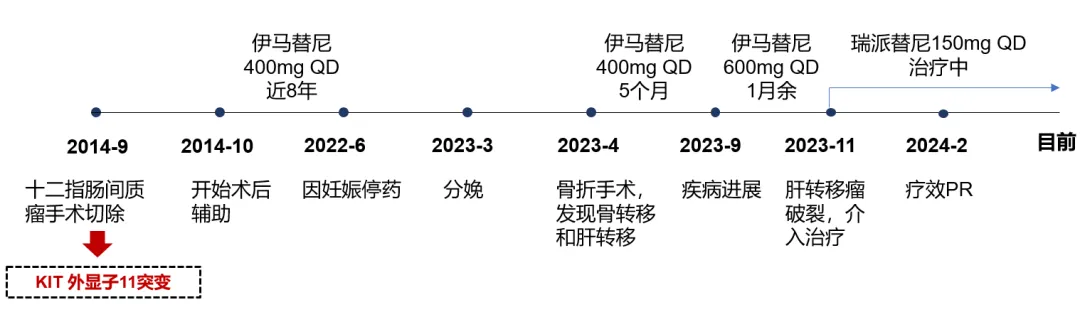
年轻女性胃肠间质瘤患者群体面临着工作、妊娠和生育方面的挑战,是临床密切关注的群体。在此分享一例年轻的KIT 11外显子突变的十二指肠间质瘤病例,患者于2014年经历十二指肠间质瘤切除术后,使用伊马替尼辅助治疗近8年时间,后因妊娠停药。分娩后因骨折发现骨转移以及CT检查发现肝转移,继续使用伊马替尼治疗后,疗效不佳,肿瘤快速进展,伊马替尼加量治疗1月余,肿瘤破裂,患者未能从伊马替尼加量治疗中获益。后结合患者基因型使用瑞派替尼进行精准个体化治疗,很快取得部分缓解(PR),且安全性可耐受,目前瑞派替尼治疗近1年,为患者带来了切实的临床获益。本病例引导我们深入思考,也为年轻胃肠间质瘤患者的临床诊疗提供了宝贵的经验和借鉴。

病例点评
张业繁教授
病例简介
基本情况
患者,女,36岁。2014-08 检查发现右侧腹部肿物,当地腹部增强CT检查提示:右侧腹部肿物,最大径8.0cm,来源于十二指肠可能大。
治疗经过
手术
2014-09 外院行剖腹探查+十二指肠间质瘤切除术+空肠营养管置入术。
术中所见:十二指肠水平部可触及肿物,直径8.0cm;
术后病理提示:胃肠间质瘤,高风险组。肿瘤大小8.0cm×5.5cm×5.5cm,核分裂象<5个/50HPF,肿瘤侵及周围肠壁;
免疫组化:CD117(+),CD34(-),DOG1(+),S-100(-), Desmin(-),Ki-67(1%+);
基因检测:KIT 11外显子突变。
伊马替尼400mg QD
2014-10 术后行伊马替尼 400mg QD 治疗至2022年,2022年因怀孕暂停用药。
2023-03-22 患者分娩
2023-04-07 患者因骨折,行手术治疗。术后病理提示:(左股骨干)瘤段截除标本,符合转移性胃肠间质瘤伴病理性骨折;免疫组化:CD117(+),DOG-1(+),CD34(小灶+)。
2023-04-24 开始再次服用伊马替尼400mg QD 治疗。
2023-04-27 胸腹盆增强CT:肝内多发稍低密度结节及肿物,大者约9.4cm×7.1cm。
2023-06-08 胸腹盆增强CT:肝内多发稍低密度转移结节及肿物,较前缩小,现大者约7.5cm×7.2cm。
2023-07-25 胸腹盆增强CT:肝内多发稍低密度转移结节及肿物,部分较前略增大,部分同前相仿,现大者约8.3cm×7.8cm。
2023-09-26 胸腹盆增强CT:肝内多发稍低密度转移结节及肿物,部分较前增大,现大者约10.3cm×8.8cm
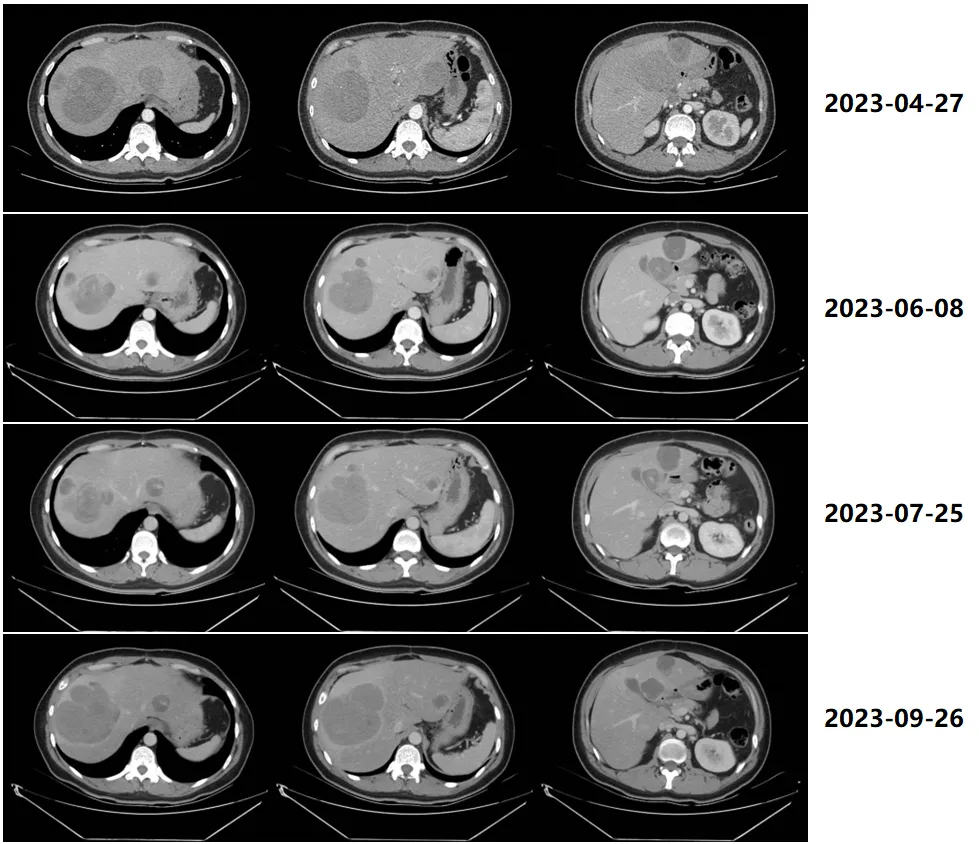
图1. 再次服用伊马替尼后,胸腹盆增强CT变化
伊马替尼加量治疗
2023-09-27 考虑到疾病进展,后续的治疗方案有换用二线药物或伊马替尼加量治疗等,结合患者意愿,选择伊马替尼加量至600mg QD。肿瘤缓慢进展。
2023-11-05 患者因剧烈腹痛至当地医院急诊就诊,考虑肝转移瘤破裂出血,行介入治疗后症状改善。
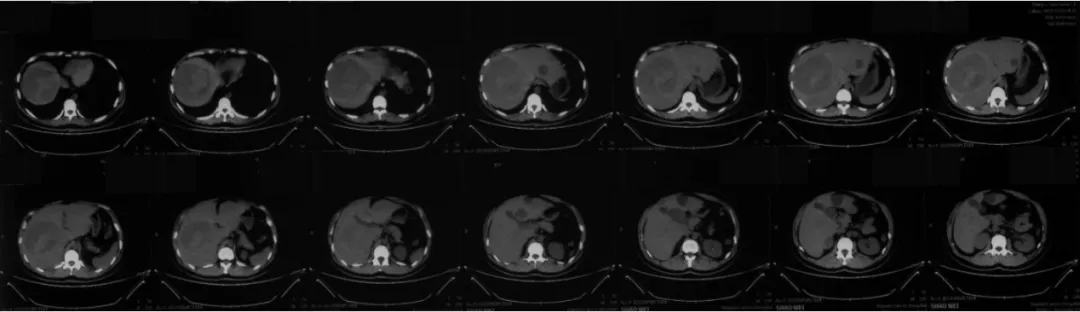
图2. 2023-11-05 外院急诊CT 疾病进展(PD)
瑞派替尼 150mg QD治疗
2023-11-23 考虑到患者无法从伊马替尼加量治疗中获益,建议患者更换药物,结合目前的循证医学证据,可选择的治疗方案包括舒尼替尼、瑞派替尼等,结合患者突变基因型及患者意愿,开始服用瑞派替尼150mg QD治疗。
2023-12-27 我院胸腹盆增强CT:肝顶部右叶为主较大肿块影,较大截面约12cm×9.3cm。
2024-02-29 外院CT复查提示:肝内多发结节、肿块较前明显缩小,较大者7.7cm×7.2cm,其内高密度影较前明显缩小,疗效达PR。
2024-05-16 CT及肝脏磁共振复查提示:肝转移瘤稳定,略缩小,较大者7.2cm×6.6cm。
2024-8-19 CT复查提示:肝转移瘤稳定,略缩小,较大者7.0cm×5.9cm。截止到目前,患者使用瑞派替尼治疗近1年。治疗期间不良反应为1级皮炎、脱发,患者耐受性好。
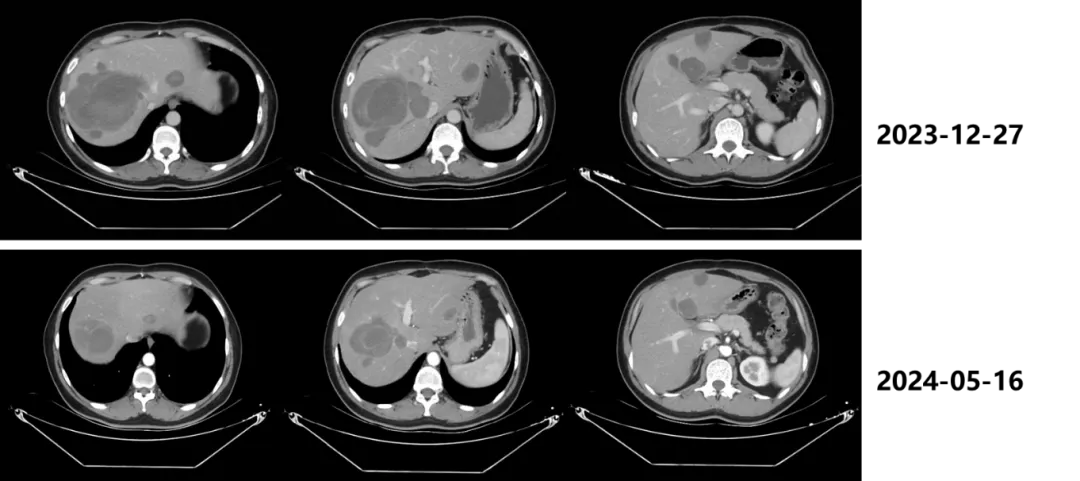
图3. 服用瑞派替尼后,胸腹盆增强CT变化
治疗小结
专家点评
张业繁教授:
本病例患者较年轻,且病程中经历了妊娠。在此类患者中,需考虑妊娠和生育阶段的药物治疗。在文献中关于妊娠与胃肠道间质瘤共存的报道很少,而关于妊娠期间使用伊马替尼的已发表数据表明,尤其是在妊娠的前3个月使用时,可能会导致畸性或流产 [1] 。因此,患者在伊马替尼治疗近8年后,因妊娠选择停用伊马替尼。
目前,对于高危胃肠间质瘤,伊马替尼辅助治疗最佳持续时间未知,CSCO指南推荐3年(Ⅰ级推荐)或5年(Ⅲ级推荐)。对于高危GIST患者,辅助伊马替尼仅仅是延迟了不可避免的复发,还是可能提供治愈性益处,也是临床讨论的热点。既往有研究表明,在无可见肿瘤病灶的情况下,经过长期伊马替尼维持治疗后的晚期胃肠间质瘤患者,中断治疗使大部分患者疾病进展,但是重新恢复伊马替尼治疗能够有效地控制肿瘤 [2] 。也有研究表明,对于严格筛选的影像学完全缓解的寡转移性胃肠间质瘤患者停用伊马替尼可能是安全的 [3] 。本例高危患者经过手术,术后使用伊马替尼治疗近8年,后因妊娠停用伊马替尼,分娩后因骨折入院,发现GIST骨转移合并肝转移,恢复伊马替尼治疗后,疾病仅得到短暂的控制,3个月复查时已发生耐药。因外院资料不可获取,也不排除患者既往有残余病灶或已发生转移。对于伊马替尼敏感的GIST患者是否可以停药仍值得进一步探讨。
目前多个研究显示,伊马替尼进展后加量治疗临床获益有限,中位无进展生存期(mPFS)仅3~4个月 [4,5] 。目前国内外指南均推荐,伊马替尼标准剂量进展后,无论局限性或广泛进展均首选换二线药物,某些情况下可考虑手术等局部治疗联合药物治疗或伊马替尼加量治疗(主要针对KIT外显子 9突变患者)。本例个案结合患者意愿使用伊马替尼加量治疗,治疗1月余发生肿瘤破裂,患者未能从伊马替尼加量治疗中获益。
按线治疗和个体化精准治疗,一直是晚期胃肠间质瘤治疗讨论的热点,伊马替尼耐药后,后续药物如何选择,如何最大化患者获益,也是临床考虑的重要方向。Ⅲ期INTRIGUE研究表明,瑞派替尼对原发KIT外显子11突变显示更好的获益趋势 [6] 。中国二线研究表明,瑞派替尼对原发KIT 11突变人群疗效显著,独立影像评估结果显示,瑞派替尼 vs 舒尼替尼的mPFS为未达到 vs 4.9个月, HR 为0.46,意味着瑞派替尼将疾病进展或死亡风险降低54%,研究者评估结果显示,瑞派替尼 vs 舒尼替尼的mPFS为13.8个月 vs 7.0个月, 瑞派替尼组的mPFS提高了近1倍 [7] 。长期随访数据显示,在KIT 11突变人群中,瑞派替尼对比舒尼替尼展现出明显的总生存期(OS)获益趋势,瑞派替尼 vs 舒尼替尼的中位OS(mOS)为 未达到 vs 28.6个月, HR 为0.58,意味着瑞派替尼组的死亡风险降低了42%,且瑞派替尼组3年OS率为56%,后续随着随访时间的进一步延长,瑞派替尼组的mOS很有可能超过3年 [8] 。安全性数据显示,中外人群安全性数据一致,瑞派替尼具有更好的安全性 [6] ,便于更好地进行疾病管理。同时发现,瑞派替尼二线治疗不影响后续舒尼替尼等TKI的疗效 [9] 。基于这些循证医学证据,结合患者KIT 11突变的基因型以及患者对生活质量更高的要求,在患者充分知情的情况下,基于患者意愿,选择了瑞派替尼治疗,治疗3个月,肿瘤缩小明显,疗效达PR,肿瘤密度也明显降低,目前已使用瑞派替尼治疗近1年,不良反应小,耐受性好。精准个体化治疗为患者带来了显著的临床获益。
综上,本例患者为一例年轻的十二指肠GIST合并骨转移和肝转移的复杂病例,且TKI治疗期间经历了妊娠,也引导我们深入思考,如何平衡患者工作、妊娠、生育和抗肿瘤治疗。目前,结合患者基因型进行精准个体化治疗,也为患者带来了切实的临床获益,为胃肠间质瘤临床诊疗带来思考和借鉴。
参考文献:
1. Zarkavelis G, Petrakis D, Pavlidis N: Gastrointestinal stromal tumors during pregnancy: a systematic review of an uncommon but treatable malignancy. Clin Transl Oncol 2015, 17(10):757-762.
2. Kang Y-K, Kim H-D, Kim HJ, et al: Interruption of imatinib in advanced gastrointestinal stromal tumor after prolonged imatinib maintenance in the absence of gross tumor lesions. Journal of Clinical Oncology, 40(16_suppl):11539-11539.
3. Hompland I, Boye K, Papakonstantinou A, et al: Discontinuation of imatinib in patients with oligo-metastatic gastrointestinal stromal tumor who are in complete radiological remission: A prospective multicenter phase II study. Journal of Clinical Oncology, 40(16_suppl):11535-11535.
4. Li J, Gong JF, Li J, et al: Efficacy of imatinib dose escalation in Chinese gastrointestinal stromal tumor patients. World J Gastroenterol 2012, 18(7):698-703.
5. Hsu CC, Wu CE, Chen JS, et al: Imatinib escalation or sunitinib treatment after first-line imatinib in metastatic gastrointestinal stromal tumor patients. Anticancer Res 2014, 34(9):5029-5036.
6. Bauer S, Jones RL, Blay JY, et al: Ripretinib Versus Sunitinib in Patients With Advanced Gastrointestinal Stromal Tumor After Treatment With Imatinib (INTRIGUE): A Randomized, Open-Label, Phase III Trial. J Clin Oncol 2022, 40(34):3918-3928.
7. Li J, Zhang J, Zhang Y, et al: Efficacy and safety of ripretinib vs. sunitinib in patients with advanced gastrointestinal stromal tumor previously treated with imatinib: A phase 2, multicenter, randomized, open-label study in China. European Journal of Cancer 2024, 196:113439.
8. Li J, Zhang J, Zhang Y, et al: 1759P Long-term updated outcomes of a phase II study of ripretinib vs. sunitinib in chinese patients with advanced gastrointestinal stromal tumor. Annals of Oncology 2024, 35:S1048.
9. Zalcberg JR, Jones RL, Blay J-Y, et al: Overall survival and long-term safety with ripretinib vs sunitinib in patients with advanced gastrointestinal stromal tumor previously treated with imatinib: Final analyses from INTRIGUE. Journal of Clinical Oncology 2024, 42(3_suppl):748-748.
责任编辑:肿瘤资讯-Linda
排版编辑:肿瘤资讯-C Y X
版权声明
本文专供医学专业人士参考,未经著作人许可,不可出版发行。同时,欢迎个人转发分享,其他任何媒体、网站如需转载或引用本网版权所有内容,须获得授权,且在醒目位置处注明“转自:良医汇-肿瘤医生APP”。











 苏公网安备32059002004080号
苏公网安备32059002004080号


