随着精准医学持续、蓬勃地发展,驱动基因突变阳性非小细胞肺癌(NSCLC)患者的治疗模式已全面迈向“有靶打靶”的时代,其中间变性淋巴瘤激酶(ALK)基因融合突变是热门靶点之一。凭借CROWN研究中一骑绝尘的临床获益[1],奠定了第三代ALK TKI洛拉替尼在晚期一线治疗中的优选地位。2024年召开的美国临床肿瘤学会(ASCO)大会及欧洲肿瘤内科学会(ESMO)大会上,CROWN研究接续更新了总人群及亚洲亚组的5年随访数据,结果显示无进展生存期(PFS)均未达到[3,4]。临床学者在此基础上应用洛拉替尼向更早期患者治疗领域推进探索:2024年世界肺癌大会(WCLC)公布了LORIN研究的中期分析结果,充分展现了洛拉替尼在局晚期ALK阳性NSCLC患者围手术期治疗中迸发的潜能。【肿瘤资讯】特邀深圳市人民医院胸外科杨林教授对该研究为临床实践提供的价值展开深入解读。
深圳市人民医院胸外科 主任医师,硕士生导师
深圳市呼吸疾病研究所 副所长
广东省医学会肺部肿瘤学分会副主任委员
广东省医疗行业协会胸外科管理分会副主任委员
广东省胸部肿瘤防治研究会副会长
广东省转化医学学会肿瘤学分会副主任委员
吴阶平医学基金会模拟医学胸外科分会常务委员
中国临床肿瘤学会肿瘤生物标志物专家委员会委员
中国医疗保健国际交流促进会胸部肿瘤学分会委员
广东省医学会胸外科分会常务委员
广东省抗癌协会肺癌专业委员会常务委员
广东省临床试验协会理事
深圳市抗癌协会肺癌专业委员会主任委员
LORIN研究关注洛拉替尼治疗ALK阳性NSCLC局晚期患者,喜获学术硕果
杨林教授:当靶向药物在驱动基因阳性晚期NSCLC患者中获得良好获益后,缘于造福患者的初心,我们临床工作者自然会尝试着将其向更早期患者应用推进。此类模式广东省人民医院钟文昭教授带领团队在EGFR突变人群中早有验证——在OPTIMAL-CTONG-0802研究基础上,EMERGING-CTONG 1103研究探索了厄洛替尼用于IIIA-N2期EGFR敏感性突变NSCLC患者的新辅助治疗,结果显示厄洛替尼组较对照组PFS显著延长(21.5个月 vs.11.4 个月,HR=0.36)[4]。
在ALK阳性人群中该模式也有初步探索——基于ASCEND-4研究结果, SAKULA单臂研究评估了塞瑞替尼新辅助治疗可切除的ALK阳性局晚期NSCLC的疗效及安全性。结果显示客观缓解率(ORR)为100%,6例患者后续接受手术治疗,5例实现了R0切除,主要病理缓解率(MPR)达57%,2例(29%)患者实现完全缓解(CR)。尽管样本量有限,但初步体现了可观的临床获益和良好的安全性[5]。
ALK TKI发展到今天,我们临床可及药物拥有“八大金刚”,其中三代ALK-TKI洛拉替尼无疑极具代表性。我们都看到今年CROWN研究系列数据的持续公布,充分证实了洛拉替尼为ALK阳性晚期患者一线治疗带来可预见的长生存获益,助其回归正常工作、生活,那么理论上在局晚期患者中应用洛拉替尼治疗有可能取得不劣于晚期患者的良好疗效。也正是基于该理论基础,钟文昭教授团队发起了II期前瞻性单臂临床试验——LORIN研究,聚焦洛拉替尼在局晚期ALK阳性NSCLC患者围手术期(含术前诱导和术后巩固)的治疗潜力。设计中体现了临床诊疗巧思和对既往探索经验的改进,数据结果为临床治疗决策提供了铺垫和参考价值。
LORIN研究纳入III期(研究者注:包括潜在可切除和不可切除)ALK阳性患者,给予3个周期洛拉替尼诱导治疗,随后由多学科诊疗(MDT)评估后续局部治疗方案(放疗或手术)。如患者达到主要病理缓解/病理完全缓解(MPR/pCR),且无N3肿瘤残留,同时手术后1个月MRD为阴性则免于巩固治疗,仅需随访,反之需要接受最长2年的洛拉替尼巩固治疗。研究的主要终点是pCR、PFS,如果至少3例患者达到pCR,则启动试验的第二阶段。研究中还进行了纵向的MRD检测和NGS分析,以评估患者的治疗反应[6]。
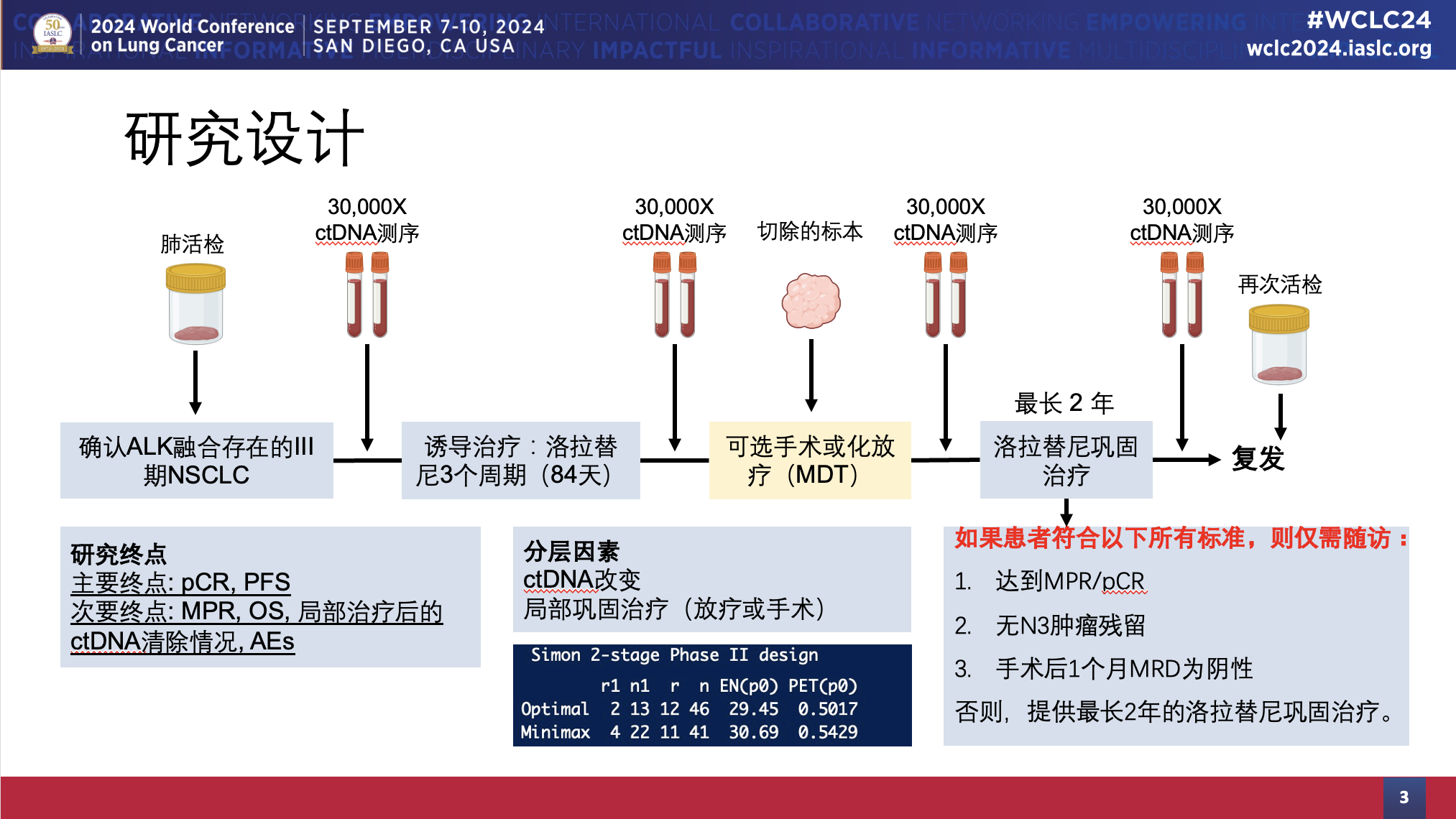
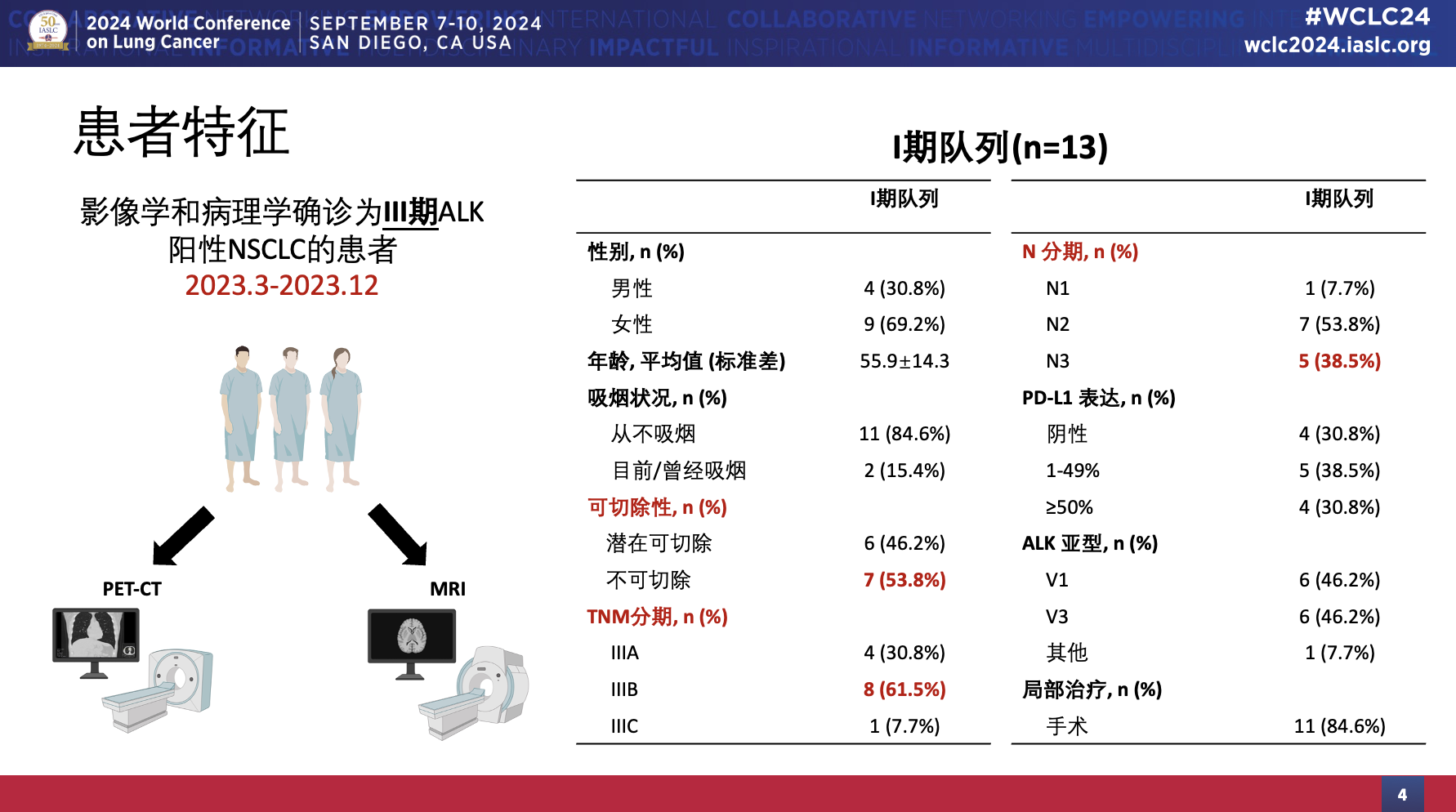
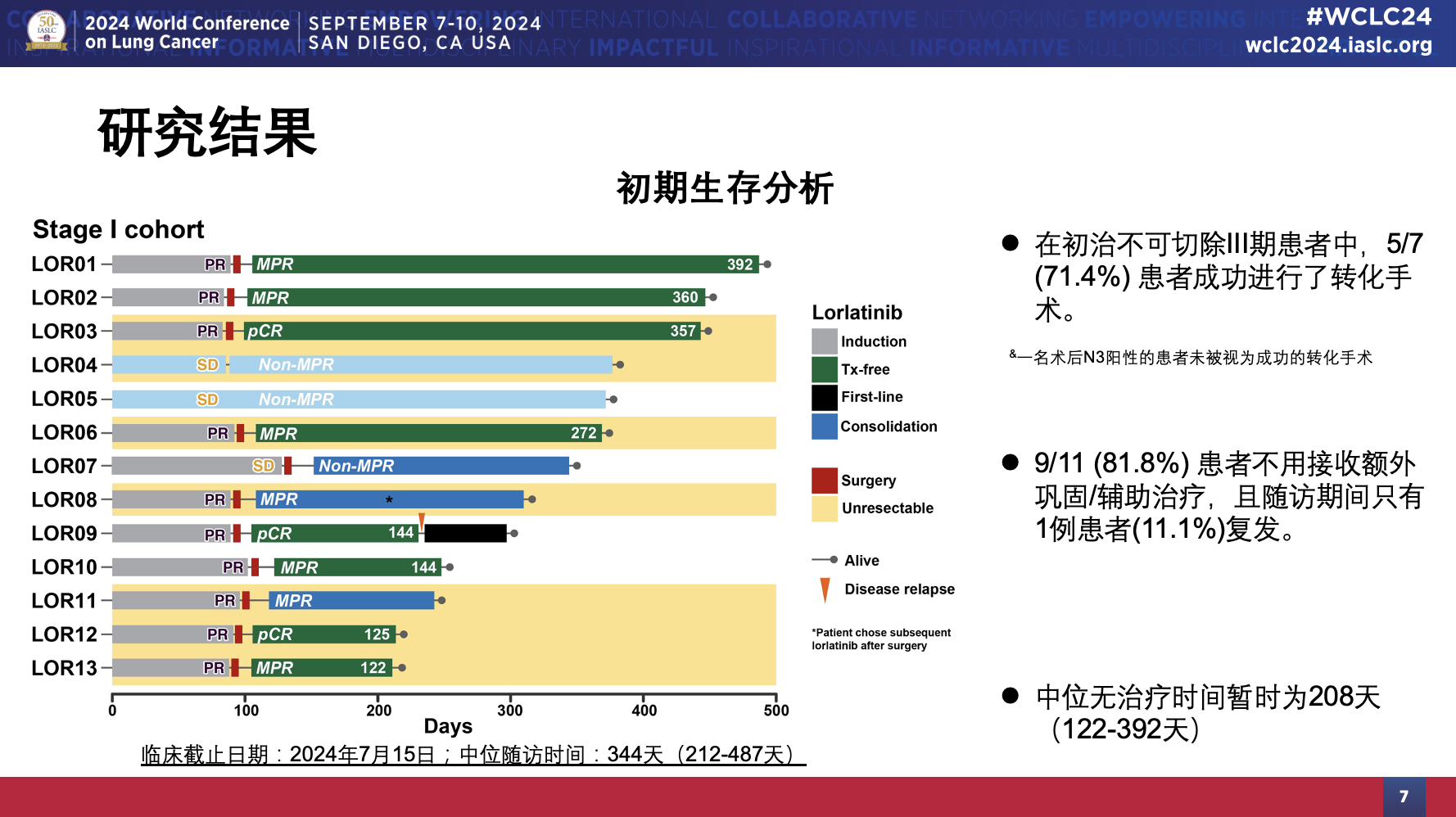
本次WCLC公布了中期分析结果(Ⅰ期队列,N=13,6例患者为潜在可切除,7例患者为潜在不可切除)[6]。临床数据截止日期:2024年7月15日;中位随访时间:344天(212-487天)。
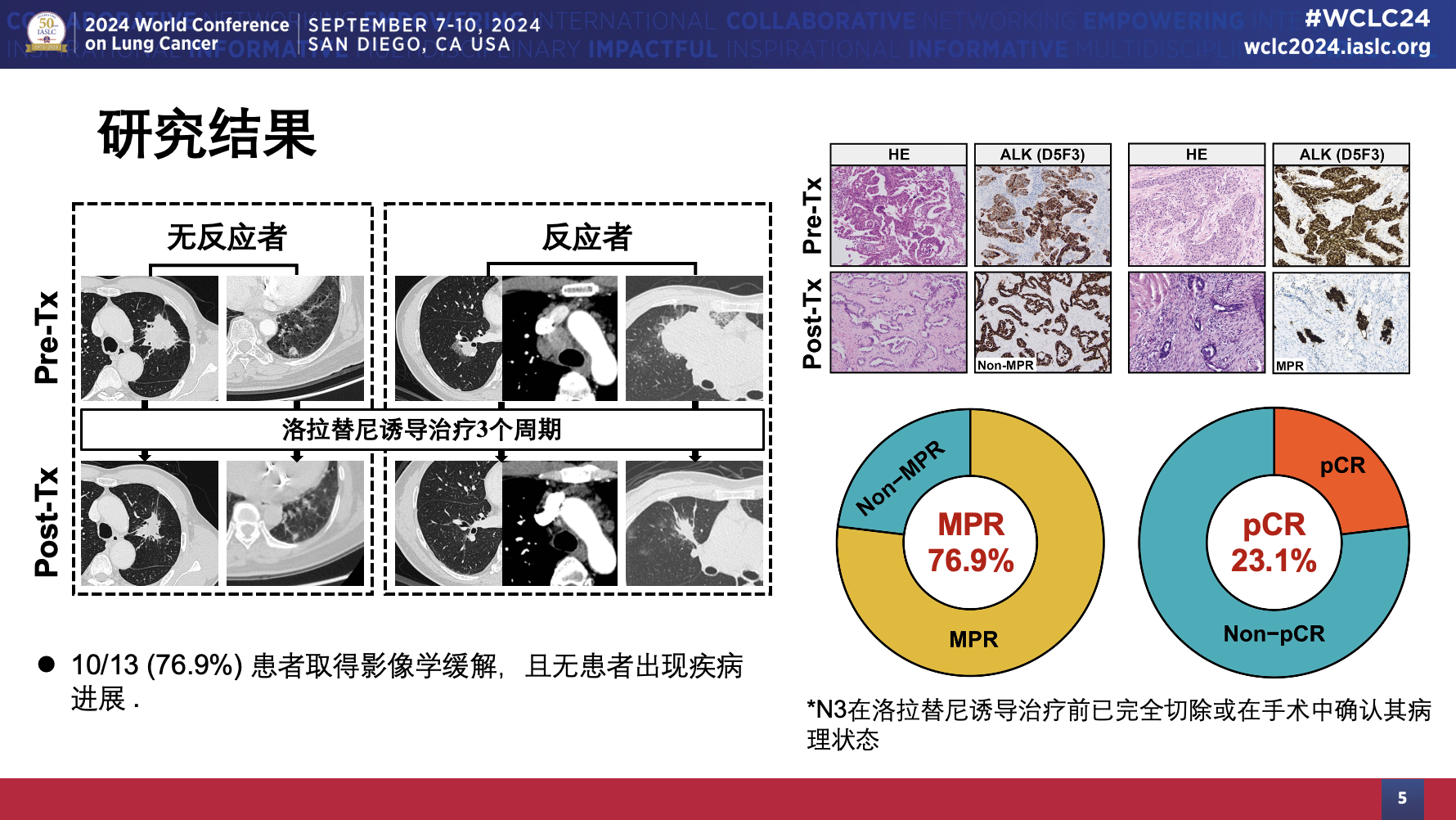
洛拉替尼诱导治疗后,76.9%(10/13)的患者取得影像学缓解,且无患者出现疾病进展。MPR/pCR率76.9%(10/13),pCR率23.1%(3/13)。
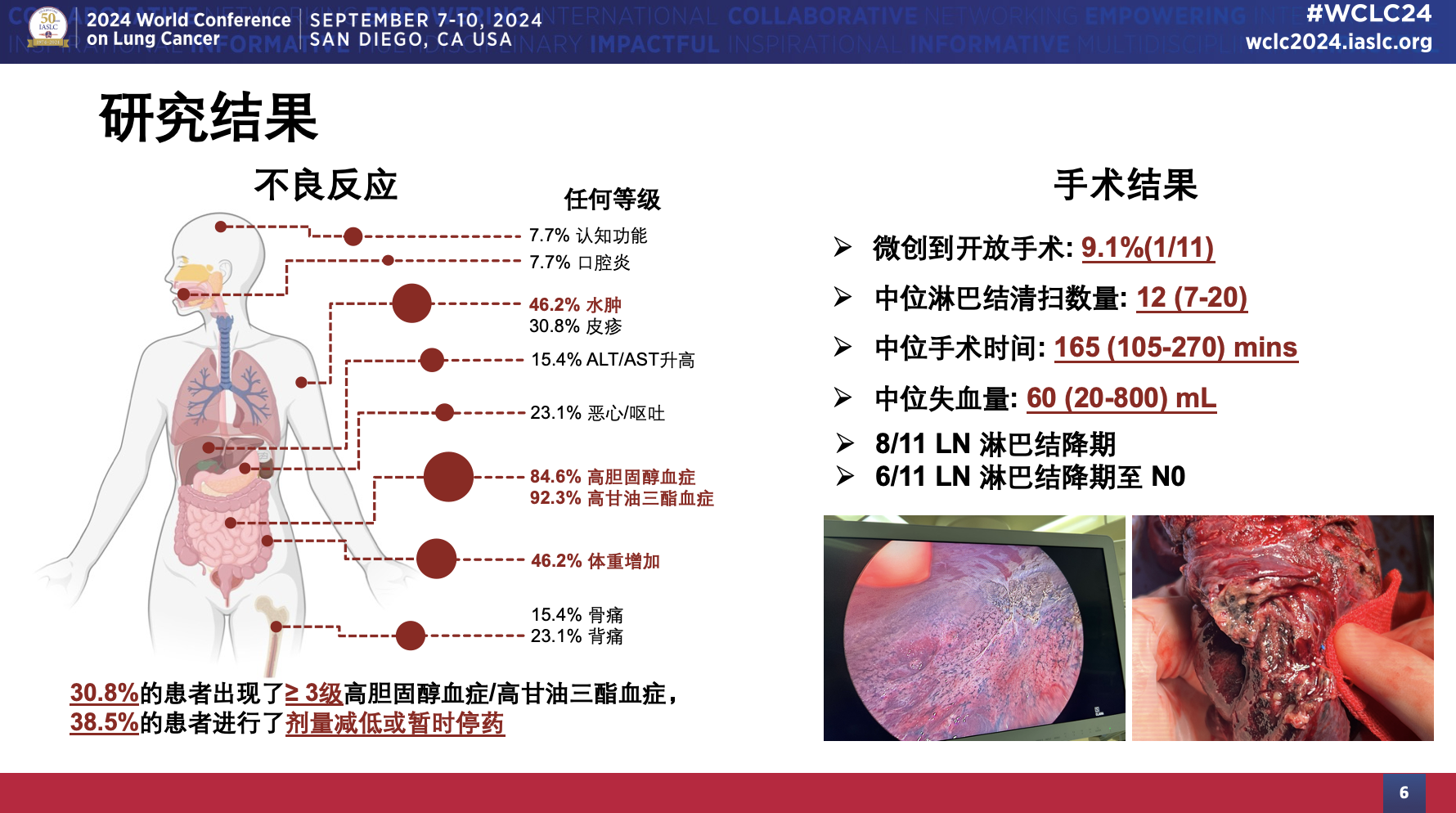
其中11例患者接受了手术切除,9.1%(1/11)的患者由微创转为开放手术,8/11(72.7%)淋巴结降期,6/11(54.5%)淋巴结降期至N0。在初始不可切除的III期患者中,71.4%(5/7)的患者成功进行转化手术。由此可见洛拉替尼的诱导治疗对于ALK阳性NSCLC局晚期患者根治性手术的机会争取或优化均发挥了关键作用。
值得一提的是,这11例接受手术的患者中有9例(81.8%)不需要接受额外巩固/辅助治疗,且随访期间仅有1例(11.1%)复发,中位无治疗时间暂时为208天(122-392天),超过6个月。这充分体现了洛拉替尼的诱导治疗为ALK阳性NSCLC局晚期患者带来了积极显著的疗效,实现有效降期,经根治性手术切除后无需辅助用药,观察可能是一种可选策略。在保证治疗效果的前提下避免了药物依赖相关的副作用,这对临床实践具有重大意义。
研究特别加入了治疗前后患者分子特征层面的探索,经过洛拉替尼诱导治疗后,MRD阳性的患者在ctDNA中未检测到ALK融合。达到MPR/pCR的10例患者中,治疗前MRD阳性的6例患者,治疗后3例MRD转为阴性。但实体瘤患者ctDNA中ALK融合的检测率有限,MRD检测在捕捉残余病灶方面具有中等效能,还需要进一步的技术改进,可作为患者预后的监测指标之一为临床提供参考,尚不能完全左右临床治疗决策。

总体而言,研究中期分析得出结论:洛拉替尼诱导治疗III期ALK阳性NSCLC患者在临床上具有可行性且相对易于管理,对于初始不可切除患者有显著提高手术转化率的可能。对于达到MPR/pCR、无N3残余病灶且术后1个月MRD阴性的患者中位无治疗期已超6个月(仍在持续随访),而符合前两条但术后MRD阳性的患者,研究者认为观察可能是一种可选策略,需要同步密切监测。
我们作为兄弟医院恭喜钟文昭教授团队发起的LORIN研究在今年WCLC大会上报告数据结果,作为胸外科医生我也有感于这项研究展现洛拉替尼为局晚期患者带来的可能获益对临床诊疗格局的现实意义,非常期待研究未来的进展更新。
局晚期患者是否可切的界定:理想和现实之间仍有等待跨越的鸿沟
杨林教授:说回到III期不可切除NSCLC患者当前的标准治疗模式,一般为同步放化疗联合免疫治疗。然而有回顾性分析显示这在ALK阳性患者中的疗效并不理想,其获益远低于整体患者群体,可能缘于肿瘤高度异质性和肿瘤微环境变化影响等多方面因素。目前,对于无法手术的III期ALK阳性NSCLC患者的最佳治疗方案尚未达成共识。尽管ALK-TKI已显著提升了ALK阳性晚期NSCLC患者的预后,但其在局晚期NSCLC中的应用效果仍需进一步研究明确。
上海交通大学附属胸科医院陆舜教授团队的一项多中心回顾性分析研究[7]以真实世界数据为基础,回答了ALK-TKI相对于放化疗和化疗在局晚期ALK阳性患者的治疗价值。研究结果显示,对于不可切除ALK阳性III期NSCLC患者,ALK-TKI、放化疗和单纯化疗的中位至疾病进展时间(TTP)分别为17.8个月、14.6个月、8.6个月。提示采用ALK-TKI一线治疗的局晚期患者获得的疗效显著优于接受放化疗或化疗的患者。
除此以外,手术切除仍是肺癌根治的重要方式。通过一定的方案,局晚期肺癌患者仍有手术切除机会。我们前面介绍到的LORIN研究对于初始不可切除的III期患者接受洛拉替尼诱导治疗后,71.4%患者可成功进行转化手术,且81.8%患者不用接受额外辅助治疗[6]。
然而,即使对于特定的治疗方案,也需根据患者特征进行筛选,以实现个体化治疗。患者的肿瘤到底可以或者不可以切除界定微妙,可能存在主观性影响。LORIN研究方案的临床应用,我认为首先是需要标准化判别III期患者肿瘤的具体状态(究竟是否可切除);其次对于完全确认局晚不可切除患者,是否可以归同于晚期患者,完全应用洛拉替尼进行全身系统治疗(去手术化),这是基于两个关键点来考量,一是局晚期靶向治疗可预期的良好疗效,二是靶向诱导治疗可能会造成肿瘤瘢痕纤维化,增大后续根治性手术剥离切除的难度和风险;再次对于药物治疗反应不敏感的患者比如原发耐药,应及时应用局部治疗手段,以避免药物低效贻误治疗时机和效果。此外,确认为潜在可切除的患者在切除治疗之前是否还需要应用药物治疗,既然判断为可切除那是否应该直接切除,仍需更明确的答案。
而这些都涉及临床如何去进行人群的精准筛选,其中仍需要大量深度的工作,例如包含分子特征差异的分层探索、靶向治疗是否可以联合化疗或者抗血管生成药物等等。
往者已矣,展望未来,多维考量,全方探索
杨林教授:如前所述,ALK阳性NSCLC局晚期患者具有高度异质性、治疗模式和预后均有显著差异等特征,在临床上让我们也很是纠结。
本次LORIN研究的报道为临床探索提供了新的进展,我们也对研究有更高的期待,希望尽可能回答该类患者的治疗疑惑,比如:①潜在可切除的概念在临床上较为模糊,是否可通过影像、分子特征同时结合手术时间和出血量等体现每例患者的手术难度,进而间接反映ALK TKI新辅助治疗对于手术开展的影响;②继续随访评估每例患者的MRD状态,且进一步细化MRD评估所包含的内容和因素等。同时也期待在此基础上,未来能开展更多、更大样本量的研究探索,给临床治疗提供更夯实的证据。
而关于ALK阳性III期不可切除NSCLC的未来治疗,可突破的潜在方向包括如下几点:第一、患者筛选,如何制定一套行之有效的筛选细则来对患者进行分层,真正做到规范化、个体化、精准化的抗肿瘤治疗;第二、生物标志物的发现和验证,通过高精尖技术的开发和优化,探索并确定能够准确预测患者对靶向疗法反应的生物标志物,为实现精准治疗策略提供科学依据;第三、克服耐药性,尽管ALK抑制剂效果显著,但耐药性问题仍旧是治疗中的一大挑战;第四、新药和新疗法的开发,针对ALK阳性NSCLC的新药开发,尤其是针对耐药突变的新药,是延续经治患者生存获益的关键;第五、综合治疗策略,探索ALK抑制剂与其他治疗方法(如放疗、化疗、免疫治疗、抗血管生成药物等)的联合使用;第六、基础研究与临床转化,加强基础研究与临床研究的结合,将基础研究成果快速转化为临床应用。通过这些创新点的研究,期待能够实现更有效的疾病管理和患者生存率的提高。
1. Solomon BJ, et al. J Clin Oncol. 2024 in press. doi:10.1200/JCO.24.00581.
2. J Clin Oncol 42, 2024 (suppl 17; abstr LBA8503)
3. z YL, et al. 2024 ESMO. Presentation Number 1279P
4. Wen-Zhao Zhong,et al.Signal Transduct Target Ther . 2023 Feb 24;8(1):76.doi:10.1038/s41392-022-01286-3.
5. Y.Zenke, et al. Neoadjuvant Ceritinib for Locally Advanced Non-Small Cell Lung Cancer with ALK Rearrangement: SAKULA Trial. 2019 WCLC P1.18-04.
6. Interim Analysis of a Phase 2 Prospective Trial of Induction Lorlatinib in Locally Advanced ALK-Positive NSCLC (LORIN).2024 WCLC.
7. S. Lu, L. Shen, Y. Yu, X. Ye. Management of Inoperable Locally Advanced Stage III ALK fusion Positive NSCLC: A Retrospective Multi-institutional Analysis. 2023 WCLC-EP08.02-40.
排版编辑:肿瘤资讯-IR











 苏公网安备32059002004080号
苏公网安备32059002004080号


