2023年11月,淋巴瘤治疗领域迎来了一个里程碑事件:国内首款CD20/CD3双特异性抗体 (简称“双抗”)格菲妥单抗(Glofitamab)在中国获批,单药用于治疗既往接受过至少两线系统性治疗的复发或难治性弥漫大B细胞淋巴瘤(R/R DLBCL)成人患者。这标志着我国淋巴瘤治疗进入了“双抗时代”。为进一步提升广大医疗工作者对双抗药物的了解,提升双抗药物临床应用的规范化水平,【肿瘤资讯】特别推出“全景双抗”医生教育专栏,旨在赋能医患,助力解锁治愈密码。本期特邀苏州大学附属第一医院金正明教授深入探讨T细胞介导的肿瘤杀伤在DLBCL治疗中的应用,尤其是双特异性抗体格菲妥单抗的研究进展,展望T细胞疗法的未来发展方向。

点击视频,观看更多精彩内容
苏州大学附属第一医院血液科
淋巴瘤亚专科负责人
中国抗癌协会淋巴瘤专业委员会委员
中华医学会血液分会淋巴瘤学组委员
江苏省肿瘤防治联盟淋巴瘤专业委员会副主任委员
江苏省抗癌协会常务委员
江苏省血液病质量管理委员会委员
中国老年医学会血液分会委员
参编【血液病学】、【卫生部抗菌药物规范使用培训教材】等,在恶性血液病诊治及造血干细胞移植领域具有丰富临床经验。
知己知彼,聚焦T细胞与肿瘤细胞之间的“攻防之道”
DLBCL是成人中最常见的非霍奇金淋巴瘤(NHL)类型,其生物学特性和临床表现高度异质。尽管以R-CHOP(利妥昔单抗、环磷酰胺、多柔比星、长春新碱和泼尼松)为代表的一线免疫化疗方案在DLBCL治疗中取得了显著的效果,但仍有约30%-40%的患者会发生复发或难治,预后不佳[1]。近年来,免疫疗法的兴起,特别是基于T细胞的治疗的T细胞疗法,为DLBCL患者带来了新的希望。
T细胞功能与肿瘤免疫逃逸
T细胞是适应性免疫系统的关键组成部分,负责细胞免疫应答的主要功能[2]。
在弥漫性大B细胞淋巴瘤(DLBCL)中,肿瘤微环境中免疫细胞的构成显著影响疾病的发展和预后。研究表明,高比例(>6%)的CD4+和CD8+ T细胞浸润与患者生存率的提高密切相关。
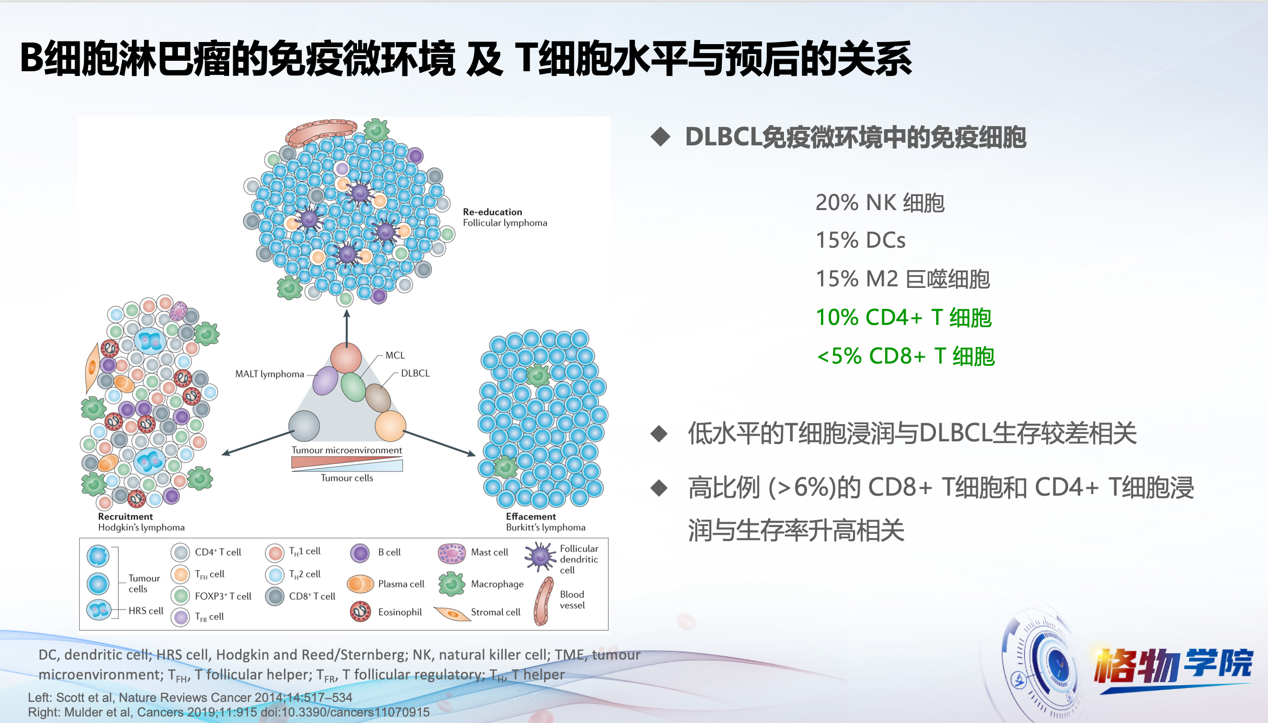
然而,许多DLBCL患者的肿瘤微环境中存在T细胞浸润不足或功能受损的现象(图1、2)[3, 4]。
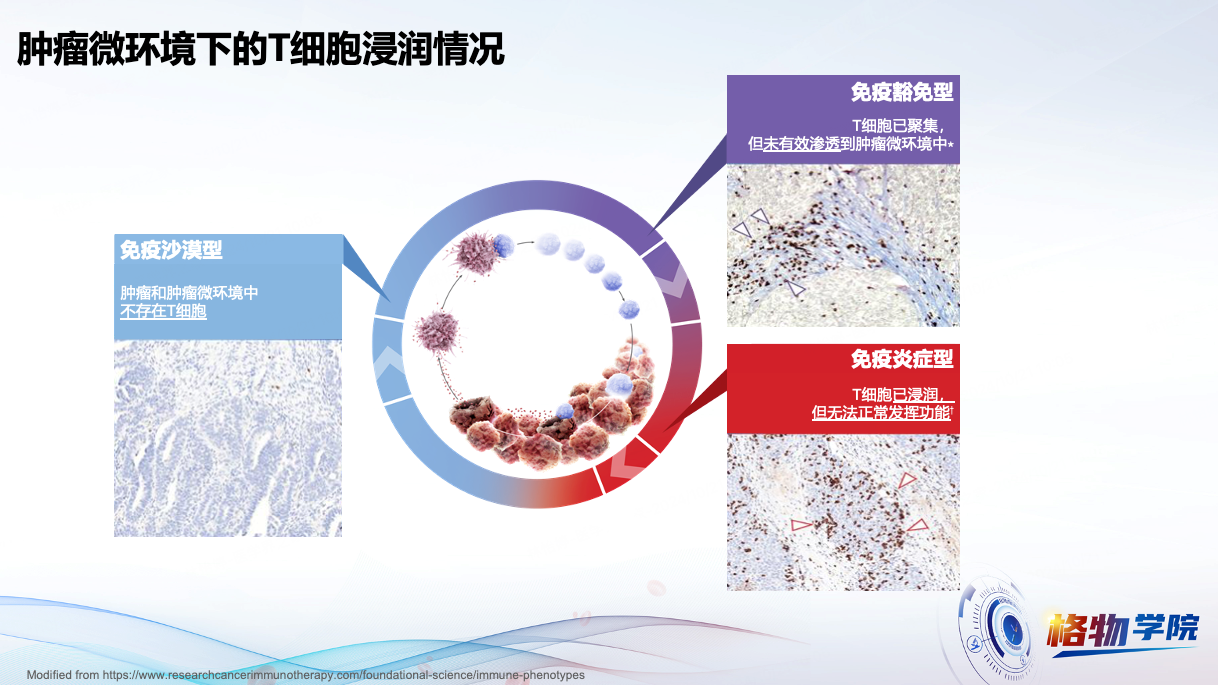 图2 肿瘤微环境下的T细胞浸润情况
图2 肿瘤微环境下的T细胞浸润情况
乘胜追击,共话T细胞介导的DLBCL肿瘤杀伤治疗
为了克服肿瘤的免疫逃逸,提高机体的抗肿瘤免疫力,科学家们开发了多种免疫治疗策略。基于T细胞的T细胞疗法,如嵌合抗原受体T细胞(CAR-T)疗法和T细胞重定向的双特异性抗体疗法,成为近年来的研究热点[5]。这些疗法通过直接激活并增强T细胞的抗肿瘤功能,旨在消除残余的肿瘤细胞,改善患者的预后。
CAR-T细胞疗法的应用
CAR-T细胞疗法是一种采用基因工程技术改造患者自身T细胞,使其表达特异性识别肿瘤抗原的嵌合受体,从而赋予T细胞直接识别并杀伤肿瘤细胞的能力[6]。在DLBCL的治疗中,针对CD19的CAR-T细胞产品,如tisagenlecleucel和axicabtagene ciloleucel[7],已获批用于复发/难治性(R/R)患者,部分患者取得了持久的完全缓解[7]。
然而,CAR-T细胞疗法也面临着诸多挑战:
首先,制备过程耗时且复杂,从细胞采集、体外扩增到输注,通常需要数周时间,且制造成本高昂[8];
其次,患者自身T细胞质量可能受到既往多线治疗的影响,导致制备失败的风险增加。据报道,tisagenlecleucel[9]和axicabtagene ciloleucel的制备失败率分别为9%和1%[10];
安全性方面,CAR-T细胞疗法可能引发严重的细胞因子释放综合征(CRS)和免疫效应细胞相关的神经毒性综合征(ICANS)。在临床试验中,3级及以上的CRS发生率高达13%-23%,严重的神经系统不良事件发生率为18%-31%,这些不良反应可能危及生命,需要专业的监测和处理[8];
最后,CAR-T细胞疗法的适用人群受到严格限制,广泛人群中的安全性和有效性数据仍需更多研究支持。
双特异性抗体疗法的崛起
T细胞重定向的双特异性抗体(BsAb)疗法逐渐引起关注。双特异性抗体具有同时结合T细胞表面CD3分子和肿瘤细胞特异性抗原(如CD19、CD20等)的能力,能够将T细胞“拉近”至肿瘤细胞周围,促进T细胞的激活和肿瘤细胞的杀伤[11, 12](图3)。
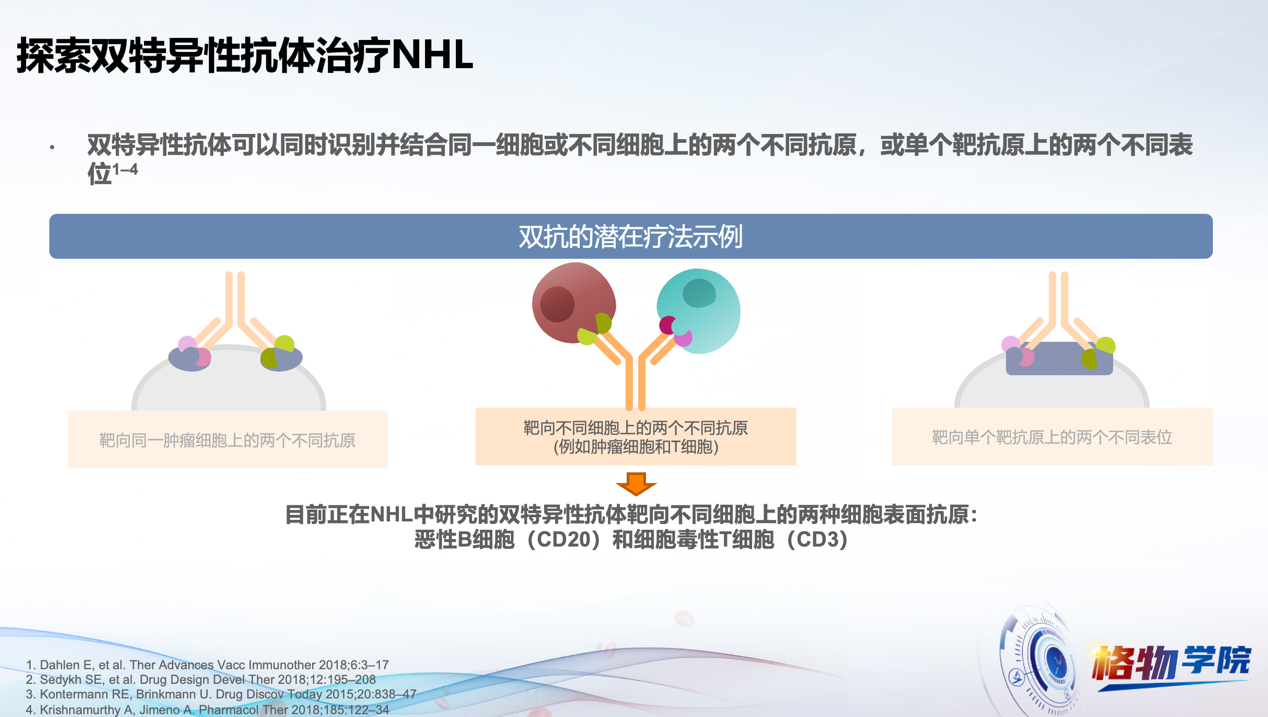
图3 探索双特异性抗体治疗NHL
Ⅰ 格菲妥单抗的作用机制与临床研究
格菲妥单抗(Glofitamab)是一种具有2:1结构的CD20xCD3双特异性抗体,含有两个结合CD20的片段和一个结合CD3的片段。与传统的1:1结构相比,2:1结构能够提高对肿瘤细胞的亲和力和选择性,从而增强T细胞介导的抗肿瘤活性[13]。
在临床研究中,格菲妥单抗在R/R DLBCL患者中展现了令人鼓舞的疗效。一项II期临床试验显示,格菲妥单抗单药治疗3L+DLBCL的疗效显著,可实现长期缓解[13, 14]:
客观缓解率(ORR)高达52%,完全缓解率(CR)达40%,中位达到CR时间仅需42天。中位完全缓解持续时间(mDoCR)为26.9个月,24个月DoCR率为55%;
不良反应方面,主要为1-2级的CRS,发生率较高,但大多可控且可逆,3级及以上CRS的发生率较低。神经毒性事件和其他严重不良反应较少见[13, 14]。
此外,Ⅲ期STRAGLO研究显示,格菲妥单抗与吉西他滨和奥沙利铂的联合方案(Glofit-GemOx)治疗2L+DLBCL,结果显示:
Glofit-GemOx治疗组中位总生存期(OS)25.5个月,相较于对照组(R-GemOx治疗组),中位OS延长近1倍(12.9个月 vs 25.5个月),显示出良好的安全性和疗效[15]。
Ⅱ 双特异性抗体疗法的优势
首先,双特异性抗体作为“即用即治”的药物,无需复杂的细胞制备过程,能够迅速应用于患者治疗,大大缩短了等待时间。其次,制造成本相对较低,具备更好的可及性。再次,双特异性抗体的剂量和给药方案可以灵活调整,不良反应更易于管理,安全性更高。
Ⅲ 莫妥珠单抗:双特异性抗体在滤泡性淋巴瘤治疗领域的新突破
除了格菲妥单抗,其他针对CD20的双特异性抗体也在DLBCL治疗中展现出潜力。莫妥珠单抗(Mosunetuzumab,Mosun)是1:1结构的靶向CD20×CD3的双特异性抗体,可重定向T细胞结合并清除B细胞,获美国食品药品监督管理局(FDA)批准用于治疗R/R滤泡性淋巴瘤(FL)[16]。已有数据显示,莫妥珠单抗在中国患者中的ORR高达88.2%,CR率为64.7%[17]。这些研究进一步证实了双特异性抗体在DLBCL治疗中的重要地位。
大有可为,解析T细胞疗法的未来方向
尽管T细胞疗法在DLBCL的治疗中取得了显著进展,仍有诸多挑战需要克服。未来的研究将重点聚焦于双特异性抗体的优化与创新,以进一步提升疗效和安全性(图4)。
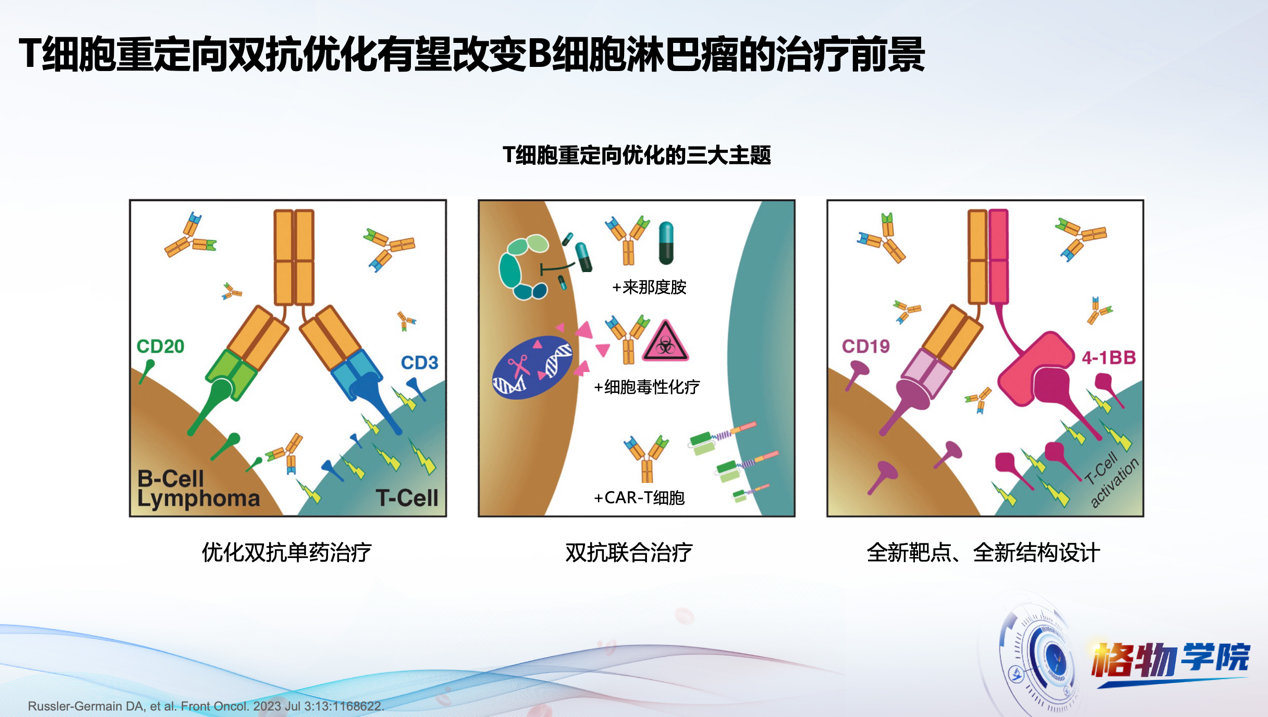 图4 双抗优化有望改变B细胞淋巴瘤的治疗前景
图4 双抗优化有望改变B细胞淋巴瘤的治疗前景
双特异性抗体的优化
Ⅰ 优化单药治疗效果
临床研究显示,靶向CD20xCD3的双特异性抗体在DLBCL治疗中效果显著且安全。优化抗体设计和给药策略有望提升单药疗效。同时,T细胞重定向治疗面临的关键问题是——确定治疗所需的药物量。早期临床试验需在药物效力的背景下,解决给药策略和疗程,以最大化疗效并减少不良反应。
Ⅱ 探索联合治疗策略
将双特异性抗体与其他疗法联合可增强疗效并克服耐药性。目前,格菲妥单抗和Pola-R-CHP的联合正在评估[18],同时Epcoritamab也在探索与化疗药物联合的潜力[19]。初步结果提示联合治疗可能提升抗肿瘤活性并改善预后。此外,双特异性抗体与免疫调节剂(如来那度胺)的联合可能进一步增强T细胞功能,未来研究将聚焦于确定最佳的联合策略。
Ⅲ 探索全新靶点和结构设计
除了现有的CD20xCD3双特异性抗体,研究者们正在开发针对全新靶点和具有独特结构设计的双特异性抗体。如靶向CD19和4-1BB的 RO7227166等, [20]。此外,还应探索双特异性抗体在特殊患者群体(如慢性乙型肝炎病毒感染者)中的安全性与有效性,以及其在一线治疗中的潜在应用,以提升患者的长期预后。
小结
在R/R DLBCL的治疗中,T细胞疗法,特别是CAR-T疗法和双抗疗法,已经成为近年来的重大突破。这些创新的治疗方法不仅为患者提供了新的治疗选择,而且也展现了其在进一步提高生存率和改善患者生活质量方面的潜力。
随着对T细胞疗法的深入研究和不断优化,预计其将在未来的临床实践中发挥更加重要的作用,持续的科研努力和临床试验将为这些治疗方法的进一步发展提供坚实的基础。我们期待着这些创新疗法能够为DLBCL患者带来更加精准和高效的治疗选择。
[1] MORSCHHAUSER F, LEUNG W, RAGHAVAN V, et al. Deciphering the Clinical Benefit of Pola-R-CHP versus R-CHOP in Different Genetic Subtypes Beyond Cell of Origin in the POLARIX Study [J]. Blood, 2023, 142: 3000.
[2] KUMAR B V, CONNORS T J, FARBER D L. Human T Cell Development, Localization, and Function throughout Life [J]. Immunity, 2018, 48(2): 202-13.
[3] SCOTT D W, GASCOYNE R D. The tumour microenvironment in B cell lymphomas [J]. Nature Reviews Cancer, 2014, 14(8): 517-34.
[4] MULDER W J M, OCHANDO J, JOOSTEN L A B, et al. Therapeutic targeting of trained immunity [J]. Nat Rev Drug Discov, 2019, 18(7): 553-66.
[5] BATLEVI C L, MATSUKI E, BRENTJENS R J, et al. Novel immunotherapies in lymphoid malignancies [J]. Nat Rev Clin Oncol, 2016, 13(1): 25-40.
[6] BAKER D J, ARANY Z, BAUR J A, et al. CAR T therapy beyond cancer: the evolution of a living drug [J]. Nature, 2023, 619(7971): 707-15.
[7] NEELAPU S S, JACOBSON C A, GHOBADI A, et al. Five-year follow-up of ZUMA-1 supports the curative potential of axicabtagene ciloleucel in refractory large B-cell lymphoma [J]. Blood, 2023, 141(19): 2307-15.
[8] PANG Y, HOU X, YANG C, et al. Advances on chimeric antigen receptor-modified T-cell therapy for oncotherapy [J]. Mol Cancer, 2018, 17(1): 91.
[9] SCHUSTER S J, TAM C S, BORCHMANN P, et al. Long-term clinical outcomes of tisagenlecleucel in patients with relapsed or refractory aggressive B-cell lymphomas (JULIET): a multicentre, open-label, single-arm, phase 2 study [J]. Lancet Oncol, 2021, 22(10): 1403-15.
[10] HARRISON R P, ZYLBERBERG E, ELLISON S, et al. Chimeric antigen receptor-T cell therapy manufacturing: modelling the effect of offshore production on aggregate cost of goods [J]. Cytotherapy, 2019, 21(2): 224-33.
[11] DAHLéN E, VEITONMäKI N, NORLéN P. Bispecific antibodies in cancer immunotherapy [J]. Ther Adv Vaccines Immunother, 2018, 6(1): 3-17.
[12] SEDYKH S E, PRINZ V V, BUNEVA V N, et al. Bispecific antibodies: design, therapy, perspectives [J]. Drug Des Devel Ther, 2018, 12: 195-208.
[13] DICKINSON M J, CARLO-STELLA C, MORSCHHAUSER F, et al. Glofitamab for Relapsed or Refractory Diffuse Large B-Cell Lymphoma [J]. N Engl J Med, 2022, 387(24): 2220-31.
[14] HUTCHINGS M, CARLO-STELLA C, MORSCHHAUSER F, et al. Glofitamab Monotherapy in Relapsed or Refractory Large B-Cell Lymphoma: Extended Follow-Up from a Pivotal Phase II Study and Subgroup Analyses in Patients with Prior Chimeric Antigen Receptor T-Cell Therapy and by Baseline Total Metabolic Tumor Volume [J]. Blood, 2023, 142: 433.
[15] ABRAMSON J K M, HERTZBERG M, ET AL. Glofitamab plus gemcitabine and oxaliplatin for relapsed/refractory diffuse large B-cell lymphoma: Results of a global randomized phase III trial (STARGLO) [J]. EHA 2024 Congress, 2024, Abstract LB3438. Presented June 15.
[16] LOPEDOTE P, SHADMAN M. Targeted Treatment of Relapsed or Refractory Follicular Lymphoma: Focus on the Therapeutic Potential of Mosunetuzumab [J]. Cancer Manag Res, 2023, 15: 257-64.
[17] LI Z Z, SHIYONG2; LIU, YANYAN3; ZHANG, LILING4; LI, DONGHANG5; LIAO, MICHAEL Z.6; ZHOU, MINGZHU5; ZHANG, YE5; WEI, MICHAEL C.6; CAO, JUNNING7*. Safety and efficacy of mosunetuzumab monotherapy in Chinese patients with relapsed or refractory follicular lymphoma [J]. 2024 CSCO, 2024.
[18] TOPP M S, TANI M, DICKINSON M, et al. Glofitamab Plus R-CHOP Induces High Response Rates with a Manageable Safety Profile in Patients with Previously Untreated Diffuse Large B-Cell Lymphoma (DLBCL): A 12-Month Analysis from a Phase Ib Study [J]. Blood, 2023, 142(Supplement 1): 3085-.
[19] KARIMI Y, THIEBLEMONT C, GHESQUIERES H, et al. Extended follow-up results beyond 2.5 years from the pivotal NHL-1 EPCORE trial: Subcutaneous epcoritamab monotherapy in patients with relapsed/refractory large B-cell lymphoma (R/R LBCL) [J]. Journal of Clinical Oncology, 2024, 42(16_suppl): 7039-.
[20] HUTCHINGS M, CARLO-STELLA C, GRITTI G, et al. CD19 4-1BBL (RO7227166) a Novel Costimulatory Bispecific Antibody Can be Safely Combined with the T-Cell-Engaging Bispecific Antibody Glofitamab in Relapsed or Refractory B-Cell Non-Hodgkin Lymphoma [J]. Blood, 2022, 140(Supplement 1): 9461-3.
[21] RUSSLER-GERMAIN D A, GHOBADI A. T-cell redirecting therapies for B-cell non-Hodgkin lymphoma: recent progress and future directions [J]. Front Oncol, 2023, 13: 1168622.
往期精彩回顾:
【1】【格物学院|第一期】张薇教授:从分子结构和作用机制出发,探讨双抗在淋巴瘤治疗中如何发光发热?
【2】【格物学院|第二期】景红梅教授:CD20/CD3 双抗在3L+ DLBCL的应用——全球及中国人群最新数据分享
【3】【格物学院|第三期】许彭鹏教授:NCCN指南更新解读——支持在DLBCL中使用格菲妥单抗
【4】【格物学院|第四期】范磊教授:CD20/CD3联合治疗在2L+DLBCL的应用、探索与思考
【5】【格物学院|第五期】赵东陆教授:格菲妥单抗治疗弥漫大B细胞淋巴瘤临床用药指导原则
点击下方,即可获得讲课幻灯

排版编辑:肿瘤资讯-邓文普











 苏公网安备32059002004080号
苏公网安备32059002004080号


