随着转移性结直肠癌治疗的不断进步,转化治疗作为一种将不可切除的转移性肿瘤转化为可切除状态的策略,得到了广泛的认可。今年以来,针对晚期肠癌靶向联合化疗的转化治疗迎来多项研究进展,特别是在RAS野生型患者中,抗EGFR单抗联合化疗的应用已成为转化治疗的关键手段,引发了关注和讨论。【爱肠学院】特邀西安市第三医院王童非教授对转移性结直肠癌转化治疗新近发表相关研究进行梳理与解读。
专家介绍
肿瘤学博士 副主任医师 硕士研究生导师
中国抗癌协会青年理事
CACA指南胃肠保护篇 执笔人
中国抗癌协会康复分会 副秘书长
中国抗癌协会头颈整合康复专委会 常务委员
中国临床肿瘤学会青年专家委员会 委员
陕西省抗癌协会转化医学专委会 常务委员
陕西省抗癌协会肿瘤个体化治疗专委会 常务委员
西安市肿瘤医学质量控制中心 副主任委员
肠癌局限性肝转移(CLM)的标准转化治疗方案包括针对左半RAS野生型患者的双药方案联合抗EGFR单抗以及针对右半或RAS/BRAF突变亚组的三药FOLFOXIRI(氟尿嘧啶、亚叶酸、奥沙利铂和伊立替康)联合贝伐珠单抗。多项临床试验表明,与双药方案(FOLFOX或FOLFIRI)相比,三药化疗方案(氟尿嘧啶/亚叶酸、伊立替康和奥沙利铂)可为mCRC患者带来更高的缓解率和切除率。此外,对于左半RAS/BRAF野生型mCRC,将抗EGFR药物(如西妥昔单抗)纳入化疗方案可以增强疗效。最近的指南推荐,对于初始不可切除或边缘可切除的CLM患者,采用强化方案以诱导更早和更深的肿瘤缩小是优选方案。因此,三药化疗联合抗EGFR药物可能是不可切除左半RAS/BRAF野生型mCRC患者的可行转化治疗方案。
2024FOLFOXIRI联合抗EGFR单抗转化研究概要
近期,国内中国医学科学院肿瘤医院发表了一项FOLFOXIRI联合西妥昔单抗作为不可切除的RAS/BRAF野生型左半结直肠癌局限性肝转移转化治疗的前瞻性双中心II期试验[1],以探讨FOLFOXIRI联合西妥昔单抗方案作为转化治疗在不可切除的RAS/BRAF野生型结直肠癌局限性肝转移患者中的疗效和安全性,主要终点是无疾病证据(NED)。次要终点包括客观缓解率(ORR)、疾病控制率(DCR)、早期肿瘤缩小(ETS)、反应深度(DpR)、无复发生存期(RFS)、无进展生存期(PFS)、总生存期(OS)和安全性。
在2019年10月至2021年10月期间,研究共入组15例患者。所有入组患者接受改良的FOLFOXIRI联合西妥昔单抗方案作为转化治疗: 西妥昔单抗用法用量为第1天500 mg/m2;改良的FOLFOXIRI包括伊立替康150 mg/m2,奥沙利铂85 mg/m2,氟尿嘧啶2400 mg/m2持续输注46小时。治疗每2周重复一次,直到疾病进展、不耐受毒性或达到可切除状态,或最多12个周期。对于严重药物相关毒性(≥3级非血液学或4级血液学毒性)允许减量。每3个周期评估一次疗效和可切除性。评估后可根治性切除的患者将接受手术。转移灶根治性切除后,建议继续化疗作为辅助治疗,总共12个围手术期周期。根据每个患者术后的身体状况,术后可进行维持治疗。对于在12个周期的诱导治疗后未达到NED的患者,继续使用氟尿嘧啶和西妥昔单抗进行维持治疗,直到疾病进展。
研究结果显示,9例(60%)患者达成NED。ORR为92.9%,DCR为100%。中位RFS为9个月(95% CI: 0~20.7个月)。中位PFS为13.0个月(95% CI: 5.7~20.5个月),中位OS未达到。最常见的3~4级不良事件为中性粒细胞减少(20%)、外周神经毒性(13.3%)、腹泻(6.7%)和痤疮样皮疹(6.7%)。
表1: 疗效结果
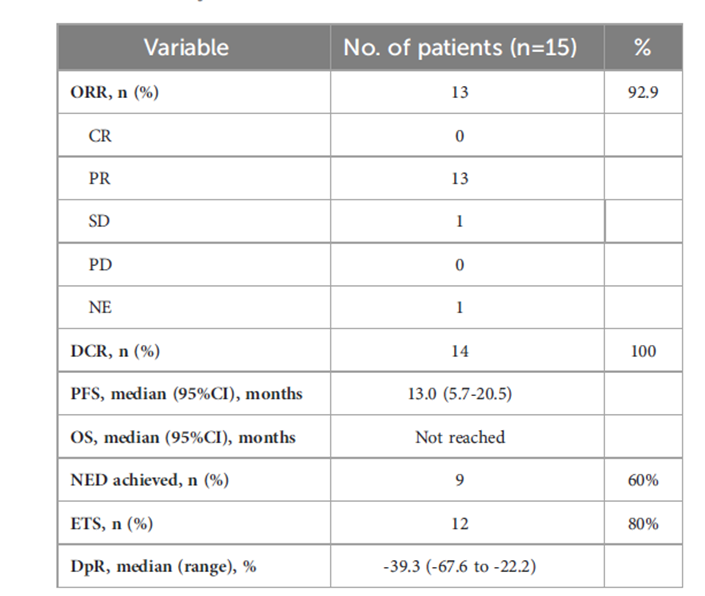
总体来说,FOLFOXIRI联合西妥昔单抗方案在不可切除的左侧RAS/BRAF野生型结直肠癌肝限性转移患者中表现出可耐受的毒性和有前景的抗肿瘤活性,其作为转化治疗方案值得进一步研究。
研究解读
转化治疗对于mCRC患者,尤其是CLM患者,是必要的。CLM与其他mCRC存在异质性,具有不同的生物学行为。多项研究已经证实,CLM的R0切除可以显著延长生存时间,这凸显了为CLM患者设计最佳转化治疗的重要性。在这项研究中,NED状态的达成率为60%。达到NED状态的患者中位PFS较未达到NED状态的患者更长,且其中位OS尚未达到。此双中心初步试验获得了良好的DpR和ETS,表明三药化疗联合西妥昔单抗可能成为CLM患者的优选转化治疗方案。研究显示肝转移灶的数量与预后密切相关,肝转移灶少于5个的患者全部(100%)达到NED状态。此外,研究还提出巨大肿块型肝转移灶的患者较双叶肝脏中多发性分布的转移灶患者可能更适合强化治疗,且预后较好。未来需要进一步研究以筛选适合该方案的患者。
FOLFOXIRI联合抗EGFR抗体方案是否可作为RAS/BRAF野生型mCRC患者的初始治疗方案存在争议的原因是根据TRIPLETE研究临床试验的阴性结果。未经过选择的患者群体可能是TRIPLETE阴性结果的原因之一。目前仍有多项临床试验正在进行,旨在继续探索该方案的临床价值。相同的三药联合抗EGFR单抗转化策略是李宇红教授在中国进行的TRICE研究,为这一领域提供了新的临床证据和应用指导。
2024TRICE转化研究全文发表更新
TRICE研究[2]是一项多中心、随机对照III期临床试验,旨在评估西妥昔单抗联合FOLFOXIRI(奥沙利铂、伊立替康和氟尿嘧啶)方案对比西妥昔单抗联合FOLFOX(奥沙利铂和氟尿嘧啶)方案在KRAS野生型mCRC患者中的疗效。该研究纳入146例患者,三药组72例,两药组74例;三药组的DpR显著高于两药组(59.6% vs 55.0%, P=0.039),转化为可切除的患者比例也大幅增加。
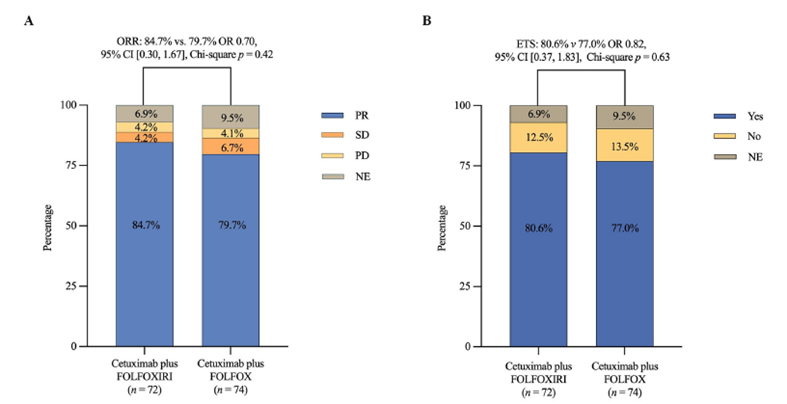
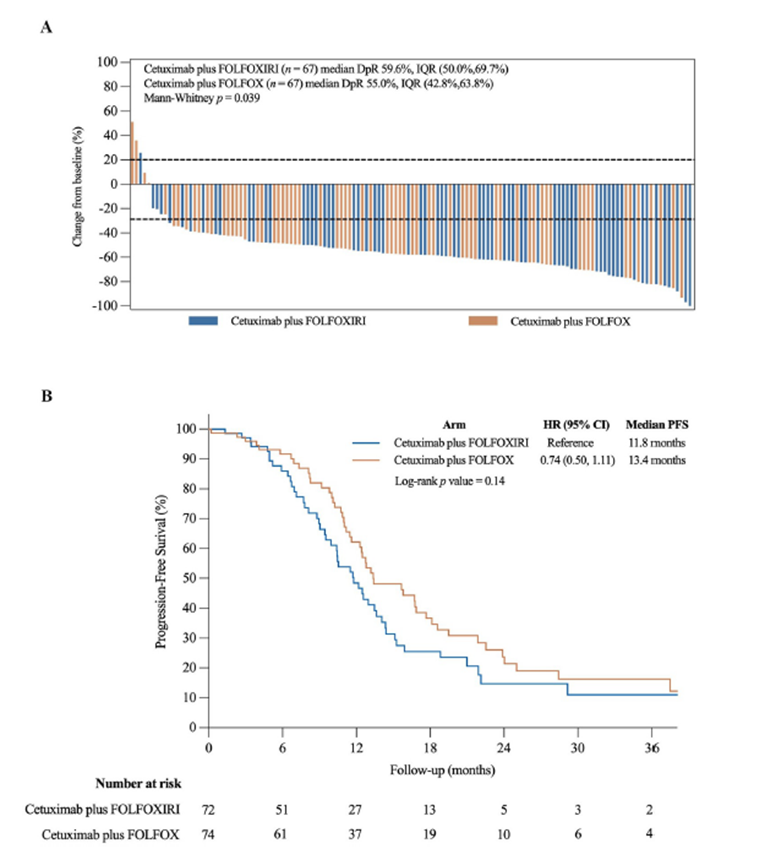
总体而言,两组的ORR数值均较高,但未取得统计学上的显著差异。三药组相比两药组的DpR有统计学差异,但没有转化为R0切除率和PFS的获益,目前该研究的OS数据尚不成熟;三药组部分不良事件发生率更高。从目前的研究结果来看,对于RAS野生型初始不可手术切除CRLM患者,仍然支持西妥昔单抗联合两药化疗是标准的一线转化治疗方案。
研究解读
TRICE研究是首项针对比较三药化疗和两药化疗联合西妥昔单抗用于转化治疗的研究。首先需要注意的是:该结果再次证实了在RAS/BRAF野生型mCRC患者的转化治疗中,西妥昔单抗联合不同强度化疗方案均能取得很高的ORR、DpR和ETS,这也与国内外权威指南的高级别推荐一致。
该研究共纳入右半患者19例(13%),总体ORR高达89.5%,ETS为73.7%,从数值上看与左半患者无明显差异。转化率(36.8%)稍低于左半患者,这可能与右半肿瘤的生物学特性相关。既往亦有几项研究支持抗EGFR单抗用于右半患者的转化治疗。结合此前PARADIGM研究、FIRE-3研究的后续生物标志物分析结果,相信未来可以在右半肠癌中探索更多可以从抗EGFR单抗中获益的人群。
另外,虽然该研究是阴性结果,但是并不能完全否定三药化疗联合西妥昔单抗在转化治疗中应用价值,主要基于以下方面:
1. TRICE研究的统计学假设是主要终点ORR从两药组的60%提高到三药组的80%。从研究结果来看,三药组和两药组的ORR分别达到了84.7%和79.7%,两药组的ORR远超预设,三药组也达到了预期。
2. 在DpR结果上,TRICE研究中三药组显著高于两药组。结合此前几项研究均展示出在RAS/BRAF野生型患者中,原发灶位于左半结肠的患者使用三药化疗联合西妥昔单抗相较于联合贝伐珠单抗可以获得更好的DpR。文章的讨论部分也特别提到,有研究证明更深的肿瘤缓解与更长的OS之间存在潜在相关性。因此,需要等待更长的随访时间待OS结果成熟,以进一步明确三药组是否会在OS上有获益。
3. TRICE研究中三药组表现与其他研究结果保持一致,即ERBIRINOX研究、MACBETH研究、VOLFI研究、FOCULM研究等均展示出显著获益,可以给予患者更好的转化机会。也进一步展示了该方案应用于中国人群的可行性和有效性。三药方案对于患者重新获得手术机会达到NED至关重要,对于单个肿瘤直径较大,转移肿瘤数目较多的患者可以积极考虑使用三药方案。
基于TRICE研究在去年ESMO年会中报告的前期结果,2024年CSCO指南进行更新:在初始不可切除转移性结肠癌的治疗(潜在可切除)诊疗方案中,对于“适合强烈治疗(RAS和BRAF均野生型)”的患者,III级推荐删除“FOLFOXIRI+西妥昔单抗”的推荐,这也引起了广泛关注与讨论。此次全文对数据的披露更加全面,对于研究结果的剖析也更加深入。
临床实践中的应用体会
在临床实践中,我们发现,对于KRAS野生型mCRC患者,西妥昔单抗联合多药化疗不仅能够有效缩小肿瘤,使更多患者达到手术切除的标准,还能通过精准的靶向治疗减少转移灶的复发风险,在个体化治疗的价值上转化治疗的效果尤为显著。在临床操作中,对于年轻、症状明显、原发肿瘤位于右半结肠及以最大程度缩瘤为目标的患者,根据患者的基因背景(如KRAS状态)和肿瘤负荷进行个体化转化治疗。
但是,真实世界的应用仍存挑战:尽管TRICE研究显示了显著的疗效,但在实际操作中,我们还需考虑患者的耐受性和并发症。对一些高龄或伴有严重合并症的患者,可能需要调整化疗剂量或采取分阶段治疗策略,以确保患者能够顺利完成整个治疗过程。
此外,多学科合作的重要性也很大,在转化治疗中,多学科团队(MDT)合作至关重要。肿瘤内科医生、外科医生、放疗医生等应紧密合作,共同评估患者的手术适应症和治疗方案,确保治疗的连续性和效果最大化。
随着更多高水平研究的开展,如TRICE研究的进一步结果,我们期待看到更多关于西妥昔单抗联合化疗在mCRC转化治疗中的新发现。正在进行的TRUST研究“初始不可切除RAS/BRAF野生型结直肠癌肝转移患者的转化治疗:mFOLFOXIRI +西妥昔单抗对比mFOLFOXIRI +贝伐珠单抗”(NCT04687631)[3],预期也即将入组完成,期待后续数据为我们提供更多的临床指导,并帮助优化治疗策略,最大化患者的生存利益。在未来的实践中,结合真实世界数据和临床研究结果,将是进一步提高转化治疗成功率的关键。随着新药物和新疗法的不断发展,转化治疗的前景将更加广阔,期待更多患者能够从中获益。
1. Yang W, Chen D, Niu Y et al. FOLFOXIRI plus cetuximab as conversion therapy for unresectable RAS/BRAF wild-type left-sided colorectal cancer with liver-limited metastases: a prospective dual-center pilot study. Front Oncol. 2024 Apr 4;14:1375906
2. Wang DS, Ren C, Li SS et al. Cetuximab plus FOLFOXIRI versus cetuximab plus FOLFOX as conversion regimen in RAS/BRAF wild-type patients with initially unresectable colorectal liver metastases (TRICE trial): A randomized controlled trial. PLoS Med. 2024 May 10;21(5):e1004389.
3. https://clinicaltrials.gov/study/NCT04687631
排版编辑:Crystal











 苏公网安备32059002004080号
苏公网安备32059002004080号


