老年女性患者,既往“高血压”病史,诊断“小细胞肺癌伴脑、脑膜、肺、左侧肾上腺、淋巴结多发转移”,PS评分1分。既往分别应用各联合方案治疗,持续时间短暂。多线耐药后使用“卡度尼利单抗联合鞘注化疗+放疗”治疗,4周期达PR,颅内转移体积显著减小,肺转移和肾上腺转移消失,未见明显不良反应,目前PFS已达15个月,仍持续治疗中。
病例分享专家
马利新
吉林省医学会肿瘤放射治疗学分会青年委员
吉林省医学会肿瘤立体定向放疗学组组员
吉林省研究型医学会放疗专委会委员
研究方向:腹部恶性肿瘤的精准放疗
病史回顾
患者
都某某,女,60岁
以“CT提示左肺上叶后段肿物”为主诉入院。
病例特点
患者2021年1月入院,入院前1年无明显诱因出现后背部疼痛,近3个月加重伴有咳嗽,查CT提示“左肺上叶后段肿物,大小约2.4cm*2.3cm;左肺门见肿大淋巴结影”。既往“高血压”病史10余年,血压最高160/110mmHg,口服“拜新同”血压控制约130/80mmHg。否认吸烟史,家族史无特殊。PS评分1分。
辅助检查
(2021-01-07)肺部多排CT:左肺上叶后段周围型肺癌,伴远端少许阻塞性炎症及左肺门淋巴结转移,大小约2.4cm*2.3cm,右肺中叶及双肺下叶少许慢性炎症,胸主动脉、冠状动脉硬化。
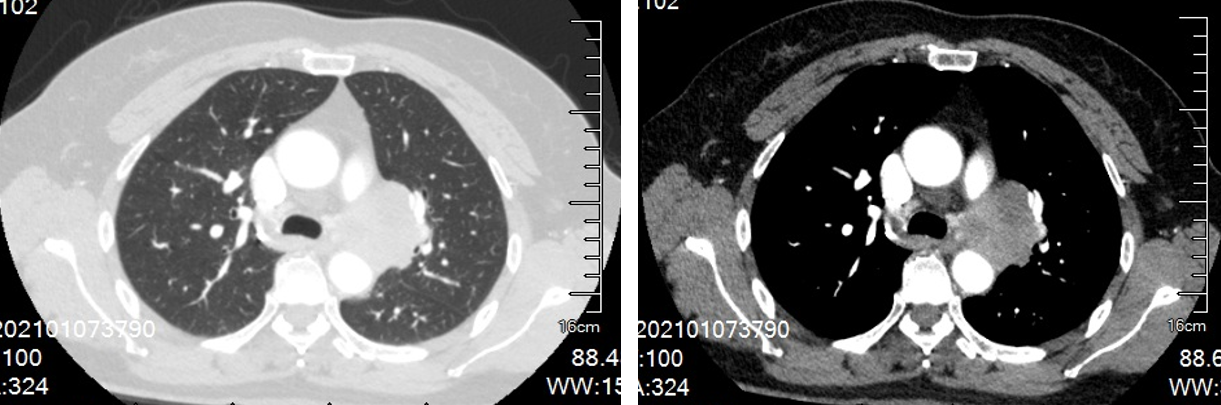
(2021-01-12)支气管镜:超声支气管镜可探及纵隔多组肿大淋巴结,其中以10L组淋巴结及4L组增大明显,最大者直径约2.99cm*2.09cm。
活检病理:(10L组淋巴结)形态结合免疫组化,符合小细胞癌。
免疫组化:CK (+)、CK7(-)、CK20(-)、CEA(-)、villin(-)、P53 (+)散在、Ki67 (+)、Syn (+)、CgA (-)、CD56 (+)、CD45(-)、E-cad(+)、P63(-)、CK5/6 (-)、P40 (-)、WT-1 (-)、CR (-)、Vim (-)、TTF-1(+)、Napsin-A (-)。
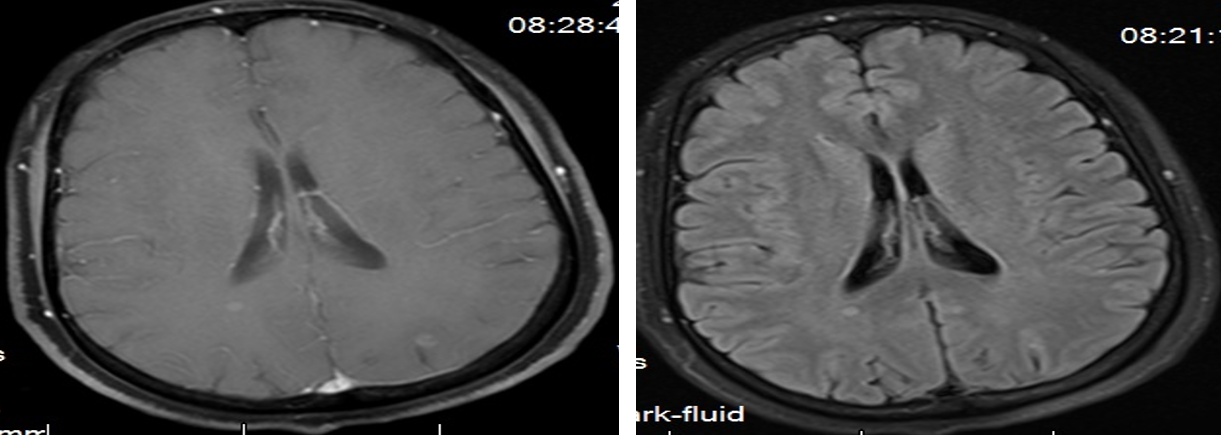
(2021-01-17)磁共振头部平扫:右侧脑室后角旁左侧顶叶类圆形等及稍长T1、稍长T2信号,大小约0.4-0.6cm,左侧额叶见小节状长T1长T2信号,大小约0.5cm。右侧脑室后角旁、左侧顶叶异常信号,考虑转移瘤可能。
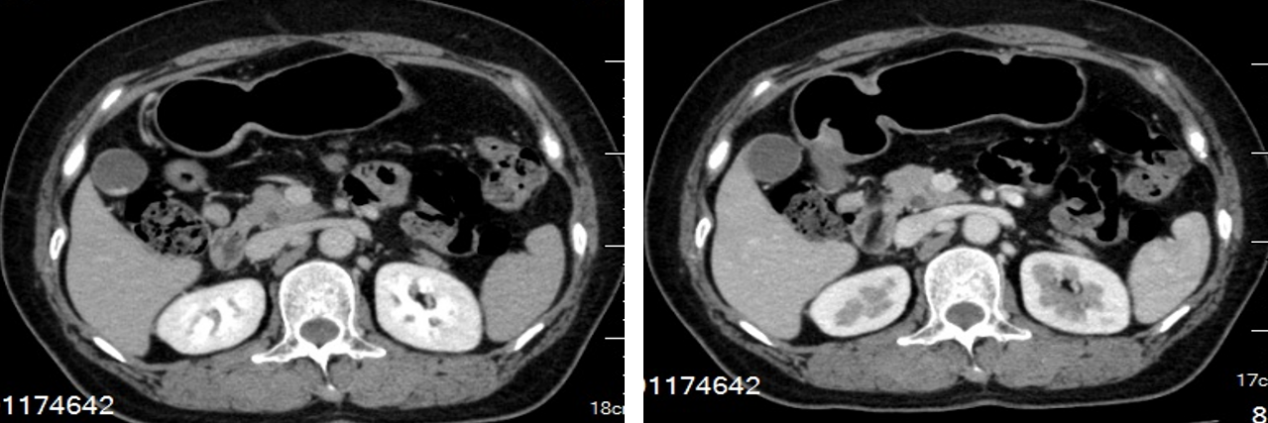
(2021-1-17)肝胆脾胰多排CT:肝左外叶见2枚类圆形异常密度影,大小约0.7-0.9cm,幽门下方、胰头旁结节影,考虑肿大淋巴结。
诊断
1、小细胞肺癌(广泛期)
2、腹腔淋巴结转移
3、脑转移
治疗
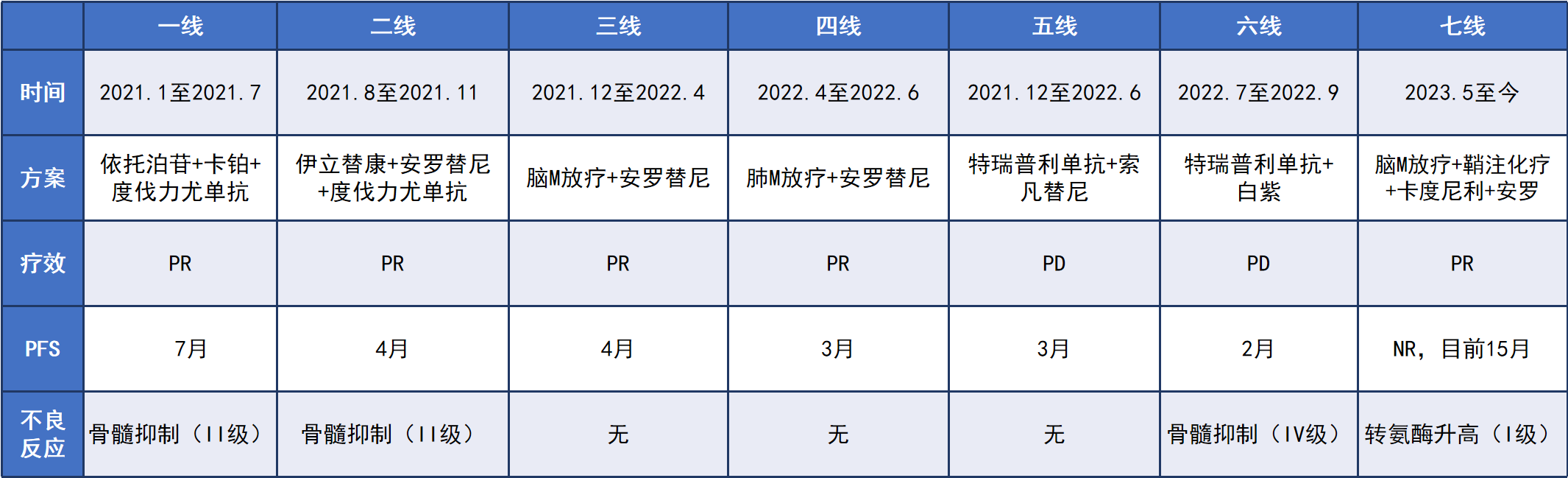
一线治疗
2021年01月起:予“度伐利尤单抗+依托泊苷+卡铂”治疗。
第2周期、第6周期治疗后,疗效评价为PR;
免疫单药维持治疗2周期后,复查提示原发灶及脑转移病灶进展,疗效评价为PD。
一线PFS为7个月。不良反应:骨髓抑制(Ⅱ级)
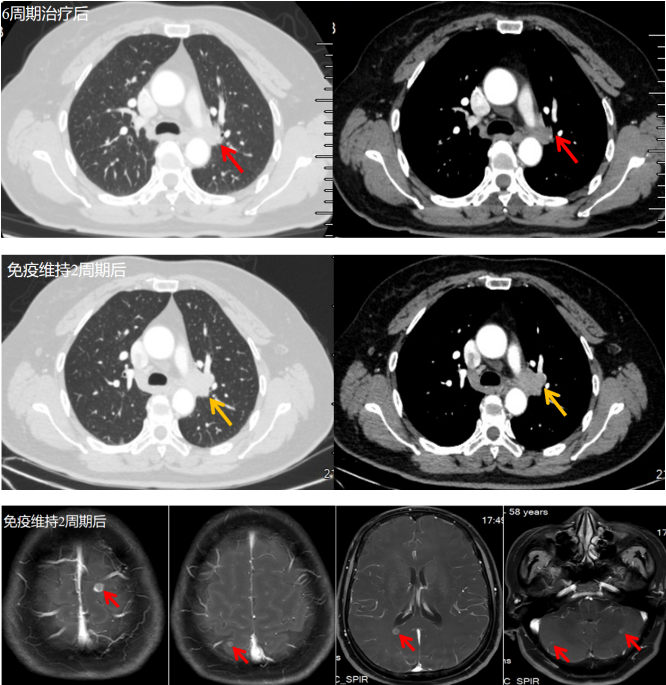
二线治疗
2021年08月起:予“度伐利尤单抗+安罗替尼+伊立替康”治疗。
2周期后,疗效评价为PR。
2021年12月:第4周期治疗后,复查提示脑转移病灶进展。
二线PFS为4个月。不良反应:骨髓抑制(Ⅱ级)
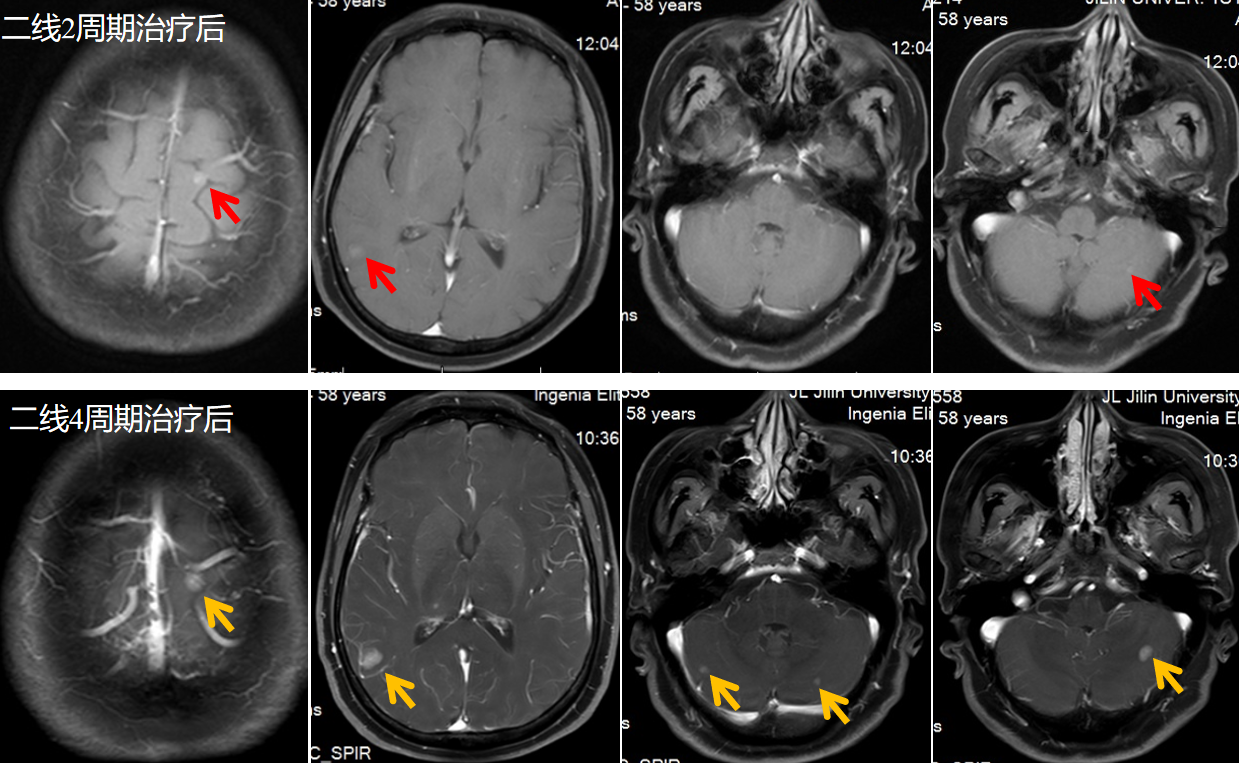
三线治疗
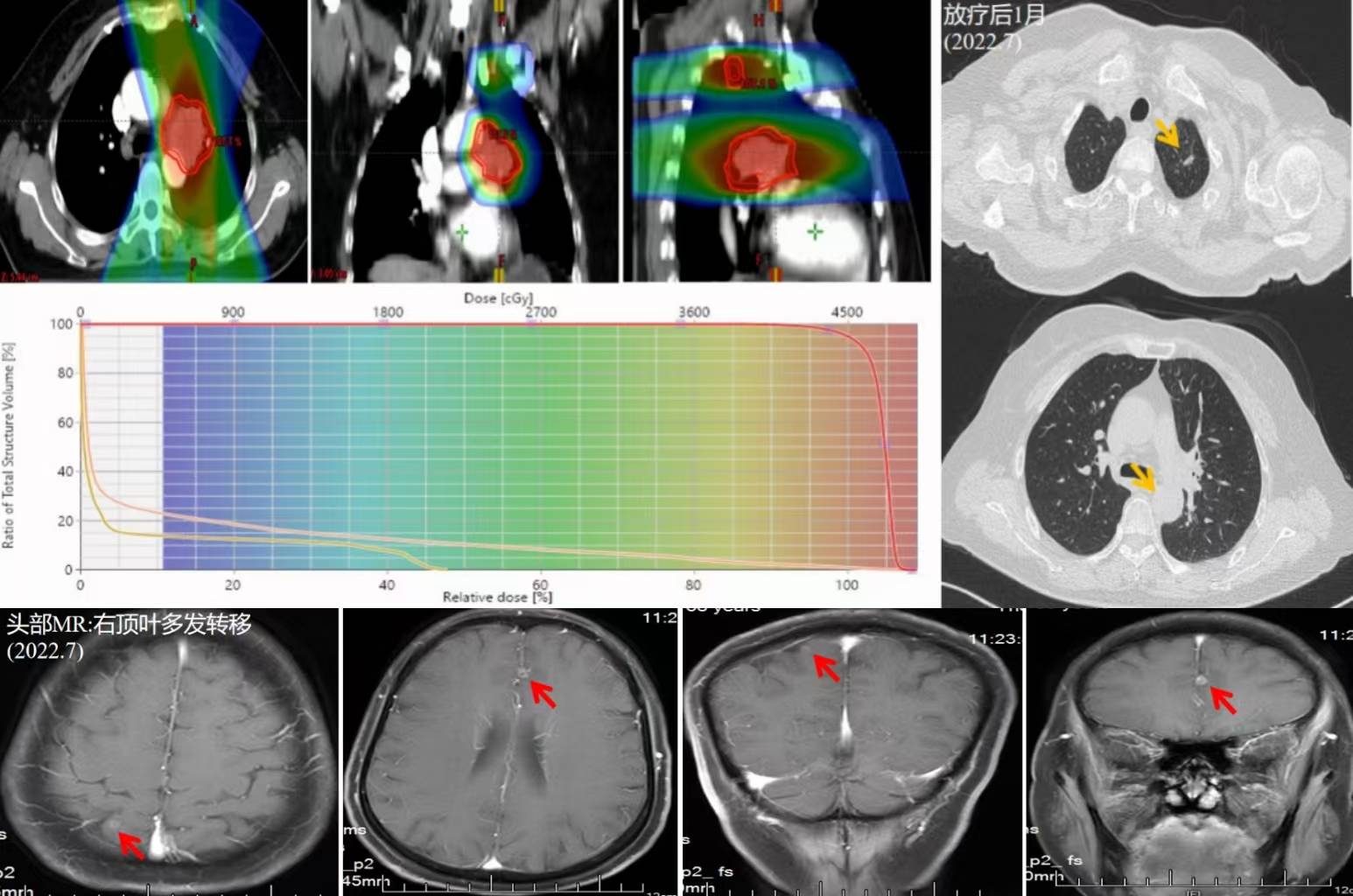
2021年12月起:予“安罗替尼+脑转移灶放疗”方案,全脑剂量:30Gy/15f,脑转移灶:45Gy/15f。脑脊液脱落细胞学:阴性。
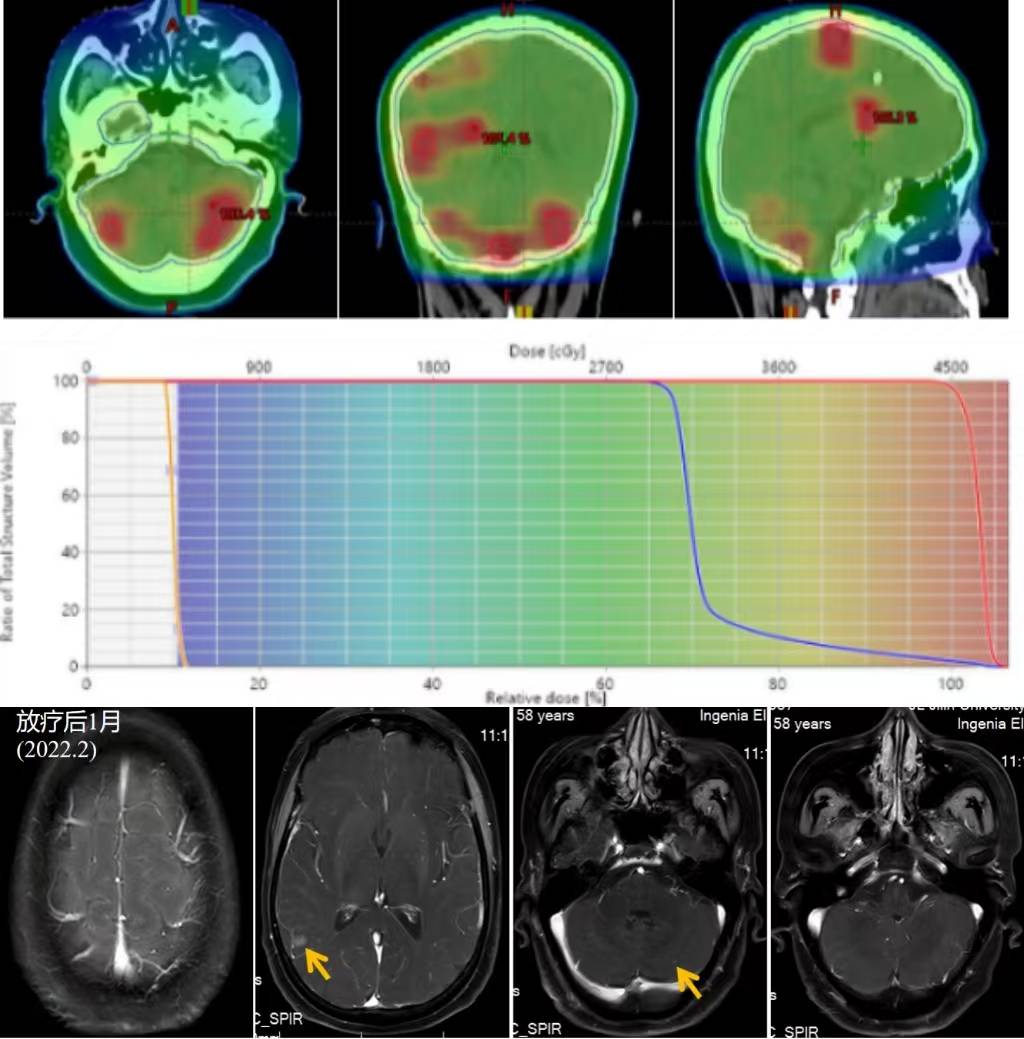
2022年04月:患者出现胸痛、痰中带血。复查CT提示肺部病灶较前进展。
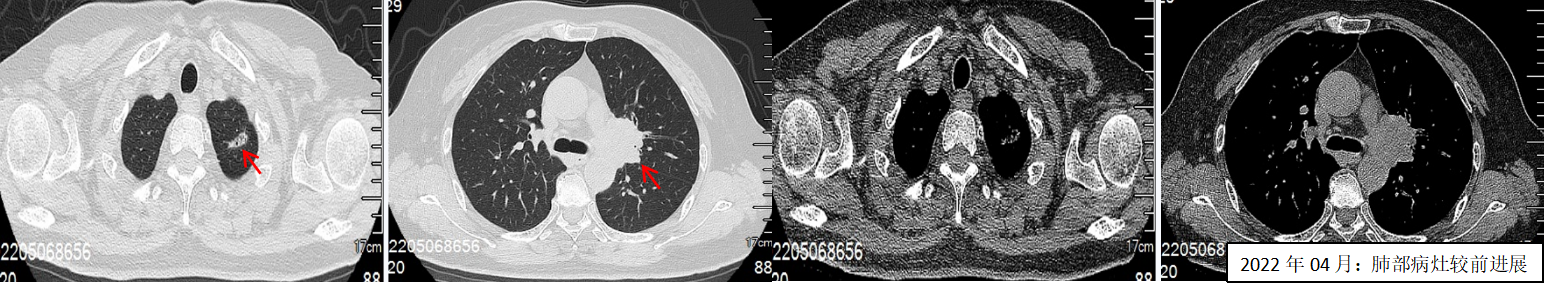
三线PFS为4个月。
四线治疗
2022年05月:予“安罗替尼+肺部病灶放疗”方案治疗,原发灶、肺门及纵隔转移淋巴结:45Gy/15f。
2022年07月:头部MR示右顶叶多发转移,出现新发脑部转移灶,疗效评价为PD。
四线PFS为3个月。
五线治疗
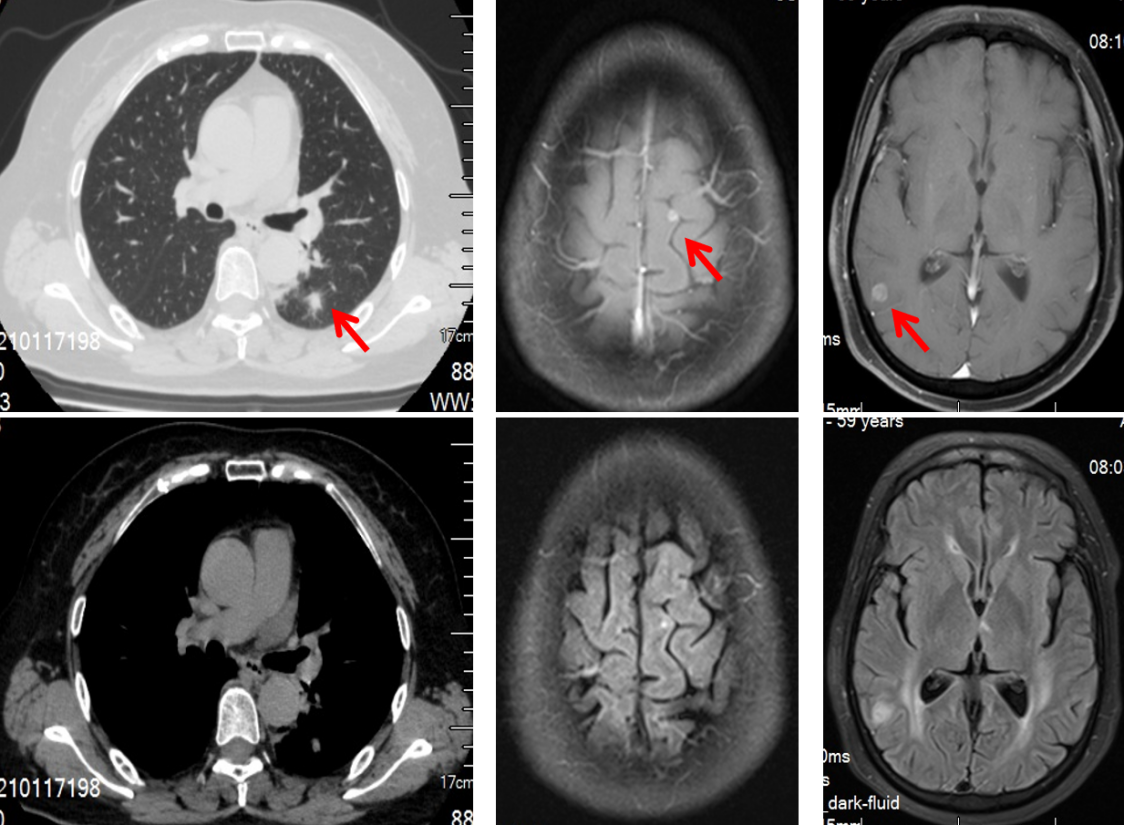
2022年07月起:予“特瑞普利单抗+索凡替尼”治疗。
2022年10月:第4周期治疗后,复查提示原发灶及脑转移灶皆进展,疗效评价为PD。
五线PFS为3个月。
六线治疗
2022年10月起:予“特瑞普利单抗+白蛋白紫杉醇”治疗,2周期后疗效评估为SD,4周期后疗效评估为PD。六线PFS为2个月。
期间患者出现骨髓抑制(Ⅳ级),予对症处理。
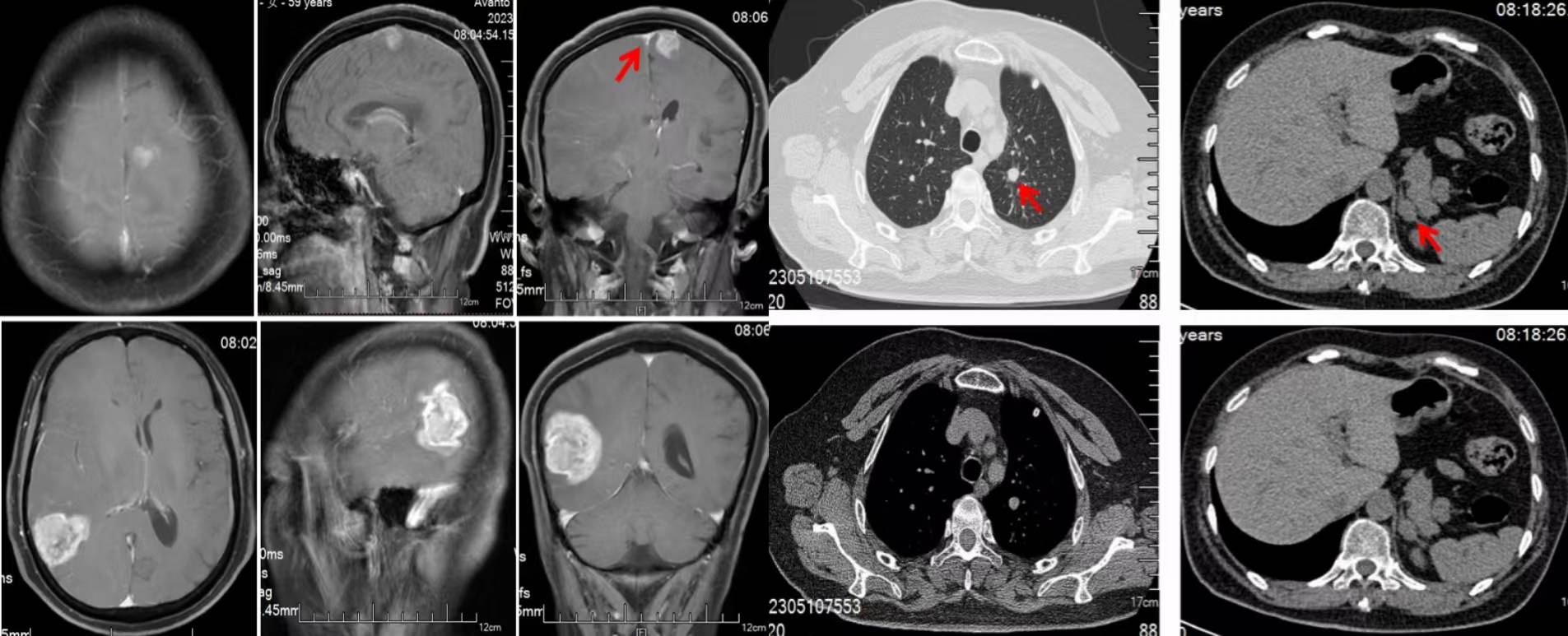
2023年05月:患者诉头痛、肢体活动不灵活。复查MR提示左侧额叶、右侧顶叶占位;脑脊液脱落细胞学:找到癌细胞;CT提示肺部病灶较前进展,肾上腺出现新发转移灶。
七线治疗
患者病情进展迅速,患者及家属治疗意愿积极。
2023年05月起:予“卡度尼利单抗+甲氨蝶呤鞘内化疗+局部放疗”治疗,脑转移灶:45Gy/15f。
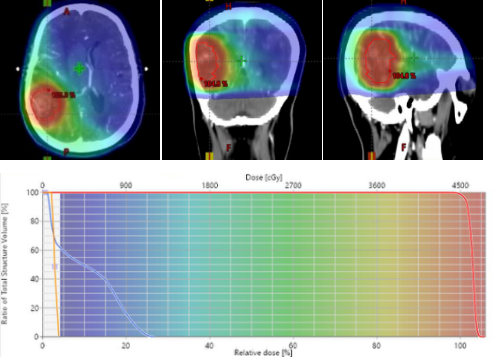
2023年07月:治疗4周期后,患者头痛及肢体活动不灵症状消失,脑转移体积显著减小,肺转移和肾上腺转移消失。疗效评价为PR。
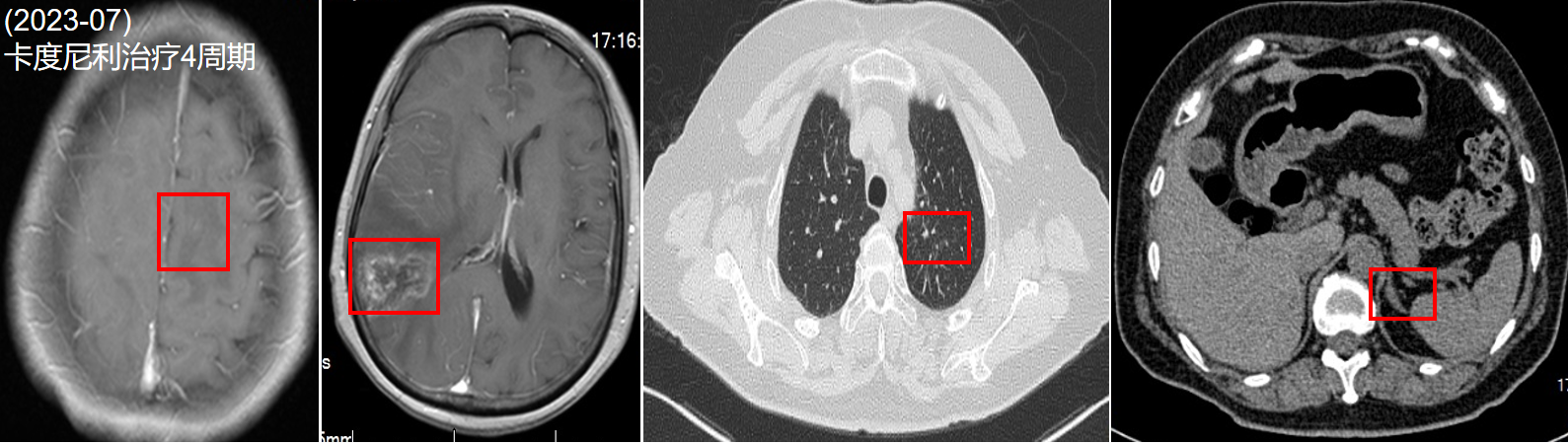
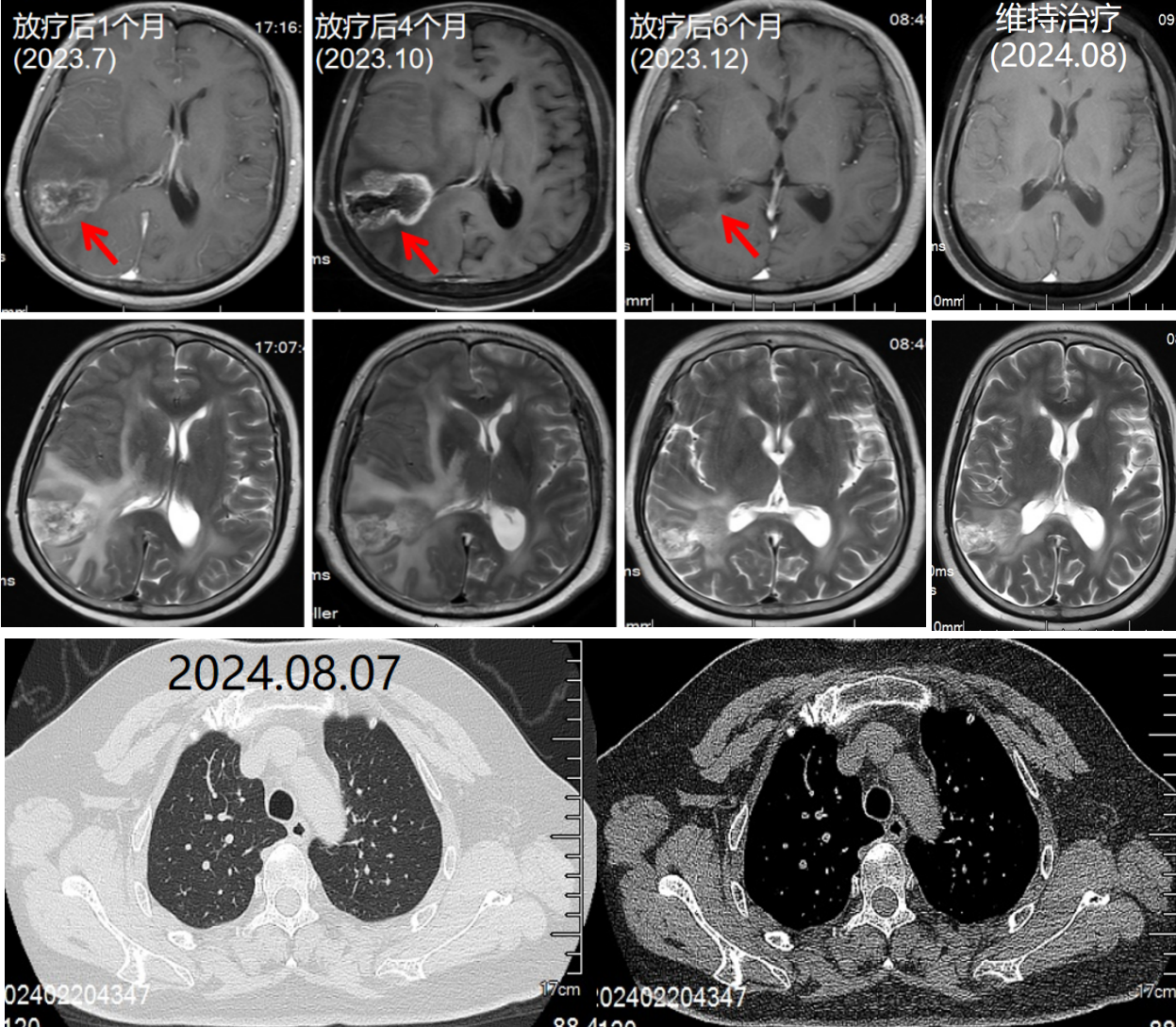
第2次放疗后右侧顶叶出现异常信号,且持续增大,考虑放射性脑损伤(DWI低信号,ADC高信号);予加用“安罗替尼”治疗,右顶叶异常信号明显减轻,肢体活动不灵症状消失。余未出现明显不良反应。继续予“卡度尼利单抗+安罗替尼”维持治疗。
2024年08月:复查颅脑MR示“符合左侧额叶、右侧颞顶叶转移瘤治疗后,较2024-06-11前片左侧额叶病灶略缩小”,复查肺部CT示“左肺上叶纵隔旁高密度影,对比2024-08-10前片相仿”。
继续该方案治疗,PFS已超过15个月。不良反应:转氨酶升高(Ⅰ级)
病例点评专家
董丽华
放射肿瘤治疗吉林省重点实验室负责人
中华医学会放射肿瘤治疗学分会委员
中国医师协会放射肿瘤治疗医师委员会委员
中国抗癌协会肿瘤放射治疗专业委员会委员
近5年,以第一作者或责任作者发表SCI论文和综述30余篇,获得国家自然科学基金面上项目2项、“十三五”国家重点研发计划项目子课题1项、省部级项目10余项,其中省级重点研发专项2项,发明专利2项,获得省部级奖2项。
一直致力于肿瘤放射治疗的临床、科研、教学工作,研究方向为胸部恶性肿瘤精准放射治疗的临床与基础研究及肿瘤的综合治疗。
免疫治疗的快速发展改变了广泛期小细胞肺癌的治疗格局,为患者带来显著的生存获益,但多数患者仍无法避免免疫耐药的结局。免疫耐药后小细胞肺癌的治疗仍是亟待解决的难题。
本病例为广泛期小细胞肺癌老年患者,随着病情进展,出现脑膜转移、肺内转移、左侧肾上腺转移。既往分别应用过PD-L1和PD-1抑制剂的联合治疗方案,虽然各线治疗均有效,但PFS时间较短。在末线治疗中,选择免疫双抗药物-卡度尼利再挑战,同时联合鞘注化疗+脑转移灶放疗”,颅外病灶疗效达CR,颅内病灶疗效达PR。治疗过程中,患者出现放射性脑损伤,应用安罗替尼后,临床症状和影像有效改善。目前卡度尼利+安罗替尼维持治疗中,至今PFS已超过15个月,耐受性良好。
脑膜转移是晚期肿瘤患者常见的致死性并发症,预后极差,自然平均生存时间仅为1个月。传统治疗方式是鞘内化疗+全脑放疗,平均生存期仅3个月。如何有效提高这部分患者的疗效和生存期,临床医生显得捉襟见肘。免疫时代的到来,为这类患者带来一线希望。既往观点认为中枢神经系统是免疫隔离的,免疫治疗效果差,主要考虑脑组织是免疫豁免器官--缺乏经典的淋巴引流系统,且血脑屏障限制T细胞浸润和免疫检查点抑制剂的透过率。但目前已经研究很清楚,中枢神经系统中存在大量功能性淋巴管,中枢神经内存在各种类型的抗原呈递细胞,包括小胶质细胞、巨噬细胞、星形胶质细胞。活化的T细胞能够穿过血脑屏障。卡度尼利作为双靶点免疫检查点抑制剂,能阻断PD-1和CTLA-4两个信号通路,在细胞毒性T细胞激活的不同阶段起作用,会进一步提高放免联合治疗的临床应答率。
该病例免疫再挑战应用卡度尼利单抗已超15个月,期间未出现明显不良反应。在此病例中,卡度尼利单抗联合鞘注化疗+放疗在脑膜转移同时颅外多发转移的患者中的疗效和安全性值得肯定,显著的疗效也为我们带来一些思考和启发:免疫双抗药物在小细胞肺癌治疗中缺乏高级别循证医学证据,对于双免治疗优势人群的筛选以及预测疗效的标志物,值得进一步探索。
排版编辑:肿瘤资讯-Shiro











 苏公网安备32059002004080号
苏公网安备32059002004080号


