根据GLOBOCAN的统计数据1,2020年全球胃癌新发病例位于第5位,死亡人数居第4位,超过70%的病例发生在亚洲,43.9%新发病例和48.6%死亡病例发生在中国。并且,中国胃癌患者初诊分期晚,近一半患者在诊断时即失去手术根治的机会2, 3。
近年来,随着证据的不断完善,免疫联合化疗已成为晚期胃癌一线标准治疗。相比于化疗时代12个月左右的总生存期(OS),免疫的加入将OS提高到15个月至18个月左右,总体客观缓解率(ORR)在50%左右4-7。
TALENT研究是由江苏省人民医院束永前主任牵头的多中心临床研究,旨在探索替雷利珠单抗联合安罗替尼+XELOX方案治疗不可切除或转移性的胃/胃食管结合部腺癌的安全性和有效性。在2023年ASCO-GI及CSCO大会上,曾汇报了初步的疗效结果。此次汇报一例转移性胃肝样腺癌患者获得转化手术机会及长期生存的病例。
病例
患者男性,66岁。2021.05出现上腹部不适。
胃镜(2021.05.18):胃窦溃疡性改变(胃MT?);病理:(胃窦大弯)腺癌,伴有肠型与肝样腺癌分化。免疫组化提示为pMMR/MSS型,HEP-1(+),AFP(+),HER2(-) 。PD-L1 CPS评分:10。基因检测:TP53基因 p.R156C,TMB 1个突变/Mb。
完善颈部+胸部+全腹部CT提示:胃窦部胃壁增厚,增强轻度强化。肝门部及肝胃间隙多发肿大淋巴结,考虑转移。肝脏S2段结节,转移可能大。
肿瘤标志物:AFP 545.80 ng/mL↑。
诊断:胃恶性肿瘤cT3N2M1,IV期(肝转移、多发淋巴结转移)。伴随诊断:HER2(-),pMMR/MSS,PD-L1 (+)。
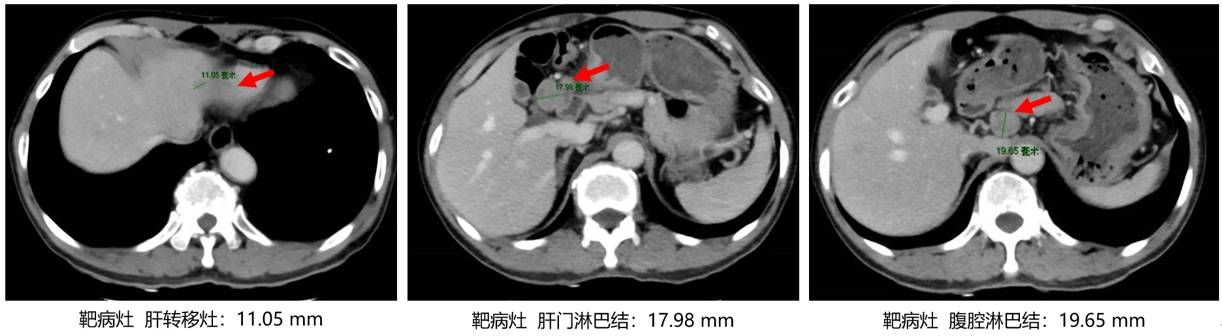
治疗过程
2021.06.02入组TALENT临床研究,予“XELOX+替雷利珠单抗+安罗替尼”方案治疗5周期。
2、4周期后疗效评价PR,且2周期后AFP降至正常。5周期后(靶病灶)肝转移灶消失。
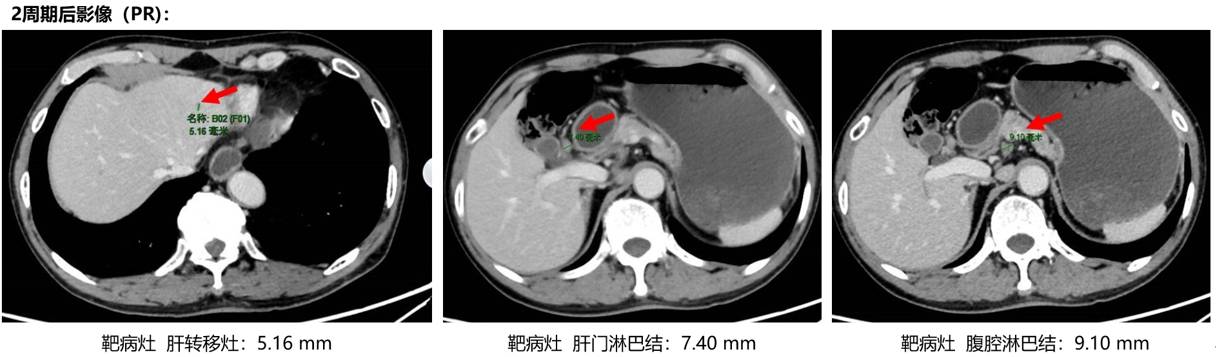
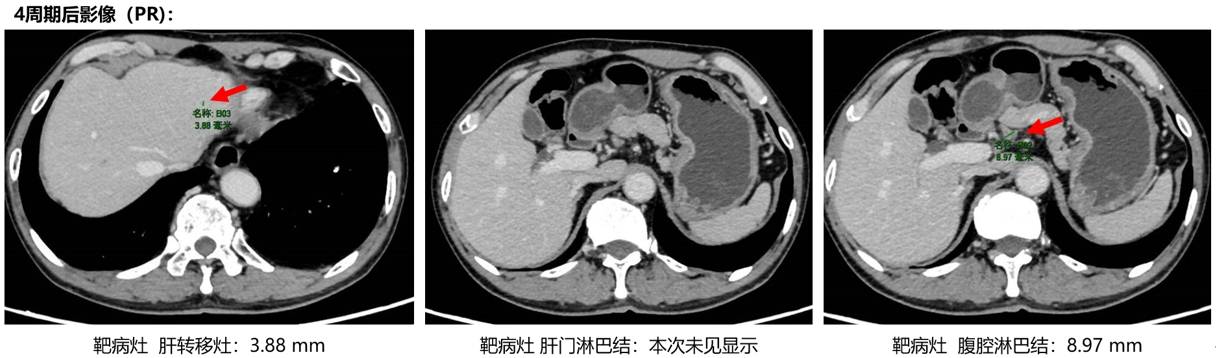
MDT讨论后于2021.11.25行“远端胃切除+残胃空肠吻合术 D2”。
术后病理:送检胃窦大弯,大小1*1*0.3cm,镜下未见肿瘤组织残留,远端、近端、吻合圈均为粘膜慢性炎。淋巴结分组:送检(1组,4sb组,5组,6组,7组,8组,9组,11组)淋巴结均未见癌累及。病理学评估:MPR。
术后影像学评估:CR。于2022.1.13开始行术后“XELOX+替雷利珠单抗+安罗替尼”治疗2周期,术后第3周期开始使用“替雷利珠单抗+安罗替尼”维持治疗,后于2023.9开始使用安罗替尼维持治疗至今,期间疗效评价维持CR。最近一次随访时间为2024.05,DFS长达2年余。
本期特邀专家——束永前 教授
江苏省人民医院肿瘤中心主任
苏州市立医院肿瘤中心主任
南京医科大学第一/第二附属医院肿瘤中心主任
国家临床重点专科建设单位主任
江苏省肿瘤精准诊疗医学创新中心主任
连续三年入选“中国高被引学者”
连续三年入选“全球高被引科学家”
2022年“全球顶尖10万名科学家”排名第163名
中国生物治疗学专业委员会副主委
中国医药教育协会腹部肿瘤专业委员会副主委
江苏省抗癌协会肿瘤复发与转移 / 化疗专业委员会主委
江苏省生物技术协会肿瘤精准医学诊疗专业委员会主委
本期特邀专家——陈晓锋 教授
江苏省人民医院肿瘤科
中国临床肿瘤学会青年专家委员会副主委
中国抗癌协会肿瘤营养专业委员会常委/副秘书长
中国抗癌协会食管肿瘤整合康复专委会常委
中国抗癌协会中西医整合结直肠癌专委会 委员
江苏省整合医学研究会遗传性肿瘤专业委员会 副主委
江苏省抗癌协会肿瘤营养专业委员会副主委
江苏省研究型医院学会肝胆肿瘤精准治疗专委会常委
江苏省抗癌协会复发与转移专业委员会青委会副主委
江苏省医学会肿瘤化疗与生物治疗分会青委会工作秘书
江苏省医师协会结直肠癌专业委员会青委会副主委
主编临床研究专著4部,发起了十余项IIT临床研究
发表SCI论文40余篇(第一/通讯)
专家点评
一方面,免疫联合化疗已成为指南推荐的晚期一线胃癌标准治疗,Rationale 305研究5是一项全球多中心的Ⅲ期、随机对照临床研究,验证了替雷利珠单抗联合化疗治疗局部晚期不可切除/转移性胃癌的疗效及安全性,也于近期发表在BMJ杂志上。 替雷利珠单抗是具有Fc段改造的PD-1单抗,可降低ADCC和ADCP效应。另一方面,抗血管生成的靶向治疗在晚期胃癌的指南中,已经进入二线治疗推荐。抗血管生成治疗与免疫治疗具有协同作用的理论基础,如血管正常化、调节免疫微环境,二者协同可以进一步提高疗效。
在上述背景下,我们设计了TALENT研究,使用“靶免化”这样的强效治疗方案,旨在针对晚期胃癌这种异质性强的肿瘤,尤其是肿瘤负荷较大、体力评分0-1分的胃癌患者,希望能达到快速缩瘤的效果。在入组的初始不可切除的65例患者中,有9例患者经过治疗后转化成功、可进行根治性手术切除,且术后3例pCR、3例MPR。上述展示的就是一个肝样腺癌患者转化成功达到术后MPR且DFS超过2年的案例。
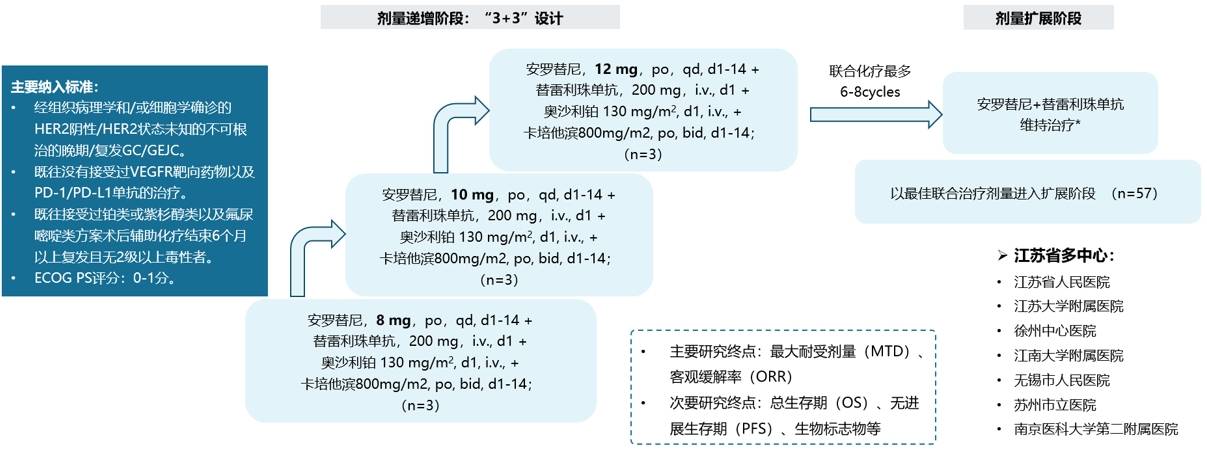
胃肝样腺癌的治疗
实际上,胃肝样腺癌(HAS)的发病率并不高(约占胃癌发病的1%),其特征为病理具有肝细胞癌分化,TP53为HAS常见的突变基因9。HAS易发生肝转移、淋巴结转移,预后差,治疗手段有限。既往的治疗方案以铂类为基础的化疗为主,目前尚无随机对照试验证实HAS的标准治疗方法。HAS和产AFP胃癌的概念有部分重叠。而在今年的最新版2024 CSCO指南中,增加了“SOX联合卡瑞利珠单抗/阿帕替尼”作为产AFP胃癌的II级治疗推荐,该推荐来源于一项36例样本的II期研究10,研究结果ORR达到55.6%,初步印证了化疗联合免疫/抗血管生成治疗对于产AFP胃癌的疗效。我们的研究设计也与此呼应。
转化手术的人群与价值
IV期胃癌患者的初始治疗选择是姑息性药物治疗。CONVO‐GC‐1研究11回顾性地分析了来自日本、韩国和中国的1206例IV期胃癌患者,提示达到R0切除的转化手术可能会带来生存获益。根据第六版日本胃癌指南的推荐,对于寡转移(包括单个肝转移)的胃癌患者可考虑在接受系统治疗后行手术切除;在CSCO指南中,对于胃癌单一远处转移者,II级推荐为系统化疗序贯手术治疗。
另一方面,我们在同时开展的SPACE研究12中看到了相似的结果:转化手术后的患者EFS较未手术患者显著延长(23.1个月 vs 8.4个月)。所以该患者在5周期后肝脏(包括肝门淋巴结)转移灶消失后,在MDT的讨论下,我们选择进行了根治性切除手术。目前,对于初始不可切除胃癌治疗后有手术指征的患者,应经过MDT充分评估,如预计可达到R0切除,选择根治性手术切除或许能进一步延长患者的生存。
1.Hyuna Sung et al., Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countrie.
2. Zheng RS et al., Cancer incidence and mortality in China, 2016. J Natl Cancer Center. 2022; 2: 1-9.
3. Lancet Public Health 2021; 6: e877–87
4. Janjigian YY, et al., First-line nivolumab plus chemotherapy versus chemotherapy alone for advanced gastric, gastro-oesophageal junction, and oesophageal adenocarcinoma (CheckMate 649): a randomised, open-label, phase 3 trial. Lancet. 2021;398(10294):27-40.
5. Qiu MZ, et al., Tislelizumab plus chemotherapy versus placebo plus chemotherapy as first line treatment for advanced gastric or gastro-oesophageal junction adenocarcinoma: RATIONALE-305 randomised, double blind, phase 3 trial. BMJ. 2024 May 28;385:e078876.
6. Xu J, et al., Sintilimab Plus Chemotherapy for Unresectable Gastric or Gastroesophageal Junction Cancer: The ORIENT-16 Randomized Clinical Trial. JAMA. 2023 Dec 5;330(21):2064-2074.
7. 2023 ESMO Virtual Plenary Resources,DOI: https://doi.org/10.1016/j.annonc.2023.01.006
8. Shen L, et al. First-line nivolumab plus chemotherapy versus chemotherapy in patients with advanced gastric cancer/gastroesophageal junction cancer/esophageal adenocarcinoma: CheckMate 649 Chinese subgroup analysis. AACR 2021. Abstr CT184.
9. Wang YK et al., AFP-producing gastric cancer and hepatoid gastric cancer. 2017 Nov 23;39(11):801-807.
10. Yakun Wang et al., Camrelizumab plus apatinib and SOX as first-line treatment in patients with alpha-fetoprotein–producing gastric or gastroesophageal junction adenocarcinoma: A single-arm, multi-center, phase 2 trial. JCO 42, 351-351(2024).
11. Yoshida K, et al., CONVO‐GC‐1 Study Group, Federation of Asian Clinical Oncology (FACO). International Retrospective Cohort Study of Conversion Therapy for Stage IV Gastric Cancer 1 (CONVO-GC-1). Ann Gastroenterol Surg. 2021 Oct 20;6(2):227-240.
12. Chen X et al., First-line camrelizumab (a PD-1 inhibitor) plus apatinib (an VEGFR-2 inhibitor) and chemotherapy for advanced gastric cancer (SPACE): a phase 1 study. Signal Transduct Target Ther. 2024 Mar 25;9(1):73.
排版编辑:肿瘤资讯-高惠
下期预告
替雷利珠单抗联合同步放化疗为无法手术的局部晚期食管鳞癌老年患者带来新希望
往期回顾:
【胃癌】转“胃”为安——一例转移性胃癌患者经替雷利珠单抗联合SOX治疗后成功转化达到病理完全缓解
【胃癌】救难“介胃”,白鱼“入”舟——一例转移性胃癌患者经替雷利珠单抗联合介入后达到完全缓解并长期获益











 苏公网安备32059002004080号
苏公网安备32059002004080号


